Medizinische Mikrobiologie: Gramnegative Stäbchen
Ernährungstechnisch anspruchsvolle Gram-negative Stäbchen
[Bearbeiten]Bordetella pertussis
[Bearbeiten]Bordetella pertussis ist der Erreger des Keuchhustens (Pertussis)
Morphologie und Eigenschaften: Bordetella pertussis ist ein kleines (ca. 0,8 x 0,4µm), kokkoides, unbewegliches, bekapseltes, Gram-negatives Stäbchen. Die Bakterien erscheinen im mikroskopischen Präparat einzeln oder paarweise gelagert. Kolonien von B. pertussis sind klein, glatt und glänzend mit einer hohen Konvexität (wie eine Quecksilberperle). Der Keim kann auf Spezialmedien innerhalb von 3 bis 4 Tagen bei 37°C in einer aeroben Atmosphäre kultiviert werden. Er wächst mit β-Hämolyse und läßt sich morphologisch nur schwer von anderen Bordetellen wie B. parapertussis und B. bronchiseptica unterscheiden.
Vorkommen: Alleiniges Habitat von B. pertussis sind die zilientragenden Epithelzellen des menschlichen Respirationstraktes.
Übertragung: Das hochkontagiöse Bakterium wird aerogen via Tröpfcheninfektion übertragen bes. im Stadium catarrhale. Der Kontagionsindex beträgt zwischen 0,8 und 1,0, das heißt, dass 80-100 % der Menschen welche mit dem Erreger in Kontakt kommen, auch erkranken. Darüberhinaus kann eine Übertragung über kontaminierte Gegenstände nicht ausgeschlossen werden, da das Pertussis-Bakterium für einige Tage außerhalb des Organismus überleben kann.
Epidemiologie: Trotz wirksamer Impfstoffe erkranken weltweit etwa 20 bis 40 Millionen Menschen an Keuchhusten, Todesfälle - meist bei Säuglingen unter 6 Monaten - sind etwa 200.000 bis 300.000 zu verzeichnen. Wegen des hohen Kontagionsindex bei nicht-immunen Menschen kann sich B. pertussis in Bevölkerungen mit niederiger Durchseuchungsrate epidemisch ausbreiten. In Regionen mit hoher Impfrate bleibt der Pertussis-Erreger endemisch, da der Immunitätsnachlaß eine Besiedelung erlaubt. Geschlecht, Jahreszeit und Klima spielen bei der Morbidität keine Rolle.
Pathogenitäts- und Virulenzfaktoren:
- Adhärenzfaktoren - Die zwei wichtigsten Adhärenzfaktoren sind das Filamenthämagglutinin (FHA) und das Pertussistoxin (PT), das sowohl als Exotoxin als auch als Adhäsin funktionieren kann. Daneben besitzt B. pertussis verschiedene antigenetisch unterschiedliche Fimbrien, die für die weitere Stabilisierung der Anheftung an die Epithelzellen des oberen Respirationstraktes verantwortlich sind. Darüber besitzt das Bakterium an der äußeren Membran die Membranproteine Pertactin und BrkA (Bordetella resistance to killing), die zur Bindung an die Wirtszellen beitragen.
- Exotoxine - Von entscheidender Bedeutung für die Pathogenese des Keuchhustens ist das Pertussistoxin (PT), das aus sechs Untereinheiten (Hexamer) aufgebaut ist und Verwandtschaft zu anderen Toxinen des AB-Typs wie dem Choleratoxin, Shigatoxin und Diphtherietoxin aufweist. Die eigentlich toxische Komponente ist das Monomer A, das von fünf anderen Untereinheiten, die zusammen das Oligomer B bilden, stabilisiert wird. Das Monomer A ist eine ADP-Ribosyltransferase, die G-Proteine modifiziert und eine veränderte Signaltransduktion innerhalb der Epithelzelle auslöst. Das PT sensibilisiert darüber hinaus den Körper für Histamin, sorgt für verstärkte Leukozytenaktivierung und erhöht die Insulinsekretion. Ein weiteres Protein, die invasive Adenylatcyclase (CyaA), kann in die Wirtszelle (Phagozyten) eindringen um dort zu einem unphysiologisch hohen cAMP-Spiegel zu führen.
- Endotoxine - Das aus dem Peptidoglykan der Zellwand gebildete Tracheale Cytotoxin (TCT) führt zur Stase der Zilienbewegung. In der äußeren Membran der Bakterien befinden sich Lipooligosaccharide, die chemisch und in ihrer Wirkung auf den Wirt den Lipopolysacchariden anderer gramnegativer Erreger ähnlich sind. Auch wenn sie bei der natürlichen Infektion keine Rolle zu haben scheinen, sind sie doch möglicherweise für einen Teil der unerwünschten Nebenwirkungen der zellulären Vakzine (Vollkeimimpfstoffe) verantwortlich.
- Die Kapsel bietet dem Erreger Schutz vor Inaktivierung durch das Komplementsystem.
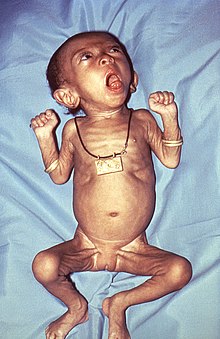
Pathogenese: B. pertussis überwindet die lokalen Immunmechanismen des oberen Respirationstraktes und kann bei völliger Gesundheit des Wirts ohne prädisponierende Faktoren eine Krankheit auslösen (hohe Pathogenität). Mittels verschiedener Adhäsine binden sich die Bakterien sehr fest an die Zellen des Flimmerepithels und können dann durch die Freisetzung von Toxinen die Erkrankung Keuchhusten (Pertussis) auslösen. Eine Invasion ins Epithel ist selten, es kommt zu (sub-)epithelialen Entzündungen und Nekrosen. Obwohl die Erreger in der Regel nicht invasiv sind, d.h. nicht in das Gewebe oder die Blutbahn gelangen, treten durch die produzierten Toxine dennoch systemische Effekte auf. Neben der Kapsel, die dem Erreger Schutz vor Inaktivierung durch Komplement bietet, sind Toxine für die Virulenz und Adhäsine für die Pathogenität verantwortlich.
Klinik: Nach einer Inkubationszeit von 1-2 Wochen durchläuft die Krankheit klassischerweise drei Stadien. Wegen der Gesamtdauer des chronischen Hustens spricht man auch vom „100 Tage Husten“:
- Stadium catarrhale mit Schnupfen und untypischem Husten, Dauer 1-2 Wochen, höchste Infektiösität
- Stadium convulsivum mit plötzlich auftretenden staccatoartigen Hustenattacken und typischem Jauchzen beim Wiedereinatmen, die teilweise begleitet werden von Erbrechen oder Ausstoßen von glasigem Schleim, Dauer 2-6 Wochen
- Stadium decrementi mit langsam abnehmenden Hustenattacken, Dauer ca. 3-6 Wochen
Komplikationen: Komplikationen treten bei Kindern im ersten Lebensjahr am häufigsten auf. Dazu gehören Pneumonie (25 % der Komplikationen), Bronchiolitis und Apnoen, die in seltenen Fällen zur Enzephalopathie (durch Hypoxie oder Einblutung) oder zum zum Tod führen können. Weiterhin kann es zu einer Otitis media kommen. Auch Krampfanfälle und durch das starke Husten verursachte Hyposphagma können auftreten.
Diagnostik: Da unter Umständen auch andere Erreger wie Bordetella parapertussis, Bordetella bronchiseptica, Chlamydia trachomatis und Adenoviren vorübergehend ähnliche Symptome wie Bordetella pertussis verursachen können, kommt der bakteriologisch-serologischen Diagnostik eine entscheidende Rolle zu. Die Diagnostik gestaltet sich schwierig. Direkt beimpfte Spezialnährböden („Hustenplatten“) funktionieren nur eingeschränkt. Serologisch läßt sich mittels ELISA spezifisches IgA nachweisen. Goldstandard ist jedoch zur Zeit die PCR.
Therapie: Die Antibiotikatherapie (Makrolide, alternativ Amoxicillin oder Cotrimoxazol) im Stadium convulsivum ist von fraglichem Nutzen. Der Husten spricht auf Hustenstiller nur schlecht an.
Immunität und Prophylaxe: Nach einer natürlichen Infektion besteht im ersten Jahrzehnt nach der Erkrankung eine tragfähige Immunität. Die wichtigste prophylaktische Maßnahme ist die aktive Immunisierung. Es existierten dafür ein Ganzkeimimpfstoff (zelluläre Vakzine) und verschiedene azelluläre Vakzinen.
- Ganzkeimimpfstoff (whole cell vaccine): aus inaktivierten Bordetella pertussis-Zellen gewonnene Lysate, früher mit mehr Nebenwirkungen behaftet
- Azelluläre Vakzine (subunit vaccines): Gemische von B. pertussis-Komponenten
Die gegenwärtig zugelassenen Präparate beider Kategorien bieten bei vollständig durchgeführtem Immunisierungsschema einen sehr guten Impfschutz, jedoch garantieren weder Impfung noch Erkrankung einen lebenslangen Schutz vor einer Infektion mit B. pertussis. Erwachsene erkranken seltener und weniger schwer als Kinder oder Säuglinge. Impfraten von mehr als 90 % sind anzustreben, um einen Kohortenschutz aufzubauen, der einen maximalen Schutz von Neugeborenen und Kindern in den ersten Lebensmonaten bietet. Die Impfung behindert nicht die Kolonisation (Relativ höhere Durchseuchung in Ländern mit hoher Impfrate).
Forschungsgeschichte: 1906 konnte ein schwer anzüchtbares Bakterium durch die Bakteriologen Jules Bordet und Octave Gengou als Erreger des Keuchhustens erstmals identifiziert werden. Zunächst wurde es als Bordet-Gengou-Bacillus den hämophilen Stäbchenbakterien zugeordnet. Bei der später notwendigen Klassifizierung wurde zu Ehren Jules Bordets die Bezeichnung Bordetella pertussis gewählt. Im Jahr 2002 wurde das Genom des Keuchhustenerregers, das aus insgesamt 3800 Einzelgenen besteht, nach über vierjähriger Forschungsarbeit von einem internationalen Forscherteam an der University of Cambridge entschlüsselt.
Weblinks: RKI - Pertussis
Brucella melitensis
[Bearbeiten]| Brucella melitensis | ||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
 | ||||||||||||||||||||
| Systematik | ||||||||||||||||||||
|
Etymologie: Der Name stammt von dem englischen Militärarzt David Bruce.
Morphologie und Eigenschaften: Brucellen sind kurze, stäbchenförmige, Gramn-egative und aerobe Bakterien.
Vorkommen: Organismen der Zoonose kommen im Urogenitalbereich von Kühen, Schafen, Schweinen u.a. Tieren vor. U.a. deshalb werden Milchprodukte in Deutschland pasteurisiert.
Krankheitsbilder: Brucellen können bei Übertragung auf den Menschen sehr selten eine zyklische Allgemeininfektion auslösen mit Allgemeinsymptomen, undulierendem Fieber und multiplem Organbefall (Knochen und Gelenke, Leber, Orchitis). Die Krankheit wird als Berufskrankheit anerkannt.
- B. m. melitensis (Schaf, Ziege) verursacht das Maltafieber
- B. m. abortus (Rind) ist der Erreger des Morbus Bang
- B. m. suis (Schwein) kann ebenfalls eine Brucellose auslösen
- B. m. ovis, B. m. canis und B. m. neotomae sind für den Menschen ungefährlich

Epidemiologie: In Mittelmeerländern sind Rohmilchprodukte ein Risiko. Ebenfalls gefährdet sind beruflich Exponierte. Der Tierbestand in Deutschland ist zur Zeit Brucellose-frei. Insgesamt ist die Erkrankung selten.
Diagnostik: Anzucht auf komplexen Medien oder in Blutkultur mit verlängerter Bebrütung. Serologischer Nachweis mit Antiseren.
Therapie: Dauertherapie mit Doxycyclin plus Aminoglykosid, alternativ Cotrimoxazol (ggf. plus Aminoglykosid) oder Doxycyclin plus Rifampicin.
Prophylaxe: Pasteurisierung von Milchprodukten, Schutzkleidung in Berufen mit Tierkontakt.
Taxonomie: Früher wurden in der Gattung Brucella zahlreiche Spezies unterschieden. Auf Grund von DNS-Stammbäumen geht man heute von nur einer Spezies Brucella melitensis aus. Die früheren Arten wurden als Biovarietäten von B. mellitensis eingestuft. In der Praxis wird jedoch meist an der alten Arteneinteilung festgehalten.
Weblinks: RKI - Brucellose
Campylobacter sp.
[Bearbeiten]| Campylobacter sp. | ||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
 | ||||||||||||||||
| Systematik | ||||||||||||||||
|
Morphologie und Eigenschaften: Campylobacter-Spezies sind Gram-negative, mikroaerophile (Vorliebe für reduzierten Sauerstoffgehalt, 5%) und polar begeißelte sowie Oxidase- und Katalase-positive Stäbchen. Die Differenzierung erfolgt biochemisch und anhand der Antibiotikasensibilität (Nalidixinsäure, Cephalothin).
Krankheitsbilder: Die Erreger C. jejuni (häufigster Erreger) und C. coli können beim Menschen eine entzündliche Durchfallerkrankung (Campylobacter-Enteritis) auslösen. Sie sind die zweithäufigsten Erreger einer solchen Infektion nach Salmonellen. Wichtigste Komplikation ist das Guillain-Barré-Syndrom.
Pathogenese: Die Bakterien der Campylobacter-Gruppe gehören, wie die Shigellen, zu den Erregern, die in die Schleimhäute des Darmes einwandern. Durch Bildung eines hitzeresistenten Enterotoxins werden vermutlich die Durchfallsymptome ausgelöst.
Übertragung: Die Übertragung der Erreger erfolgt vor allem durch Lebensmittel tierischer Herkunft, besonders ungenügend gegartes Geflügelfleisch und nicht pasteurisierte Milch. Darüber hinaus sind die Erreger in den Ausscheidungen gesunder Haustiere zu finden und können häufig in Oberflächengewässern nachgewiesen werden. Da sich Campylobacter in rohem Fleisch vermehren stellen sie eine Gefahr beim Grillen dar.
Epidemiologie: In den Industrie- und Entwicklungsländern werden 5 bis 10% der Durchfallerkrankungen durch Campylobacter hervorgerufen (z.B. USA schätzungsweise 2 Mio. Campylobacter-Infektionen pro Jahr).
Therapie: Erythromycin, alternativ Chinolone, es gibt Multiresistenzen
Weblinks: RKI - Campylobacter-Infektionen
Helicobacter pylori
[Bearbeiten]| Helicobacter | ||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
 | ||||||||||||||||||
| Systematik | ||||||||||||||||||
|
Morphologie und Eigenschaften: Helicobacter pylori ist ein Gram-negatives, schraubenförmiges, begeißeltes, mikroaerophiles Bakterium, das im menschlichen Magen vorkommt.
Krankheitsbilder: Heute wird H. pylori für 80% der Magengeschwüre und praktisch alle Duodenalulzera sowie für die chronisch aktive B-Gastritis verantwortlich gemacht, bei denen eine verstärkte Sekretion von Magensäure auftritt. Weiterhin sollen MALT-Lymphome großteils durch die durch H. pylori induzierte Immunantwort verursacht sein. Eine Rolle in den Genese des Adenokarzinoms des Magens wird für möglich gehalten.
Pathogenitäts- und Virulenzfaktoren:
- Adhärenzmechanismen
- Das Enzym Urease ermöglicht dem Bakterium das Überleben im sauren Magensaft durch Bildung einer (basischen) Ammoniakwolke um das Bakterium, welche die Säure neutralisiert.
- Zytotoxin VacH und CagH
- Einen weiteren Faktor für die Entstehung der Entzündungsreaktion, entdeckte ein internationales Forscherteam am Institut Pasteur in Paris. Demnach dringt das Bakterium mit einem nadelartigen Fortsatz in die Zellen der Magenschleimhaut ein. Hierbei wird ein Peptidoglycan injiziert – der Keim selbst bleibt außerhalb der Zellen. Im Inneren der Zellen bindet das Peptidoglycan an ein spezifisches Rezeptormolekül, wodurch eine Reaktionskette in Gang gesetzt wird, die letztlich zur Entzündung der Magenschleimhaut führt. Offensichtlich wird H. pylori im Gegensatz zu vielen anderen pathogenen Keimen ohne diesen Eindringvorgang nicht vom Immunsystem erkannt, da die dafür zuständigen Oberflächenrezeptoren der Zellen nicht an das Bakterium binden. Der von den Forschern entdeckte Injektionsmechanismus kommt nicht bei allen Stämmen von H. pylori vor. Dies erklärt warum nur ein Teil der infizierten Menschen an Magenschleimhautentzündung erkranken. Literatur: Jérôme Viala et al.: Nature Immunology (Online-Vorabveröffentlichung, DOI: 10.1038/ni1131)
Pathogenese: H. pylori provoziert eine Immunantwort des Körpers, da die Immunozyten jedoch im Schleim und in der saueren Umgebung des Magens nicht überleben können, zerfallen sie und geben Zytokine und Zerfallsprodukte in die Umgebung ab und unterhalten die chronische Entzündung. Die Infektion mit dem Bakterium bedingt im Allgemeinen eine verstärkte Sekretion von Magensäure. Folgen sind Ulzera und die Induktion von MALT-Lymphomen.


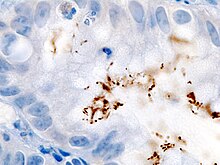

Übertragungsweg: Vermutlich fäkal-orale Übertragung. Epidemiologische Daten weisen außerdem auf die Möglichkeit von oral-oralen oder einen gastro-oralen (Kontakt mit durch H. pylori infiziertem Magenschleim bei Erbrechen) Übertragungsmechanismus hin. Der Magen gilt nach derzeitigem Kenntnisstand als das Hauptreservoir für die Keime, was die letzteren Auffassungen stärkt. Ferner wird auch eine mögliche Übertragung durch Schmeißfliegen diskutiert. Es wurde eine zeitlang behauptet, dass das Vorkommen des Bakteriums im Zusammenhang mit dem sozioökonomischen Status steht. Jedoch haben Arbeiten aus der Schweiz und Deutschland diese Ansicht nicht stützen können. So sind etwa 7 % der Jugendlichen in der Schweiz und Deutschland von H. pylori befallen, unabhängig vom Status. Nach bisherigen Untersuchungen sind etwa 50 % der älteren Erwachsenen mit dem Bakterium kontaminiert. Jedoch bekommt nicht jeder ein Ulcus! Bei einer Beseitigung des Bakteriums besteht nur ein einprozentiges Risiko einer Wiederansteckung.
Epidemiologie: Mit einer Prävalenz von weltweit ca. 50% ist die H. pylori-Infektion eine der häufigsten chronischen bakterielle Infektionen. Hierbei ist die Infektionsrate in Entwicklungsländer sehr viel höher als in den Industrienationen. In Deutschland sind insgesamt ca. 33 Millionen Menschen mit H. pylori infiziert, von denen ungefähr 10 bis 20 % eine peptische Ulkuskrankheit entwickeln. Für das weltweit verbreitete Bakterium konnten insgesamt 370 Stämme nachgewiesen werden, die in Details ihrer DNA-Sequenzen sehr große Unterschiede aufweisen. Für Epidemiologen und Ethnologen gleichermassen interessant ist die Tatsache, dass die Völkerwanderungen des Menschen und die Verbreitung von H. pylori gemeinsame Wurzeln haben.
Diagnostik: Der Nachweis des H. pylori geschieht durch mehrere Probeentnahmen aus Antrum und Corpus des Magens und dem direkten mikroskopischen Nachweis, der Kultur oder indirekt über den Nachweis der Urease. Auch der Harnstoff-Atemtest kann das Bakterium mit hoher Wahrscheinlichkeit nachweisen. Beim Atemtest trinkt der Patient eine 13C Isotopen-markierte Harnstofflösung. Harnstoff wird durch die Urease gespalten und 13C markiertes Kohlendioxid abgeatmet, welches dann nachgewiesen werden kann. Da 13C ein stabiles Isotop ist, ist der Test ungefährlich. Möglich ist auch der Nachweis des Keimes im Stuhl (PCR). Zuletzt besteht auch die Möglichkeit des Antikörpernachweises im Blut (Serologie).
Therapie: Die Therapie von H. pylori besteht aus der Kombination eines Protonenpumpenhemmers mit zwei Antibiotika (Eradikationstherapie). Hierfür gibt es zahlreiche "Rezepte":
| Therapieform | Protonen-pumpen-hemmer | Antibiotikum | Antibiotikum | Anmerkung |
|---|---|---|---|---|
| french triple | Omeprazol | Clarithro-mycin | Amoxicillin | gutes Ansprechen |
| italian triple | Omeprazol | Clarithro-mycin | Metronidazol | 25 % Resistenz bei Metronidazol |
Bei den Antibiotika werden Amoxicillin oder Metronidazol zusammen mit Clarithromycin kombiniert. Nach 7-tägiger Behandlung ist mit über 95 % Erfolgsrate zu rechnen. Die Therapie mit Protonenpumpenhemmer, Amoxicillin und Clarithromycin („french triple“) erzielt die höchsten Eradikationsraten. Die zweite gängige Behandlung besteht aus Protonenpumpenhemmer, Metronidazol und Clarithromycin („italian triple“). Letztere bietet sich insbesondere bei Penicillinallergie an, da in diesem Fall Amoxicillin nicht verwendet werden darf.
Alternativ bietet die Quadruple-Therapie die Möglichkeit zur Eradikation. Hierbei wird ein Protonenpumpenhemmer mit Tetracyclin und Metronidazol sowie Wismut kombiniert. Bei 10-tägiger Anwendung ist der Erfolg 95 %. Hierbei wird der Protonenpumpenhemmer über die Tage 1 bis 10 der Therapie appliziert, die beiden Antibiotika und Wismut über die Tage 4 bis 10.
Mittels einem ¹³C-Harnstoff-Atemtest (nicht invasiv in der Ausatemluft) kann etwa sechs Wochen nach Therapieende der Erfolg nachgewiesen werden. Ursachen für Misserfolge können neben mangelnder Compliance eigentlich nur Antibiotika-Resistenz sein, daher vor einem neuen Therapieversuch den Keim kulturell anzüchten. Die Rezidivrate beträgt 5 % pro Jahr.
Nicht jede Helicobacter-pylori-Infektion muss behandelt werden. Bei einem Magen- oder Zwölffingerdarmgeschwür mit nachgewiesenem H. pylori sowie beim Helicobacter-assoziierten MALT-Lymphom ist die Therapie jedoch zwingend erforderlich.
Ethnologie: Bei einem Vergleich des Bakteriengenoms wurde festgestellt, dass es bevorzugt innerhalb von Familien weitergegeben wird. Das führt dazu, dass Bakterienstämme in unterschiedlichen geographischen Bevölkerungsgruppen genetisch unterscheidbar sind. Die europäischen Stämme der Bakterien stammen beispielsweise aus dem Nahen Osten und aus Asien. Durch Vergleiche des Bakterienerbgutes sollte es möglich sein, die Ausbreitung der Bakterien, und somit indirekt Wanderbewegungen der Menschheit nachzuvollziehen.
Entdeckungsgeschichte: Dem deutschen Arzt und Forscher Robert Koch (1843-1910) gelang es im 19. Jahrhundert Bakterien durch Kultivierung, Mikroskopie und Übertragung in einen Kausalzusammenhang mit Infektionskrankheiten zu bringen. Er ebnete so den Weg in die medizinische Mikrobiologie und beschrieb die Bakterien - wie H. pylori. Bereits vor über 70 Jahren wurden spiralige Mikroorganismen im Magen nachgewiesen. Die Idee von Magenbakterien als Krankheitsursache von Magen- und Duodenalulzera konnte sich allerdings nicht gegen die Alternativhypothesen "Übersäuerungsproblem" und „psychosomatisch“ durchsetzen, da man weithin annahm, dass das saure Magenmilieu eine Magenflora ausschließe.
Barry Marshall und J. Robin Warren aus Perth (Western Australia), entdeckten H. pylori 1983 (wieder), wurden damit aber von der medizinischen Forschung lange Zeit nicht ernst genommen. Marshall u.a machten 1985 heroische Selbstversuche und konnten durch Trinken von Helicobacter-Lösungen tatsächlich bei sich selbst eine akute Gastritis auslösen. 1989 gelang es ihnen dann allgemeines Gehör zu finden und das Bakterium wurde weltweit als Ursache von Ulcus und Gastritis akzeptiert. Im Dezember 2005 wurden Warren und Marshall für ihre Arbeiten zu H. pylori je zur Hälfte mit dem "Nobelpreis für Physiologie oder Medizin" ausgezeichnet.
Ursprünglich wurde der Organismus Campylobacter pyloridis genannt (nach dem Pylorus). Später wurde es in Campylobacter pylori umbenannt, damit es besser zu den Namen anderer krankmachender Keime im Magen-Darm-Trakt passt. 1989 wurde es endgültig wegen des Bestandes an Enzymen und Funktionen Helicobacter pylori genannt.
Andere Arten von Helicobacter wurden seitdem auch in den Mägen anderer Säugetiere und Vögel entdeckt.
Aussichten: 2005 trafen sich am Max-Planck-Institut für Infektionsbiologie in Berlin Helicobacter-Experten aus Nordamerika, China und Europa, um über die Entwicklung und den Einsatz eines Impfstoffs zu diskutieren. Nach Thomas F. Meyer, Direktor des MPI für Infektionsbiologie, wird „die Gefährlichkeit von H. pylori immer noch generell unterschätzt. Mehr als die Hälfte aller Menschen ist damit infiziert, und man muss davon ausgehen, dass etwa zehn Prozent der Weltbevölkerung einmal im Leben an einem Magengeschwür erkranken“. Ein Teil davon leidet danach an einem Magenkarzinom, das weltweit jährlich etwa 750.000 Opfer fordert. Es ist zehn- bis zwanzigfach häufiger als der seltene Speiseröhrenkrebs. Um den Zusammenhang dieser Krebsform, dem Sodbrennen mit dem Verschwinden des Magenkeims H. p. geht es vor einer Entscheidung über die Impfstrategie. Malfertheiner u. a. schlagen im American Journal of Gastroenterology die Impfung vor allem in Ländern mit hohem Magenkrebsrisiko vor, also vor allem in China, Japan und den Staaten Lateinamerikas. Eine Rolle bei der künftigen Entscheidung kann auch das Interesse der Pharmaindustrie spielen, die das sichere Geschäft mit den Antibiotika verständlicherweise hoch einschätzt. Die Berliner Forscher warnen vor verfrühter Hoffnung auf die Möglichkeit zur Impfung. Ein zuverlässiger Impfstoff sei vor 2010 nicht verfügbar.
Genomforschung: Bereits im Jahr 1997 wurde die erste komplette Genomsequenz eines Vertreters der Art Helicobacter pylori publiziert. 1999 wurde eine zweite Sequenz veröffentlicht womit sich erstmals die Möglichkeit ergab, die Genomsequenzen von zwei Isolaten derselben Bakterienart zu vergleichen. Dabei zeigte sich, dass sich die beiden Isolate in etwa 10% der Gene unterschieden. Literatur: Tomb, J.-F. et al., 1997. The complete genome sequence of the gastric pathogen Helicobacter pylori. Nature 388:539-547 und Alm RA et al., 1999. Genomic-sequence comparison of two unrelated isolates of the human gastric pathogen Helicobacter pylori. Nature 397:176-80.
Weblinks: RKI - Helicobacter pylori
Legionellen
[Bearbeiten]| Legionella sp. | ||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
 | ||||||||||||||||||
| Systematik | ||||||||||||||||||
|
Von den über 40 Legionellen-Arten sind u.a. L. pneumophila, L. micdadei, L. bozemani und L. dumoffi humanpathogen und lösen pulmonale Legionellosen aus. Legionella pneumophila ist der häufigste Erreger (70-80 %) der Legionärskrankheit und des Pontiac-Fiebers.
Morphologie und Eigenschaften: L. pneumophila ist ein obligat aerobes, gramnegatives, unbekapseltes und sporenloses Stäbchen-Bakterium mit meist monopolarer Begeißelung. Im Nativpräparat finden sich meist kurze Stäbchen, während in Kultur meist unterschiedlich große Stäbchen-Bakterien (2-20µm) vorherrschen. Legionellen benutzen v.a. Aminosäuren als Energiequelle. Zucker können nicht zu Säuren verstoffwechselt werden. Legionellen sind auf Cystein und Eisen(III)-Ionen im Nährmedium angewiesen, daher findet man sie in der freien Natur in der Regel in Kombination mit autotrophen Mikroorganismen (z.B. Eisen-Mangan-Bakterien) oder als Endosymbionten in Amöben (z.B. Acanthamoeba, Naegleria, Hartmanella), die den Legionellen Schutz bieten und bei der Verbreitung von L. pneumophila eine wichtige Rolle zu spielen scheinen. Legionellen bilden keine Urease und Nitratase, sind jedoch Katalase positiv. Sie sind gegen Austrocknung sehr empfindlich. Bei einer Temperatur von 60°C überleben sie etwa fünf Minuten.
Infektionsweg: L. pneumophila findet sich weltweit in Erd- und Gewässerproben. Infektionsquelle für den Menschen sind Warmwasserleitungen mit nicht ausreichend erhitztem Wasser, Klimaanlagen und Kühltürme. Die Übertragung erfolgt in der Regel aerogen, meist durch Einatmen von erregerhaltigen Aerosolen aus Klima-Anlagen oder Wasserhähnen. Es wird geschätzt, dass nur 10% der Infektionen wirklich zu einer Erkrankung führen. Eine Mensch-zu-Mensch-Übertragung findet nicht statt.
Epidemiologie: Legionellosen treten meist sporadisch, seltener in kleinen Epidemien auf. In den USA schätzt man, dass ca. 30 Erkrankungsfälle pro Jahr und 100.000 Einwohnern auftreten. Die Legionellosen haben in den Sommermonaten einen Höhepunkt. In endemischen Gebieten schätzt man, dass etwa 5% der Pneumonien auf Legionellen zurückzuführen sind.
Krankheitsbilder: Die Legionärskrankheit verläuft als atypische, interstitielle Pneumonie mit Fieber, Durchfällen, Kopfschmerzen und Desorientiertheit. Sie betrifft häufig immungeschwächte Menschen (z.B. Alkoholiker, HIV-Erkrankte). Die Letalität beträgt unbehandelt im Mittel etwa 10%, kann aber bis zu 80 % betragen.


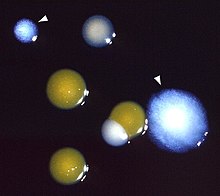
Das Pontiac-Fieber ist eine akute, selbstlimitierende respiratorische Erkrankung mit Husten und Schnupfen, die meist nach sieben Tagen spontan ausheilt.
Inkubationszeit: Die Inkubationszeit der Legionärskrankheit beträgt zwei bis zehn Tage. Die des Pontiac-Fiebers nur ein bis zwei Tage.
Pathogenese: L. pneumophila adhäriert an Wirtszellen über einen Pilus und induziert eine besondere Form der Phagozytose (sog. coiling phagocytosis), entgeht aber der intrazellulären Abtötung und vermehrt sich in nicht aktivierten phagozytierenden Zellen. L. pneumophila induziert eine z.T. nekrotisierende Entzündung der Alveolen. Die Abwehr von L. pneumophila als intrazellulärer Erreger ist wahrscheinlich von T-Lymphozyten abhängig. Diese aktivieren die erregerhaltigen Makrophagen, so dass die Erreger im Inneren der Phagozyten vernichtet werden können. L. pneumophila produziert Exotoxine (z.B. Hämolysin) und Enzyme. Die Rolle im Krankheitsgeschehen dieser Exotoxine ist noch nicht abschließend geklärt. Das Protein MIP (macrophage infectivity potentiator), ein 24 kDA Protein, scheint bei der Phagozytose-Induktion beteiligt zu sein.
Diagnostik:
- Antigennachweis: Ein L. pneumophila-Antigennachweis kann im Urin durchgeführt werden (ELISA, allerdings nur Serogruppe 1 von L. pneumophila).
- Mikroskopie: In der Gram-Färbung lassen sich Legionellen schlecht färben. Daher benutzt man meist Fluoreszenz-markierte polyklonale Antikörper.
- Anzucht: Die Anzucht kann aus Lungenbiopsien, Bronchialsekret und einer bronchoalveolären Lavage (BAL) gelingen. Wichtig ist, dass dem Labor die Verdachtsdiagnose einer Legionellose mitgeteilt wird, da der Erreger auf Routine-Nährböden nicht anzuziehen ist. Die Anzucht kann auf gepufferten Kohle-Hefe-Agar mit Zusatz von α-Ketoglutarat (α-BCYE Agar) gelingen. Kolonien erscheinen bei kapnophiler Bebrütung nach 2-7 Tagen.
- PCR: Die PCR ermöglicht einen schnellen Erreger-Nachweis. Die Spezifität und die Sensitivität sind jedoch noch offen.
- Serologie: Im Blut können Antikörper gegen L. pneumophila nach etwa zehn Tagen nachgewiesen werden (IF, EIA, Western blot).
Therapie: Die Therapie der Legionärskrankheit erfolgt meist mit Makroliden (z.B. Erythromycin), evtl. plus Rifampicin, alternativ können auch Fluorchinolone eingesetzt werden. Die Infektion ist nach dem Infektionsschutzgesetz meldepflichtig.
Prophylaxe: Trinkwasseruntersuchungen, Sanierung möglicher Infektionsquellen durch Erhitzen oder Chlorierung.
Historisches: L. pneumophila wurde erst 1976 entdeckt, als bei einer Tagung der American Legion in Phildadelphia eine Epidemie unter den teilnehmenden Veteranen auftrat. 29 der 182 erkrankten Veteranen verstarben damals. Die Legionärskrankheit erhielt davon ihren Namen.
Weblinks: RKI - Legionellose
Pasteurella multocida
[Bearbeiten]Aerobes, gramnegatives Stäbchen der Mundflora von Katzen und Hunden. Häufiger Erreger bei Katzenbißverletzung. Kann zu rasch progredienten Weichteilinfektionen führen.
D.: Kultur
Th.: Ohne Infektionszeichen: Wundreinigung und -desinfektion, Antibiotische Therapie bei Biss ins Gesicht oder an den Händen, ansonsten abzuwägen. Bei Weichteilinfektion: Chirurgische Wundsanierung, Ampicillin oder Amoxicillin plus Clavulansäure.
HACEK-Gruppe
[Bearbeiten]Haemophilus sp.
[Bearbeiten]| Haemophilus | ||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Systematik | ||||||||||||||||||
|
Morphologie und Eigenschaften: Die 16 Arten der Gattung Haemophilus sind kurze, gramnegative, unbewegliche Stäbchen, die die Schleimhäuten von Menschen und Tieren bewohnen und verschiedene Erkrankungen auslösen können. Beinahe alle Haemophilus-Arten sind in der Lage, ohne Sauerstoff zu überleben, allerdings sind sie meistens eher aerob (fakultativ aerob). Der Name der Gruppe kommt von ihrer besonderen Vorliebe für Nährböden mit Blut- oder Hämoglobinzusätzen, auf denen sie in Kultur gehalten werden können. Die ernährungstechnisch anspruchsvollen Bakterien wachsen bis auf H. hämolyticus nicht auf normalem Blutagar, lassen sich aber auf Kochblutagar heranzüchten.
Medizinisch bedeutsame Arten:
Haemophilus influenzae (HiB)
[Bearbeiten]Die invasive Haemophilus Influenzae B-Infektion ist eine der schwersten bakteriellen Infektionen in den ersten fünf Lebensjahren. Der Erreger ist ausschließlich humanpathogen und findet sich vor allem auf den Schleimhäuten der oberen Atemwege. Bei Erkrankungen gefundene Exemplare sind fast immer bekapselt. Etwa 50 % der gesunden Bevölkerung sind von diesem Keim besiedelt, davon 5 % mit dem bekapselten Typ.
Kultur: Haemophilus Influenzae B benötigt zum Wachsen Hämin (Faktor X) und NAD bzw. NADPH (Faktor V). Die Kultur gelingt demnach auf Kochblutagar oder auf Blutplatten, die mit S. aureus beimpft sind, der NAD zur Verfügung stellt („Ammenphänomen“).
 |
 |
 | |
 | |
 |
Infektionsweg: Übertragung von Mensch zu Mensch über Tröpfcheninfektion
Inkubationszeit: Zwei bis fünf Tage.
Pathogenitäts- und Virulenzfaktoren:
- Adhäsine
- Pili
- IgA-Protease
- Polyribitolphosphat-Kapsel: 95 % der invasiven Infektionen werden durch Kapseltyp B verursacht, unbekapselte Stämme verursachen meist nur lokale Infektionen.
Krankheitsbilder: Fieberhafte Infektionen der Atemwege wie Otitis media, Sinusitis, Bronchitis und Pneumonie in allen Altersklassen. Lebensbedrohliche Komplikationen, von denen vorwiegend Kinder betroffen sind, sind die eitrige Meningitis, die Sepsis und die Epiglottitis (DD: Pseudokrupp). Weitere mögliche Manifestationen umfassen Pleuritis, Perikarditis, Arthritis und Osteomyelitis. Klinisch sind die Kinder mit Epiglottitis schwer krank, haben starke Halsschmerzen, sprechen, husten und schlucken nicht (Speichel läuft aus dem Mund) und es besteht Erstickungsgefahr.
Diagnostik: Klinik, Bei V.a. Epiglottitis ist die Inspektion des Mundraumes wegen Erstickungsgefahr zu unterlassen!
Therapie: Aminopenicilline (Amoxicillin, Ampicillin) plus BLI oder parenterale 3a/b-Cephalosporine, ferner Makrolide und Cotrimoxazol.
Prophylaxe: Schutzimpfung: Ab vollendetem zweiten Lebensmonat erfolgen drei Impfungen im Abstand von vier Wochen mit Kombinationsimpfstoffe, im 11. bis 14. Lebensmonat dann eine vierte Impfung. Bei verspäteter erster Impfung nach dem 18. Lebensmonat erfolgt nur eine Impfung. Bereits zwei Jahre nach Einführung der Impfung in Deutschland im Jahre 1990 sind HiB-Infektionen um mehr als 80% zurückgegangen. Wurden in den 80er-Jahren noch etwa 50 Fälle jährlich registriert, waren es in den vergangenen Jahren durchschnittlich etwa acht. Meist werden Kombinationsimpfstoffe eingesetzt, die u.a. die HiB-Komponente beinhalten. Über Impfreaktionen wie leichte Temperaturerhöhung, Rötung und Schwellung an der Einstichstelle wird gelegentlich berichtet. Im Allgemeinen treten diese Reaktionen nach der zweiten und dritten Impfung etwas häufiger auf. Geimpft werden sollten unbedingt alle Patienten ohne Milz oder deren Milz nur eingeschränkt arbeitet (Splenektomierte sollten auch unbedingt gegen Meningokokken und Pneumokokken geimpft sein).
Weblinks: RKI - Haemophilus influenzae
Haemophilus ducreyi
[Bearbeiten]Haemophilus ducreyi ist der Erreger des weichen Schanker (auch Ulcus molle), einer bei uns meldepflichtigen Geschlechtskrankheit. Die Krankheit und damit auch ihr Erreger kommen vor allem in den tropischen Regionen in Afrika, Südostasien und Lateinamerika vor. Sichtbares Zeichen der Krankheit sind rundliche Geschwüre an den Schamlippen und im Scheidenvorhof der Frau bzw. an der Glans penis und am Penisschaft des Mannes sowie die Mitbeteiligung der regionären Lymphknoten. Seit 2003 ist auch das Genom dieses Bakteriums bekannt.
Therapie: Makrolide, alternativ Cotrimoxazol oder parenterale Cephalosporine 3a.
Haemophilus parainfluenzae
[Bearbeiten]Haemophilus parainfluenzae ist ein nur gering pathogener Bewohner des Mundrachenraums. In seltenen Fällen kann er eine Endokarditis auslösen.
Haemophilus aegypticus
[Bearbeiten]Haemophilus aegypticus, auch als Koch-Weeks-Bacillus bezeichnet, ist morphologisch nicht von H. influenzae zu unterscheiden. Er ist vor allem in Nordafrika und anderen tropischen und subtropischen Kontinenten verbreitet und der Erreger der als purulente Konjunktivitis bekannten Augenbindehautentzündung.
Haemophilus aphrophilus
[Bearbeiten]Haemophilus aphrophilus kann Abszesse und Endokarditis hervorrufen.
Apathogene Haemophilus sp.
[Bearbeiten]Haemophilus parahaemolyticus, Haemophilus paraprophilus und Haemophilus haemolyticus verursachen keine Erkrankungen.
Anders als die anderen Vertreter der Gattung ist H. haemolyticus in der Lage, das Hämoglobin des Blutes zu spalten und zu nutzen.
Actinobacillus actinomycetem comitans
[Bearbeiten]Aerobes, gram-negatives, unbewegliches Stäbchenbakterium.
Krankheitsbilder: Juvenile Parodontitis, Endokarditis, Perikarditis, Meningitis, Knochen- und Weichteilinfektionen.
Cardiobacterium sp.
[Bearbeiten]Eikenella corrodens
[Bearbeiten]Mikroaerophile, gramnegative, kokkoide und unbewegliche Stäbchenbakterien. Teil der menschlichen Mundflora. Häufiger Erreger bei Bissverletzungen durch Menschen.
D.: Kultur
Th.: Amoxicillin plus Clavulansäure
Kingella sp.
[Bearbeiten]Ernährungstechnisch weniger anspruchsvolle Gram-negative Stäbchen
[Bearbeiten]Anaerobe Stäbchen
[Bearbeiten]Gram-negative, anaerobe Stäbchen gehören bei Mensch und Tier zur normalen Bakterienflora. Als Opportunisten können sie unter für sie günstigen Umständen (reduzierte Immunität, Eintritt in sterile Körperhöhlen, Verletzungen u.a.m.) endogene, eitrige oder septische Infektionen verursachen. Die Anaerobier können solitär oder als Teil aerob-anaerober Mischinfektionen auftreten.
Bacteroides fragilis
[Bearbeiten]| Bacteroides fragilis | ||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
 | ||||||||||||||||||
| Systematik | ||||||||||||||||||
|
Bacteroides fragilis gehört, wie die übrigen Mitglieder der Bacteroides, zu den Gram-negativen, obligat anaeroben und nicht sporenbildenden Stäbchen-Bakterien. Bacteroides sp. gehören bei Mensch und Tier zur physiologischen Bakterienflora und spielt eine wichtige Rolle bei der Kolonisationsresistenz. B. fragilis findet sich häufig bei Mischinfektionen mit aeroben bzw. fakultativ anaeroben Bakterien.
Morphologie und Eigenschaften: Bacteroides fragilis ist ein obligat anaerobes, Gram-negatives und nicht sporenbildendes Stäbchenbakterium. Gegen Umwelteinflüsse ist Bacteroides fragilis auf Grund der Empfindlichkeit gegenüber Sauerstoff relativ empfindlich. Das Bakterium ist galleresistent, spaltet Saccharose und ist nicht pigmentiert. Die Identifizierung erfolgt biochemisch.
Pathogenitäts- und Virulenzfaktoren: B. fragilis bildet z.T. eine Kapsel, die es in Kombination mit anderen anti-phagozytären Substanzen vor der Phagozytose schützt. Das Lipopolysaccharid (LPS) von Bacteroides fragilis unterscheidet sich von dem der aeroben Bakterien und entfaltet nur eine geringere Toxizität im Wirtsorganismus. Der Mikroorganismus besitzt zur Verbesserung der Adhärenz Fimbrien. Außerdem finden sich unterschiedliche Exotoxine und Enzyme.
Krankheitsbilder: Bacteroides fragilis als wichtigster Erreger und Bacteroides thetaiotaomicron finden sich häufig in aerob-anaeroben Mischinfektionen, so z.B. bei Peritonitis, gynäkologischen Infektionen (z.B. Adnexitis), intraabdominellen Abszessen nach abdominalchirurgischen Eingriffen, Aspirationspneumonien, Sinusitiden und Hirnabszessen sowie bei Patienten mit konsumierenden Grunderkrankungen.
Vorkommen und Übertragung: Bacteroides fragilis gehört nicht zu den typischen Umweltkeimen. Er gehört vielmehr zur normalen Bakterien-Flora des Menschen. Die Besiedelung des Menschen durch Bacteroides sp. findet meist während der ersten Lebensjahre statt. Infektionen sind daher meist endogen, d.h. von der physiologischen Flora des eigenen Körpers ausgehend.
Pathogenese: Als Bestandteil der physiologischen Flora ist B. fragilis nur gering pathogen. Infektionen entstehen durch Keimverschleppung in eigentlich sterile Körperbereiche. Häufig erfolgt zunächst eine Infektion durch aerobe bzw. fakultativ anaerobe Bakterien. Diese senken den Sauerstoff-Partialdruck im infizieren Gewebe und schaffen Anaerobiern wie Bacteroides sp. ein optimales Mileu. Isolate aus Infektionsherden bilden meist eine Kapsel, die sich jedoch nach mehreren Subkultur-Schritten häufig nicht mehr findet.
Epidemiologie: Etwa 5-10 % der Sepsis-Fälle, die durch Gram-negative Stäbchen hervorgerufen werden, gehen auf Infektionen durch Bacteroides sp. zurück. B. fragilis ist dabei der häufigste isolierte Keim der Bacteroides.
Diagnostik:
- Anzucht: B. fragilis lässt sich unter strikt anaeroben Bedingungen auf Spezialnährböden anzüchten. Bakterien der Bacteroides-fraglilis-Gruppe bilden meist nach zwei Tagen 1–3 mm große, grau-glänzende Kolonien. Zur Differenzierung der Bacteroides-fragilis-Gruppe sind biochemische bzw. gaschromatographische Untersuchungen notwendig.
- Mikroskopie: Die Gram-Färbung und die Färbung mit gruppenspezifischen Fluoreszenz-markierten Antikörpern kann die Diagnose sichern.
Therapie: Nekrosen und Abszesse müssen chirurgisch saniert werden, da Antibiotika meist nicht in ausreichender Menge in das Infektionsgebiet vordringen. Gegen Aminoglykoside sind Bacteroides primär resistent, sekundär auch gegen β-Laktamase-sensible Penicilline und Cephalosporine. Zum Einsatz kommen daher v.a. Nitroimidazole (Metronidazol), Aminopenicilline plus BLI, Piperazillin/Tazobactam und Carbapeneme (Imipenem). Die entsprechenden Antibiotika kommen meist schon bei Verdacht zum Einsatz, da die bakteriologische Diagnostik zu lange dauert. Bei Operationen im Darmtrakt wird häufig eine Chemoprophylaxe durchgeführt, um eine Infektion durch Anaerobier zu verhindern.
Historie: Veillon und Zuber beschrieben 1898 Bacteroides fragilis (damals noch Bacillus fragilis) erstmals als Erreger einer Appendizitis.
Porphyromonas spp.
[Bearbeiten]Morphologie und Eigenschaften: P. asaccharolytica, P. endodontalis, P. gingivalis und P. salivosa sind Gram-negative, obligat anaerobe Bewohner der normalen Mund-, Darm- und Urogenitalflora.
Krankheitsbilder: Porphyromonaskann unter opportunen Bedingungen eitrige Entzündungen und Abszesse auslösen, z.B. Entzündungen im Oropharyngeal-, Peridontal- und Urogenitalbereich. Weiterhin kann das Bakterium an aerob-anaeroben Mischinfektionen teilhaben, wie intraabdominelle Abszesse, Hirnabszesse, Lungenabszesse und Empyem und er kann bei Haut- und Weichteilinfektionen sowie Infektionen beim diabetischen Fuß eine pathogene Rolle spielen.
Diagnostik: Kultur unter anaeroben Bedingungen auf herkömmlichen Nährmedien.
Therapie: Clindamycin oder Metronidazol sind die 1. Wahl. Weiterhin können Penicilline (Penicillin G, Amoxicillin, Piperacillin/Tazobactam), Carbapeneme und Chloramphenicol eingesetzt werden.
Prevotella spp.
[Bearbeiten]Morphologie und Eigenschaften: Die zahlreichen Spezies der Gattung Prevotella sind Gram-negative, anaerobe Mikroorganismen der physiologischen Mund-, Darm-, und Urogenitalflora
Arten (Auswahl): P. bivia, P. buccae, P. buccalis, P. corporis, P. denticola, P. disiens, P. gingivalis, P. heparinolytica, P. intermedia, P. loescheii, P. melaninogines, P. nigrescens, P. oralis, P. oulorum, P. pallens
Krankheitsbilder: Die Krankheitsbilder entsprechen denen von Porphyromonas: Eitrige Entzündungen und Abszesse im Oropharyngeal-, Peridontal- und Urogenitalbereich (P. disiens, P. bivia). Aerob-anaerobe Mischinfektionen (intraabdominelle, Hirn-, Lungenabszesse und Empyem), Haut- und Weichteilinfektionen, Wundinfektionen.
Diagnostik: Kultur unter anaeroben Bedingungen auf herkömmlichen Nährmedien.
Therapie: Clindamycin oder Metronidazol. Ferner eignen sich Aminopenicilline, Cefoxitin, Chloramphenicol und Carbapeneme
Fusobakterien
[Bearbeiten]Morphologie und Eigenschaften: Fusobacterium spp. sind obligat anaerobe, Gram-negative, spindelförmige und unbewegliche Stäbchen. Sie sind meist Teil der normalen Mund- und Darmflora.
Arten (Auswahl): F. alocis, F. mortiferum, F. necrophorum, F. nucleatum, F. periodonticum, F. sulci, F. ulcerans, F. varium
Krankheitsbilder: Einige Fusobakterien können eitrige und gangränöse Infektionen hervorrufen. Zu den Krankheitsbildern gehören die Angina Plaut-Vincent (F. nucleatum in Symbiose mit Treponema vincentii), Abszesse - oft als Mischinfektion - in verschiedenen Körperregionen (orofazial, cervical, Atemwege, Abdomen, weibliches Genitale), Infektionen von chirurgischen und Bisswunden, Weichteilinfektionen, Endokarditis und die Postangina-Sepsis (Peritonsillarabszess, Jugularvenenthrombose).
Diagnostik: Kultur unter anaeroben Bedingungen auf herkömmlichen Nährmedien.
Therapie: Penicillin G und Ampicillin sind die 1. Wahl. Alternativen sind Clindamycin und Metronidazol.
Aerobe Stäbchen mit oxidativem Glucosestoffwechsel
[Bearbeiten]Pseudomonas aeruginosa
[Bearbeiten]| Pseudomonas aeruginosa | ||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
 | ||||||||||||||||
| Systematik | ||||||||||||||||
|
|

Morphologie und Eigenschaften: Pseudomonas aeruginosa (lat. aerugo Grünspan) ist ein gramnegatives, aerobes und Oxidase-positives Stäbchenbakterium. Es ist lophotrich begeißelt (büschelige Flagellen an beiden Polen) und besitzt zusätzlich Haftfimbrien. P. aeruginosa ist nicht zur Gärung befähigt (Nonfermenter), und kann daher nur aerob existieren. In verschiedenen Nährmedien setzt er Farbstoffe wie Fluorescein/Pyoverdin (gelbgrün), Pyozyanin (blaugrün), Pyorubin und Pyomelanin frei. Die oft unregelmäßig begrenzten Kolonien sind metallisch-grün glänzend und zeigen β-Hämolyse. Charakteristisch ist ein süßlicher Geruch nach Lindenblüten oder Weintrauben (Aminoacetophenon).
Vorkommen: P. aeruginosa ist ein ernährungstechnisch anspruchsloser, ubiquitär vorkommender Boden- und Wasserkeim und kann aus Pflanzen, Früchten, Lebensmitteln und dem Darmtrakt von Mensch und Tier isoliert werden. Als bedeutender Erreger nosokomialer Infektionen und Feuchtkeim findet er sich besonders in Leitungswasser, Bädern, Waschbecken, Spülmaschinen und sogar (unterdosierten) Desinfektionslösungen.
Übertragung: meist aus der Umwelt (Naßzonen), seltener von Mensch zu Mensch
Pathogenitäts- und Virulenzfaktoren:
- Haftfimbrien
- Biofilm-Bildung
- Neuraminidase
- Lipopolysaccharide (LPS) -> interagieren mit CFTR
- Exotoxin A (ToxA), eine ADP-Ribosyltransferase, die den Elongationsfaktor EF2 inaktiviert (ähnlich dem Diphtherietoxin)
- Exoenzym S (ExoS), welches Zytoskelett- und G-Proteine hemmt
- Zytotoxin, welches transmembrane Poren erzeugt
- Metalloproteinasen, die Interzellularbestandteile wie Elastin, Kollagen und Laminin hydrolysieren
- Zwei Phospholipasen C mit Membranaktivität

Gramfärbung von
P. aeruginosa - Multiple Antibiotikaresistenzen (ß-Laktamasen, Effluxmechanismen, mutiertes Carbapenem-Transportprotein u.a.)
Krankheitsbilder: Typisch sind opportunistische Infektionen wie Pneumonien (bei Cystischer Fibrose, Beatmung, Hitzetrauma), Wundinfektionen (bes. bei Verbrennungen, postoperativ), chronische Pyelonephritiden, Endokarditis (bei i.v.-Drogenabusus), nosokomiale Sepsis, Katheter-assoziierte Infektionen (z.B. Harnwegsinfektionen bei Blasenkatheter), ulzerierende Keratitis (Kontaktlinsen), Osteomyelitis, Dermatitis/Follikulitis, die maligne Otitis externa u.a.m.
Therapie: häufig Multiresistenzen!
- ß-Lactam-Antibiotika (Azlocillin, Piperacillin plus BLI) plus evtl. ein Aminoglykosid (Tobramycin)
- Cephalosporine parenteral 3b (z.B. Ceftazidim, Cefepim)
- Ciprofloxazin bei Harnwegsinfektion
- alternativ Carbapeneme
Acinetobacter sp.
[Bearbeiten]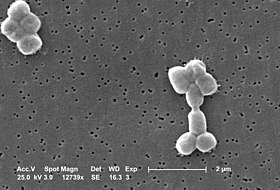
| Acinetobacter sp. | |||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Systematik | |||||||||||||||||
|
Morphologie und Eigenschaften: Acinetobacter sind Gram-negative, chemoorganotroph lebende und damit aerobe, Oxidase-negative Stäbchenbakterien.
Vorkommen: Acinetobacter spp. sind häufige Boden- und Wasserbewohner.
Krankheitsbilder: Nosokomiale Infektionen wie Wundinfektionen, Atemwegsinfekte, sekundäre Meningitis (Meningitis nach Schädelhirntrauma, neurochirurgischen Eingriffen) und Sepsis. Häufigster Vertreter der etwa 20 bekannten Spezies ist A. baumannii, daneben werden auch A. lwoffi, A. junii, A. haemolyticus und A. johnsnii nachgewiesen.
Therapie: Oft Multiresistenzen durch Bildung von β-Lactamasen und Aminoglykosid-modifizierenden Enzymen. Am besten scheinen noch Carbapeneme zu wirken.
Aerobe Stäbchen mit fermentativem Glucosestoffwechsel
[Bearbeiten]Vibrio cholerae
[Bearbeiten]| Vibrio cholerae | ||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
 | ||||||||||||||||
| Systematik | ||||||||||||||||
|
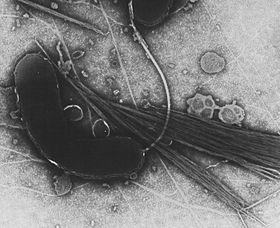
Vibrio cholerae ist der Verursacher der Cholera (griech.: Gallenbrechdurchfall).
Morphologie und Eigenschaften: Das Gram-negative, gekrümmte, kommaförmige und hochbewegliche Bakterium Vibrio cholerae gehört zur Gattung der Vibrionen und umfasst 70 Stämme. Es ist fakultativ anaerob, Oxidase-positive und gehört zu den Fermentern.
Epidemiologie: Die klassische Cholera wurde durch den Biovar O1/Biovar cholerae verursacht, heute herrscht vor allem der resistentere Biovar O1/Biovar eltor vor. 1998 gab es weltweit 300.000 Cholera-Fälle mit 11.000 Toten und Schwerpunkt in Afrika. Cholera tritt häufig in Entwicklungsländern auf, in denen Trinkwasser- und Abwassersystem nicht voneinander getrennt sind. In den Industrieländern ist meist eine ausreichende und hygienisch einwandfreie Versorgung der Bevölkerung gewährleistet, so dass Cholerafälle selten sind. Der letzte größere Choleraausbruch in Deutschland war in Hamburg im Jahr 1892. Die Krankheit kann epidemisch auftreten und ist in Deutschland meldepflichtig und eine Quarantäneerkrankung der WHO.
Pathogenitäts- und Virulenzfaktoren: Das phagenkodierte Choleratoxin ist aus zwei A- und fünf B-Proteinuntereinheiten aufgebaut. Der A1-Teil des Toxins ADP-ribosyliert die α-Untereinheit stimulatorischer Gs-Proteine und inaktiviert dadurch die GTPase-Aktivität, die für das Abschalten des G-Proteins (Umsetzung von GTP zu GDP) verantwortlich ist. Es kommt zu einem Überschuss des Second Messengers cAMP durch Daueraktivierung der Adenylatcyclase. Die erhöhte Produktion von Proteinkinase A führt zum gesteigerten Einbau von sekretorischen Ionenkanälen in die Darmmukosa, was den massiven Elektrolyt- und sekundären Wasserverlust erklärt.
- Die Pathogenität und Virulenz wird hervorgerufen durch die Integration von zwei Bakteriophagen in das Genom des Bakteriums. Namentlich sind dies VPIΦ (Vibrio Pathogenicity Island) und CTXΦ (Choleratoxin). Der Prozess der Infektion des Bakteriums durch die Bakteriophagen vollzieht sich in zwei Stufen: Zuerst ist nur die DNA von VPIΦ im Genom enthalten. Diese Gene kodieren für den TCP-Faktor (Toxin Coregulated Pili). Dadurch bildet das Bakterium spezielle Pili aus, mit denen es sich an der Oberfläche der Mikrovilli der Darmzellen festhaften kann. Diese Pili bilden nun auch die Rezeptoren für den Phagen CTXΦ. Nachdem dieser in die Bakterienzelle gelangt ist, integriert er sich ebenfalls in das Chromosom (lysogener Phage). Dadurch kann der ACF (Accessory Colony Factor) gebildet werden, und es kommt zur Ausschüttung von Choleratoxin A und B. Da beide Phagen die Zelle jedoch nicht lysieren sondern aktiv aus der Zelle austreten und nur noch schlecht aktiviert werden können verbleibt CTXΦ gemeinsam mit VPIΦ in der Zelle und vermehrt sich mit. VPIΦ selbst ist aufgrund einer Mutation nicht mehr infektionsfähig für andere Bakterien.
 |
 |
Krankheitsbild: Die Cholera ist eine schwere, bakterielle Infektionskrankheit, die vorwiegend den Dünndarm befällt. Sie kann extremen Durchfall und starkes Erbrechen verursachen, was zu einer schnellen Exsikkose mit Elektrolytverlust führen kann. Obwohl die meisten Infektionen asymptomatisch verlaufen (ca. 85 %), beträgt die Letalität bei Ausbruch der Krankheit unbehandelt zwischen 20 und 70 %. Klinisch verläuft die Cholera nach einer Inkubationszeit von 2-3 Tagen meist in drei Stadien:
- Stadium mit Brechdurchfall mit häufig dünnflüssigem Stuhl, oft mit Schleimflocken durchsetzt ("Reiswasserstuhl") und selten Bauchschmerzen.
- Stadium des Flüssigkeitsmangels (Exsikkose). Dabei kommt es zu Untertemperatur und zu einem auffälligen Gesichtsausdruck mit spitzer Nase, eingefallenen Wangen und stehenden Hautfalten.
- Stadium der allgemeinen Körperreaktion mit Fieber, Benommenheit, Verwirrtheit, Koma und Ekzem. Komplikationen wie zum Beispiel eine Lungenentzündung, eine Parotitis und eine Sepsis können hinzukommen. Menschen mit der Blutgruppe 0 sind gefährdeter.
Diagnostik:
- Die Diagnose erfolgt anhand der typischen Beschwerden, die bei einer Person in einem Gebiet mit bekannter Choleragefahr auftreten und
- Anhand des bakteriologischen Erregernachweises im Stuhl oder in Erbrochenem. Die Anzucht geschieht in sog. Peptonwasser bei pH 9.
Infektionsweg: Cholera wird in der Regel durch Trinkwasser verursacht, welches mit Choleraerregern verunreinigt ist. Choleraerreger finden sich vor allem in Fäkalien, sowie in Fluss- und Meerwasser, welches mit Fäkalien belastet ist. Außerdem können Fische und andere Nahrungsmittel aus Flüssen und dem Meer mit Choleraerregern verunreinigt sein.
Geschichte: Der Erreger wurde erstmals von Filippo Pacini 1854 als gekrümmtes, kommaförmiges und hochbewegliches Bakterium beschrieben. Robert Koch hat 1883 zusammen mit Fischer und Georg Theodor August Gaffky (1850-1918) in Ägypten den Erreger aus dem Darm von verstorbenen Patienten in Reinkultur angezüchtet.
Die Cholera wurde seit etwa 600 v. Chr. im Gangestal in Indien beobachtet. Um 1831 gelangt die Krankheit erstmals nach Europa. Um 1892 grassiert die Cholera in Afghanistan und gelangt nach Russland. Robert Koch, der als Entdecker des Cholera-Erregers gilt, vermutete, dass russische Amerika-Auswanderer sie mit nach Hamburg gebracht haben. Es gibt jedoch starke Zweifel an dieser Hypothese, da die ersten Cholerafälle unter den Hamburgern entdeckt wurden. Durch die fehlende Aufklärung der Bevölkerung und zu wenig Kläranlagen wurde der Ausbruch des Erregers stark begünstigt. Allein in Hamburg starben mehr als 8600 Personen.
Die letzte größere Choleraepidemie brach 1991 in Peru aus und breitete sich auch nach Ecuador, Kolumbien, Mexiko und Nicaragua aus. Am 9. Februar rief die peruanische Regierung den nationalen Notstand aus. Von den rund 400.000 damals in Südamerika Erkrankten starben schätzungsweise 12.000.
Therapie: Ausgleich von Volumen- und Elektrolytverlust bevorzugt i.v. ist die wichtigste Massnahme. Ein Antibiotikum vom Fluorchinolon-Typ, z.B. Ciprofloxacin reduziert die Krankheitsdauer und Erregerausscheidung. Auch auf Chinolone und Cotrimoxazol spricht der Erreger an. Mit diesen Maßnahmen kann die Sterblichkeitsrate von 60% auf unter 1% gesenkt werden.
Prophylaxe: Die beste Vorbeugung ist hygienisch einwandfreies Trinkwasser. Auch eine parenterale Impfung ist möglich, wird allerdings nicht allgemein empfohlen. Neuere Schluckimpfungen sind wirksamer und besser verträglich.
Weblinks: RKI - Cholera
Aeromonas sp.
[Bearbeiten]Enterobacteriaceae
[Bearbeiten]Enterobakterien sind Oxidase-negative, aerob oder fakultativ aerob lebende Mikroorganismen, die ihre Energie durch Fermentation (Gärung und/oder oxidative Fermentation) gewinnen.
Escherichia coli
[Bearbeiten]| Escherichia coli | ||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
 | ||||||||||||||||||
| Systematik | ||||||||||||||||||
|
Escherichia coli ist ein Gram-negatives, stäbchenförmiges und peritrich begeißeltes Bakterium, das im menschlichen und tierischen Darm vorkommt. Es gehört zur Familie der Enterobacteriaceae. Benannt wurde es 1919 nach seinem Entdecker Theodor Escherich. Es gehört zu den am besten untersuchten Organismen der Welt.
Morphologie und Eigenschaften: E. coli ist ein säurebildendes, Gram-negatives, stäbchenförmiges und peritrich begeißeltes Bakterium. Es ist fakultativ anaerob und kann Energie sowohl durch Atmung als auch durch gemischte Säuregärung gewinnen. Das Bakterium dient als Fäkalindikator in der Trinkwasser- und Lebensmittelhygiene. E. coli stimuliert im Colon die IgA-Sekretion und produziert Vitamin K. Die Teilungsrate ist mit einer Generationszeit von 20min relativ hoch. Auf Blutagar wachsen weissliche Kolonien ohne Hämolyse, auf MacConkey-Agar himbeerote, typischerweise eingedellte Kolonien.
Pathogenität: E. coli bildet einen Großteil der normalen Darmflora und verhindert durch seine Anwesenheit die Ansiedelung von pathogeneren Keimen. Als fakultativ pathogener und oft an nosokomialen Infektionen beteiligter Krankheitserreger verursacht er 70-80 % der akuten und 40-50 % der chronischen Harnwegsinfekte, weiterhin Peritonitis (nach Operationen im Bauchraum), Wundinfektionen, Meningitis bei Neugeborenen (Infektion unter der Geburt), Sepsis und andere Krankheitsbilder.
Pathogenitäts- und Virulenzfaktoren: Zum Anheften an bestimmte Zellen der Harnwege besitzen die Bakterien so genannte P-Fimbrien oder PAP (pyelonephritis assoziated pili). Weiterhin kommen Fimbrien und Hämolysine vor. Das Kapselantigen K1 von bestimmten Kapsel tragenden E. coli ist an der Neugeborenenmeningitis beteiligt (s.u.).
Obligat pathogene E-coli-Stämme:
- Einige Stämme von E. coli sind für den Menschen obligat darmpathogen. Hier unterscheidet man einige Subtypen mit unterschiedlichen Pathogenitätsfaktoren:
- EHEC - Enterohämorrhagische E. coli
- ETEC - Enterotoxische E. coli
- EPEC - Enteropathogene E. coli
- EIEC - Enteroinvasive E. coli
- EAEC - Enteroaggregative E. coli
- DAEC - Diffus adhärente E. coli


- Pathogenese bei pathogenen E. coli-Stämmen:
- Darminfektionen wurden vornehmlich unter dem Namen EHEC-Colitis (Enterohämorrhagische Colitis) bekannt. EHEC-Infektionen zählen zu den häufigsten Lebensmittelvergiftungen und betreffen v.a. Säuglinge, Kleinkinder und Immunsupprimierte. Infektionsquellen sind Rinder, Rohmilch, infizierte Menschen oder Trinkwasser. Die Infektionsdosis liegt bei 20-100 Keimen. Das Bakterium enthält ein Toxin mit dem Namen „Verotoxin“, da es toxisch auf Verozellen wirkt, einer Zelllinie aus Affennierenzellen sowie die Shiga-like-toxins 1 und 2 (SLT-1, SLT-2). Bei einer Infektion droht ein Hämolytisch-urämisches Syndrom (HUS) mit dauerhaften Nierenschäden durch thrombosierende Nierenkapillaren. Weitere Komplikationen sind eine thrombotisch- thrombozytopenische Purpura (TPP), neurologische Ausfälle, chronische Pankreatitis, Glucose-Intoleranz, Diabetes mellitus und Dickdarmstrikturen. Antibiotika sollten bei EHEC nicht eingesetzt werden, um nicht zusätzlich Toxine durch Bakterienzerfall freizusetzen.
- Der Stamm ETEC ist ein häufiger Erreger der Reisediarrhoe (Montezumas Rache). Grund für diese Erkrankung ist ein hitzelabiles Enterotoxin vom A/B Typ (LT I und LT II). Das 73 kDa große Protein besitzt zwei Domänen, von denen eine an ein G-Gangliosid der Zielzelle bindet (Bindende Domäne). Die andere Domäne ist die Aktive Komponente, die ähnlich dem Choleratoxin die Adenylatcyclase und die Guanylatcyclase aktiviert. Ergebnis ist eine toxinvermittelte, sekretorische Diarrhoe. Die genetische Information erhält das Bakterium von einem lysogenen Phagen durch Transduktion. Weiterhin enthält der ETEC-Stamm noch ein hitzestabiles Toxin (ST), dessen Funktion allerdings noch nicht vollständig bekannt ist.
- Bei Säuglingen löst der Stamm EPEC Durchfall (Mikrovilli-Zerstörung) aus und führt zu Gedeihstörungen.
- Auch EIEC zerstören die Darmschleimhautzelle, indem sie in sie eindringen und das Krankheitsbild der bakteriellen Ruhr imitieren.
- Diagnostik: Erregernachweis: Anzucht auf Selektivnährböden (McConkey-Sorbitol), Toxinnachweis (SLT) mittels ELISA, Gruber-Agglutination
- Therapie: Ausgleich von Wasser- und Elektrolytverlust. Evtl. Antibiotika (Ampicillin plus BLI, parenterale Cephalosporine 2, 3a oder 3b, alternativ Gyrasehemmer oder Cotrimoxazol) in schweren Fällen, bei EHEC-Stämmen sind Antibiotika allerdings kontraindiziert (Gefahr der Niereninsuffizienz)! Der Infektionsnachweis ist meldepflichtig!
- Prophylaxe: Seit Ende 2004 gibt es in Deutschland einen zugelassenen Impfstoff (Dukoral). Dieser imitiert die B-Untereinheit des hitzelabilen ETEC-LT (s.o.) und gleichzeitig die sehr ähnliche B-Untereinheit des Cholera-Toxins. Auf diesem Wege bildet der Körper eine Immunantwort gegen beide Toxine aus (Kreuzreaktivität).
E. coli in der Forschung: Aus E. coli gelang Jonathan Beckwith 1969 als erstem die Isolierung eines einzelnen Gens. Das relativ kleine Genom dieses Prokaryoten (ca. 4,65 ·106 Basenpaare, entspricht etwa 5000 Genen) wurde als eines der ersten vollständig sequenziert.
E. coli ist die in der Molekularbiologie am meisten verwendete Bakterienart. Das komplette Genom ist mittlerweile entschlüsselt worden und viele Einzelstämme wurden isoliert. In der modernen Biotechnologie wird das Bakterium zur industriellen Biosynthese von Insulin, unterschiedlicher Aminosäuren und anderer Verbindungen eingesetzt. Gerade hierfür ist E. coli prädestiniert, da es zur residenten Darmflora gehört und daher beim Menschen keine Allergien verursacht (gegenseitige Anpassung).
Seit 1988 führte Richard Lenski ein Langzeitexperiment über die Evolution von E. coli durch.
Weblinks: RKI - EHEC-Infektionen, RKI - Hämolytisch Urämisches Syndrom (HUS)
Shigellen
[Bearbeiten]| Shigella sp. | ||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Systematik | ||||||||||||||||||
|
Etymologie: Benannt wurden Shigellen nach dem japanischen Bakteriologen Kiyoshi Shiga, dem Entdecker des Erregers der Bakterienruhr.
Morphologie und Eigenschaften: Shigellen sind Gram-negative Stäbchenbakterien der Familie Enterobacteriaceae und leiten sich von E. coli ab (E. coli plus ein 200kB-Virulenzplasmid). Die Bakterien sind unbeweglich (im Ggs. zu E. coli) und fakultativ anaerob. Die Kultur gelingt aus möglichst frischem Stuhl auf Normal- und Selektivnährböden. Die Identifizierung erfolgt biochemisch und mittels Objektträgeragglutination mit Gruppenseren.
Virulenzfaktoren:
- Endotoxine
- Shigella dysenteriae produziert das so genannte Shiga-Toxin, ein Zytotoxin, welches zu einer schwerer wiegenden Vergiftung führt als bei Infektionen mit anderen Shigella-Gruppen und synergistisch mit Endotoxinen z.B. ein Hämolytisch-urämisches Syndrom (HUS) verursachen kann (Vgl. E. coli).
Krankheitsbilder: Alle 4 bekannten Shigella-Artengruppen sind medizinisch relevant als Erreger der Shigellosen, besser bekannt als Bakterienruhr (ruora (altdeutsch): heftige Bewegung), und wurden bislang nur beim Menschen und Primaten nachgewiesen. Die Krankheitssymptome (hauptsächlich Fieber, blutig-eitrige Diarrhoe, postinfektiöse Arthritis) stellen eine Reaktion auf die Einwanderung der Bakterien in das Darmgewebe dar.

Shigella-Artengruppen:
- Gruppe A, Shigella dysenteriae: Die Shiga-Toxin-produzierenden Bakterien der Gruppe A sind hauptsächlich in den Tropen und Subtropen verbreitet. Besonders schwer sind Infektionen mit dem Serotyp A (auch Shiga-Kruse-Bakterium), da diese Bakterien neben den normalen Giften auch ein Nervengift bilden.
- Gruppe B, Shigella flexneri: Infektionen dieser Gruppe verlaufen in der Regel weniger schwer als die der Gruppe A, die Bakterien sind weltweit verbreitet.
- Gruppe C, Shigella boydii: Boyd-Bakterien finden sich vor allem in Vorderindien und Nordafrika, Infektionen mit ihnen sind selten und meist harmlos.
- Gruppe D, Shigella sonnei: Diese auch als Kruse-Sonne-Bakterien bekannten Arten stellen vor allem in Mitteleuropa die häufigsten Shigellen dar und verursachen besonders bei Kindern den harmlosen Sommerdurchfall.
Epidemiologie und Übertragung: Weltweit werden jährlich ca. 160 Mio. Menschen infiziert, von denen ca. 1 Mio. sterben. Dabei handelt es sich meist um Kinder, ältere und immungeschwächte Patienten. In Deutschland sind nur S. flexneri und S. sonnei endemisch. Pro Jahr werden über 1.000 Fälle gemeldet, von denen allerdings 70 % importiert sind, darunter praktisch alle Fälle von S. dysenteriae und S. boydii. Die Infektionsdosis ist mit 10-200 Keimen sehr gering. Verbreitet werden Shigellen fäkal-oral, teilweise auch durch Fliegen.
Therapie: Nach Schweregrad symptomatisch oder antibiotisch nach Antibiogramm. Gutes Ansprechen meist auf Ampicillin, Cotrimoxazol und Ciprofloxacin (Cave: HUS!).
Weblinks: RKI - Shigellose
Klebsiellen
[Bearbeiten]| Klebsiellen | ||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
 | ||||||||||||||||||||
| Systematik | ||||||||||||||||||||
|
Etymologie: Klebsiellen wurden nach dem ostpreußischen Bakteriologen Edwin Klebs benannt, geboren 1834 in Königsberg und gestorben 1913 in Bern (Schweiz).
Morphologie und Eigenschaften: Klebsiellen sind Gram-negative, fakultativ anaerobe Stäbchenbakterien der Familie der Enterobacteriaceae. Die Bakterien sind unbeweglich und von einer Polysaccharidkapsel umgeben, die auch für die typischen schleimigen Kolonien verantwortlich ist. Auf MacConkey-Agar wachsen rosa, auf Blutagar weißlich, glänzende Kolonien.
Von den 4 Klebsiella-Arten ist nur Klebsiella pneumoniae als Bewohner des Magen-Darm-Traktes und opportunistischer Krankheitserreger medizinisch relevant. Andere Klebsiella-Arten leben im Boden, im Wasser und auf Getreide. Alle Arten sind unempfindlich gegen Penicillin.
Klebsiella pneumoniae


Klebsiella pneumoniae ist auch bekannt als Friedländer-Bakterium und gehört zur normalen Darmflora des Menschen. Im Normalfall ist das Bakterium ungefährlich, bei Immunschwäche kann es jedoch als Krankheitserreger auftreten und nosokomiale Infektionen wie Harnwegsinfektionen, Wundinfektionen und die Friedländer-Pneumonie verursachen. Das Bakterium gilt im Krankenhaus als Problemkeim und kann auf Neugeborenen- und onkologischen Stationen zu kleinen Epidemien führen.
Pathogenitäts- und Virulenzfaktoren:
- Polysaccharidkapsel -> Phagozytoseschutz
- Zunehmende Multiresistenzen durch Breitspektrum-β-Lactamasen (ESBL-Stämme) seit Anfang der 80iger.
Therapie: Nach Antibiogramm, wirksam sind oft Cephalosporine parenteral 3a/b (ggf. plus Aminoglycosid), Monobactame, Cotrimoxazol und Gyrasehemmer.
Proteus mirabilis
[Bearbeiten]| Proteus mirabilis | ||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Systematik | ||||||||||||||||
|
Morphologie und Eigenschaften: Proteus mirabilis sind Gram-negative, fakultativ anaerobe, nicht sporenbildende, peritrich begeißelte und damit sich lebhaft bewegende stäbchenförmige Bakterien. Sie bilden das Enzym Urease, das Harnstoff spalten kann. Dabei entsteht Ammoniak, der den pH-Wert des Mediums, zum Beispiel von Urin erhöht und dem Bakterium damit bessere Wachstumsbedingungen gewährt (ein niedriger pH-Wert wird von den meisten Bakterien schlecht toleriert). Lactose kann es nicht verstoffwechseln. Die Bakterien können problemlos auf gängigen Kulturmedien kultiviert werden. Sie bilden dabei auf Gelmedien oft nicht umschriebene Kolonien wie die meisten anderen Bakterien, sondern können sich flächig auf dem Medium ausbreiten („Schwärm-Phänomen“). Die Identifizierung erfolgt biochemisch. P. mirabilis ist in der Regel ein harmloser Saprophyt (Destruent organischer Stoffe). Die Bakterien sind in ihrer Länge sehr unterschiedlich, dies führte zur Benennung nach dem alten griechischen Meeresgott Proteus, der sich durch große Wandlungsfähigkeit auszeichnete. Das Genom von P. mirabilis wird momentan vom Sanger Institute (Cambridge, Großbritannien) entschlüsselt.


- Das Schwärm-Phänomen (syn. Schwärmen) findet man typischerweise beim Wachstum von Proteus-Bakterien-Stämmen auf festen Nährböden. Anders als bei anderen Bakterien bilden sich hier kaum Kolonien. Stattdessen findet sich auf der Agar-Platte ein feiner Bakterien-Rasen mit konzentrischen Ringen. Das Schwärmen beruht auf der Fähigkeit von bestimmten Proteus-Stämmen bei eingeschränkter Beweglichkeit der Geißel auf Grund einer hohen Bakterien-Dichte sich zu einem Synzytium mit mehreren Kernäquivalenten zu fusionieren (sog. Schwärmer-Form). Dieses Synzytium besitzt eine etwa um den Faktor 500 höhere Geißelexpression und ist damit enorm beweglich. Das Schwärmen läßt sich durch Kultur auf Cysteine-Lactose-Electrolyte-Deficient-Agar (CLED-Agar) unterdrücken.
Krankheitsbilder: P. mirabilis ist ein fakultativ pathogener (opportunistischer) Krankheitserreger, der auch bei Gesunden häufig im Dickdarm vorkommt. Bei Immungeschwächten kann P. mirabilis Harnwegsinfektionen, Wundinfektionen, Sepsis und Pneumonie verursachen.
Bei chronischen Harnwegsinfektionen durch Proteus mirabilis kann durch die Erhöhung des Urin-pH-Wertes (Urease) die Entstehung von Harnsteinen begünstigt werden.
Epidemiologie: P. mirabilis ist ein seltener Krankheitserreger. Harnwegsinfekte werden in ca. 5-10 % der Fälle durch dieses Bakterium verursacht. Bei Pneumonie und Sepsis bewegt sich der Anteil um 2 %. Diese Zahlen gelten für ambulant erworbene Infektionen, bei nosokomialen Infektionen liegt die Rate tendenziell etwas höher. Die Übertragung erfolgt hauptsächlich über die Hände und kontaminierte Instrumente.
Diagnostik: Die Diagnosestellung erfolgt durch Kultivierung des Erregers aus Blut- und Urinkulturen, Bronchialsekret oder Bronchoalveolärer Lavage. Nach Anlegen einer Reinkultur kann die Spezies am einfachsten mit biochemischen Methoden („Bunte Reihe“) bestimmt werden.
Therapie: Die Behandlung einer Infektion durch P. mirabilis sollte, wann immer möglich, nach Resistenzprüfung (Antibiogramm) durchgeführt werden. Die anfängliche kalkulierte Therapie kann z.B. mit Amoxicillin plus BLI, einem parenteralen Cephalosporin der 3. Generation, Cotrimoxazol oder mit einem Fluorchinolon erfolgen. Carbapene und Monobactame sind ebenfalls Alternativen.
Problematisch für die Therapie ist insbesondere die Fähigkeit des Bakteriums, extended-spectrum-β-Lactamasen (ESBL) zu produzieren. Damit können die Bakterien Antibiotika vom β-Lactam-Typ (z.B. Penicilline, Cephalosporine) unwirksam machen.
Geschichte: Proteus mirabilis wurde 1885 von dem Erlanger Pathologen Gustav Hauser entdeckt.
Enterobacter sp.
[Bearbeiten]| Enterobacter sp. | ||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Systematik | ||||||||||||||||
|
Enterobacter sp. sind Gramn-negative, begeißelte Stäbchenbakterien und kommen in fast allen Lebensräumen einschließlich des menschlichen Darmes vor, wo sie zur normalen Darmflora gehören.
Insgesamt existieren 5 Arten, von denen Enterobacter aerogenes und Enterobacter cloacae selten als Erreger von Harnwegsinfekten, Meningitis oder Atemwegsinfekten auftreten.
Therapie: Carbapeneme sind die Antibiotika der 1. Wahl. Weiterhin können Piperacillin plus BLI, parenterale Cephalosporine der 3. Generation, Monobactame, Aminoglykoside und Flourchinolone angewendet werden.
Citrobacter sp.
[Bearbeiten]
| Citrobacter sp. | ||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Systematik | ||||||||||||||||||||
|
Morphologie und Eigenschaften: Citrobacter sp. sind Gram-negative Stäbchenbakterien der Familie Enterobacteriaceae. Die drei Citrobacter-Arten C. freundii, C. koseri und C. amalonaticus nutzen ausschließlich Citrat als Kohlenstoffquelle.
Vorkommen: Verbreitet sind die Citrobacter-Arten in beinahe allen Lebensräumen wie etwa dem Boden, im Wasser und in Abwässern. Außerdem kommen sie als Teil der Darmflora im Magen-Darm-Trakt des Menschen vor.
Krankheitsbilder : Citrobacter sp. spielen eine (geringe) Rolle als als Erreger opportunistischer Infektionen.
Therapie: Carbapeneme oder Chinolone (beide ggf. plus Aminoglykosid), Monobactame und Fosfomycin können für die initiale Therapie angewendet werden.
Serratia marcescens
[Bearbeiten]| Serratia marcescens | ||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
 | ||||||||||||||||
| Systematik | ||||||||||||||||
|
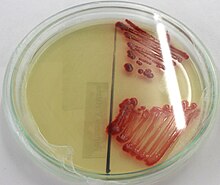
Morphologie und Eigenschaften: Serratia marcescens ist ein gramnegatives, fakultativ anaerobes, nicht sporenbildendes, sich aktiv mit peritrich angeordneten Geißeln bewegendes, stäbchenförmiges Bakterium. Es produziert die hydrolytischen Enzyme DNase, Gelatinase und Lipase. Die Bakterien können problemlos auf gängigen Medien kultiviert werden. Sie bilden in der Regel ein rotes Pigment (Prodigiosin, von lateinisch prodigium = Wunderzeichen, siehe unter Historisches), wodurch die Kolonien rot gefärbt sind. Das Genom von Serratia marcescens wurde vom Sanger Institute (Cambridge, Großbritannien) vollständig sequenziert. Es besteht aus einem einzigen in sich geschlossenen DNA-Strang und hat eine Länge von 5,1 MBp.
Vorkommen: S. marcescens kommt ubiquitär im Boden, Wasser, auf Tieren und Pflanzen vor und sind in der Regel harmlose Saprobionten (Destruenten organischer Stoffe).
Krankheitsbilder: Opportunistische Infektionen wie Harnwegsinfekte, Sepsis und Pneumonie.
Therapie: Serratia marcescens bildet oft extended-spectrum-β-Lactamasen (ESBL). Die kalkulierte Therapie kann mit einem parenteralen Cephalosporin der 3. Generation (z.B. Cefotaxim), einem Fluorchinolon (Ciprofloxacin) oder einem Carbapenem begonnen werden.
Historisches: Serratia marcescens wurde 1819 auf verdorbener Polenta von dem Pharmazeuten Bartalomeo Bizio aus Padua entdeckt.
Man schreibt diesem Bakterium das "Wunder von Bolsena" zu. Der Priester Peter von Prag soll nach Zweifeln am Dogma der Transsubstantiation 1263 in Bolsena das Brot für die Kommunion gebrochen und dabei Blutstropfen darauf entdeckt haben. Er soll seine Zweifel gestanden haben und eine Prozession mit Hostien nach Orvieto zu Papst Urban IV. veranstaltet haben. Dieser führte daraufhin das Fronleichnamsfest (Processione del Corpus Domini) ein und ließ den Dom zu Orvieto errichten. Heute nimmt man an, dass die "Blutstropfen" durch Prodigiosin rot gefärbte Kolonien von Serratia marcescens waren (siehe Bild 1), die auf Brot und Hostien einen guten Nährboden finden („Hostienphänomen“) und darauf wachsen, wenn diese Materialien nicht ausreichend trocken gehalten werden. Das Wunder von Bolsena ist auf einem Fresko des italienischen Malers Raffael in den Stanzen des Vatikans (Stanza d'Eliodoro) dargestellt (Die Messe von Bolsena).
Schon bei der Belagerung von Tyros 332 v. Chr. unter Alexander dem Großen sollen "Blutflecken" auf dem Brot der Soldaten aufgetreten sein, die Alexander als Glückszeichen deutete. Auch später kam das Phänomen der "blutenden Hostien" wiederholt vor, vermutlich bei Aufbewahrung von Hostien in Sakristeien, die im Sommer noch kühl sind und deren Luft deshalb eine hohe relative Luftfeuchtigkeit aufweist. Das Phänomen führte unter anderem in Wilsnack (Prignitz) 1383 zu Wallfahrten zum Wilsnacker Wunderblut mit zahlreichen Beteiligten, die etwa 170 Jahre andauerten.
„Blutende“ Hostien wurden auch oft zum Vorwand für Judenverfolgungen genommen. Man warf den Juden vor, sie hätten die Hostien gestochen und so zum Bluten gebracht. Herzog Wenzel von Luxemburg soll 1369 Juden vertrieben haben, weil in Brüssel "Blutflecken" auf Hostien aufgetreten waren.
1825 will man in Enkirch an der Mosel Blut in Mehl gefunden haben.
Der ursprüngliche Name des Bakteriums Bacterium prodigiosum und die Bezeichnung des von ihm gebildeten Farbstoffs Prodigiosin gehen auf den Zusammenhang mit diesen scheinbaren Wundern zurück: lateinisch prodigium "Wunderzeichen".
Salmonellen
[Bearbeiten]| Salmonellen | ||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
 | ||||||||||||||||||||
| Systematik | ||||||||||||||||||||
|

Morphologie und Eigenschaften: Salmonellen sind Gram-negative, 2-3 µm große, sporenlose und vorwiegend bewegliche, peritrich begeißelte, fakultativ anaerobe, kurze Stäbchen aus der Familie der Enterobacteriaceae. Sie sind eng verwandt mit der Gattung Escherichia. Auf Blutagar wachsen rosa, auf Leifson-Agar schwarze Kolonien.
Vorkommen: Salmonellen gehören (bis auf die an den Menschen adaptierten Typhus/Paratyphus-Serovare) zu den Zoonosen, die sowohl Tiere als auch über die Lebensmittelkette den Menschen infizieren und krank machen können. Die Erreger kommen weltweit vor.
- Salmonellen sind außerhalb des menschlichen bzw. tierischen Körpers wochenlang lebensfähig. In getrocknetem Kot sind sie über 2,5 Jahre lang nachweisbar. Durch Hitzeeinwirkung sterben Salmonellen bei 55°C nach 1 Stunde, bei 60°C nach einer halben Stunde ab. Um sich vor einer Salmonellen-Infektion zu schützen wird die Erhitzung des Lebensmittels auf 70°C im Kern für mindestens 10 min. empfohlen. Durch Einfrieren werden die Bakterien nicht abgetötet. In sauren Medien sterben die Bakterien rasch ab. Gebräuchliche Desinfektionsmittel töten die Salmonellen innerhalb weniger Minuten.
Infektionswege:
- Durch Unsauberkeit im Lebensmittelbereich, insbesondere in Großküchen
- Über Ausscheidungen erkrankter, aber auch klinisch gesund erscheinender Menschen und Tiere (gefährdet: andere Tiere, Pflegepersonal)
- Verunreinigtes Oberflächenwasser
- Durch unhygienisch und schlecht aufgetautes Geflügel (viele Bakterien befinden sich im Tauwasser)
- Durch Eier, die von salmonellenpositivem Geflügel stammen
Arten, Subspezies und Serovare - Überblick: Alle humanpathogenen Salmonellen gehören zur Subspezies S. enterica enterica Serovar, i.d.R. abgekürzt als S. Serovar. Man unterscheidet zwischen den Enteritis-Salmonellen und den Typhus/Paratyphus-Salmonellen, wobei letztere aufgrund spezieller Virulenzfaktoren und eines Kapselproteins (Virulenz-Antigen) schwerere Erkrankungen verursachen (z.B. Salmonella enterica enterica Typhi, kurz S. Typhi und S. Paratyphi). S. Typhi kommt beim Tier nicht vor und ist an den Menschen adaptiert.
Gastroenteritis-Salmonellen (z.B. S. enterica enterica Enteritidis, kurz S. Enteritidis, S. Typhimurium, S. Cholerasuis u.a.m) verursachen beim Menschen meist spontan ausheilende Durchfallerkrankungen, die in der Regel nicht antibiotisch behandelt werden müssen. Allerdings können bei Risikogruppen, wie Säuglingen, Kleinkindern, alten Menschen, HIV-Patienten und immungeschwächten Patienten schwere Erkrankungen (Allgemeininfektionen) hervorgerufen werden.
Epidemiologie: In Deutschland gehören Salmonellosen zu den meldepflichtigen Erkrankungen nach §6 bzw. §7 des Infektionsschutzgesetzes. Die amtlichen Meldungen sind seit 1990 von ca. 200.000 auf ca 58.000 Fälle in 2005 zurückgegangen. Fälle von Typhus und Paratyphus belaufen sich in Deutschland auf etwa 200-300 pro Jahr.
Historie und Nomenklatur:
- 1880 wurde der Erreger des Typhus abdominalis beim Menschen von Karl Joseph Eberth und Robert Koch entdeckt.
- 1884 gelang Georg Gaffky die Züchtung des Erregers in Reinkultur.
- 1885 fand Daniel Elmer Salmon, nach dem die Gattung Salmonella benannt wurde, die "Schweinecholera"-Bakterien.
Die Nomenklatur der Salmonella-Arten ist traditionell gewachsen. In der Fleischbeschau und Lebensmittelüberwachung werden Salmonellen auch als "Fleischvergifter" bezeichnet.
Die meisten „Salmonellenarten“ sind nach heutiger Kenntnis lediglich Serovare der Art Salmonella enterica. Es gibt nach dem Kaufmann-White-Schema insgesamt mehr als 2.500 Salmonellen-Serovare, die sich aufgrund des Vorkommens von unterschiedlichen O- und H-Antigenen unterscheiden. Die O-Antigene bestehen aus den Lipopolysacchariden (LPS) der Zellwand (O, da ohne hauchförmiges Wachstum in Kultur) und die H-Antigene aus den Proteinbausteinen der Flagellen (H für hauchförmiges Wachstum), mit denen sich die Salmonellen fortbewegen können. Zusätzlich verfügen einige Arten über ein Kapselantigen (K-Antigen) und Fimbrien bzw. Pili (F-Antigen).
Pathogenitäts- und Viruenzfaktoren:
- O-Antigen (= somatisches Antigen), lokalisiert in der Zellwand, Lipopolysaccharide, thermostabil, Formaldehydunbeständig -> Endotoxine
- H-Antigen (= Geißelantigen), thermolabil, Formaldehydbeständig ->Beweglichkeit
- K-Antigen (= Kapselantigen), besteht aus 3 Fraktionen mit unterschiedlicher Wärmeempfindlichkeit und wird der Zellwand zugerechnet -> Phagozytoseschutz
- F-Antigen (= Fimbrienantigen) -> Anheftung
Subspezies (früher: Subgenus I - VII)
- S. enterica enterica, vereint die Serovare mit Bedeutung für den Menschen und homoiotherme Tierarten (Enteritische und Typhus/Paratyphus-Gruppe)
- S. enterica salamae
- S. enterica arizonae
- S. enterica diarizonae
- S. enterica houtenae
- S. enterica indica
Epidemiologische Gruppen:
Einordnung der Serovare nach der Anpassung an bestimmte Wirte
- An den Menschen angepasste Serovare, die bei diesem Typhus oder Paratyphus verursachen (z.B. S. Typhi, S. Paratyphi A, B und C).
- An bestimmte Tierarten angepasste Serovare, die tierspezifische Erkrankungen hervorrufen und für andere Tierarten und den Menschen nicht von Bedeutung sind S. Dublin (Rind), S. Choleraesuis (Schwein), S. Abortusovis, S. Abortusequi (Schaf, Pferd).
- Serovare ohne spezielle Wirtsanpassung, die bei allen Tierspezies als Erreger von Enteritiden auftreten und beim Menschen Lebensmittelvergiftungen hervorrufen.
- Serovare ohne spezielle Wirtsanpassung, die bei Mensch und Tier als Erreger von Salmonellosen auftreten und eine hohe Virulenz besitzen.
Medizinisch bedeutsame Vertreter:
- S. Arizonae, bei Kaltblütern, Geflügel, Säugetieren
- S. Choleraesuis (Bacillus Paratyphus B und C), Darmkommensale des Schweines, pathogen bei Immunschwäche; Menschen können sich durch den Verzehr vom Fleisch erkrankter Schweine infizieren.
- S. Enteritidis, Vorkommen im Darm von Rindern, Nagern, Enten (auch deren Eiern) und Menschen; Erreger des Kälberparatyphus und akuter Gastroenteritis des Menschen.
- S. Paratyphi
- S. Paratyphi A, rein humanpathogen, Erreger des "Paratyphus A" (Paratyphöse Gastroenteritis), Übertragung durch Kontakt und infektiöse Lebensmittel oder Wasser.
- S. Paratyphi B, in Mitteleuropa meist humanpathogen, Erreger des "Paratyphus B", Übertragung durch Kontakt und infektiöse Lebensmittel, Wasser oder Fliegenkot.
- S. Typhi, Vorkommen in gemäßigten und subtropischen Zonen, humanpathogener Erreger des Typhus abdominalis, Übertragung durch Kontakt und infektiöse Lebensmittel, Wasser oder Fliegenkot. 3 - 5 % aller Erkrankten bleiben Dauerausscheider.
- S. Typhimurium, Erreger einer meist tödlich verlaufenden, fieberhaften Darminfektion bei Vögeln und Säugetieren, durch kontaminierte Lebensmittel. Auslöser der Salmonellenenteritis ("Lebensmittelvergiftung") des Menschen.
Diagnostik: Kultur aus Stuhl (Selektivmedien wie Leifson, XLD-Agar), Blut oder Gewebe. Differenzierung biochemisch, per Gruber-Agglutination (Antigen- bzw. Erregernachweis) oder Widal-Agglutination (serologischer Antikörper-Nachweis).
Salmonellose
Epidemiologie: Im Gegensatz zu S. Typhi und S. Paratyphi, deren einziger bislang bekannter Wirt der Mensch ist, sind die übrigen Salmonellen-Serotypen Zoonosen und sind in tierischen Produkten (Fleisch, Milch, Eiern, Muscheln, etc.) zu finden. Darüber hinaus können Salmonellen auch bei der Schlachtung und Verarbeitung durch mangelhafte Hygiene und durch Salmonellenausscheider im Personal auf Lebensmittel übertragen werden. Durch den Kot infizierter Tiere und Menschen verunreinigtes Trinkwasser ist demgegenüber in Ländern mit ungenügenden hygienischen Standards die wichtigste Infektionsquelle. Die Infektionsdosis für einen gesunden erwachsenen Menschen liegt bei 10.000 bis 1.000.000 Keimen. Bei Abwehrschwäche bzw. Säuglingen, Kleinkindern und alte Menschen wurden auch Erkrankungen bereits bei Infektionsdosen unter 100 Keimen beobachtet.
In den USA hat sich die Erkrankungsrate in den letzten 25 Jahren verdoppelt. Insgesamt wird vor allem eine Zunahme der Infektionen durch kontaminierte Hühnereier beobachtet. Ursache ist, dass S. Enteritidis bei Hühnern Infektionen der Tuben und Ovarien verursacht, so dass die Eier die Erreger schon enthalten, bevor sich eine Schale bildet. Zusätzlich können die Keime v.a. bei hoher Luftfeuchtigkeit und hoher Umgebungstemperatur auch dünne oder beschädigte Eischalen durchwandern.
In der Schweiz ist die Anzahl der an das Bundesamt für Gesundheit gemeldeten Fälle seit 1999 rückläufig. In Deutschland erkrankten im Jahr 2003 ca. 63.000 und im Jahr 2004 ca. 57.000 Menschen an einer gesicherten Salmonellen-Infektion, womit sich der seit 1992 rückläufige Trend fortsetzte. 2004 wurden 52 bestätigte Todesfälle im Zusammenhang mit einer solchen Infektion gemeldet. Das Nationale Referenzzentrum für Krankenhaushygiene (NRZ) schätzt zumindest in den Jahren 1999 und 2000, dass dabei weiterhin etwa 10 % der tatsächlich vorkommenden Erkrankungsfälle gemeldet wurden. Die Serovare S. Enteritidis und S. Typhimurium sind die am häufigsten nachgewiesenen Erreger.
Krankheitsbilder: Die Symptome einer Salmonellen-Infektion im engeren Sinn sind Erbrechen und Durchfall (Gastroenteritis). Diese können wenige Stunden bis drei (maximal sieben) Tage nach dem Verzehr des befallenen Lebensmittels auftauchen. (Die mittlere Inkubationszeit beträgt 20-24h.) Die Erkrankungdauer beträgt in der Regel nur wenige Stunden oder Tage. In diesen unkomplizierten Fällen erfolgt keine antibiotische Behandlung - einerseits um die weitere Entwicklung multiresistenter Stämme zu verhindern, andererseits, da dadurch die Bakterienausscheidung verlängert werden kann.
Bis zu 5% der Infizierten erleiden systemische Verläufe mit Fieber zwischen 38 und 39°C, massiven Flüssigkeitsverlusten, rascher Gewichtsabnahme und der Notwendigkeit stationärer Einweisung und antibiotischer Therapie. Gefährdet sind hier v.a. Kinder, ältere und immungeschwächte Personen.
Als problematisch ist zu betrachten, dass man durch bestimmte Salmonellenstämme zum Dauerausscheider werden kann.
Diagnostik:
- Erregernachweis: Blutkultur (erste Woche nach der Infektion), Gruber-Widal-Reaktion (serologischer Antikörpersuchtest) (zweite Woche), Anzucht aus Stuhl (dritte Woche)
- Differenzierung: Die Abgrenzung gegen Shigellen und Proteus gelingt auf Selektivnährmedien (XLD-Agar, Hectoen-Agar).
- Die Identifizierung des Subtyps erfolgt über die Grubersche Antigenanalyse: Nachdem die isolierten Keime zunächst mit einer omnivalenten Antikörper-Suspension (Typhus-Paratyphus-Enteritidis-Serum, kurz: TPE-Serum) vorgetestet wurden, folgen gruppenspezifische Antikörper-Suspensionen und zuletzt monospezifische Antikörper. Schrittweise lässt sich so der Erreger in das Kaufmann-White-Schema einordnen, was für epidemiologische Aspekte sinnvoll ist.
Als Parameter für die Einteilung werden die O-Antigene (somatische Antigene), die spezifisch für jeden Subtyp sind, herangezogen.
Therapie: Die Therapie ist primär symptomatisch, eine Antibiose kann die Erregerausscheidung verlängern. Bei invasiven Verläufen, Patienten unter einem Jahr oder mit schweren Grunderkrankungen ist eine Antibiose indiziert, z.B. mit Cotrimoxazol. Die Resistenzbestimmung ist auch hier obligat.
Prophylaxe: Salmonellen vermehren sich bei Temperaturen von 10 bis etwa 50°C. Die Lagerung von rohen Lebensmitteln im Kühlschrank (bei ca. 4-7°C) verhindert ein übermäßiges Ausbreiten der Erreger. Sie werden nur sicher abgetötet, wenn im Inneren des Lebensmittels für mindestens 10 Minuten Temperaturen von über 70°C erreicht werden. Salmonellen vermehren sich zwar nicht bei der Tiefkühllagerung, überleben aber. Deshalb muss bei Lebensmitteln wie Geflügel die Auftauflüssigkeit weggeschüttet werden. Eier sollen gekocht oder gebraten werden, bis das Eigelb fest ist. Industriell gefertigte Eiprodukte müssen pasteurisiert werden.
Meldepflicht: Erkrankungsfälle sind meldepflichtig, da allerdings nicht bei jedem Brechdurchfall eine Erregerbestimmung durchgeführt wird, wird geschätzt, dass maximal 5-10% der Erkrankungsfälle auch gemeldet werden.
Weblinks: RKI - Salmonellose
Typhus
Als (deutsch) Typhus (von (griech.) typhos: Dunst, Nebel, Schwindel), auch Bauchtyphus oder typhoid fever genannt, werden schwere fieberhafte Infektionskrankheiten bezeichnet, welche meist mit Durchfall verbunden sind und durch Salmonellen (Salmonella enteritica enterica Serovar Typhi, kurz S. Typhi) hervorgerufen wird. Unbehandelt können die Krankheiten zum Tod führen. In Deutschland und Österreich sind sowohl der Verdacht als auch Erkrankung und Tod an Typhus meldepflichtig.
Epidemiologie:: Der Erreger des Typhus abdominalis, einer zyklischen Allgemeininfektion, S. Typhi wird fäkal-oral übertragen z.B. durch verunreinigtes Wasser und Nahrungsmittel und ist vor allem in Entwicklungsländern verbreitet. Fälle in den Industrienationen sind meist durch Fernreisen eingeschleppt. Bei Reisen in tropische Gebiete (z.B. Indien) sollte eine Immunisierung erwogen werden, die jedoch nur einen partiellen Schutz bietet. Weltweit erkranken jährlich etwa 16 Millionen Menschen.

Klinik: Die Inkubationszeit beträgt durchschnittlich 10 Tage, Extremwerte von 3 bis zu 60 Tagen sind beobachtet worden. Es kommt zunächst zu unspezifischen Allgemeinsymptomen wie Mattigkeit und Kopfschmerzen sowie zu einem treppenförmigem Fieberanstieg. Nach ca. 8 Tagen wird ein Stadium von anhaltendem hohen Fieber (40 bis 41°C) erreicht, das über Wochen andauern kann (Fieberkontinuum). Dabei findet sich eine relative Bradykardie (relativ zur Körpertemperatur zu niedrige Herzfrequenz). Hinzu kommen bisweilen Bewusstseinsstörungen (daher der Name), Splenomegalie, ein rötlich-fleckförmiges Exanthem am Oberkörper und der charakteristische erbsenbreiartige Durchfall. Darmperforationen, Haarausfall, Knocheneiterungen und Meningitis sind möglich. Während der langen Genesungsphase sinkt das Fieber stufenweise ab.
In der Folge bleiben einige Erkrankte (ca. 5%) Dauerausscheider der Salmonellen, da diese in der Gallenblase und den Gallenwegen persistieren. Diese Personen können, ohne selbst noch Krankheitszeichen zu zeigen, etliche andere anstecken.
Diagnostik: Die Stellung der Diagnose stützt sich auf die typische Klinik zusammen mit der Anamnese (Reise in tropische Regionen), Blutbild (Leukozytose, Eosinophilie) und den Erregernachweis durch Blutkulturen oder aus dem Stuhl. Im Serum lassen sich auch spezifische Antikörper nachweisen.
Therapie: Bei der antibiotischen Therapie finden unter anderem Gyrasehemmer (Ciprofloxazin) und parenterale Cephalosporine der 3. Generation Anwendung. Ferner sind Amoxicillin plus BLI und Cotrimoxazol geeignet. Wichtig ist zudem die Substitution der Wasser- und Elektrolytverluste durch die Durchfälle. Dauerausscheidern ist eine Cholezystektomie zu empfehlen. Bei adäquater Behandlung liegt die Sterblichkeit unter 1 %.
Prophylaxe: Hygiene ist der beste Schutz. Die auf Tropenreisen üblichen Maßnahmen, das heißt der Verzicht auf unzureichend gegarte Speisen und Leitungswasser, sollten auf jeden Fall beachtet werden. Obst, das unmittelbar vor dem Verzehr geschält wurde, ist sicher. Die Impfprophylaxe bietet nur einen Schutz von 60-75 %, mildert aber im Erkrankungsfall den Verlauf.
Meldepflicht: Typhus muss bei Verdacht, Erkrankung oder Tod dem zuständigen Gesundheitsamt gemeldet werden. Auch Dauerausscheider sind meldepflichtig.
Typhus levissimus / Typhus ambulatorius: Diese Krankheit wird heute im deutschen Sprachraum als Fleckfieber geführt. Dass es sich um eine eigenständige Erkrankung handelt, entdeckte 1847 William Jenner in London. Im angloamerikanischen Sprachraum ist das deutsche „Fleckfieber“ nach wie vor der „typhus“ und der deutsche „Typhus“ das „typhoid fever“.
Weblinks: RKI - Typhus
Paratyphus
Als Paratyphus bezeichnet man ein abgeschwächtes Krankheitsbild des Typhus, verursacht durch den Erreger Salmonella enterica enterica Paratyphi A, B, oder C, kurz S. Paratyphi A, B, oder C. A und C kommen überwiegend in wärmeren Klimazonen vor, während B weltweit verbreitet ist. Paratyphus ist eine zyklische Allgemeininfektion. Die Erkrankung ist meldepflichtig.
Pathogenese: Die Ansteckung erfolgt fäkal-oral durch verunreinigte Nahrungsmittel und Trinkwasser oder über Schmierinfektion. Die Inkubationszeit beträgt 1-2 Wochen. Die Symptome sind ähnlich wie beim Typhus:
- Mattigkeit, Kopfschmerzen.
- Typischer Hautausschlag (Roseolen) im Brust- und Bauchbereich.
- Treppenförmiger Fieberanstieg.
- Nach etwa acht Tagen anhaltend hohes Fieber (40 bis 41°C), manchmal wochenlang.
- Komplikationen: Bewusstseinsstörungen, Milzschwellung, Durchfall, Darmdperforation, Haarausfall, Knocheneiterungen, Meningitis.
- Stufenweises Absinken des Fiebers mit langer Rekonvaleszenz.
Diagnostik: Die Diagnostik erfolgt in der ersten und zweiten Krankheitswoche über eine Blutkultur, ab der zweiten Woche sind die Erreger im Stuhl nachweisbar. Es kommt zu einem deutlichen Anstieg von Antikörpern.
Therapie: Antibiotika über zwei Wochen. Zur Kontrolle des Therapieerfolgs wird der Stuhl auf Salmonellen untersucht. Einige Patienten entwickeln sich zu Dauerausscheidern.
Meldepflicht: Paratyphus muss bei Verdacht, Erkrankung oder Tod dem zuständigen Gesundheitsamt gemeldet werden. Auch Dauerausscheider sind meldepflichtig.
Weblinks: RKI - Paratyphus
Yersinien
[Bearbeiten]Wichtige Spezies:
- Y. enterocolitica ist der Erreger der enteralen Yersiniose, einer fieberhaften Enterocolitis oder Enteritis als Folge einer Nahrungsmittelvergiftung. Häufig treten Begleitscheinungen wie Erythema nodosum, eine Yersinia-Arthritis oder die Reiter-Krankheit mit Ekzemen der Handinnenflächen und der Fußsohlen auf. Therapeutisch können Ciprofloxacin, Doxycyclin und Cotrimoxazol eingesetzt werden.
- Y. pseudotuberculosis ist der Erreger der Pseudotuberkulose
- Y. pestis ist der Erreger der Pest
Yersiniosen können mit Chloramphenicol, Tetracyclinen oder Cotrimoxazol behandelt werden.
Yersinia pestis
| Yersinia pestis | ||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Systematik | ||||||||||||||||||
|
Yersinia pestis wurde von Alexandre Émile Jean Yersin 1894 entdeckt und ursprünglich nach Louis Pasteur Pasteurella pestis getauft, später jedoch Yersin zu Ehren umbenannt.
Morphologie und Eigenschaften: Yersinia pestis ist ein Gram-negatives, unbegeißeltes, sporenloses, fakultativ anaerobes Stäbchenbakterium. Es zählt zu den Enterobakterien und ist der Erreger der Lungen- und Beulenpest. Mit einigen weiteren Bakterien bildet es die Gattung Yersinia.
Pathogenitäts- und Virulenzfaktoren:
- Extotoxine
- Endotoxine
- Kapselbildung
Krankheitsbilder: Die Pest (pestis (lat.): Seuche) ist eine ansteckende Krankheit, die in mehreren großen Pandemien wiederholt erhebliche Teile der Weltbevölkerung betraf, wodurch die Menschheitsgeschichte nachhaltig beeinflusst wurde. Den Verlauf der europäischen Geschichte prägte vor allem eine große Pestepidemie im 14. Jahrhundert, die als "Schwarzer Tod" zwischen 1347 bis 1353 schätzungsweise 25 Millionen Todesopfer forderte, was einem Drittel der damaligen europäischen Bevölkerung entsprach.
Da jedoch zu dieser Zeit noch jegliche Mittel zur exakten Diagnose der Krankheit sowie eindeutig verwertbare Augenzeugenberichte fehlten, ist nicht zweifelsfrei erwiesen, dass es sich bei der damaligen Epidemie um einen Ausbruch der Pest im eigentlichen Sinne (durch Yersinia pestis) handelte oder vielleicht eher um ein virales hämorrhagisches Fieber, wie manche Forscher glauben.
Verlaufsformen der Pest: Man unterscheidet vier Erscheinungsformen der Pest: Beulenpest auch Bubonenpest genannt (bubo (gr.): Beule), Pestsepsis, Lungenpest sowie die abortive Pest. Bei Pandemien treten alle Formen der Erkrankung auf, am häufigsten jedoch die Beulenpest und die Lungenpest. Aus einer Beulenpest entwickelt sich ohne Behandlung fast immer eine Pestsepsis, die zu einer Lungenpest führt.
Beulenpest
Bei der Beulenpest erfolgt die Ansteckung gewöhnlich durch den Biss eines Rattenflohs, der den Erreger als Zwischenwirt in sich trägt. Durch den Wirtswechsel wird das Bakterium von einem infizierten auf ein bislang gesundes Wirtstier übertragen, nachdem es sich im Floh vermehrt hat.
Als stationärer Parasit ist der Rattenfloh eigentlich eng an sein Wirtstier gebunden. Er befällt den Menschen erst dann, wenn er keinen geeigneten Wirt mehr findet. Daher ging zumindest der Beulenpest immer ein massenhaftes Rattensterben voraus.

Die Inkubationszeit liegt bei wenigen Stunden bis sieben Tagen. Die Symptome sind Fieber, Kopf- und Gliederschmerzen, starkes Krankheitsgefühl und Benommenheit. Später kommt es zu Bewusstseinsstörungen. Der Name Beulenpest stammt von den stark geschwollenen, sehr schmerzhaften Beulen am Hals, in den Achselhöhlen und in den Leisten, die durch die Infektion der Lymphknoten und Lymphgefäße im Bereich des Flohbisses entstehen. Diese Beulen können bis zu zehn Zentimeter groß werden und sind aufgrund von Einblutungen blau-schwarz gefärbt. Die Geschwüre zerfallen, nachdem sie eitrig eingeschmolzen sind.
Die Beulenpest als solche ist nicht tödlich und die Beulen sind nach Öffnung heilbar. Allerdings kommt es bei bis zu 75 % der unbehandelten Patienten zur Pestsepsis und auch zur Lungenpest oder zu einer Streuung der Erreger mit ausgedehnten Hautblutungen. Diese Formen führen unbehandelt zum Tod.
Die Beulenpest verbreitet sich im Winter langsamer als im Sommer, da der Überträgerfloh bei Temperaturen unter 12°C in eine Kältestarre fällt. Der epidemische Höhepunkt dieser Pestart fiel stets mit der Fortpflanzungszeit der Flöhe im Herbst zusammen.
Pestsepsis
Die Pestsepsis entsteht durch Infektion von außen, zum Beispiel über offene Wunden oder als Komplikation der beiden anderen schweren Verlaufsformen. Die Infektion bewirkt hohes Fieber, Schüttelfrost, Kopfschmerzen und ein allgemeines Unwohlsein, später großflächige Haut- und Organblutungen. Die Pestsepsis ist unbehandelt immer tödlich, in der Regel spätestens nach 36h. Heute kann durch die Behandlung mit Antibiotika die Sterblichkeit deutlich gesenkt werden.
Lungenpest
Wenn die Erreger bei einer Beulenpest über die Blutbahn im Verlaufe einer Pestsepsis in die Lunge geraten, spricht von sekundärer Lungenpest. Wird sie durch eine Tröpfcheninfektion von Mensch zu Mensch übertragen, spricht man von primärer Lungenpest.

Die Lungenpest verläuft heftiger als die Beulenpest, weil die Abwehrbarrieren der Lymphknoten durch direkte Infektion der Lunge umgangen werden. Sie beginnt mit Atemnot, Husten, Blaufärbung der Lippen und schwarz-blutigem Auswurf, der extrem schmerzhaft abgehustet wird. Daraus entwickelt sich ein Lungenödem mit Kreislaufversagen, welches unbehandelt nach zwei bis fünf Tagen zum Tod führt.
Die Inkubationszeit beträgt nur ein bis zwei Tage, die Sterblichkeitsrate liegt hier bei 95%.
Abortive Pest
Die abortive Pest ist die harmloseste Variante der Pest. Sie äußert sich meist nur in leichtem Fieber und leichter Schwellung der Lymphknoten. Nach überstandener Infektion werden Antikörper gebildet, die eine lang anhaltende Immunität gegen alle Formen der Krankheit gewährleisten.
Übertragungswege:
- „Am Morgen des 16. April trat der Arzt Bernard Rieux aus seiner Wohnung und stolperte mitten auf dem Flur über eine tote Ratte (...) Am selben Abend sah er aus dem Dunkel des Gangs eine dicke Ratte auftauchen, mit feuchtem Fell und unsicherem Gang. Das Tier blieb stehen, schien sein Gleichgewicht zu suchen, wendete sich gegen den Arzt, blieb wieder stehen, drehte sich mit einem leisen Schrei im Kreis und fiel schließlich zu Boden, wobei aus den halb geöffneten Lefzen Blut quoll...“
Mit diesen Zeilen leitet der französische Literaturnobelpreisträger Albert Camus seinen 1947 erschienenen Roman "Die Pest" ein. Wenn das Werk Camus auch fiktiv ist, so beschreibt er doch treffend das große Rattensterben, das einer Pestepidemie vorauszugehen pflegt. Flöhe, insbesondere der Rattenfloh Xenopsylla cheopsis spielen bei der Übertragung des Pesterregers auf den Menschen eine entscheidende Rolle.

Mit Y. pestis infizierte Flöhe übertragen die Erkrankung beim Wirtswechsel z.B. von der Wanderratte oder der Hausratte auf den nächsten Wirt. Der Rattenfloh bevorzugt dabei als neuen Wirt wiederum Ratten, für die die Pesterkrankung ebenso tödlich ist wie für den Menschen. Fehlt es an Ratten, nimmt der Rattenfloh auch Menschen als neue Wirte an und infiziert dann auch diese mit der Zoonose. Etwa 30 Floharten sind als Überträger von Pestbakterien denkbar, darunter auch der Menschenfloh (Pulex irritans). Das Pestbakterium kann darüber hinaus längere Zeit auch ohne tierischen Wirt überleben – beispielsweise in Erde, Staub, Kot oder in Tierkadavern.
Neben der indirekten Ansteckung durch den Floh als Zwischenwirt ist die direkte Ansteckung an infizierten Nagetieren oder Menschen über offene Wunden und Speichel möglich. Gelangt der Erreger in den Lungenkreislauf entsteht die sekundäre Lungenpest mit hochinfektiösem blutigem Auswurf, die auf Kontakpersonen als primäre Lungenpest übertragen werden kann. Ist der Sprung des Pestbakteriums aus einer Nagerpopulation auf den Menschen erst einmal vollzogen, stellt die direkte Ansteckung sehr rasch den hauptsächlichen Infektionsweg dar. Bereits 100 bis 200 eingeatmete Erreger genügen für eine Infektion.
Auch Raubtiere, die infizierte Ratten gefressen haben, können Bakterien und Flöhe übertragen. Hauskatzen erkranken ebenfalls an der Pest, von Hunden ist dies jedoch nicht bekannt. Diese Übertragungswege sind im Normalfall selten, spielen jedoch im Rahmen von größeren Pandemien eine Rolle.
Wilde Nagetierpopulationen als Rückzugsgebiet des Pestbakteriums

Die Pestbakterien kommen auch heute noch in wild lebenden Nagetierpopulationen vor – wie beispielsweise bei den Präriehunden, Erdhörnchen und Murmeltieren. Diese Populationen sind die natürlichen Reservoire des Pestbakteriums, von denen aus gelegentlich häusliche Nager wie beispielsweise Ratten infiziert werden.
Während in Europa und Australien keine infizierten Tierpopulationen bekannt sind, kommen solche im Kaukasus, in Russland, in Südostasien, der Volksrepublik China, der Mongolei, Süd- und Ostafrika, Mittel- und Südamerika sowie im Südwesten der USA vor.
Nach Nordamerika gelangte der Erreger dabei über ein Handelsschiff während einer Pestepidemie, die ab 1894 in Südostasien grassierte. Obwohl nur sehr wenige Menschen in Nordamerika an der Pest erkrankten, infizierte der Erreger die amerikanische Eichhörnchenpopulation. Gelegentlich kommt es daher auch heute noch in Nordamerika zu Übertragungen von Tier zu Mensch. Meist sind es Jäger, die sich bei einem Nagetier anstecken; Norman F. Cantor verweist jedoch auch auf einen nordamerikanischen Fall aus den 1980er Jahren, bei dem eine Frau ein Eichhörnchen mit einem Rasenmäher überfuhr und sich dabei mit der Pest infizierte.
Der Pestausbruch in der indischen Stadt Surat im Jahre 1994 bestätigt daher die Aussage, die Camus bereits 1947 gegen Ende seines Romans Die Pest macht:
- „Während Rieux den Freudenschreien lauschte, die aus der Stadt empor drangen, erinnerte er sich daran, dass diese Fröhlichkeit ständig bedroht war. Denn er wusste, was dieser frohen Menge unbekannt war und was in den Büchern steht: Dass der Pestbazillus niemals ausstirbt oder verschwindet, sondern jahrzehntelang in den Möbeln und der Wäsche schlummern kann, dass er in den Zimmern, den Kellern, den Koffern, den Taschentüchern und den Bündeln alter Papiere geduldig wartet und dass vielleicht der Tag kommen wird, an dem die Pest zum Unglück und zur Belehrung des Menschen ihre Ratten wecken und erneut aussenden wird (...)“
Weltweit registriert die WHO etwa 1.000 bis 3.000 Pestfälle pro Jahr, meistens in Form kleinerer, örtlich begrenzter Epidemien. In Europa gab es den letzten dokumentierten Pestausbruch im Zweiten Weltkrieg. Man nimmt an, dass die Pest gegenwärtig in Europa nicht mehr existiert.
Diagnostik: Der mikrobielle Nachweis wird unter BSL-3-Bedingungen aus Sputum, Blut oder Bubonenaspirat erhoben durch Kultur, Giemsa-/Wright-Färbung (bipolar) und Nachweis des F1-Kapselantigens. Antikörper lassen sich ab dem zehnten Krankheitstag nachweisen.
Therapie: Die Pest wird mit älteren Aminoglykosiden (Streptomycin) plus Doxycyclin, alternativ mit Cotrimoxazol behandelt. Die Heilungsaussichten sind gut.
Prophylaxe: Es stehen Schutzimpfungen zur Verfügung, die allerdings eine Immunität lediglich für drei bis sechs Monate gewähren und dies auch nur bei der Beulenpest, nicht aber bei der Lungenpest. Die Autoren Eberhard-Metzger und Ries weisen jedoch auf die schlechte Verträglichkeit dieser Schutzimpfungen hin. Die WHO empfiehlt die Impfung daher nur Risikogruppen, zu denen beispielsweise Bauern, Landarbeiter und Jäger in Regionen zählen, in denen infizierte Nagetierpopulationen verbreitet sind.
Weitere Maßnahmen, um eine Pestepidemie einzudämmen, sind verbesserte Hygiene, Bekämpfung der Ratten und die Verhinderung des Transports von Ratten auf Schiffen. Da nach dem Tod der Ratten die Flöhe ihren Wirt wechseln, müssen die Menschen mit Insektiziden vor den Flöhen geschützt werden.
Quarantäne und Meldepflicht: Die Pest gehört neben den Pocken, Cholera und dem Hämorrhagischen Fieber in Deutschland zu den vier Quarantäne-Krankheiten. Patienten, die daran erkrankt sind, müssen in speziellen Infektionsabteilungen abgeschirmt werden. Länderübergreifende Quarantäneregelungen für Schiff-, Luft-, Zug- oder Kraftfahrzeugverkehr sind im internationalen Sanitätsreglement von 1971 festgehalten. Verdacht, Erkrankung und Tod durch Pest sind meldepflichtig nach dem Infektionsschutzgesetz. Die Meldungen werden von den Gesundheitsämtern an die Landesgesundheitsbehörde und das Robert-Koch-Institut weitergeleitet. Das Robert-Koch-Institut meldet sie gemäß internationalen Vereinbarungen an die WHO.
Die Pest als biologische Waffe: Die Pest wird von der WHO zu den zwölf gefährlichen biologischen Kampfstoffen gezählt. Zu diesem sogenannten „schmutzigen Dutzend“ gehören neben der Pest auch Milzbrand-, Tularämie-, Pocken-, Ebola- und Marburg-Erreger.
Der erste historisch belegte Einsatz der Pest als biologische Waffe fand 1346 in der russischen Hafenstadt Kaffa statt, als der Tartarenführer Khan Djam Bek Pestleichen über die Mauern der Stadt werfen ließ und die Belagerten vor der Pest die Flucht ergriffen.
Während des zweiten Chinesisch-Japanischen Krieges stellte die japanische Armee im "Einheit 731" genannten Gefangenenlager bei Harbin in der Mandschurei Waffen her, die mit Pest infizierte Flöhe enthielten und deren Einsatz in der Republik China in den Jahren 1940 bis 1942 lokale Pestausbrüche verursachten. Bei der Zerstörung der Produktionsstätten durch die japanische Armee 1945 bei Kriegsende kamen mit Pest infizierte Ratten frei und lösten in den Provinzen Heilongjiang und Jilin eine Epidemie mit über 20.000 Todesopfern aus.
Die USA setzten Pesterreger als biologische Waffe im Koreakrieg ein.
Zur Zeit des Kalten Krieges beschäftigten sich russische Wissenschaftler mit dem Einsatz von Pesterregern als biologische Waffe. Wie der ehemalige russische Forscher für biologische Waffen Ken Alibek berichtete, gelang es Russland Ende der 1980er Jahre, die Pest in eine sprühfähige Form zu bringen und gegen Antibiotika resistent zu machen.
In Deutschland beschäftigt sich das Robert-Koch-Institut mit den Gefahren durch biologische Kriegsführung. Dort wurde auch die Informationsstelle des Bundes für biologische Sicherheit (IBBS) eingerichtet. Wie groß die Gefahr eines Angriffs mit biologischen Kampfstoffen tatsächlich ist, ist umstritten. Die IBBS rät nicht zu einer Impfung gegen die Pest in Deutschland. Diese Empfehlung gilt sowohl für die Bevölkerung insgesamt als auch für Risikogruppen.
Geschichte:
Pest, Pocken und Milzbrand
Große Pandemien sind bereits aus der Bibel überliefert: Die Pest gehört zu den Plagen, die in der biblischen Erzählung Ägypten heimsuchen, und sie löst auch das Massensterben der Philister aus, die sich der jüdischen Bundeslade bemächtigt hatten. Da jegliches Mittel zur Diagnostik ebenso wie eindeutig verwertbare Augenzeugenberichte fehlten, ist nicht zweifelsfrei erwiesen, dass es sich bei den Pandemien, die uns aus der Zeit bis zum späten Mittelalter überliefert wurden, wirklich um Pestausbrüche handelte. Historiker nennen eine Vielzahl möglicher anderer Krankheiten. Das Spektrum reicht von Ebola-ähnlichen Krankheiten, Pocken, einer durch Kühe übertragenen Milzbrand-Infektion bis zu Gonorrhoe. Was die Ansteckungswege und die Symptomatik betrifft, kommen als Alternative zur Pest neben den Pocken eher Fleckfieber, Cholera und Typhus in Frage.
Letztendlich stammt das Wort Pest vom lateinischen pestis und bedeutet wie auch das griechische loimós nichts anderes als Seuche. Es steht darüber hinaus für Unglück, Verderben, verderbliche Person oder Sache, Scheusal, Unhold, Qual, Leiden, Hungersnot. Die klassischen Texte, vom altorientalischen Gilgamesch-Epos (um 1800 v.Chr.), von der Aeneis über die Ilias bis zur Bibel, bezeichnen daher alle großen Seuchen als Pest. Von den im nachfolgenden genannten Krankheitswellen sind viele Historiker jedoch überzeugt, dass Auslöser der Epidemien tatsächlich der Pesterreger war.
Antike bis Frühmittelalter
Die große Seuche im antiken Griechenland
Eine Seuche, der viele Menschen zum Opfer fielen, wurde bereits im antiken Griechenland um 430 v. Chr. von Thukydides ausführlich beschrieben. Thukydides berichtet, wie die Krankheit, die jäh in einer entscheidenden Phase des Peloponnesischen Krieges auftrat, im mit Kriegsflüchtlingen überbevölkerten Athen zu wüten begann.
- "Die Körper lagen, während sie verendeten, einer über dem anderen; einige wälzten sich, nach Wasser lechzend, auf den Wegen, die zu den Brunnen führten, halb tot auf der Erde. Die geweihten Stätten, in denen man sich eingerichtet hatte, lagen voller Leichen, die Menschen waren da gestorben, wo sie sich hinbegeben hatten. Vor einer solchen Entfesselung des Leids achteten sie, da sie nicht wußten, was aus ihnen würde, überhaupt nichts mehr, nicht göttliche, nicht menschliche Ordnung." (Thuk. II 52)
Perikles, der berühmte athenische Feldherr und Politiker, starb laut Thukydides an den Folgen der Seuche, ebenso wie eine große Anzahl anderer Athener. Diodor schätzte, dass Athen damals ein Drittel seiner Bevölkerung verlor.
Zwei Jahre lang wütete die Epidemie in Athen und trug mit zu Athens Niederlage im Peloponnesischen Krieg bei, den Athen gegen Sparta führte.
Ob dieser Seuche durch Pesterreger ausgelöst wurde, ist heute jedoch umstritten. Viele Historiker unterstellten lange Zeit, dass es sich hierbei entweder um die Pest oder um die Pocken handelte. Da Thukykides jedoch die typischen Charakteristika wie die Pestbeulen und die schwärzlichen Flecken auf der Haut nicht beschrieb und die beschriebenen Symptome in ihrer Gesamtheit auf keine heute bekannte Krankheit passen, wurden von Historikern und Medizinern lange Zeit auch andere Erreger diskutiert.
Bei neuen Grabungen unter der Leitung des Archäologen Manolis Papagrigorakis konnten als Erreger inzwischen Typhus-Bakterien identifiziert werden. Um Spuren des Keimes zu finden, öffneten die Archäologen ein Grab auf dem antiken Friedhof Kerameikos in Athen und bargen hieraus drei Zahnwurzeln aus der Anfangszeit der Tragödie. In mehreren Gentests konnten sie in den Zahnresten das Erbmaterial von Typhus-Bakterien nachweisen.
Typhus verbreitet sich vor allem unter schlechten hygienischen Bedingungen. Sie ist extrem ansteckend, löst heftigen Durchfall und starkes Fieber aus. In Athen führte der Ausbruch der Epidemie zu einem dramatischen Bevölkerungsrückgang und einem Zusammenbruch des sozialen Gefüges mit fatalen wirtschaftlichen Konsequenzen und einem militärischen und politischen Niedergang - durchaus vergleichbar mit den Auswirkungen späterer, eindeutig belegter Pestepidemien.
Die Pest im Römischen Reich
Auch das Römische Reich wurde mehrfach von großen Epidemien getroffen. Die erste war die so genannte "Antoninische Pest" zur Zeit des Kaisers Marc Aurel (161–180), die von den aus den Partherkriegen 166 zurückkehrenden Soldaten verbreitet wurde. Ob es sich bei dieser Epidemie um die Pest handelte, ist allerdings ebenfalls unklar. Pestwellen mit tiefgreifenden Auswirkungen auf das Römische Reich traten insbesondere in der Zeit zwischen 250 und 650 n. Chr. auf.
Die so genannte "Justinianische Pest" zur Zeit Kaisers Justinians (527–565), die 542 in Konstantinopel ausbrach, trug möglicherweise zum Misserfolg der Restauratio imperii bei und gilt als die größte antike Pestepidemie Europas. Sie brach zunächst im Orient aus von wo aus sie sich rasant im ganzen Mittelmeergebiet ausbreitete.
Anhand der detaillierten Schilderungen des spätantiken Historikers Prokopios geht die Forschung zumeist davon aus, dass es sich bei dieser Seuche tatsächlich um die Beulenpest handelte, die vielleicht zusammen mit anderen Krankheiten auftrat. 544 ließ Justinian, der selbst erkrankt gewesen war, aber überlebt hatte, das Ende der Pestepidemie verkünden. Diese brach jedoch 557 erneut aus, kehrte im Jahre 570 nochmals wieder und trat bis zur Mitte des 8. Jahrhunderts in etwa zwölfjährigem Rhythmus immer wieder in Erscheinung. Gegen 770 verschwand die Seuche dann für über fünf Jahrhunderte.
Vom frühen Mittelalter an bis zum Ausbruch des so genannten Schwarzen Todes in der zweiten Hälfte des 14. Jahrhunderts schien Europa von der Pest weitgehend verschont geblieben zu sein.
Der "Schwarze Tod" – die mittelalterlichen Pestepidemien

Mit der Bezeichnung "Schwarzer Tod" wird heutzutage die große Pestepidemie bezeichnet, die in Europa von 1347 bis 1353 wütete.
Verbreitung
Die Seuche war offenbar in den 30er Jahren des 14. Jahrhunderts in Zentralasien ausgebrochen und breitete sich entlang der Handelswege auch in Richtung Europa aus. 1347 erreichte sie das an der Krim gelegene Kaffa. Kaffa, das heutige Feodosija, war als genuesische Handelsstadt eng in das Handelsnetz der Genueser eingebunden, das sich über den gesamten Mittelmeerraum erstreckte. Von Schiffen verbreitet erreichte die Krankheit noch im selben Jahr die Küstenstädte Konstantinopel, Kairo sowie das sizilianische Messina. Im März 1348 hatte die Epidemie über den Landweg bereits Toulouse erreicht, im Mai erkrankten die ersten Opfer in Paris, im August starben die ersten in Avignon an der Pest. Deutschland, Norwegen, Schweden und Irland wurden 1349 von der Pest erreicht.
Man schätzt, dass etwa 20 bis 25 Millionen Menschen, rund ein Drittel der damaligen Bevölkerung Europas, durch den Schwarzen Tod umkamen. Über die Anzahl der Opfer in Asien und Afrika liegen keine seriösen Angaben vor. Jegliche Zahlen sind jedoch mit Vorsicht zu genießen, da zeitgenössische Quellen die Anzahl der Toten eher zu hoch ansetzten, um den Schrecken und die Unbarmherzigkeit dieser Pandemie zu unterstreichen.
Der Schwarze Tod wütete nicht gleichmäßig in Europa, sondern ließ einige wenige Gebiete fast unberührt. Große Teile Polens, Belgiens und Süddeutschlands blieben beispielsweise von dieser ersten Pestwelle verschont. Auch Mailand entging der Heimsuchung durch die Pest, während in Florenz vier Fünftel der Bürger starben. In der Einleitung zu seiner Novellensammlung "Decamerone" schildert Giovanni Boccaccio eindrucksvoll, wie verheerend sich die Epidemie auswirkte:

- "So konnte, wer – zumal am Morgen – durch die Stadt gegangen wäre, unzählige Leichen liegen sehen. Dann ließen sie Bahren kommen oder legten, wenn es an diesen fehlte, ihre Toten auf ein bloßes Brett. Auch geschah es, dass auf einer Bahre zwei oder drei davongetragen wurden, und nicht einmal, sondern viele Male hätte man zählen können, wo dieselbe Bahre die Leichen des Mannes und der Frau oder zweier und dreier Brüder und des Vaters und seines Kindes trug." (Boccacio, "Decamerone")
Gesellschaftliche Auswirkungen
Viele der Menschen empfanden die Pest als Gottesstrafe. Religiöse Bewegungen entstanden spontan im Gefolge oder in Erwartung der Pest: Eine der auffälligsten waren die Bewegung der Flagellanten, die sich als Buße für ihre eigenen Sünden so wie die der Gesellschaft in öffentlichen Umzügen selbst geißelten und in den Städten Reue und Umkehr predigten. Sie verstanden sich als direkte Mittler zwischen Himmel und Erde – ohne Einschaltung der kirchlichen Autoritäten. Papst Klemens VI. verbot daher bereits 1348 öffentliche Selbstgeißelungen, ohne dieses Verbot jedoch durchsetzen zu können.

Bereits Anfang 1348 war das Gerücht aufgekommen, die Pest werde durch Brunnenvergiftung verbreitet. In der Karwoche wurden in der Provence erstmals Juden wegen der Pest verfolgt; der Vorwurf, sie träufelten Gift in Brunnen und Quellen und verbreiteten so die Pest, ist wenig später in den Quellen zu finden. In Savoyen bekannten sich im Herbst 1348 jüdische Angeklagte unter der Folter solcher Vergehen für schuldig. Die Geständnisse fanden rasch Verbreitung und bildeten die Basis für eine Welle von Judenpogromen vor allem im Elsass, in der Schweiz und in Deutschland. Nicht selten gerieten die Juden dabei zwischen die Fronten älterer Auseinandersetzungen, so etwa in Straßburg. Die Lage der jüdischen Minderheit im Reich war durch die Auseinandersetzungen zwischen den Häusern der Wittelsbacher und der Luxemburger äußerst prekär.
Nach dem Abflauen einer ersten Pogromwelle etwa im März 1349 war diese Großwetterlage für den Beginn einer zweiten Welle verantwortlich: Im Kampf um die Loyalität einzelner Städte (Frankfurt am Main, Nürnberg) gab Karl IV. die Juden den Interessen der städtischen Führungsgruppen preis. Die oft behauptete Verantwortung der Flagellanten für die Judenpogrome lässt sich in den seltensten Fällen nachweisen, am ehesten noch für Köln. In den meisten Fällen gilt, dass die Juden noch vor dem Eintreffen der Pest ermordet wurden. In Böhmen und Österreich wurden sie von der Landesherrschaft, in Regensburg von der Stadtgemeinde geschützt.
Langfristig bewirkte und beschleunigte die Pest durch den massiven Bevölkerungseinbruch einen tief greifenden Wandel der mittelalterlichen Gesellschaft, deren langfristige Wirkungen auch positiv bewertet wurden. So bezeichnete David Herlihy die Pest als "die Stunde der neuen Männer": Die Entvölkerung ermöglichte einem größeren Prozentsatz der Bevölkerung den Zugang zu Bauernhöfen und lohnenden Arbeitsplätzen. Unrentabel gewordene Böden wurden aufgegeben, was in manchen Regionen dazu führte, dass Dörfer verlassen oder nicht mehr wiederbesiedelt wurden (sogenannte Wüstungen). Die Zünfte ließen nun auch Mitglieder zu, denen zuvor die Aufnahme verweigert worden war, und während der Markt für landwirtschaftliche Pachten zusammenbrach, stiegen die Löhne in den Städten deutlich an.
Zweifel
Die Identifikation der mittelalterlichen Seuchen mit der durch Yersinia pestis verursachten Pest wurde und wird nach wie vor mehrfach angezweifelt, so durch die Historiker David Herlihy, Samuel K. Cohn und Sue Scott, den Zoologen Chris Duncan und den Anthropologen James Wood. Dabei trifft insbesondere der Einwand, dass weder die damalige rasante Ausbreitungsgeschwindigkeit noch die historisch beschriebenen Krankheitszeichen mit den bei einer Beulenpest zu erwartenden übereinstimmten. Auch war damals keine zu erwartende Epizootie bei Hausratten beobachtet worden.
Alternativ wird nunmehr die Möglichkeit diskutiert, dass es sich entweder um Milzbrand oder eine langsame Variante eines hämorrhagischen Fiebers gehandelt haben könnte. Ein Argument dafür liefert auch eine Mutation des Gens CCR5 im Menschen, bei der 32 Basenpaare nicht vorhanden sind. Diese Mutation mit dem Namen CCR5Δ32 wird in ca. 10% der europäischen Bevölkerung gefunden, nicht aber in Asien oder Ostafrika. Mathematische Modelle zur Verbreitung dieser Mutation lassen auf einen großen Selektionsdruck vor etwa 700 Jahren schließen, dem Zeitpunkt der Pest in Europa. Diese Mutation könnte somit ein genetischer Überlebensvorteil des Pesterregers gewesen sein. Die Veränderung auf dem CCR5-Gen bietet heute dem homozygotischen Träger einen beschränkten Schutz vor einer HIV-Infektion. Wenn es nur von einem Elternteil vererbt wird, verzögert es den Ausbruch von AIDS durchschnittlich um drei Jahre. Vor Y. pestis schützt diese Mutation dagegen nicht. Bei der im Mittelalter als Pest bezeichneten Krankheit könnte es sich somit um ein direkt von Mensch zu Mensch übertragenes virales hämorrhagisches Fieber gehandelt haben.
Neuzeit
15. bis 19. Jahrhundert
Nach einer schweren Pestepidemie, die 1347 begann, endemisierte die Seuche: In lokalen Epidemien suchte sie in den nächsten drei Jahrhunderte in nahezu regelmäßigen Abständen verschiedene Gebiete Europas heim. In der Stadt St. Gallen beispielsweise trat die Pest zwischen 1500 und 1640 mindestens vierzehn Mal auf. Nach 1580 kam es außerdem in Zyklen von vier bis fünf Jahren zu Pockenausbrüchen, an denen vor allem jüngere Kinder starben.
Der nur drei Wochen dauernden Pestepidemie von 1555 im hessischen Nidda fielen 300 Menschen zum Opfer. Das war ein Drittel der Bevölkerung dieser Stadt. Ähnliches gilt für die kleine Stadt Uelzen, die zu Beginn des 16. Jahrhunderts ungefähr 1200 Einwohner hatte. Uelzen gehört zu den Städten, die bereits im 16. Jahrhundert genaue Register über ihre Einwohner führten. So weiß man, dass im Jahr 1566 in Uelzen genau ein Viertel der Einwohner starben, nämlich 295, von denen 279 der Pest erlagen. 1597 - Uelzens Einwohnerschaft war mittlerweile auf ungefähr 1600 Einwohner angestiegen - starben 554 Einwohner, davon 510 an der Pest.
Zu weiteren schweren Epidemien kam es 1665/1666 in London mit etwa 99.000 Toten und 1678/1679 in Wien zu der Zeit, als dort der sogenannte "liebe Augustin" lebte. Die letzten Pestepidemien trafen Europa im 18. Jahrhundert: Von 1709 bis 1711 wütete die Pest in Ostpreußen; starben dort gewöhnlich pro Jahr 15.000 Menschen (von einer Einwohnerschaft von etwa 600.000), kamen in diesen drei Jahren insgesamt 230.000 Menschen ums Leben.
Aus Sorge vor einem Ausbruch auch in Berlin ließ König Friedrich I. (Preußen) dort ein Pesthaus errichten, aus dem die Charité hervorging. Im Mai 1720 trat die Pest wieder in Marseille und in der Provence auf und verschwand erst wieder 1722. Nachdem 1771 in Moskau eine weitere Pestepidemie aufgetreten war, blieben weitere Pestepidemien in Europa aus.

Das Erlöschen der Pest in Europa bringt man damit in Zusammenhang, dass seit dem 16. Jahrhundert die Hausratte allmählich von der Wanderratte verdrängt wurde. Da die Wanderratte scheuer ist als ihre Vorgängerin, kommt es weniger häufig zu direkten Kontakten zwischen Mensch und Tier, was eine Ansteckung durch infizierte Flöhe reduziert. Der Historiker Vasold, der sich sehr intensiv mit der Pest beschäftigte, weist jedoch darauf hin, dass der Ausbruch in Moskau im Jahre 1771 zu einem Zeitpunkt erfolgte, als die Wanderratte die Hausratte schon längst verdrängt hatte.
Eine weitere mögliche Erklärung ist, dass sich der Pesterreger genetisch verändert hat oder dass Ratten immun gegen den Pesterreger wurden und nach der Infizierung durch den Floh nicht mehr starben, so dass es für die Flöhe keine Notwendigkeit mehr gab, abzuwandern. Auch die Fortschritte im Gesundheitswesen und die Verbesserung der Hygiene haben zum Ausbleiben der Pestepidemien beigetragen.
Die letzte Pandemie begann in der 2. Hälfte des 19. Jahrhunderts in Zentralasien und kostete während der nächsten 50 Jahre weltweit rund 12 Millionen Menschenleben. Während dieser Pestepidemie konnte der Erreger identifiziert und der Übertragungsweg erklärt werden.
Die Pest heute
Die Pest ist auch heute noch nicht besiegt: Von 1979 bis 1992 meldete die WHO 1451 Todesfälle in 21 Ländern. In den USA gab es beispielsweise 1992 dreizehn Infektionen und zwei Todesfälle.
Die letzte größere Pestepidemie ereignete sich von August bis Oktober 1994 im indischen Surat. Die WHO zählte 6.344 vermutete und 234 erwiesene Pestfälle mit 56 Toten. Der dort festgestellte Pesterreger wies dabei bislang noch nicht beobachtete Eigenschaften auf. Er zeichnete sich durch eine schwache Virulenz aus und gilt aufgrund einiger molekularbiologischer Besonderheiten als neuartiger Erregerstamm.
Im Februar 2005 breitete sich die Lungenpest im Nordwesten Kongos aus. Nach Berichten der WHO gab es 61 Tote. Durch das Eingreifen der Organisation Ärzte ohne Grenzen konnte eine weitere Verbreitung verhindert werden.
Die Pest in Literatur und Kunst:

Kaum eine andere Katastrophe prägte die kollektive Vorstellung von Machtlosigkeit, Untergang und Unglück so sehr wie die Heimsuchung durch die Pest.
Die frühesten Seuchenberichte stammen von antiken Autoren wie Homer, Thukydides, Lukrez, Prokopios von Caesarea und Ovid. In Buch VII, 501-613 seiner Metamorphosen berichtet er sehr detailliert über die Pest von Aegina.
Vor allem jedoch die Pestepidemie des 14. Jahrhunderts hat sich stark auf Kunst und Literatur ausgewirkt. Die Menschen erwarben sogenannte Pestblätter, um sich mit Hilfe der darauf abgebildeten Heiligen vor der Pest zu schützen. Boccaccio schrieb vor dem Hintergrund der Pest, die 1348 in Florenz wütete, seine Novellensammlung „Decamerone“: Sieben Damen und drei junge Männer fliehen vor der Pest aus Florenz auf einen Landsitz. In einem bemerkenswerten Kontrast zu der Düsterkeit und Dramatik der Pestschilderungen stehen hierbei die erotisch-heiteren Geschichten, die sich die zehn Florentiner zur Unterhaltung erzählen. Sie finden einen Ausweg aus der Katastrophe in einem leichteren Leben. Die außergewöhnliche Situation der Pest gibt ihnen die Möglichkeit, in ihren Erzählungen die mittelalterlichen Normen und Werte zu hinterfragen.
In Lübeck entstand 1350 unter dem Eindruck der verheerenden Pestepidemie das Gemälde "Totentanz" in der neu erbauten Marienkirche. Im selben Jahr schuf Francesco Traini die Wandmalereien des Campo Santo von Pisa. Der Tod ist hier kein Knochenmann, sondern eine schwarz gekleidete, alte Frau, die mit wehenden Haaren und einer breitschneidigen Sichel in der Hand auf eine Gruppe sorgloser, junger Menschen herabfährt. Zu den Meisterwerken der Sepulkralkunst, das auf das veränderte Bild des Todes in der spätmittelalterlichen Kunst hinweist, zählt auch das gegen Ende des 14. Jahrhunderts entstandene Grabmal des Kardinals La Grange. Der Kardinal ist als fast nackter, verwesender Leichnam dargestellt und die Inschrift mahnt alle noch Lebenden, wie nichtig das Leben sei: „Was blähst du dich auf in deinem Stolz. Staub bist du und Staub musst du werden, ein verfaulter Kadaver, die Speise der Würmer“.
Die vermutlich erste medizinische Dissertation über die Pest verfasste der aus Nidda stammende Arzt Johannes Pistorius der Jüngere: De vera curandae pestis ratione (Über die rechte Art, die Pest zu behandeln), Frankfurt 1568.
In Wien entstand 1879 die – als solche heute oft gar nicht mehr erkannte – Pestballade"O du lieber Augustin, alles ist hin." (vgl. Marx Augustin), die der Pest einen Galgenhumor entgegensetzt.
1722 erschien in London Daniel Defoes „Journal of the Plague Year“ (zu deutsch: „Die Pest zu London“). Die Erzählung wurde zu einem Zeitpunkt veröffentlicht, als ein Pestausbruch in Südfrankreich eine erneute Heimsuchung durch diese Krankheit befürchten ließ, und fand eine breite Leserschaft. Lange Zeit galt sie als Augenzeugenbericht des Pestausbruchs im Jahre 1665. Defoe war jedoch zum Zeitpunkt des Ausbruches noch ein Kind von vier oder fünf Jahren; die Erzählung aber schildert den Pestausbruch aus der Sicht eines erwachsenen Mannes, der in sachlichem Ton die Ereignisse beschreibt und mitleidsvoll und einfühlsam die Reaktionen seiner Mitbürger verfolgt. Gemeinsam mit „Robinson Crusoe“ und „Moll Flanders“ begründete diese Erzählung den Ruf von Daniel Defoe als Schaffer der Kunstform des realistischen Romans.

In den "I Promessi Sposi" schildert Alessandro Manzoni das Wüten der Pestepidemie im Mailand des Jahres 1630. Seiner Darstellung liegen Berichte mehrerer Zeitzeugen zugrunde, namentlich die „Historiae Patriae“ des Historiografen Giuseppe Ripamonti (1573 – 1643) und die Pestchronik des Arztes Alessandro Tadino („Ragguaglio dell’origine et giornali successi della gran peste contagiosa, venefica et malefica, seguita nella città di Milano...“), die 1648 erschienen war. Johann Wolfgang Goethe – vermutlich der erste deutsche Leser von Manzonis Roman (dieser hatte ihm die "Promessi Sposi" gleich nach dem Druck des dritten Bandes 1827 zugesandt) – bemerkte zwar, der Autor stehe in den Pestkapiteln „als nackter Historiker“ da und bemängelte das „umständliche Detail“ bei Dingen „widerwärtiger Art“. Dessen ungeachtet gilt die erbarmungslos präzise Schilderung der Seuche in den „Promessi Sposi“ heute als ein Glanzpunkt der italienischen Prosa. – Mit Ereignissen in Mailand während des Pestjahrs 1630 beschäftigt sich auch Manzonis 1829 entstandene „Storia della Colonna Infame“.
Edgar Allan Poe schuf 1842 die Erzählung "Die Maske des Roten Todes", die eigentlich durch einen Zeitungsbericht über eine Choleraepidemie in Paris inspiriert war, aber Ähnlichkeit zu anderen Pesterzählungen aufweist. Obwohl eine Krankheit (der Rote Tod, Red Death) das halbe Land dahinrafft, gibt der Herzog Prince Prospero, der auf sein Schloss geflüchtet ist, einen pompösen Maskenball. Die Rahmenhandlung, bei der man vor der Epidemie in den Hedonismus flieht, erinnert hier an Boccaccios Decamerone, doch nimmt Poes Geschichte eine andere Wendung. Am Ende dringt der Rote Tod auch in das Schloss ein, und weil sich der Herzog nicht um sein Land gekümmert hat, wütet die Epidemie weiter.
In der Rahmennovelle „Die schwarze Spinne“ verarbeitete Jeremias Gotthelf 1843 alte Sagen über einen Handel mit dem Teufel zu einer gleichnishaften Erzählung über die Pest.
Arnold Böcklin schuf zu diesem Thema 1889 in Italien das Bild „Pest/Der Schwarze Tod“, das heute im Basler Kunstmuseum ausgestellt ist. Böcklin personifiziert die Pest in seinem Bild als fliegendes, blindes Monstrum, vor dem es kein Entrinnen gibt. Die Sense und die skelettartige Gestalt greifen auf die mittelalterliche Todessymbolik zurück.
Albert Camus schrieb den Roman „Die Pest“ (fr. „La Peste“) über einen neuzeitlichen Pestausbruch in der algerischen Stadt Oran (publiziert 1947). Darin trifft ein Arzt trotz der Aussichtlosigkeit und Absurdität des Kampfes gegen die Pest auf Menschlichkeit und Solidarität. Die Pest wird hierbei oft als Symbol auf den Nationalsozialismus interpretiert.
Zitierte Werke
- Boccaccio; Il decamerone - Eine englische Übersetzung aus der Einleitung, aus der die obigen Zitate stammen, findet sich unter Introduction to il decamerone
- Albert Camus: Die Pest, 1947
- Thukydides berichtet in seinem Werk über den Peloponnesischen Krieg ausführlich über die Seuche, die die Athener heimsuchte. Neben der "Reclam"- (oder der "Bibliothek der Alten Welt") Übersetzung ist diese auch nachlesbar unter folgender englischsprachiger Website: "Peloponnesischer Krieg": Thukydides; "Der Peloponnesische Krieg" (Reclam), hrsg. von H. Vrestka und W. Rinner, Stuttgart 2000. ISBN 3-150-01808-0
Literatur und Weblinks:
- Manolis J. Papagrigorakis, Christos Yapijakis, Philippos N. Synodinos, Effie Baziotopoulou-Valavani: DNA examination of ancient dental pulp incriminates typhoid fever as a probable cause of the Plague of Athens in "International Journal of Infectious Diseases", Volume 9 ISSN 1201-9712
- Pauline Allen: The Justinianic Plague, in: Byzantion 49 (1979), S. 5-20.
- Klaus Bergdolt: Der schwarze Tod in Europa, Becksche Reihe, C.H. Beck Verlag, München 2003, ISBN 3-406-45918-8
- Norman F. Cantor: In the Wake of the Plague – The Black Death and the Word it made, London 1997, ISBN 0-7434-3035-2
- Claudia Eberhard Metzger, Renate Ries: Verkannt und heimtückisch – Die ungebrochene Macht der Seuchen, Basel 1996, ISBN 3-7643-5399-6
- Franz-Reiner Erkens: Buße in Zeiten des Schwarzen Todes: Die Züge der Geissler, in „Zeitschrift für historische Forschung“, 26. Band 1999, Berlin, S. 483–513
- František Graus: Pest - Geißler - Judenmorde. Das 14. Jahrhundert als Krisenzeit, Göttingen 1987, ISBN 3-525-35622-6
- David Herlihy: Der Schwarze Tod und die Verwandlung Europas, Berlin 1997, ISBN 3-8031-3596-6
- Kay Peter Jankrift: Krankheit und Heilkunde im Mittelalter, Wissenschaftliche Buchgesellschaft, ISBN 3-534-15481-9
- Arno Karlen; Die fliegenden Leichen von Kaffa - Eine Kulturgeschichte der Plagen und Seuchen, Berlin 1996, ISBN 3-353-01054-8
- Mischa Meier (Hg.): Pest. Die Geschichte eines Menschheitstraumas, Klett-Cotta, Stuttgart 2005, ISBN 3608943595. Gesamtdarstellung der Pestgeschichte von der Antike bis in die Moderne.
- William Naphy, Andrew Spicer: Der schwarze Tod, Magnus Verlag, Essen 2003, ISBN 3-88400-016-0
- Norbert Ohler: Sterben und Tod im Mittelalter, Patmos Paperback, ISBN 3-491-69070-6
- Jacques Ruffié, Jean-Charles Sournia: Die Seuchen in der Geschichte der Menschheit, Stuttgart 1987, ISBN 3-423-30066-3
- Barbara Tuchman: Der ferne Spiegel – das dramatische 14. Jahrhundert, Düsseldorf 1980, ISBN 3-546-49187-4
- Manfred Vasold: Die Ausbreitung des Schwarzen Todes in Deutschland nach 1348, in Historische Zeitschrift Band 277, 2003, S. 281–308
- Manfred Vasold: Pest, Not und schwere Plagen - Seuchen und Epidemien vom Mittelalter bis heute, München 1991, ISBN 3-406-35401-7
- Manfred Vasold: Die Pest, Konrad Theiss Verlag, Stuttgart 2003, ISBN 3-8062-1779-3
- Stefan Winkle: Kulturgeschichte der Seuchen, 2000, ISBN 3933366542
- Karl Georg Zinn: Kanonen und Pest, Opladen 1989, ISBN 3-531-12107-3
- Sue Scott, Christopher Duncan: Return of the Black Death: The World's Greatest Serial Killer, John Wiley & Sons, Canada 2004, ISBN 0470090006
- RKI - Pest
- www.cdc.gov/ CDC - CDC Plague Home Page
- www.edjewnet.de/ Das jüdische Museum Göppingen - Pest und Judenverfolgung


