Medizinische Mikrobiologie: Paramyxoviridae
Die Paramyxoviren sind ebenfalls kugelförmig, aber mit 150-250nm etwas größer als die Orthomyxoviren. Das Virion ist helikal gebaut und besteht aus einer Lipidschicht, die mit "Stacheln" (Spikes) besetzt ist und ein virusspezifisches Antigen trägt. Zu den typischen Vertretern gehören das Masernvirus, das Mumpsvirus und auch das Rinderpest-Virus sowie der Erreger der Newcastle-Krankheit (atypische Geflügelpest) der Vögel.
Systematik der Paramyxoviridae:
- Paramyxoviridae
- Paramyxovirinae
- Paramyxoviren
- Parainfluenzavirus (1, 3)
- Morbilliviren
- Masernvirus
- Rubulaviren
- Parainfluenzavirus (2, 4)
- Mumpsvirus
- Paramyxoviren
- Pneumovirinae
- Pneumoviren
- Humanes Respiratory-Syncytical-Virus (RSV)
- Metapneumoviren
- Humanes-Metapneumo-Virus (HMPV)
- Pneumoviren
- Paramyxovirinae
Paramyxovirinae
[Bearbeiten]Respirovirus/Rubulavirus
[Bearbeiten]Human parainfluenza virus
[Bearbeiten]
| Human parainfluenza virus | ||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Systematik | ||||||||||||||||||||||
| ||||||||||||||||||||||
| Morphologie | ||||||||||||||||||||||
| umhüllt, helikal | ||||||||||||||||||||||
Das weltweit verbreitete Parainfluenzavirus aus der Paramyxoviridae-Familie löst die Parainfluenza aus, ein Krankheitsbild mit grippeähnlichen Symptomen. Die Durchseuchungsrate bei Kindern bis 10 Jahren liegt bei 90%. Die Übertragung erfolgt durch Tröpfcheninfektion. Parainfluenza kann eine bakterielle Superinfektion nach sich ziehen. Der Infektionsverlauf ist stark von der Disposition und Konstitution abhängig. Parainfluenza-Viren kommen in vier Serotypen vor. Das Virus besitzt eine einsträngige RNA und trägt Hämagglutinine und Neuraminidase in der Lipidhülle.
Morbillivirus
[Bearbeiten]| Morbillivirus | ||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Systematik | ||||||||||||
| ||||||||||||
| Morphologie | ||||||||||||
| umhüllt, helikal | ||||||||||||
Morbillivirus ist eine Virus-Gattung aus der Paramyxoviridae-Familie. Es handelt sich um hochinfektiöse, behüllte Viren mit einem helikalen Nukleokapsid. Das Genom besteht aus einer einzelsträngigen, nicht-segmentierten RNA negativer Polarität. Die Virushülle trägt Spikes aus Glycoproteinen mit Hämagglutinin-, Neuraminidase- und hämolytischer Aktivität.
Die Virus-Replikation vollzieht sich im Zytoplasma und in der Zellmembran infizierter Zellen.
Morbilliviren sind meist empfindlich gegenüber Wärme, Austrocknung, fettlösenden Stoffen und den meisten Desinfektionsmitteln.
Arten:
- Masern-Virus
- Pest der kleinen Wiederkäuer-Virus
- Rinderpest-Virus
- Staupe-Virus
- Seehund-Staupevirus
Masernvirus
[Bearbeiten]| Morbillivirus | ||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
 | ||||||||||||||
| Systematik | ||||||||||||||
| ||||||||||||||
| Morphologie | ||||||||||||||
| umhüllt, helikal | ||||||||||||||
Das Masernvirus ist ein ausschließlich humanpathogener, etwa 120–140nm großer Erreger aus der Familie der Paramyxoviren (Genus Morbillivirus). Der Mensch der einzige Reservoirwirt, der Erregers wird nur von Mensch zu Mensch übertragen, so dass eine Ausrottung leicht möglich wäre. Von ihm gibt es mehrere stabile Genotypen, in Mitteleuropa C2 und D6, die eine Verfolgung der globalen Infektionswege ermöglicht. Weiterhin existiert nur ein stabiler Serotyp, was die Impfstoffherstellung einfacher gestaltet. Die Lipidhülle, die zur hohen Kontagiosität beiträgt enthält das Glykoprotein Hämagglutinin, jedoch keine Neuraminidase. Das Virus reagiert sehr empfindlich gegenüber äußeren Einflüssen wie erhöhten Temperaturen, Licht, UV-Strahlen, Detergenzien und Desinfektionsmitteln.
Krankheitsbild: Das Masernvirus löst die Masern (Morbilli) aus, eine hochansteckende, systemische Infektionskrankheit, die nach überstandener Erkrankung eine lebenslange Immunität hinterlässt.
Geschichte: Erste Berichte über die Masern gehen auf das 7. Jahrhundert zurück und werden dem jüdischen Arzt Al-Yehudi zugeschrieben. Die erste ausführliche Beschreibung der Masern verdanken wir dem persischen Arzt Abu Bakr Mohammad Ibn Zakariya al-Razi [1], Anfang des 10. Jahrhunderts, der angab, sie würden „mehr gefürchtet als die Pocken“.
Den Namen „Morbilli“, was so viel wie „kleine Pest“ bedeutet, erhielten die Masern während der ausgedehnten Epidemien des Mittelalters, da damals wie heute viele Kinder an den Masern starben. 1882 veröffentlichte der französische Arzt Antoine Louis Gustave Béclère seine Aufsehen erregende Arbeit „Die Ansteckung mit Masern“.
1954 wurde das Virus erstmalig isoliert, ab 1963 war der erste Impfstoff erhältlich. Zuvor bekam aufgrund der hohen Kontagiosität des Erregers beinahe jeder die Masern: Es handelte sich um ein Ereignis im Leben, das unweigerlich - meist schon im Kindesalter - auftrat und auf das man warten konnte. Mehr als die Hälfte der Kinder bekam die Masern vor dem 6. und 90% vor dem 15. Lebensjahr. Hatte man die Krankheit überstanden, so war man für den Rest des Lebens immun.
Epidemiologie: Der Erreger kommt weltweit vor und ist in mehreren Entwicklungsländern noch weit verbreitet. In verschiedenen Ländern wurde er durch gut organisierte Impfkampagnen bereits ausgerottet. 1984 legte die WHO einen Zeitplan für die Elimination der Masern bis zum Jahr 2000 fest – tatsächlich starben 2003 jedoch weltweit nach Angaben der WHO noch etwa 530.000 Menschen – davon die Mehrzahl Kinder – an Masern. Maserninfektionen sind für ungefähr die Hälfte aller durch Impfung vermeidbaren Todesfälle verantwortlich. Der neue Zeitplan sieht die weltweite Ausrottung des Virus – bei entsprechender Anstrengung – jetzt für das Jahr 2007 vor. Rückblick:
- Die Anzahl der Masernerkrankungen in den USA sank von 800.000 im Jahre 1958 auf einige wenige Fälle in den letzten Jahren, wobei alle Erreger von ungeimpften Personen aus Europa und Asien importiert worden waren, was durch die Bestimmung des Genotyps nachgewiesen werden konnte. Einen dramatischen Anstieg der Fälle gab es in den Jahren 1989–1991, wo binnen drei Jahren über 55.622 Erkrankungsfälle berichtet wurde, von denen 123 tödlich endeten. Hauptsächlich waren Kleinkinder aus hispanoamerikanischen und afroamerikanischen Familien betroffen, wo die Rate an ungeimpften Kindern 4–7x höher lag als bei den Betroffenen der übrigen weißen Bevölkerung. Zwischenzeitig treten genuine Masernerkrankungen in allen amerikanischen Staaten von Kanada bis Argentinien mit Einschluss der Karibik kaum noch auf.
- In Finnland mit seinen 5,2 Mio. Einwohnern gab es von 1996 – 2000 vier Masernfälle. Auch diese waren aus dem Ausland importiert.
- In Deutschland wurden im Jahre 2005 778 Masernfälle gemeldet. 2005 kam es in Deutschland zu zwei größeren Masernausbrüchen, im Februar starb ein 14-jähriges Mädchen in Hessen, im Mai wurden 110 Fälle aus Oberbayern gemeldet. Anfang 2006 wurden Masernhäufungen aus Nordrhein-Westfalen (bisher 1.354 Fälle bis 31. Mai, Schwerpunkte in Duisburg, Mönchengladbach und im Kreis Wesel) und Baden-Württemberg (bisher 83 Fälle bis zur Kalenderwoche 15, Schwerpunkt in Stuttgart und im Kreis Esslingen) gemeldet. Expertenschätzungen gehen davon aus, dass eine hohe Dunkelziffer existiert und die Zahl der Krankheitsfälle wesentlich höher liegt als die der Meldungen.
- In Österreich, das für Masern bis 2001 keine Meldepflicht kannte, wurde vom Institut für Virologie des AKH in Wien ein freiwilliges Meldesystem geschaffen, das etwa 8% der österreichischen Bevölkerung abdeckt. Somit konnten für den Zeitraum von 1993–1997 etwa 28.000–30.000 Masernfälle für ganz Österreich hochgerechnet werden, wobei besonders 1996 und 1997 ein beinahe epidemisches Auftreten von Masernerkrankungen zu verzeichnen war. Insgesamt dürfte die Durchimpfungsrate in Österreich somit nur unwesentlich besser sein als in Deutschland. Wären die Richtlinien hier ähnlich streng wie in den USA, würde man schon 2.700 Erkrankungen in fünf Jahren nicht mehr akzeptieren.
- In Rumänien kam es zwischen dem 1. Dezember 1996 und dem 30. September 1997 zu einer Masern-Endemie mit 20.034 Erkrankungen und 13 Todesfällen.[2] Im Dezember 2005 gab es eine neuerliche Masernepidemie in Rumänien. Etwa 4000 Kinder waren erkrankt, 10 gestorben [3].
Diagnose: Die Diagnose ist in unkomplizierten Fällen nur über den serologischen Nachweis von IgM-Antikörpern zu führen. Dies wird heute methodisch meist mit Hilfe eines Enzymimmunoassay (ELISA) erreicht, in manchen Labors wird auch noch die Komplementbindungsreaktion (KBR) oder der Hämagglutinationshemmtest (HHT) durchgeführt.

Der direkte Erregernachweis (RT-PCR aus Virus-RNA oder Virusanzucht in Zellkulturen) ist aufwändiger als der indirekte Antikörpernachweis und bleibt eher spezielleren Fragestellungen vorbehalten.
Die Diagnose anhand des „typischen“ Masernexanthems ist mit einer Fehlerhäufigkeit von 50% behaftet. Im Epidemiefall kann die Diagnose dennoch häufig klinisch gestellt werden, insbesondere von erfahrenen Untersuchern.
Meldepflicht: In Deutschland sind durch das 2001 in Kraft getretene Infektionsschutzgesetz (IfSG, § 6) Krankheitsverdacht, Erkrankung und Tod ebenso wie der direkte oder indirekte Nachweis des Masernvirus mit Namen meldepflichtig geworden. Bei Krankheitsverdacht oder Erkrankung besteht Tätigkeits- und Aufenthaltsverbot in Gemeinschaftseinrichtungen.
In Österreich besteht Meldepflicht seit Dezember 2001 (BGBl. II Nr. 456/2001 Verordnung: Anzeigepflichtige übertragbare Krankheiten).
In der Schweiz besteht seit März 1999 Meldepflicht (Melde-Verordnung, SR 818.141.1).
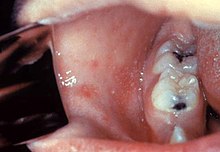
Krankheitsverlauf/Symptome: Typisch für die Masern ist ein zweiphasiger Krankheitsverlauf: Auf die Inkubationszeit von 10 bis 14 Tagen folgt das 3–4 Tage dauernde, uncharakteristische Prodromalstadium, auch Initialstadium genannt. Dieses äußert sich durch eine Entzündung der Schleimhäute des oberen, teilweise auch des mittleren Atemtraktes und der Augenbindehäute. Die katarrhalischen Beschwerden umfassen Rhinitis, trockene Bronchitis, Konjunktivitis, Fieber bis 41°C, Übelkeit, Hals- und Kopfschmerzen kommen. Erst danach, etwa am 12. – 13. Tag, geht die Krankheit in das typische Exanthemstadium über, in dem ein Schleimhaut-Enanthem am weichen Gaumen auftreten kann. Typisch sind auch die sog. Koplikflecken an der Wangenschleimhaut gegenüber den Prämolaren. Der Fieberverlauf ist häufig zweigipflig, wobei der erste Gipfel während des Prodromal-, der zweite während des Exanthemstadiums auftritt.
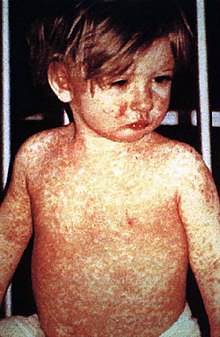
Am 14.–15. Tag breitet sich ein makulopapulöses, zum Teil konfluierendes Exanthem – hinter den Ohren (retroaurikulär) beginnend – innerhalb von 24 Stunden von oben nach unten über den ganzen Körper aus. Nach weiteren 4 – 5 Tagen bilden sich die Symptome in der Regel zurück. Als Überbleibsel des Exanthems kann eine kleieförmige Schuppung für kurze Zeit bestehen bleiben. Begleitend treten häufig Lymphknotenschwellungen auf.
Atypische Verläufe kommen in verschiedenen Situationen vor: Säuglinge mit Leihimmunität durch mütterliche Antikörper oder Patienten, die Antikörperpräparate erhalten haben, erkranken an mitigierten (abgeschwächten) Masern. Bei Personen mit Immundefizienz kann der Verlauf nach außen hin atypisch oder symptomarm sein, so kann beispielsweise der typische Hautausschlag fehlen („weiße Masern“), während sich innerlich z.B. eine progrediente Riesenzellpneumonie oder die Masern-Einschlusskörper-Enzephalitis entwickeln kann, die mit einer Letalität von etwa 30% verbunden ist.
Während und nach der Erkrankung an Masern kommt es regelhaft zu einer insgesamt 4–6 Wochen dauernden Immunschwäche. Diese kann anderen Infektionserregern den Weg bereiten und stellt daher eine zusätzliche Gefahr für das erkrankte Kind dar.
In unkomplizierten Fällen folgt eine rasche Erholung und eine lebenslang anhaltende Immunität.
Komplikationen: Etwa 20% aller Maserninfektionen gehen mit Komplikationen einher, wobei Mittelohrentzündungen und Lungenentzündungen die häufigsten sind. Das Robert-Koch-Institut gibt an, dass die Letalität bei Masern der Literatur zufolge bei 1:10.000 bis 1:20.000 liege, bei einem Ausbruch in den Niederlanden 1999/2000 starben drei von knapp 3.000 Betroffenen, die Centers for Disease Control and Prevention (CDC) geben für die USA eine Sterblichkeit von ca. 1:500 bis 1:1.000 an. In Entwicklungsländern liegt die Letalität wesentlich höher (laut Literaturangaben bis zu 25%). Zum Tode führende Komplikationen sind meist die Masernpneumonie oder die Masernenzephalitis.
Masernkrupp
Durch eine Kehlkopfentzündung mit Schwellung der Schleimhaut kommt es zu Heiserkeit und Atemnot bereits im Vorstadium (DD.: Pseudokrupp).
Masernpneumonie
1. Primäre Masernpneumonie: Dabei handelt es sich um eine interstitielle Pneumonie mit Bronchiolitis, die sich hauptsächlich als Atemstörung äußert. Mittels körperlicher Untersuchung ist sie schwer zu diagnostizieren, so dass ein Röntgenbefund erforderlich ist.
2. Bronchopneumonie als bakterielle Superinfektion: Sie tritt insbesondere nach oder bei einer interstitiellen Viruspneumonie auf, ist aber auch isoliert möglich durch die masernbedingte Immunsuppression (s. o.).
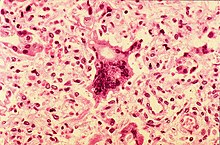
3. Riesenzellpneumonie: Eine seltene Pneumonie mit vielkernigen, von den Alveolarepithelien abstammenden Riesenzellen, pathognomonisch für Masern (Masernriesenzellen) und Keuchhusten, selten auch bei Diphtherie oder Grippe zu beobachten.
Keratitis
Die Entzündung der Hornhaut mit multiplen, punktförmigen, epithelialen Läsionen ist eine weitere Komplikation der Masern. In Entwicklungsländern sind die Masern eine der häufigsten Ursache der Erblindungen von Kindern (besonders im Zusammenhang mit Vitamin-A-Mangel).
Enzephalomyelitis
Die akute postinfektiöse Enzephalitis tritt mit einer Wahrscheinlichkeit von in 0,1 % auf. Die Entzündung des Gehirns und seiner Häute entwickelt sich 3–10 Tage nach Exanthembeginn, bei Patienten über sechs Jahren häufiger als bei Kleinkindern. Symptome sind Fieber, Kopfschmerz, Bewusstseinstrübung und meningeale Reizung (Nackensteifigkeit, Erbrechen) mit Rückgang nach 1–3 Tagen. Bei leichten Formen ist keine Krankenhauseinweisung notwendig. Schwere Verlaufsformen äußern sich in epileptischen Anfällen und neurologischen Funktionsstörungen. Die Ausbreitung ist herdförmig oder diffus. Häufigkeit: Nach Einführung der Masernimpfung sank die Zahl ständig und liegt derzeit in Deutschland bei < 10/Jahr. Letalität: 20%; Defektheilungen: 20–40%.
Subakute sklerosierende Panenzephalitis (SSPE)
Die SSPE ist eine generalisierte Entzündung des Gehirns. Sie ist selten, endet aber in 100% der Fälle letal. Die Angaben über die Häufigkeit von SSPE schwanken zwischen 7–11 Fälle pro 100.000 Masernfällen. Die Erkrankung tritt Monate bis zu zehn Jahre, im Durchschnitt 6-8 Jahre nach einer Maserninfektion auf. Die absolute Häufigkeit der SSPE ist durch die Masernimpfung deutlich reduziert worden. Der Verlauf ist langsam progredient über 1–3 Jahre (slow virus infection), in 10% tritt ein akuter Verlauf (3–6 Monate) auf, in weiteren 10% ein langsamerer Verlauf (länger als drei Jahre).
1. Stadium: psychische Störungen und Demenz 2. Stadium: Myoklonien, epileptische Anfälle 3. Stadium: Dezerebrationssyndrom
Im EEG finden sich typische Veränderungen, die nahezu wegweisend für die SSPE sind (Radermecker-Komplex). Mittlerweile wurde ein Masernvirus mit einem defekten M-Protein isoliert: „SSPE-Virus“
Weitere Komplikationen:
Innenohrschädigung mit Ertaubung, Diarrhoe, Blinddarmentzündung, generalisierte Lymphadenitis, Thrombozytopenische Purpura.
Vorbeugung:
Quarantäne
Nach dem deutschen Infektionsschutzgesetz (IfSG, §9) aus dem Jahre 2001 dürfen infizierte Kinder solange nicht die Schule oder den Kindergarten besuchen, bis sie keine Viren mehr ausscheiden.
Impfung
Die Impfung gegen Masern wird üblicherweise als Masern-Mumps-Röteln-Kombinationsimpfung (MMR-Impfstoff) durchgeführt, in der Regel zwischen dem 12. und 15. Lebensmonat, möglichst bis zum Ende des 2. Lebensjahres, um den frühestmöglichen Impfschutz zu erreichen. Damit ist nach einmaliger Impfung bei 90 % der Kinder ein ausreichender Impfschutz vorhanden. Da bei einer Durchimpfungsrate von weniger als 95 % mit sporadischen Masernepidemien (alle drei bis sieben Jahre) zu rechnen ist, müssen mit einer zweiten Impfung – frühestens vier Wochen nach der ersten – Impflücken geschlossen werden, um Impfversagern den entsprechenden Impfschutz zu gewähren. Nach dem Impfkalender der Ständigen Impfkommission am Robert-Koch-Institut ist die zweite MMR-Impfung bei allen Kindern im Alter von 15–23 Monaten vorgesehen.
Steht bei einem Kind die Aufnahme in eine Kindereinrichtung an, kann die MMR-Impfung auch vor dem 12. Lebensmonat, jedoch nicht vor dem 9. Lebensmonat erfolgen, da im 1. Lebensjahr im Blut des Säuglings noch vorhandene mütterliche Antikörper die Impfviren neutralisieren können (Lebendimpfung, die Vermehrung der Impfviren ist erforderlich). Sofern die Erstimpfung vor dem 12. Lebensmonat erfolgte, sollte die MMR-Impfung bereits im 2. Lebensjahr wiederholt werden.
Auch wenn von Eltern oder Impflingen angegeben wird, dass eine Masern-, Mumps- oder Rötelnerkrankung bereits durchgemacht wurde, sollte die zweite MMR-Impfung durchgeführt werden. Anamnestische Angaben über eine Masern- oder Rötelnerkrankung sind ohne mikrobiologisch-serologische Dokumentation der Erkrankungen unzuverlässig und nicht verwertbar. Es gibt keine Hinweise auf Nebenwirkungen nach mehrmaligen Masern-, Mumps- oder Rötelnimpfungen.
Die Eliminierung der Masern ist ein erklärtes Ziel der deutschen Gesundheitspolitik. „Es ist dafür Sorge zu tragen, dass die zweite MMR-Impfung so früh wie möglich, spätestens jedoch bis zum vollendeten 18. Lebensjahr nachgeholt wird; bei Mädchen wird damit auch der unverzichtbare Schutz vor einer Rötelnembryopathie gesichert.“[4]
Österreich: Zwei Teilimpfungen im 2. Lebensjahr mit einem Mindestabstand von einem Monat. Wiederholungen der Impfung werden bei Schuleintritt im 7. Lebensjahr und im 13. Lebensjahr vom öffentlichen Gesundheitsdienst kostenlos angeboten. (Österreichischer Impfplan 2006)
Impfkomplikationen
Von Impfreaktionen sind die Impfkomplikationen abzugrenzen, die zu vorübergehenden oder anhaltenden Schäden oder gar zum Tod führen können. Prinzipiell ist ein direkter Zusammenhang mit einer Masernimpfung schwer zu beweisen. So soll bei einer von 200.000 Impfungen ein Impfschaden mit bleibenden Folgen auftreten und auf ca. 500.000 Impfungen ein Todesfall kommen. Da es sich bei der Masernimpfung um eine Impfung mit einem abgeschwächten Lebendimpfstoff handelt, können in 3–5 % der Fälle so genannte Impfmasern auftreten. Diese stellen eine abgeschwächte Form der Masern dar: eine Konjunktivitis, eine Tracheitis, ein feinfleckiger Hautausschlag und sehr selten eine Otitis media können auftreten. Schwerwiegendere Folgen bei besonders empfänglichen Kindern sind denkbar oder möglich.
Fieber und lokale Impfreaktionen wie Rötung, Schmerzen und Schwellungen an der Injektionsstelle können wie bei allen Impfungen vorkommen und sind als harmlose Nebenwirkungen zu betrachten.
Weblinks: RKI - Masern
Rubulavirus
[Bearbeiten]Mumpsvirus
[Bearbeiten]| Mumps virus | ||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
 | ||||||||||||||
| Systematik | ||||||||||||||
| ||||||||||||||
| Morphologie | ||||||||||||||
| umhüllt, helikal | ||||||||||||||
Mumps (Parotitis epidemica, Salivitis epidemica), umgangssprachlich auch Ziegenpeter genannt, ist eine ansteckende Virusinfektion, die durch den Erreger Paramyxovirus parotitis, ein umhülltes RNA-Virus aus der Familie der Paramyxoviridae, Genus Paramyxovirus, verursacht wird. Die Mumps zählt zu den Kinderkrankheiten.
Epidemiologie: Mumps kommt auf der ganzen Welt endemisch vor. Der Mensch ist das einzige Erregerreservoir. Vor Einführung der allgemein empfohlenen Impfung erkrankten die meisten Kinder zwischen dem zweiten und 15. Lebensjahr, Jungen häufiger als Mädchen. Seit Einführung der Impfung ging die Zahl der Erkrankungen drastisch zurück. Die Übertragung erfolgt durch Tröpfcheninfektion, direkten Kontakt oder seltener durch speichelverschmutzte Gegenstände. Das Virus wird auch im Urin und der Muttermilch ausgeschieden. Patienten sind drei bis fünf, maximal sieben Tage vor Ausbruch der Erkrankung bis in die frühe Rekonvaleszenz, aber maximal bis zum neunten Tag nach Ausbruch der Erkrankung kontagiös. Die Parotitis epidemica hinterlässt in der Regel eine lebenslange Immunität. Zweiterkrankungen sind möglich, aber selten. Die Inkubationszeit beträgt zwölf bis 25, im Mittel 16 bis 18 Tage.
Symptome: Die Mumps zeigt eine große Variabilität im Erscheinungsbild. Mindestens 30 bis 40% der Infektionen verlaufen symptomlos (stille Feiung). Am häufigsten treten Fieber und eine ein- oder noch häufiger beidseitige entzündliche Schwellung der Ohrspeicheldrüse (Parotitis) auf. Nicht selten sind auch andere Speicheldrüsen (einschließlich der Bauchspeicheldrüse (Pankreatitis)) betroffen. Das zentrale Nervensystem ist klinisch relevant in drei bis 15% in Form einer aseptischen Meningitis betroffen. Diese kann bereits eine Woche vor bis zu drei Wochen nach Beginn der Ohrspeicheldrüsenentzündung oder auch isoliert auftreten. Während oder nach der Pubertät kommt es bei 25 bis 30% der männlichen Betroffenen zu einer Hodenentzündung (Mumpsorchitis). Diese beginnt am Ende der ersten Krankheitswoche mit erneutem Fieberanstieg, starker Schwellung und Druckschmerzhaftigkeit meist nur eines Hodens. Seltene Manifestationen sind Eierstockentzündung, Schilddrüsenentzündung, Entzündung der Iris, Herzmuskelentzündung, Nierenentzündung und Mumpsenzephalitis.
Komplikationen: Mumps ist eine akute, selbstlimitierende, gutartige Erkrankung. Todesfälle kommen heutzutage praktisch nicht mehr vor. Chronische Erkrankungen des Zentralnervensystems werden vereinzelt beschrieben. Nach Mumpsmeningitis kann in etwa 1:10.000 Infektionen eine Innenohrschwerhörigkeit auftreten. Auch die Mumpsenzephalitis kann z.B. Lähmungen als bleibende Schäden verursachen. Nach Mumpsorchitis kann es zu einer einseitigen Hodenatrophie kommen. Unfruchtbarkeit ist jedoch ungewöhnlich. Nach heutiger Auffassung besteht kein direkter kausaler Zusammenhang zwischen Mumps und Diabetes mellitus Typ I. Bei Mumps während der Schwangerschaft ist im ersten Drittel mit einer erhöhten Rate an Aborten zu rechnen. Eine Mumpsembryopathie ist nicht bekannt. Neugeborene und junge Säuglinge erkranken selten. Unbehandelt kann die Krankheit auch zum Tode führen.

Diagnose: Bei typischer Symptomatik im Rahmen einer Epidemie kann die Diagnose klinisch gestellt werden. Im Einzelfall kann die Diagnose durch Bestimmung der spezifischen Antikörper im Serum bestätigt werden (z.B. mittels ELISA). In besonderen Fällen ist auch die Virusanzucht oder der Nachweis mumpsspezifischer RNA durch PCR aus Rachenabstrich, Speichel, Liquor, Urin oder Biopsiematerial möglich. Ein hinweisender Befund kann die Erhöhung der S-Amylase sein. Die Immunität einer Person kann leicht durch Bestimmung mumpsspezifischer IgG-Antikörper festgestellt werden.
Therapie: Es gibt keine spezifische antivirale Behandlung. Eine symptomatische Behandlung ist selten erforderlich und beschränkt sich meist auf fiebersenkende Maßnahmen. Bei schweren Verläufen sind unter Umständen Kortikosteroide indiziert.
Prophylaxe: Es existiert eine Lebendimpfung aus abgeschwächten, auf Hühnerfibroblasten gezüchteten Mumpsviren. Er ist entweder als monovalenter Impfstoff oder in Kombination mit abgeschwächten Masern- und Röteln-Viren erhältlich. Die exakte Dauer des Impfschutzes ist nicht bekannt. In der Regel wird die Impfung sehr gut vertragen. Gelegentlich kann kurzdauerndes Fieber und eine leichte Schwellung der Ohrspeicheldrüse auftreten. Eine Impfmeningitis kommt beim heutzutage verwendeten Impfstamm nicht mehr vor. Die Mumpsimpfung gehört in Deutschland zu den von der STIKO allgemein empfohlenen Impfungen und soll als Kombinationsimpfung mit der Masern- und Röteln-Impfung (MMR) ab dem elften bis zum 14. Lebensmonat und eine Wiederholungsimpung zur Schließung von Impflücken frühestens vier Wochen nach der ersten Impfung verabreicht werden. Gegenanzeigen gegen die Impfung sind Schwangerschaft, allergische Reaktionen auf Impfstoffbestandteile und angeborene oder erworbene T-Zell-Defekte. Eine gesicherte Hühnereiweißallergie stellt allerdings keine Kontraindikation dar! Auch Personen mit humoralen Immundefekten, Granulozytenfunktionsstörungen, Asplenie oder asymptomatischer HIV-Infektion dürfen geimpft werden. Nach Mumpskontakt kann eine Erkrankung durch eine Impfung in der frühen Inkubationszeit nicht sicher verhindert werden. Dennoch wird die Impfung empfohlen, da sie vor Ansteckung bei nachfolgender Exposition schützt. Spezielle Mumpsimmunglobuline zur passiven Impfung gibt es nicht. Hospitalisierte Patienten mit Mumps sollen von anderen Patienten getrennt werden. Nach Abklingen der Symptome können Kinder frühestens neun Tage nach Ausbruch der Erkrankung Gemeinschaftseinrichtungen wieder besuchen.
Weblinks: RKI - Mumps
Pneumovirinae
[Bearbeiten]Pneumovirus
[Bearbeiten]Human respiratory syncytial virus (RSV)
[Bearbeiten]| Human respiratory syncytial virus | ||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
 | ||||||||||||||||
| Systematik | ||||||||||||||||
| ||||||||||||||||
| Morphologie | ||||||||||||||||
| umhüllt, helikal | ||||||||||||||||
Das humane respiratorische Synzytial-Virus (RSV, Typ A und B) ist ein behülltes Virus mit einzelsträngiger Minus-RNA aus der Gruppe der Paramyxoviren.
Es wird meistens über Tröpfcheninfektion übertragen und verursacht obere Atemwegsinfekte mit Schnupfen, Husten, Bronchitis und Mittelohrentzündung. Es gibt auch tierpathogene Stämme, die Infektion von Kälbern mit bovinen RSV hat einen ähnlichen Verlauf wie beim Kleinkind und wird aus diesem Grunde zu Modelluntersuchungen zur Entwicklung von Impfstoffen und Therapeutika genutzt.
Die Infektion kann akut verlaufen und in schweren Fällen eine intensivmedizinische Überwachung notwendig machen. Das Virus lässt sich mittels immunologischer Testverfahren (ELISA) nachweisen. Zur Therapie eignet sich dann evtl. das Virostatikum Ribavirin, dessen Wirkung in Placebo-Studien jedoch nicht belegt werden konnte.
Eine Erkrankung erzeugt keine andauernde Immunität, es kann lebenslang zu Re-Infektionen kommen, die bei gesunden Menschen milde verlaufen. Für immungeschwächte Menschen mit hohem Risiko besteht die Möglichkeit einer passiven Immunisierung, die (aus Kostengründen) nur speziellen Risikofällen vorbehalten ist. Diese erzeugt auch lediglich eine Wirkungsdauer von ca. einem Monat.
Weblinks: RKI - Erkrankungen durch Respiratory Syncytial Viren (RSV)
Quellen
[Bearbeiten]- ↑ http://www.medicine-worldwide.de/persoenlichkeiten/al_razi.html
- ↑ http://www.cdc.gov/nip/diseases/measles/history.htm
- ↑ http://www.dgk.de/web/dgk_content/de/masern_12-05.htm
- ↑ Impfempfehlungen der Ständigen Impfkommission (STIKO) Juli 2005
