Anorganische Chemie für Schüler/ Metalle und Redoxreaktionen & Energiediagramm
Wiederholung aus der 8. Klasse - Beispiele für Oxidationen
- Rosten von Eisen
| Eisen | + | Sauerstoff | Eisenoxid
|
+ | Energie |
| 4 Fe | + | 3 O2 | 2 Fe2O3 | + | e- |
- Verbrennung von Kohlenstoff
| Kohlenstoff | + | Sauerstoff | Kohlenstoffdioxid | + | Energie |
| C | + | O2 | CO2 | + | e- |
- Oxidation von Kupfer
| Kupfer | + | Sauerstoff | Kupferoxid | + | Energie |
| Cu | + | O2 | CuO | + | e- |
- Oxidation = Vereinigung mit Sauerstoff
| Stoff x | + | Sauerstoff | Stoff x-oxid | + | Energie |
Die Reaktion von Kupferoxid mit Wasserstoff - eine Redoxreaktionen
Seit ca. 2 Milliarden Jahren gibt es Sauerstoff auf unserem Planeten. Metalle sind seit der Entstehung unseres Planeten vorhanden. Da fragt man sich natürlich, in welcher Form eigentlich so wichtige Metalle wie Eisen oder Kupfer vorliegen? Durch Jahrmillionen des Kontaktes mit Sauerstoff liegen sie natürlich in oxidierter Form vor. Die Oxide sind in der Regel für die Menschen nicht zu gebrauchen gewesen, da sie oft Verunreinigt und noch dazu Spröde sind. Die Menschen zogen Waffen und Gegenstände aus Stein vor. Demzufolge nannte man diese Periode der Geschichte auch Steinzeit.
Aber 3000 Jahre v.Chr. änderte sich das plötzlich. Die Waffen der sich bis dahin mit Faustkeilen bewaffneten Steinzeitmenschen hatten sich verändert. Ab der Bronzezeit vor ca. 5000 Jahren hat der Mensch Metallwerkzeuge hergestellt. Was muss passiert sein? Die Menschheit hatte eine ihrer wichtigsten Erfindungen gemacht - sie konnte aus Kupferoxid das Metall Kupfer herstellen und dieses weiter zu Bronze verarbeiten. Bronze war dem Stein natürlich überlegen, da sie formbar war.
Also welche Leistung hat der Mensch am Übergang von der Stein- zur Bronzezeit vollbracht?
Oxidation muss umgekehrt worden sein
Was ist also das Ziel aus chemischer Sicht? (Wenn eine Oxidation die Vereinigung mit Sauerstoff ist...)
Die Abgabe/ Entzug von Sauerstoff aus dem Metalloxid (=Reduktion)
2. Reaktion von Kupferoxid mit Wasserstoff
Versuchsbeschreibung
(Schwarzes) Kupferoxidpulver wird im Wasserstoffstrom erhitzt.[1]

Beobachtung
Flamme wird kleiner, rötliches Produkt, Kondenswasser im Glasrohr, exotherme Reaktion
Schlussfolgerung
Was ist mit dem Kupferoxid geschehen? Es hat seinen Sauerstoff abgegeben!

Redoxreaktionen
Einem 8. Klässler, wäre allerdings am Ende der 8. Klasse noch etwas anderes aufgefallen… Fällt Dir nichts auf? Na klar, es findet doch auch eine Oxidation statt. Wasserstoff vereinigt sich schließlich mit Sauerstoff es liegt beides vor.
Das führt zu folgendem Rätsel: Muss immer beides vorliegen? Ist dies nun ein Sonderfall, oder gar ein Irrtum?
Diese Frage zu beantworten ist recht einfach, wenn Du Dir einen Vergleich vorstellst: Du bekommst Taschengeld von Deinen Eltern. Zum Austausch eines Geldscheins gehören immer zwei Leute. Einer der den Schein aufnimmt und einer, der ihn abgibt, oder? Es ist nicht nur etwas Dir passiert, sondern auch mit dem der Dir Taschengeld gibt. Du wirst reicher, die andere Person ärmer.
Wie kann man nun eine Redoxreaktion erkennen?
Historische Herstellung von Kupfer aus Kupferoxid
Menschen in der Bronzezeit hatten keinen Wasserstoff als Red-Mittel[2], sondern sie verwendeten ein anderes vorhandenes Reduktionsmittel. Nur welches Element vereinigt sich leicht mit Sauerstoff und reagiert dabei am besten zu einem Gas (damit keine Verunreinigungen entstehen)?
Die Menschen nahmen damals Kohlenstoff. Man hat ihn damals noch überirdisch gefunden und musste nicht tief graben.

Versuchsbeschreibung
In einer Verbrennungsschale wird Kohlenstoff (fein) verteilt und eine Mulde gebildet. Hinein wird schwarzes Kupfer(II)-oxid gefüllt. Alles wird leicht mit C bedeckt. Mit einem feinen Stab (z.B. Schaschlikstab) werden wenige Löcher hineingestochert! 10-15 min bei geschlossenem Deckel erhitzen! Dann alles in ein Becherglas mit Wasser kippen, damit es sauber wird.
Beobachtung
Exotherme Reaktion, rötliches Produkt am Boden,
Eine anschließende Untersuchung des entstehenden Gases mit Kalkwasser zeigt eine Trübung des Kalkwassers.
Schlussfolgerung

es liegt eine Redoxreaktion vor, da Sauerstoff zwischen Kupfer und Kohlenstoff ausgetauscht wird. Kohlenstoffdioxid kann man in einem Bestätigungsexperiment durch den Kalkwassertest nachweisen.
Aufgaben:
- Formuliert mal eine Reaktionsgleichung, die kennzeichnend für die Eisenzeit ist.
- Welche Gefahr besteht beim Erhitzen des Glasrohrs, wenn es mit Wasserstoff durchflutet wird?
Informationen zur Bronzezeit
In dieser Periode begannen die Menschen erste Werkzeuge aus Bronze herzustellen. Dazu war Kupfer notwendig, welches sie aus Kupferoxid gewonnen hatten. Der Beginn dieses wichtigen Zeitabschnittes war ab ca. 3000 Jahre v. Chr.
Bronze war das wichtigste Rohmaterial v. a. für Schmuckgegenstände und Waffen. Für die Herstellung der Bronze brauchte man Kupfer (Bronze = 60% Kupfer plus Zinn und manchmal etwas Zink). Ein solches Gemisch von Metallen nennt man Legierung.
Das Wort Kupfer kommt übrigens vom Wort Cypern, da wahrscheinlich dort, die erste europäische Produktion begann. Viele Jahrtausende vorher konnten allerdings schon die Chinesen Bronze herstellen. Weitere frühe Funde stammen aus Anatolien und Ägypten. Dort wurde Kupfererz wurde schon vor 6000 v. Chr. verhüttet. In Mitteleuropa ist die Verarbeitung von Kupfererz seit etwa 3000 v. Chr. bekannt.
| frühe Bronzezeit | (Anfang 17.Jh.-16. Jh. v. Chr.) |
| mittlere Bronzezeit | (15. bis 13.Jh. v. Chr.) |
| späte Bronzezeit | (12.-9.Jh. v. Chr.) |
Abgelöst wurde die Bronzezeit durch die Eisenzeit, in der Bronze zwar weiterhin für Kult- und Alltagsgegenstände verwendet, in der Technik und Waffenherstellung aber vom Eisen verdrängt wurde.
Die Erfindung der Bronze führte auch zu Fortschritten in Handel und Seefahrt. Schließlich mussten auch die Rohstoffe transportiert werden. Es bildeten sich in dieser Periode wichtige Städte, an Flüssen und am Meer entstanden viele neue Häfen. Dies führte zu einer Entwicklung der Kulturen im größten Teil Europas, in Teilen Nordafrikas und in vielen Teilen Asiens.
Heute weiß man darüber einiges, da man viele historische Funde untersucht und genau datiert hat. Zu den Funden gehören Schmuckstücke (Armringe, Ketten, Schnallen, Nadeln) und Waffen (Messer, Dolche, Äxte, Pfeilspitzen, Schwerter).
Zusatzinformationen:
Aufgaben:
Vervollständige die folgenden Reaktionsgleichungen, kennzeichne Oxidation und Reduktion:
| Mg | + | H2O | ? + ? | |
| Pb | + | C | ? + ? | |
| Mg | + | CO2 | ? + ? | |
| H2 | + | O2 | ? + ? | |
| CuO | + | Zn | ? + ? | |
| CuO | + | Mg | ? + ? |
Eisen, das wichtigste Metall
- Eisen kommt nicht elementar (gediegen) vor, sondern nur vereinigt als Erz (z.B. mit Sauerstoff).
- Eisen ist zusammen mit Nickel vermutlich der Hauptbestandteil des Erdkerns.
- Mit einem Anteil von fünf Prozent ist Eisen aber auch eines der häufigsten Elemente der Erdkruste.
- Eisen ist das zehnthäufigste Element im Universum.
- Eisenerz wird im Tagebau (Brasilien, Australien, China u.a.) und Untertagebau (Deutschland, Frankreich u.a.) gewonnen.
- Eisen ist mit 95% das weltweit am häufigsten genutzte Metall.
- Wenn Eisen oxidiert, bildet es keine feste Schutzschicht. Der dabei entstehende Rost zerstört Eisen vollständig.
- Stähle sind Legierungen des Eisens mit 0,002 % bis 2,06 % Kohlenstoff (und anderen Metallen).
- Eisen ist eines von drei ferromagnetischen Metallen (Kobalt und Nickel sind die übrigen).
- Obwohl Eisen ein wichtiges Spurenelement für den Menschen ist, kann zu viel Eisen im Körper giftig sein.
In der Natur kommt Eisen (fast) nie gediegen (d.h. als Element) vor. Bekannte Eisenverbindungen sind:
- Fe2O3 sowie FeO (Eisenoxid)
- Fe3C (Eisencarbid)
- Fe(CO)5 (Eisencarbonyl) sowie Fe2(CO)9
- Fe(SCN)3 (Eisen(III)-thiocyanat, Eisenrhodanid)
Zusatzinformationen:
Die Eisenzeit
In Mitteleuropa beginnt die Eisenzeit etwa ab dem 8. Jahrhundert v. Chr. Sie begann aber schon vorher in Anatolien ca. 1200 v. Chr. Diese Methode verbreitete sich von dort nach Indien, China und den Mittelmeerraum. Über Italien gelangte das Wissen dann nach Nordeuropa. Die Eisenzeit ist nach der Steinzeit und der Bronzezeit die dritte Periode der Menschheitsgeschichte. In Europa und dem Mittelmeerraum folgte darauf die Antike oder die Völkerwanderungszeit.
In dieser Zeit entdeckten die Menschen einen Weg, nun auch Eisenoxid zu reduzieren, um daraus Eisen für Werkzeuge und Waffen herzustellen.
Die Thermit®-Reaktion

Material: Blumentopf, Alufolie, Magnesiumpulver, Magnesiumband (oder eine Wunderkerze), Aluminiumpulver, Aluminiumgrieß, rotes Eisenoxid.
Diese Reaktion dient dazu, Eisen aus dem Oxid herzustellen. Der Reaktionspartner ist dabei das unedlere Aluminium. Diese Reaktion ist stark exotherm - man muss also mit höchster Vorsicht arbeiten und dringend eine feuerfeste Unterlage benutzen. Es kann passieren, dass mehrere tausend °C heißes Metall herumspritzt, daher Schutzbrille aufsetzen und Sicherheitsabstand einhalten!
Versuchsbeschreibung
Mischen von 15 g getrocknetem Fe2O3 und 5 g Al-Grieß (oder Pulver), ebenfalls trocken. Das Gemisch gibt man in einen Blumentopf, in welchem eine Toilettenpapierrolle steht. Der Rand wird mit Sand gefüllt. Auf das Gemisch gibt man etwas Magnesiumpulver und zündet alles mit einem Magnesiumband oder einer geeigneten Wunderkerze.

Beobachtung
heftige Reaktion mit heller Flamme, Funken, sehr heißes, rot glühendes, flüssiges Produkt, welches magnetisch ist.
Schlussfolgerung
Bei der Reaktion von Eisenoxid mit Aluminium entsteht Eisen. Dabei werden sehr große Energiemengen frei. Diese Reaktion wird z. B. zum Schweißen von Eisenbahnschienen verwendet.
Der Hochofen
Bei der Thermit®-Reaktion entsteht stark verunreinigtes Eisen. Es ist durchzogen mit Resten von Aluminiumoxid. Außerdem wäre Aluminium ein sehr teurer Reaktionspartner, um Eisen herzustellen. Großtechnisch gibt deshalb einen anderen (besseren & preiswerteren) Weg, große Eisenmengen herzustellen. Die dazu notwendige Industrieanlage nennt sich „Hochofen“.
Betrachtet man mal ein Bild einer Eisenhütte mit Hochofenanlage, ist man über die Größenverhältnisse erstaunt. Ein kleiner Fleck auf dem Bild könnte ein Schiff sein, welches gerade voll beladen ist mit dem Ausgangsstoff Eisenoxid.
Mögliche Eisenerze als Ausgangsstoffe:
| Formelzeichen | Name |
| FeO | Eisenoxid, auch Magnetkies genannt |
| Fe2O3 | Hämatit (=Roteisenstein) |
| Fe3O4 | Magnetit |
| FeCO3 | Siderit (=Eisenspat oder auch Spateisenstein genannt) |
| FeS2 | Pyrit (Eisenkies bzw. Katzengold genannt)) |
Wozu ist eine so große Anlage notwendig? brauchen wir alle denn soviel Eisen? Ja, man kann leicht den Jahresverbrauch eines Landes durch die Anzahl der Einwohner teilen und stellt fest, dass jeder Mensch in Deutschland pro Jahr mehr als 100 kg Eisen „benötigt“. Dies wird natürlich nicht nur für Dinge des Haushalts verwendet, sondern auch für Autos, Brücken, Autobahnleitplanken usw.
Im Hochofen entsteht Roheisen. Der Reaktionspartner des Eisenoxid ist hierbei Koks (ausgeglühte Steinkohle). Als Konsequenz enthält das entstehende Roheisen 4-5 Prozent Kohlenstoff als Verunreinigung und ist dadurch recht spröde. Will man eine bessere Qualität erreichen, muss man das Roheisen veredeln.
Gusseisen enthält 2 - 6,5% Kohlenstoff und weitere Legierungselemente, wie beispielsweise Silizium und Mangan. In Abhängigkeit von der Abkühlgeschwindigkeit liegt der Kohlenstoff im Gusseisen als Karbid oder elementar als Graphit vor. Gusseisen ist sehr hart und spröde. Es lässt sich gewöhnlich nicht verformen. Es wird z. B. verwendet für Gullydeckel.
Durch das Windfrischen, einen Vorgang zur Veredlung mit Sauerstoff, der in den heißen Stahl geblasen wird, entsteht Stahl, der zwischen 0,1% und 2,1% Kohlenstoff enthält. Im Gegensatz zu Gusseisen ist er verformbar. Durch Legieren, v. a. mit Nickel, kann er härter und rostfrei gemacht werden.
Die Vorgänge im Hochofen
- nach Hochofen
Ein Hochofen ist eine Anlage in Schachtofenbauweise, in der Eisen durch Reduktion von Eisenoxid gewonnen wird. Er ist meist zwischen 25-30 m hoch, die Gesamtanlage kann bis zu 60 m hoch sein.
Der Hochofen wird schichtweise mit zwei wesentlichen Rohstoffen von oben gefüllt: dem so genannten Möller (=als Träger des Eisenoxids und mit Zuschlagstoffen wie Kalk und Kies), und dem Hochofenkoks als Energieträger und Reduktionsmittel. Die Rohstoffe werden mit Förderkübeln über einen Schrägaufzug zur Einfüllöffnung oben am Hochofen befördert und entleert.
Am Fuß des Hochofens oxidiert das aus Koks und Sauerstoff aus der Luft gebildete Kohlenstoffmonoxid zu Kohlenstoffdioxid, der dazu notwendige Sauerstoff wird dem Eisenoxid entzogen, das dadurch zu Eisen reduziert wird.
- Verbrennung des Koks, liefert Verbrennungsenergie
- Erzeugung des Reduktionsmittels Kohlenstoffmonooxid
- Reduktion des Eisenoxids zu elementarem Eisen
Der verflüssigte Hochofeninhalt wird unten am Ofen durch eine Öffnung entnommen. Diese Öffnung ist normalerweise verschlossen und wird periodisch beim so genannten Abstich angebohrt. Der ausfließende Inhalt wird in der an den Ofen angrenzenden Abstichhalle über ein Rinnensystem im Boden geleitet. Die meisten Hochöfen besitzen zwei Abstichvorrichtungen: Eine für die Schlacke und eine etwas tieferliegende für das flüssige Eisen. Hier trennt die Dichte die beiden Stoffe.
Die im Hochofenprozess entstehende Schlacke ist ein wertvoller Rohstoff: sie kann nach Aufmahlen in einer Schlackenmahlanlage als Hüttenzement vielfältig eingesetzt werden.
Die Außenwand des Hochofens wird über eine Wasserkühlung permanent gekühlt. Dennoch herrschen in der Anlage Temperaturen von über 50°C. Ein Arbeiter kann sich trotz gekühlter Schutzanzüge nur wenige Minuten in der Nähe des Hochofens aufhalten.
Mittlere Hochöfen erreichen Tagesleistungen von bis zu 6.000 t, große Hochöfen von bis zu 13.000 t Roheisen.
Hochöfen sind mindestens rund 10 Jahre ununterbrochen in Betrieb. Nach dem Ende dieser so genannten Ofenreise muss der eigentliche Hochofen umfangreich überarbeitet und die Außenhaut ersetzt werden
Im Labor kann man den Hochofenversuch simulieren:
Versuchsbeschreibung
In ein Glasrohr werden Eisenoxid (pulvriges Eisen) und gekörnte Aktivkohle gefüllt. Das Rohr wird von außen erhitzt und mit einem Fön durchgepustet.
Beobachtung
Aufglühen, das rote Eisenoxid wird dunkel
Schlussfolgerung
Die Kohle verbrennt unvollständig. Es entsteht das giftige Gas Kohlenmonoxid. Das Eisenoxid reagiert mit dem Kohlenmonoxid zu Eisen.
Zusammenfassende Reaktion:
Aufgaben:
- Warum werden die Außenwände gekühlt?
- Warum wird der Hochofen nicht Nachts abgeschaltet?
- Der Hochofen hat eine nach oben auslaufende Form. Warum?
Der Hochofenprozess
Der Aufbau und die Temperaturzonen im Hochofen

Ein Hochofen ist eine bis zu 40m hohe Industrieanlage, in der Eisen aus Eisenoxid gewonnen wird. Er wird von oben mit Förderbändern oder mit so genannten „Hunten“, das sind Metallwagen auf Schienen, gefüllt. Dazu wird ein Gemisch aus Eisenoxid und Koks (das Reduktionsmittel) und Kalk zur Auflockerung gebildet. Dieses Gemisch wird auch Möller genannt.
In oberen kälteren Regionen reagiert Fe2O3 in geringer Hitze zu dem Zwischenprodukt Fe3O4, welches aufgrund seiner höheren Dichte weiter absinkt. Weiter unten ist es durch die ablaufenden Redoxreaktionen und durch zugeführte heiße Luft viel heißer. Hier findet die Umwandlung von Fe3O4 zu einem weiteren Zwischenprodukt satt (FeO). Dies hat eine noch höhere Dichte und es sinkt noch weiter ab. Im heißesten Bereich finden dann die Hauptreaktion statt, bei der aus Kohlenmonoxid und Eisenoxid dann Kohlenstoffdioxid und Roheisen entstehen. Aufgrund seiner hohen Dichte sammelt sich das Roheisen am Boden des Hochofens (darauf schwimmt nur noch die Schlacke aus Kalk und Erzresten, welche alle eine geringere Dichte als Roheisen haben). Das Roheisen wird dann durch eine Keramiköffnung regelmäßig entnommen. Man lässt es über Rinnen im Boden der Abstichhalle fließen.
Die als Abfallprodukt entstehende Schlacke ist ein wichtiger und auch wertvoller Rohstoff. Sie dient beispielsweise als Hüttenzement.
Genaue chemische Reaktionen im Hochofen
- Energie liefernde Verbrennung des Kokses.
- Erzeugung des gasförmigen Reduktionsmittels Kohlenstoffmonoxid.
- Reduktion des Eisenoxids zu elementarem Eisen.
- Es entsteht der stärker eisenhaltige Magnetit (Magneteisenstein).
- Es entsteht Eisen(II)-oxid.
- Es entsteht metallisches Eisen, das sich unten im Hochofen ansammelt.
- Eisenoxid und siliziumhaltiges Roheisen reagieren zu Eisen (Stahl) und Siliziumdioxid.
Zusatzinformationen
Veredelung des Roheisens
„Windfrischen“
Roheisen aus dem Hochofen ist verunreinigt und besitzt einen viel zu hohen Kohlenstoffgehalt. In flüssiges (kohlenstoffhaltiges) Roheisen wird bei hohen Temperaturen Sauerstoff geblasen. Das Eisen wird wegen der hohen Temperatur nicht oxidiert, aber der Kohlenstoff vereinigt sich umgehend. Es entsteht das Gas Kohlenstoffdioxid, welches den Reaktionsraum verlässt. Das Roheisen wird nun Stahl genannt und enthält nun deutlich weniger Kohlenstoff und ist damit qualitativ wesentlich hochwertiger.
Durch weitere Zusätze, wie z. B. Chrom oder Nickel kann der Stahl weiter veredelt werden. Cr / Ni - Stahl („Nirosta“)
Energiebeteiligung bei chemischen Reaktionen
Tipp: Flipchartähnliche Pappen bauen und mit Magneten von Schülern in Diagramme setzen lassen
Versuchsbeschreibung

Beobachtung
- selbstständiges, heftiges Durchglühen
- Rauchbildung
- weißlicher Feststoff
Schlussfolgerung
Zink vereinigt sich mit Schwefel zu Zinksulfid unter Energiefreisetzung.
| 0 | 0 | +II-II | ||
| Zn | + | S | ZnS + E |
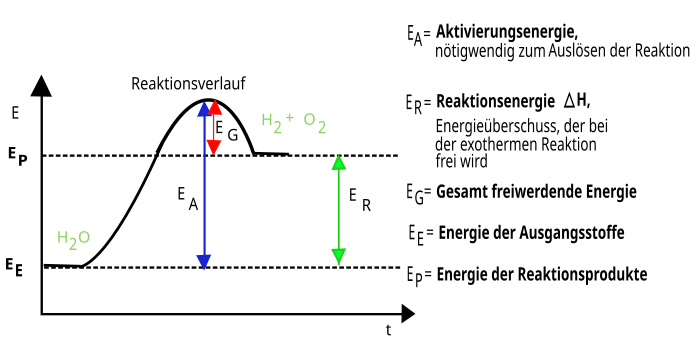
Energiediagramm (exotherme Reaktion)

Die freiwerdende Energie kann dabei als Wärme, Licht oder in anderen Formen vorliegen. Chemische Reaktionen, bei denen ständig Energie zugeführt werden muss,
damit sie überhaupt ablaufen, nennt man endotherme Reaktionen.Energiediagramm (endotherme Reaktion)
| exotherme Reaktionen | endotherme Reaktionen |
| Verbrennungen (Kohle, Magnesium usw.) | Erhitzen von Kaliumnitrat und Kalium |
| Entzündung von Schwefel-Eisen-Gemisch | Zersetzung von Quecksilberoxid |
| Neutralisation | Zersetzung von Wasser |
| Magnesium mit Salzsäure | |
Neutralisation (lässt sich leicht zeigen)
|
Der Katalysator
Versuchsbeschreibung
Verbrennung von Zuckern mit und ohne Braunstein (Asche)
| V | B | S |
| Entzünden von Zucker | Karamellisation | Änderung des Aggregatzustandes |
| Entzünden von Zucker-Braunstein Gemisch | Zucker brennt | Zucker brennt Aufstellen der Gleichung mit Oxidationszahlen. |
| 0 +I -II | 0 | IV-II | +I -II | |||||
| C6H12O6 | + | 6O2 | 6CO2 | + | 6H2O | + | E |
Aufgaben:
Entscheide bei folgenden Reaktionen, ob es sich um einen exo- oder endothermen Vorgang handelt!
- Beim Entladungsvorgang einer Autobatterie werden Bleiverbindungen verändert, und elektrische Energie wird abgegeben.
- Holz wird zum Heizen von Häusern verwendet.
- Der Mensch und viele Wirbeltiere sind gleichwarm: Die Körpertemperatur bleibt aufgrund der chemischen Umsetzung von Nährstoffen und Sauerstoff bei der Atmung konstant.
- Die Explosionen in Verbrennungsmotoren werden in mechanische Energie umgewandelt.
- Bauxit enthält einen großen Prozentsatz an Aluminiumoxid. Die Gewinnung von Aluminium wird stets dort durchgeführt, wo billige elektrische Energie zur Verfügung steht.
- Quecksilberoxid lässt sich durch Erhitzen in Quecksilber und Sauerstoff zerlegen. (Zersetzung)
- Pflanzen speichern bei der Photosynthese Sonnenenergie in chemischer Form in energiereichen Verbindungen (Traubenzucker, Sauerstoff).
- Eine starke Säure einer Autobatterie wird zum Entsorgen neutralisiert
Übung: Reduktions- und Oxidationsvermögen von Metallen I
Material: je Gruppe: Bunsenbrenner, Reagenzglasklammer, 2 Reagenzgläser,
Führe diese Versuche nicht außerhalb des Chemieunterrichts durch! Sie sind sehr gefährlich und unberechenbar!
Kann man eigentlich durch das pure stattfinden von Reaktionen beurteilen, ob ein Metall edler oder unedler als ein anderes ist? Führe dazu die folgenden beiden Versuche durch und entscheide, welches der beiden Elemente edler ist.
| Oxidationsmittel: | CuO | (wird bei Redoxreaktion reduziert) |
| Reduktionsmittel: | Fe | (wird bei Redoxreaktion oxidiert) |
CuO ist Ox-Mittel für Eisen, Cu aber nicht für FeO
Der edlere Stoff lässt sich „schwerer“ oxidieren und ist eher bereit seinen Sauerstoff abzugeben

Reduktions- / Oxidationsvermögen einiger Metalle und Nichtmetalle II
Problemstellung: Kann man weitere Metalle/ Metalloxide in diese Reihe von edeln und unedlen Metallen einordnen (und wie geht man experimentell am einfachsten vor?)
Führe diese Versuche niemals selbst durch!
Sie sind sehr gefährlich und unberechenbar!

Wiederholungsfragen für Zuhause & das Schwimmbad
Verschwenderisch leichte Wiederholungsfragen (Klasse 8 und Klasse 9)
- Wiederhole die Elementsymbole. Erstelle dann eine Übersicht über alle Elemente, die auf „-stoff“ enden.
- Beschreibe, was man erhält, wenn man Säure und Lauge gleicher Konzentration mischt. Wie nennt man diese Reaktion? Was ist bei deren Durchführung zu beachten?
- Nenne 6 Säuren und 3 Laugen mit Formel!
- Was sagt der Massenerhaltungssatz aus? Was sagt der Energieerhaltungssatz aus?
- Stelle die Reaktionsgleichung der Bildung folgender Stoffe auf: Fe2O3 ; Schwefeldioxid ; Schwefeltrioxid ; P4O10. Welcher Stoff entsteht, wenn man Phosphoroxid und Wasser mischt?
- Welcher Stoff entsteht, wenn man Kohlenstoffdioxid und Wasser mischt?
- Stickstoffdioxid reagiert mit Wasser zu Salpetersäure und Salpetriger Säure. Erstelle die Reaktionsgleichung.
- Wenn Du unsicher mit Reaktionsgleichungen bist, löse noch einmal einige Gleichungen von den 3 Reaktionsgleichungs-Arbeitsblättern
Fragen zum Periodensystem und zum Atombau
- Nach welchen Kriterien ist das PSE aufgebaut? Erkläre dazu die Begriffe Hauptgruppen, Perioden & Ordnungszahl, Alkalimetalle, Erdalkalimetalle, Halogene und Edelgase!
- Woran kann man erkennen, dass das Elemente im PSE nicht nach der Massenzahl angeordnet sind?
- Zeichne den kompletten Aufbau der folgenden Atome (welche von Ihnen haben Edelgaskonfiguration?): Bor, Lithium, Helium, Silicium. Calcium.
Fragen zu Metallen, Redoxreaktionen & Energiediagramm
- Erkläre den Versuch zur Reduktion von Kupferoxid!
- Was versteht man unter Oxidation, Reduktion und Redoxreaktion? Erkläre mit einem Beispiel!
- Woran erkennt man Redoxreaktionen?
- Liegt bei dem Luftballon-Explosionsversuch eine Redoxreaktion vor? Begründe mit einer Reaktionsgleichung!
- Nenne drei Wege (mit Reaktionsgleichung) aus CuO das metallische Element zu gewinnen!
- Was ist der Hochofenprozess? Erkläre umfassend !
- Beschreibe das Thermit®-Verfahren!
- Wie unterscheidet sich der Hochofenprozess vom Thermit®-Verfahren, wo liegen Gemeinsamkeiten?
- Wie kann aus Bleioxid (PbO) Sauerstoff und Blei gewonnen werden?
- Ist die Zersetzung von Wasser eine Redoxreaktion? Zeichne den Versuchsaufbau und begründe!
- Kann man zu Kohlenstoffdioxid verbrannten Kohlenstoff wieder zurückgewinnen? (schwere Aufgabe)
- Zum Knobeln: Benzin (C8H18) verbrennt an der Luft zu Wasser und Kohlenstoffdioxid. Erstelle die Reaktionsgleichung und dass passende Energiediagramm. Liegt eine Redoxreaktion vor? Begründe.
- Erkläre die Begriffe „endotherme Reaktion“ und „exotherme Reaktion“ mit je einer Beispielreaktion und zeichne das passende Energiediagramm. (Vergisst Du die Achsen zu beschriften, schreibe alle Fragen 137 mal ab!!!)
- Was ist ein Katalysator? Nenne Aufgaben und beschreibe sein Verhalten z. B. bei der Verbrennung von Zucker. Erstelle die Reaktionsgleichung [Zucker: C6H12O6] und zeichne anschließend ein Energiediagramm der katalytischen Zuckerverbrennung.
- Vergleiche Kupfer und Eisen hinlänglich ihrer Eigenschaften.
- Nenne Eigenschaften von Aluminium? Wie wird es herstellt?
- Ist Natrium ein Metall? Welche typischen Metalleigenschaften erfüllt es, welche nicht?
- Ein Stück Natrium wird auf Wasser gelegt. Beschreibe die Reaktion. Stelle die Reaktionsgleichug auf. Liegt eine Redoxreaktion vor?
- Ist die folgende Aussage richtig? „Die Alkalimetalle zeigen eine Abstufung der Eigenschaften“.
- Gilt diese Aussage auch für die Halogene?
- Vergleiche die Reaktion von ZnO + Cu mit der Reaktion von CuO + Zn. Welches der beiden Metalle ist edler?
- CuO reagiert mit Mg explosionsartig. Stelle eine Reihung (edel/ undel) der Metalle Au, Ag, Cu, Mg, Na und Zn auf
- In der Natur kommen die meisten Metalle als Oxid vor (also nicht als Element). Gold, Silber und Kupfer hingegen auch in gediegener Form (= als Element). Was vermutest Du als Ursache?
- Warum hat die „Erfindung“ der Eisenherstellung länger gedauert als die der Kupferherstellung?
- Ist Bronze ein Element?




















