Innere Medizin kk: diffus großzelliges B-Zell-Lymphom
Zurück zur Übersicht

Das Wichtigste
[Bearbeiten]- Das diffus großzellige B-Zell-Lymphom (DLBCL) ist eine bösartige Erkrankung des lymphatischen Systems
- Es ist mit 30% das häufigste Non-Hodgkin-Lymphom bei Erwachsenen.
- Die Diagnose ergibt sich vor allem aus einer Lymphknotenentnahme und Gewebsuntersuchung.
- Ausdehnung und Befalls der Lymphknoten sieht man am besten im CT und im Ultraschall.
- Die Krankheit lässt sich meist gut mit einer Chemotherapie behandeln.
ICD
[Bearbeiten]C83 Diffuses Non-Hodgkin-Lymphom
Abk
[Bearbeiten]- DLBCL Diffus large Blood Cell Lymphoma
- Internationaler Prognostische Index (IPI)
- CHOP Therapie Schema
- R-CHOP Therapie Schema
- NHL = Non Hodgin Lymphom
Häufigkeit
[Bearbeiten]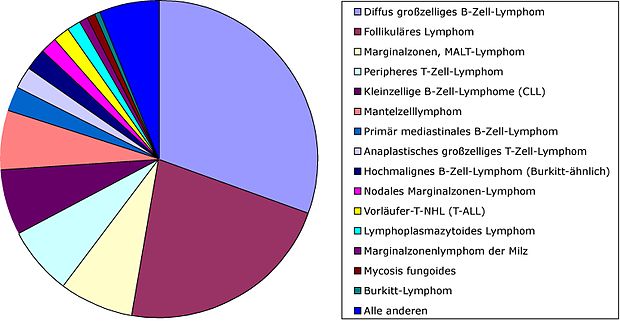
In Deutschland wurden zwischen 2009 und 2010 jeweils über 7.000 Neuerkrankungen registriert. Die Erkrankungswahrscheinlichkeit steigt mit zunehmendem Alter, wobei das durchschnittliche Erkrankungsalter bei ca 70 Jahren liegt, Männer sind etwas häufiger betroffen als Frauen.
Pathogenese und Ursachen
[Bearbeiten]Die molekulare Pathogenese des DLBCL ist komplex und betrifft unter anderem das BCL-6-Gen auf Chromosom 3 (BCL-6 ist ein Transkriptionsrepressorprotein), bei ca 30% der DLBCL ist dieses Gen verändert. Eine andere mit 30% ebenfalls häufige Mutation ist die Translokation t(14;18) im BCL2-Gen, dessen Protein-Produkt die Apoptose normalerweise hemmt. Letztere Mutation geht mit einer schlechten Prognose einher.
Risikofaktoren für die Entstehung eines DLBCL (wie für alle malignen Lymphome) können sein:
- primäre oder erworbene Störungen des Immunsystems
- z.B. Immunsuppression, Autoimmunerkrankungen, chronische Antigenstimulation
- vorausgegangener M. Hodgkin
- virale (z.B. Hepatitis-C) und bakterielle Infektionen
- genetische Prädispositionen
- eventuell Exposition gegenüber chemischen Noxen
Ein DLBCL kann sich auch sekundär aus einem niedrigmalignen Lymphom entwickeln, zB aus einer CLL, einem follikulären Keimzentrums Lymphom, einem Immunozytom oder einem MALT-Lymphom.
Subgruppen
[Bearbeiten]Das DLBCL wird nach der Kiel-Klassifikation in folgende morphologische Subgruppen unterteilt:
- Zentroblastisches Lymphom (häufigste Form und bessere Prognose als immunoblastisches)
- immunoblastisches Lymphom
- T-Zell- oder Histiozytenreiches Lymphom (ungünstigere Prognose)
- Anaplastisches Lymphom
Klinisch wird das DLBCL nach primärem Befall unterteilt:
- 60% sind primär nodal
- extranodale Lymphome , häufig Magen-Darm-Trakt (Cave: ist kein MALT-Lymphom)
Seltenere klinische Formen sind als eigene Krankheitsentitäten aufzufassen:
- das primär mediastinale Lymphom (etwa 10%), betrifft v.a. jüngere Patienten und manifestiert sich mit Atembeschwerden und oberer Einflussstauung
- das intravaskuläres Lymphom ist selten und kann sich in der Haut, den Nieren, der Lunge oder dem ZNS manifestieren
- primäre Körperhöhlen-Lymphome, ebenfalls selten, eine Manifestierung als primäres Ergusslymphom ist möglich
Klinik/Symptome
[Bearbeiten]Die meisten Beschwerden sind uncharakteristisch. Bei dem primär nodalen DLBCL fällt die rasch zunehmende meist schmerzlose Lymphknoten- oder Milzschwellung auf. Bei extranodalem Befall treten unterschiedliche Symptome auf
- bei Befall des Magen-Darm-Trakts (meist Magen oder Ileozökal) kommt es zu Verddauungsbeschwerden, Blutungen oder aber auch nur zu diffuser Zunahme des Bauchumfangs.
- beim primär mediastinalen Lymphom Atembeschwerden/ Einflussstauung
- seltenere siehe oben
Nur etwa 10-20% der Patienten entwickeln eine B-Symptomatik mit
- Fieber,
- Schweißausbrüchen,
- und/oder Gewichtsverlust
Wenn sich das DLBCL im Knochenmark ausbreitet, kann es zu einer Hemmung der normalen Blutbildung mit entsprechenden Panzytopenie-Symptomen kommen.
Diagnostik
[Bearbeiten]
- Anamnese und körperliche Untersuchung (v.a. Lymphstationen, Leber, Rachenring)
Staging:
- Labor:
- Blutbild, Diff-Blubild, LDH, Eiweißelektrophorese, Im Verlauf: Elektrolyte und Harnsäure (Tumorlysesyndrom), Vitamin D Bestimmung bei Rituximab-Gabe
- Infektionsserologie v.a. auch vor der Therapie: Hep-Viren, Toxoplasmen, CMV, EBV,
- Rö-Thorax, Abdomen-Sono, CT Hals, Brust- und Bauchraum und Becken, international empfohlen ist die PET-CT, je nach Beschwerden evtl ÖGD/Coloskopie
- Histologische Sicherung: Biopsie (chirurgisch oder in Ausnahmen mit Stanznadel) und KM-Punktion. Charakteristisch sind die Oberflächenmarker CD20, an das zum Beispiel auch der zur Therapie eingesetzte monoklonale Antikörper Rituximab bindet, sowie CD19, CD22 und CD79a. Wichtig ist auch die Information, wie teilungsaktiv die Lymphomzellen sind, was mit dem Ki67-Antikörper untersucht wird.
- bei KM-Befall Lumbalpunktion
Differentialdiagnosen
[Bearbeiten]Therapie
[Bearbeiten]Die Therapieintention ist primär kurativ. Standard-Strategie für das diffus großzellige B-Zell-Lymphom ist die R-CHOP:
- R für anti-CD20 Antikörper Rituximab (Hierfür vorher Vit D bestimmen)
- C Cyclophosphamid
- H Doxorubicin
- O Vincristin
- P Prednison oder Dexamethason
R-CHOP kann im Abstand von zwei (R-CHOP-14) oder drei Wochen (R-CHOP-21) gegeben werden, wobei R-CHOP-14 bei bestimmten Patientengruppen anscheinend bessere Ergebnisse erzielt als R-CHOP-21. Die Anzahl der R-CHOP-Durchgänge (= Zyklen) richtet sich nach dem IPI (Risikoscore) und bewegt sich meist zwischen sechs und acht Zyklen. Bei jungen Hochrisikopatienten werden in der Regel acht Zyklen mit R-CHOEP-14, bei dem über drei Tage zusätzlich Etoposid (= E) gegeben wird.
Komplikationen
[Bearbeiten]Bei großer Tumorlast ( sogenannte Bulk-Disease ) und bei Befall des Darms sind die massiven Nekrosen zu bedenken, die während und nach der Chemotherapie durch Einschmelzung der Tumormasse entstehen. Es besteht hierbei die Gefahr einer Darmperforation. Ebenso kann es zum sogenannten Tumorlysesyndrom kommen. Man erkennt es an einer massiven Kalium-, Calcium-, und Harnsäureerhöhung durch den schnellen Zelltod der Tumorzellen. Hierfür sollte prophylaktisch Allopurinol (300mg 1-0-0) gegeben werden und eine großzügige Flüssigkeitsgabe erfolgen. Unter Immunsuppression kann es zu Infektionen kommen. Charakteristisch sind Infekte mit Pneumocystis jiroveci. Hier bietet sich eine Prophylaxe und Therapie mit Cotrimoxazol, an.
Prognose
[Bearbeiten]Wird das diffus großzellige B-Zell-Lymphom nicht behandelt, so behindern Anhäufungen von Lymphomzellen die Funktion der betroffenen Organe und können innerhalb von wenigen Monaten zum Tod führen. Andererseits reagieren die sich schnell teilenden Zellen sehr empfindlich auf Chemotherapie, Strahlentherapie und Immuntherapie mit monoklonalen Antikörpern, so dass die überwiegende Mehrheit der Patienten mit dieser Erkrankung heute geheilt werden kann. Dies gelingt mittlerweile bei 80 Prozent aller Patienten, wobei die Heilungsraten zwischen 50 Prozent (ältere Hochrisikopatienten) und 98 Prozent (junge Niedrigrisikopatienten ohne Bulk) liegen. Alle DLBCL-Patienten, die nach einer adäquaten Behandlung zwei Jahre ohne Rückfall bleiben, haben eine normale Lebenserwartung
Nachsorge
[Bearbeiten]Im ersten Jahr nach Abschluss der Therapie alle drei Monate: • Befragung des Patienten nach dessen Gesundheit und Wohlbefinden (= Zwischenanamnese) • körperliche Untersuchung • Kontrolle der Laborwerte • bildgebendes Verfahren (CT Hals, Kopf, Bauch- und Brustraum sowie Becken) Im zweiten Jahr können die Abstände der Nachsorgeuntersuchungen auf vier Monate, danach auf sechs Monate bis zur Vollendung des fünften Jahres nach Therapieende ausgedehnt werden. Praktisch alle Rezidive treten innerhalb der ersten zwei Jahre nach Abschluss der Primärtherapie auf.
Weblinks
[Bearbeiten]- https://www.onkopedia.com/de/onkopedia/guidelines/diffuses-grosszelliges-b-zell-lymphom/@@view/html/index.html
- Gute ausführliche Übersicht
