Organische Chemie für Schüler/ Kohlenstoff als Bindungspartner
Die Atombindung bei Wasserstoff & Kohlenstoff
[Bearbeiten]-
Punkt-Kreuz-Diagramm
-
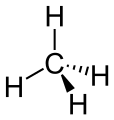
CH4
-
2 e- sind jeweils ein Strich
Ionen gibt es nur in Kristallen oder gelöst in Wasser. Bei Kohlenwasserstoffen liegt beides nicht vor.
Sie verbinden sich mit einer anderen Methode, der Atombindung. Dazu überlappen die äußeren Elektronenwolken und bilden einen gemeinsamen Bereich (dieser wird auch Molekülorbital genannt[1]). Damit gehört das Valenzelektronen-Paar beiden Atomen in gleicher Weise und sie erhalten Edelgaskonfiguration.
Vom Kohlenstoffatom gehen in der Regel 4 Elektronenpaarbindungen ab (oder es liegen Doppel- oder Dreifachbindungen vor, dann sind es entsprechend weniger). Meistens ist Kohlenstoff dabei mit Kohlenstoff oder mit Wasserstoff verknüpft (aber auch Sauerstoff, Schwefel und Stickstoff (u.a.) sind möglich). Je länger dabei eine Kohlenstoffkette ist, desto fester und dickflüssiger wird eine Substanz.
Tipp: Bei Problemen mit dem Erstellen von Atombindungen, lies nochmals das Arbeitsblatt „Regeln zum Erstellen von Valenzstrichformeln“ im Kapitel „Atombindung“.
Kohlenstoff als Bindungspartner
[Bearbeiten]Kohlenstoff ist ein Element der 4. Hauptgruppe, d.h. es hat vier Außenelektronen. Es fehlen also 4 Valenzelektronen zum Erreichen der Edelgaskonfiguration. Das Ausbilden von 4 Atombindungen bietet sich an, um diesen Zustand zu Erreichen. Dabei bilden die Außenelektronen des Kohlenstoffatoms mit den Außenelektronen der Reaktionspartner gemeinsame Bindungselektronenpaare. Am stabilsten sind dabei Kohlenstoff-Kohlenstoff-Bindungen.
-
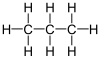
Butan
-
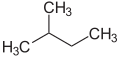
iso-Pentan
-
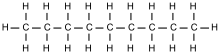
Cyclo-Hexan
Beim Verbrennen organischer Substanzen wird viel Energie freigesetzt. Diese stammt aus den Bindungen und wird von den Menschen bei der Verbrennung fossiler Brennstoffe (Erdöl, Erdgas), Holz und Kohle genutzt. Auch die Verbrennung von Kunststoffen in Müllverbrennungsanlagen setzt diese Energie frei. Kein Wunder, denn auch Kunststoffe sind Kohlenwasserstoffverbindungen.
Kettenförmige Kohlenwasserstoffe (ohne Mehrfachbindungen) nennt man Alkane. Ringförmige entsprechend Cycloalkane. Ketteförmige Kohlenwasserstoffe mit Doppelbindungen, werden Alkene, mit Dreifachbindungen Alkine genannt.
Die einfache Verknüpfung von Kohlenstoff mit anderen Nichtmetallen über Atombindungen ermöglicht eine schier unendliche Anzahl an möglichen Kombinationen. Mehr als 5 Millionen sollen in der Natur zu finden sein! Im Labor entstehen täglich neue.
Obwohl in der anorganischen Chemie viel mehr Elemente reagieren, sind bisher nur ca. 150 000 Verbindungen bekannt. Im Vergleich dazu schätzt man die Anzahl an organischen Verbindungen auf ca. 10 Millionen.
Ausnahmen: Kohlenstoffverbindungen, die als anorganisch gelten.
- Oxide des Kohlenstoffs (z.B. CO, CO2)
- Kohlensäure (H2CO3)
- Salze der Kohlensäure (z.B. Kalk CaCO3)
Die homologe Reihe der Alkane
[Bearbeiten]Zusatzinformationen:
Eigenschaften der Alkane - Schmelz- und Siedepunkte
[Bearbeiten]| Kettenlänge | Name | Smp. [°C] | Sdp. [°C] | Kettenlänge | Name | Smp. [°C] | Sdp. [°C] |
|---|---|---|---|---|---|---|---|
| CH4 | Methan | -183 | -161 | C16H34 | Hexadekan | 18 | 287 |
| C2H6 | Ethan | -183 | -88 | C17H36 | Heptadekan | 21 | 302 |
| C3H8 | Propan | -189 | -42 | C18H38 | Oktadekan | 29 | 317 |
| C4H10 | Butan | -138 | -0,5 | C19H40 | Nonadekan | 33 | 330 |
| C5H12 | Pentan | -130 | 36 | C20H42 | Eicosan | 36,7 | 343 |
| C6H14 | Hexan | -95 | 69 | C21H44 | Henikosan | 40,5 | 356 |
| C7H16 | Heptan | -91 | 98 | C22H46 | Dokosan | 42 | 370 |
| C8H18 | Oktan | -57 | 126 | C23H48 | Trikosan | 49 | 380 |
| C9H20 | Nonan | -51 | 151 | C24H50 | Tetrakosan | 52 | 391 |
| C10H22 | Dekan | -30 | 174 | C25H52 | Pentakosan | 54 | 402 |
| C11H24 | Undekan | -26 | 195 | C26H54 | Hexakosan | 56,4 | 412 |
| C12H26 | Dodekan | -12 | 215 | C27H56 | Heptakosan | 59,5 | 442 |
| C13H28 | Tridekan | -5 | 234 | C28H58 | Octakosan | 64,5 | 432 |
| C14H30 | Tetradekan | 5,5 | 253 | C29H60 | Nonakosan | 63,7 | 440 |
| C15H32 | Pentadekan | 9,9 | 270 | C30H62 | Triakontan | 65,8 | 450 |

Was macht die Alkane so besonders?
[Bearbeiten]- Die von Methan abgeleiteten Verbindungen werden als Alkane bezeichnet.
- Alkane kommen als unverzweigte Ketten, verzweigte Alkane oder als cyclischen Alkane vor.
- Alkane mit der gleichen Summenformel, aber verschiedener Strukturformel nennt man Isomere (so gibt es zwei C4H10 Moleküle, drei C5H12 Moleküle und 4,111,846,763 mögliche C30H62 Isomere ;-) ).
- In Alkanen bilden Kohlenstoffe 4 Einfachbindungen aus, Wasserstoffe bilden immer nur eine!
- Die Alkane C1 bis C4 sind bei Raumtemperatur gasförmig. Ab C14H30 sind Alkane bei Raumtemperatur Feststoffe.
- Bei Raumtemperatur flüssige Alkane sind wasserklare Flüssigkeiten mit stark aromatischem Geruch, der an Benzin erinnert. Je länger die Kohlenstoffkette wird, desto dickflüssiger, öliger werden sie. Der Geruch lässt entsprechend nach.
- Alkane könne auch in Ringen auftreten. Man nennt sie dann Cycloalkane.
- Alkane werden auch wegen der Abwesenheit von Doppelbindungen als gesättigt bezeichnet.
- Rein kettenförmige Alkane werden auch als n-Alkane (z.B. n-Heptan) bezeichnet. Verzweigte Alkane werden als iso-Alkane bezeichnet.
- Je länger die Kohlenstoffkette (also mit zunehmender Molekülmasse), desto höher liegen Schmelz- und Siedepunkte des Alkans. Ursache sind steigenden van der Waals-Kräfte aufgrund zunehmender Kettenlänge.
Allgemeine Formel der zyklischen Alkane: Cn H2n
Lange unverzweigte Alkane bilden lineare Zick-Zack-Ketten aus.Alkangemische
[Bearbeiten]a) Paraffin
[Bearbeiten]Ein Gemisch langkettiger (C18-C45) Alkane wird als Paraffin bezeichnet. Eine allgemeine Summenformel kann somit nicht angegeben werden. Die molare Masse liegt damit zwischen 275-600 g/ mol.
Es ist weiß, mit einer leichten Transparenz. Es entsteht z.B. als Produkt der Erdöldestillation. Paraffin ist geruchlos. Hartparaffin schmilzt zwischen 50 und 60 °C, Weichparaffin bei etwa 45 °C.
- Verwendung von Paraffin
- als Kerzenwachs
- Mikrowachs
- Ceresin
- Lackpoliturzusatz
- Petroleumersatz (Brennstoff für Öllampen)
- Vaseline
- Ausgangsstoff bei der Herstellung von Kaugummi
b) Benzin
[Bearbeiten]Benzin ist eine Mischung aus verschiedenen leichten Kohlenwasserstoffen. Es befinden sich neben Alkanen auch Cycloalkane, Alkene (mit Doppelbindungen) und Alkine (mit Dreifachbindungen) im Gemisch. Benzin wird durch fraktionierte Destillation aus Erdöl oder auch im geringen Maße durch Kohleverflüssigung gewonnen.
Zusatzinformationen Paraffin Benzin
Isomerie
[Bearbeiten]In Campinggaskartuschen findet man in der Regel das Gas Butan, da es einen Siedepunkt von ca. 0,5°C hat, lässt es sich unter etwas Druck leicht verflüssigen. Das komprimierte Gas wird dadurch flüssig, obwohl in solchen Campinggaskartuschen nicht allzu starker Druck vorliegt.
Untersucht man das enthaltene Gas genau, so findet man meist zwei verschiedene Gase, welche allerdings eine identische Anzahl an Kohlenstoff und Wasserstoffatomen haben.
-
n-Butan, Smp.: -139 °C, Sdp.: -0,6 °C
-
iso-Butan, Smp.: -160 °C, Sdp.: -12 °C
Von Butan existieren zwei Formen, diese werden Isomere genannt. Beide sind gasförmige, farblose, gesättigte Kohlenwasserstoffe. Sie unterscheiden sich jedoch hinsichtlich ihrer Eigenschaften. Vor allem Schmelz- und Siedepunkte sowie die Dichte unterscheiden sich deutlich. In anderen Eigenschaften sind sie sich ähnlicher.
Die Ursache für die höheren Schmelz- und Siedepunkte des n-Butans liegen in der besser Ausbildung von Van der Waals-Kräften. Diese bilden sich im allgemeinen bei kettenförmigen Molekülen immer besser aus. Dadurch halten die Ketten besser „zusammen“ und man benötigt mehr Energie (in diesem Fall Temperatur) um die Moleküle so stark ins schwingen zu versetzen, dass sie den Aggregatzustand ändern.
Moleküle mit verzweigten Ketten haben immer geringere Siedepunkte als unverzweigte, weil die Van der Waals-Kräfte sich zwischen Ketten besser ausbilden als bei ungleichmäßig geformten Molekülen.
Aufgabe:
- Zeichne alle Isomere von Pentan, Hexan, Heptan usw.
Die Isomerenanzahl wächst sehr rasch mit steigender Kohlenstoffzahl.
- C7H16: 9 Isomere
- C8H18: 18 Isomere
- C10H22: 75 Isomere
- C15H32: 4347 Isomere
- C20H42: 366319 Isomere
- C30H62: 4,111,846,763 Isomere
Die Zahl der tatsächlich existierenden Isomere ist kleiner, als die Zahl der theoretisch möglichen!
Stoffvielfalt durch Isomerie
[Bearbeiten]| Butan | Pentan | Hexan | Octan |
|---|---|---|---|
| 2 Isomere | 3 Isomere | 5 Isomere | 17 Isomere |
Smp: -138,3°C Sdp: -0,5°C |
Smp: -130°C Sdp: 36°C |
Smp: -56,8 Sdp: 125,7 | |
 Smp: -159,4v°C Sdp: -11,7°C |
-159°C 28°C |
Zusatzinformationen Isomerie
Isomere von Heptan und Oktan
[Bearbeiten]- http://www.guidobauersachs.de/oc/heptanisomere.gif
- http://www.guidobauersachs.de/oc/oktanisomere.gif
Konformations-Isomerie am Beispiel des Ethans
[Bearbeiten]- H3C―CH3
Kohlenstoff ist sp³-hybridisiert und die C-C-Bindung frei drehbar.
Zwei Möglichkeiten der Darstellung:
[Bearbeiten]
| ekliptische (verdeckte) Konformation | gestaffelte Konformation | |
|---|---|---|
| Newman-Projektion |  | |
| Kugel-Stab-Modell |  | |
Einfache Reaktionen der Alkane
[Bearbeiten]- Alkane sind gut brennbar. Alkane dienen z.B. als Energieträger für Verbrennungsmotoren (Diesel, Benzin, Kerosin) sowie zum Heizen von Häusern. Dabei gilt folgende allgemeine Reaktionsgleichung → es entstehen immer Wasser und Kohlenstoffdioxid:
- CnH2n+2 + (2n +1) O2 → n CO2 + (n+1) H2O + E
- Je länger die Kette, desto gelber die Flamme (und desto höher die Leuchtkraft), weil mehr Ruß durch unvollständige Verbrennung entsteht.
- Alkane brennen erst oberhalb der Verdampfungstemperatur, da zum Brennen ein Alkangas-Luftgemisch notwendig ist.
- Innerhalb der Explosionsgrenze explodieren Alkane. Die Explosionsgrenze ist bei Alkanen nicht einheitlich!

- Eine typische Reaktion ist die Halogenierung von Alkanen durch radikalische Substitution (z.B.: Brom wird zu n-Hexan gegeben). Anschließend wird mit Sonnenlicht oder dem Overhead-Projektor belichtet. Der Nachweis findet durch Universalindikatorpapier (über dem RG) statt.
Vorkommen und wichtige Beispiele der Alkane
[Bearbeiten]1. Methan
[Bearbeiten]- Vorkommen
- Hauptbestandteil von Erdgas. Auch in aus Steinkohle gebildetem Stadtgas enthalten. Dazu findet eine trockene Destillation von Steinkohle unter Luftausschluss bei 1200 °C statt. Der Rest wird als Koks bezeichnet.
- Methan entsteht in der Natur bei: - Fäulnisprozessen (z.B. im Komposthaufen, in Sümpfen und im Klärschlamm der Kläranlage- der Cellulosegärung der Wiederkäuer- unterirdisch in Steinkohlegruben als Grubengas (Gefahr, da die „schlagenden Wetter“ (Methan-Luft-Explosionen) die durch einen Funken entstehen können.
- Es entsteht bei Vedauungsvorgängen von Wiederkäuern sowie beim Reisanbau (Anteil des Reisanbaus an der weltweiten Methanproduktion ca. 17 %!).
- Eigenschaften und Verwendung
- farb- und geruchloses Gas (Wieso heißt es eigentlich in Krimis immer: „Es riecht nach Gas.“? Weil es einen Zusatzstoff enthält der den typischen Geruch auslöst um Gas erkennbar zu machen!)
- Methan ist in Wasser unlöslich
- brennbar: CH4 + 2 O2 → CO2 + 2 H2OH = -888 kJ/mol
- geringere Dichte als Luft
- explosives Luft/Methan-Gemisch(Explosionsgrenze 10% - 90% CH4)
- wichtigen Rohstoff der chemischen Industrie. So wird Beispielsweise Wasserstoff durch thermische Spaltung oder durch Reaktionen mit Wasserdampf (an Nickel-Katalysatoren) gewonnen, durch Hitzespaltung gewinnt man Acetylen (Ethin) C2H2:
- CH4 + E → C + 2H2 (bei 1200°C)
- CH4 + H2O → CO + 3H2 (bei 800-900°C, an einem Nickelkatalysator)
- 2 CH4 → C2H2 + 3H2
Zusatzinformationen: Methan
2. Propan:
[Bearbeiten]- Tritt als Begleiter des Erdöls, im Erdgas und in Crackgasen auf.
- Wird als Stadtgas zum Beheizen von Häusern verwendet.
- Treibgas in Sprays
Zusatzinformationen: Propan
3. Butan und sein Isomer:
[Bearbeiten]- n-Butan und Isobutan sind Flüssiggase, die bei der Erdöldestillation anfallen. Sie kommen im Erdöl und Erdgas vor.
- in Wasser ist Butan so gut wie unlöslich (nur 150 ml/l).
- Beide Isomere verhalten sich chemisch ähnlich (beide sind brennbar und werden von den Halogenen Chlor und Brom unter Lichteinfluss angegriffen.
- n-Butan wird seit dem FCKW-Verbot als Treibgas in Spraydosen verwendet.
- Beide Isomere werden in Feuerzeugen, oft im Gemisch mit Propan, eingesetzt.
- Butan wird (trotz der Brennbarkeit) im Kühlschrank als Kältemittel eingesetzt
- manche Solarkollektoren verwenden Isobutan als Wärme(über)träger.
Zusatzinformationen: Butan
4. Pentan und seine Isomere:
[Bearbeiten]- Es gibt drei Isomere des Pentans.
- Der Flammpunkt liegt bei -49 °C, die Zündtemperatur bei 309 °C.
- Löslichkeit: 0.36 g/l (16 °C) in Wasser.
- Pentan wird heutzutage als FCKW-freies Kältemittel in Kühlschränken und Klimaanlagen verwendet.
Zusatzinformationen:
Cycloalkane
[Bearbeiten]Du kennst jetzt die kettenförmigen Alkane, man nennt sie auch aliphatische Alkane. Ihre Kette kann verzweigt oder unverzweigt sein. Wenn Kohlenstoffatome sich in einem Ring anordnen, nennt man diese auch Cycloalkane.
Die Eigenschaften der Cycloalkane sind mehr oder weniger die typischen physikalischen und chemischen Eigenschaften der Alkane. In der Natur spielen zyklische Ringsysteme als Bestandteile vieler pflanzlicher und tierischer Stoffe eine große Rolle. Allerdings liegen dort oft Cycloalkane mit mehreren Mehrfachbindungen vor. Diese haben dann deutlich andere Eigenschaften als die Alkane.

Cyclopropan ist ein brennbares Gas mit einem Sdp. von -33°C, es ist reaktionsfreudig, da die Bindungswinkel zwischen den einzelnen Kohlenstoffatomen stark vom üblichen Tetraederwinkel abweichen und somit die Ringe unter einer gewissen inneren Spannung stehen. Durch eine Reaktion kann der Ring aufgebrochen werden, was viel Energie freisetzt.
Cyclobutan ist ebenfalls ein brennbares Gas. Sein Sdp. liegt bei 12,5°C. Es ist aus den gleichen Gründen ebenfalls reaktionsfreudig.
Cyclopentan ist eine farblose Flüssigkeit, die leicht entzündbar ist. Der Sdp. liegt bei 49°C.
Cyclohexan ist ebenfalls eine farblose Flüssigkeit. Sein Sdp. liegt bei 81°C. Es ist nicht so reaktionsfreudig, da hier ein sehr „entspannter“ Tetraederwinkel vorliegt. Obwohl der Ring planar gezeichnet ist, so ist er es nicht!
| Name | Summenformel | Sdp. | Ringspannung | Strukturformel |
|---|---|---|---|---|
| Cyclopropan | C3H6 | -33°C | 115 | 
|
| Cyclobutan | C4H8 | -12°C | 110 | 
|
| Cyclopentan | C5H10 | 59°C | 27 | 
|
| Cyclohexan | C6H12 | 81°C | 0 | 
|
Zusatzinformationen: Cycloalkane
Stabilität der cyclischen Alkane
[Bearbeiten]Allgemeine Formel der cyklischen Alkane: CnH2n
- Homologe Reihe
- Cyclopropan (C3H6): sehr instabil
- Cyclobutan (C4H8): stabil
- Cyclopentan (C5H10): stabil
- Cyclohexan (C6H12): stabil
- Cycloheptan (C7H14): instabil
- Cyclooctan (C8H16): stabil
Alkene und Alkine
[Bearbeiten]
Ethen (Trivialname Ethylen) ist ein farbloses, süßlich riechendes Gas. Es ist das einfachste Alken und enthält eine Doppelbindung. Man spricht auch von einem ungesättigten Kohlenwasserstoff.
Wenn man den räumlichen Bau anschaut, sieht man schnell, dass es ein planares Molekül ist, welches einen Bindungswinkel von 120° hat.

Ethen wird als Pflanzenhormon verwendet. So werden z.B. noch grüne Bananen gepflückt, transportiert und dann kurz vor Verkauf mit Ethen begast, welches sie zum Reifen bringt.
Auch reife Früchte wie Bananen geben Ethen ab, so dass unreifes Obst, wie Tomaten, in Gegenwart von Bananen weiter reifen.
Des weiteren ist es Ausgangsstoff für sehr viele chemische Synthesen und zur Kunststoffherstellung (PE - Polyethylen, Polystyrol (=Styropor) sowie Polyester u.a.). Auch der Alkohol Ethanol kann daraus hergestellt werden.
Vorsicht: Ethen ist hochentzündlich. Bei einem Luftvolumenanteil von 3 - 36% bildet es explosive Gemische. In hoher Konzentration wirkt es auch als Betäubungsmittel.

Ethin:Ethin (Trivialname Acetylen) ist ebenfalls ein farbloses, leicht süßlich riechendes Gas. Beide Kohlenstoffatome sind über eine Dreifachbindung miteinander verbunden. Es ist der einfachste Vertreter aus der homologen Reihe der Alkine:
Der räumlichen Bau ist planar (kettenförmig) (Bindungswinkel von 180°).
Es brennt mit stark rußender Flamme. Im richtigen Gemisch mit Sauerstoff werden dabei Temperaturen von bis zu 3100°C erreicht. Aus diesem Grunde wird es als Schweißgas verwendet.
Ethin-Luftgemische zwischen 2-82% Luftvolumenanteil sind hochexplosiv. Unter hohem Druck zerfällt es, so dass es in Schweißflaschen nur mit geringem Druck gelagert werden kann.
Die Löslichkeit in Wasser beträgt Normalbedingungen nur 1,23 g/l, wohingegen die Löslichkeit in Alkohol und Aceton sehr gut ist.
Außer zum Schweißen ist dieses Gas besonders gut für chemische Synthesen als Ausgangsstoff geeignet. Außer Kunststoffen wie Polyvinylchlorid[2] (PVC) werden auch viele organische Säuren wie Essigsäure daraus hergestellt.
Zusatzinformationen
Die Genfer Nomenklatur von organischen Verbindungen (IUPAC) - Teil 1
[Bearbeiten]- Es wird die längste Kohlenstoffkette gesucht und die Kohlenstoffatome werden entsprechend nummeriert. Dabei spielt es keine Rolle, ob von Links oder rechts gelesen wird!
- Bei Doppelbindungen wird die Endsilbe „-an“ durch die Silbe „-en“ ersetzt. Die Endung „-in“ wird für Dreifachbindungen verwendet. Die Kette wird dann so nummeriert, dass die Doppel- (bzw. Dreifach-) Bindung die niedrigste Ziffer erhält. Die Lage der Mehrfachbindungen im Molekül wird durch die Nummer des Kohlenstoffatoms bezeichnet, das in der Mehrfachbindung die kleinere Nummer trägt. Sie wird vor (oder früher auch nach) dem Namen des Alkens stehen. Treten mehrere Mehrfachbindungen auf, wird ein „di, tri... “ vor die Endsilbe eingesetzt.
Propen
(1,5)-Heptdien - Seitengruppen werden mit den Namen der entsprechenden Alkane (Alkene/ Alkine) und der Endung „-yl“ gekennzeichnet. Ihre Anzahl wird, (wenn von 1 abweichend) durch die Silben Di-, Tri-, Tetra-, Penta- gekennzeichnet: Vor die Bezeichnung des Restes kommt die Nummer der Stelle der Verzweigung. Treten z.B. zwei Methyl Reste auf, so kommt noch die Silbe „di“ hinzu. Die Seitengruppen werden in alphabetischer Reihenfolge genannt (also -ethyl vor -methyl).
→ 3-Ethyl, 4-Methyl-Heptan → 3, 3-Dimethyl-1-Hepten - Mehrere Doppelbindungen werden durch die Endsilbe „-dien“ gekennzeichnet. Verbindungen mit Doppel- und Dreifachbindungen werden durch die Endungen „-enin“ gekennzeichnet. Sind viele Mehrfachbindungen (oder funktionelle Gruppen) vorhanden, kann die Zahl auch direkt vor das -en oder -in gestellt werden: z.B. 1-Buten = But-1-en.
→ 3-Ethyl, 4-Methyl-(1,5)-Heptdien → 5 Ethyl, 2,5-Dimethyl-(1,6)-Heptenin - Wichtig: Die Nummerierung der Kohlenstoffkette (siehe 1.) ist so durchzuführen, dass nicht nur Mehrfachbindungen, sondern auch Seitenketten eine möglichst niedrige Nummer erhalten.
Zusatzinformationen:
Übungen zur Nomenklatur organischer Verbindungen (Domino)
[Bearbeiten]Im Benzin enthaltene Alkane und Alkine
[Bearbeiten]Benzin ist ein Gemisch. Es enthält mehrere verschiedene Alkane, Cykloalkane, Alkene und Cycloalkene. Hier ein Ausschnitt eines typischen Benzins:
- Aufgaben
- Ordne die folgenden Namen den einzelnen Verbindungen zu:
1,3 Diethyl-Cyclo-Pentan, 2,4,5 Trimethyl-Heptan, 1,2 Dimethyl-Cyclohexan, 3,4, Dimethyl-Octan, 3 Isopropyl-Hexan, Oktan, Benzol (=1,3,5-Hextrien), Heptan, 2,2,4 Trimethyl-Heptan, 1,3,5 Trimethyl-Benzol, 3 Methyl-Pentan, Isopropyl-4-Propyl-Benzol, 4 Ethyl-3 Methyl-Heptan, 3,4 Dimethyl-Heptan, (1-Methyl-Propyl)-Cyclopentan, Isobutyl-Benzol. - Wie kann man die unterschiedliche Zusammensetzung des Gemisches „Benzin“ erklären?
Bindungswinkel und Drehbarkeit
[Bearbeiten]a) Alkane
[Bearbeiten]Erinnere Dich an das Kapitel „Atombindung“. Nach der Elektronenpaarabstoßungstheorie stoßen sich Elektronen voneinander ab. Deshalb haben auch Bindungselektronenpaare immer einen größtmöglichen Abstand voneinander. Ein Atom mit vier Bindungen (also genauso wie der Kohlenstoff in Methan, Ethan usw.) liegt also nicht so vor, wie wir ihn oft zeichen:
-
Einfache Darstellung, welche oft ausreicht - aber nicht exakt ist!
-
Der Bindungswinkel ist tatsächlich aber nicht 90°C. → Ein größerer Winkel ist möglich!
Maximale Abstoßung liegt bei einem Winkel von 109,5° vor. Die räumliche Gestalt, welche entsteht, wenn man die H's verbindet, nennt man Tetraeder.
Dies ist die räumliche Anordnung, wie sie bei sehr vielen Molekülen, welche 4 Bindungspartner haben vorliegt, ermöglicht den größtmöglichen Abstand zwischen den Bindungspartnern.
Hintergrund ist die Abstoßung der Elektronenwolken untereinander (und im Übrigen auch die der Atomkerne). Elektronen und Atome „versuchen“ jeweils einen möglichst großen Abstand voneinander zu bekommen.
b) Alkene
[Bearbeiten]
In Alkenen liegen am Doppelbindungs-“C“ nur 3 Bindungen vor (die Doppelbindung zählt nur einmal, da sie ja nur EINE Doppelbindung ist!). Der Bindungswinkel beträgt 120°.
Die Doppelbindung ist nicht frei drehbar!
[Bearbeiten]b) Alkine
[Bearbeiten]
Ein C mit Dreifachbindung hat nur 2 Bindungen. Somit ist der maximale Abstand erreicht, wenn ein Bindungswinkel von 180° vorliegt!
Die Dreifachbindung ist nicht drehbar!
[Bearbeiten]Funktionelle Gruppen
[Bearbeiten]- Alle Seitenketten oder besonderen Substituenten (das sind Atome, welche H in der Kohlenstoffkette ersetzen) werden funktionelle Gruppen genannt. Auch Seitenketten (mit oder ohne Doppelbindung) gelten als funktionelle Gruppen.
- Sind andere Atome als C oder H in funktionellen Gruppen beteiligt, führen diese in der Regel zu polaren Atombindungen und somit oft zu Dipolen. Dies hat wiederum Einfluss auf Siede- und Schmelzpunkte sowie die Löslichkeit in polaren Lösungsmitteln. Es gilt, je stärker der Dipol, desto eher löst sich der Stoff auch in Wasser.
- Funktionelle Gruppen sind leichter angreifbar als die Hauptkette. Hier finden also oft die Reaktionen statt.
- Hat man als funktionelle Gruppen neben den Alkylresten auch Halogene oder Sauerstoff, Stickstoff oder Mehrfachbindungen, so werden diese (wenn man es sehr genau mit der Nomenklatur nimmt) in folgender Reihenfolge benannt:Brom vor Chlor vor Sauerstoff vor Stickstoff vor Doppelbindungen vor Alkylketten
- Hintergrund dieser Anordnung ist die Massenzahl: 35Br > 17Cl > 8O > 7N > 6C)
- Seitenketten mit Einfachbindungen enden auf -yl (Methyl, Ethyl usw.), Seitenketen mit Doppelbindungen enden auf -enyl (Ethenyl, Propenyl usw.).
- Alternativ zum cis/trans-Bennenungssystem wurde ein weiteres, das E/Z-System eingeführt (siehe Wikipedia unter Nomenklatur!)
- Auch Mehrfachbindungen zwischen zwei Kohlenstoffen der Hauptkette gelten als funktionelle Gruppe. Sie werden oft bei Reaktionen aufgespalten! → Moleküle mit Mehrfachbindungen sind deutlich reaktiver als reine Alkane!
- Die funktionelle Gruppe eines aromatischen Benzolringes wird als „Phenyl“ bezeichnet, also die Atomgruppe –C6H5.
Verschiedene graphische Darstellungsmöglichkeiten von organischen Verbindungen
[Bearbeiten]Organische Verbindungen sind im Aufbau komplex. Durch ihre dreidimensionalen Aufbau ist es schwierig, sie zweidimensional auf Papier darzustellen. Hier eine Übersicht über verschiedene Darstellungsweisen:
- a) Summenformel
Die Summenformel beschreibt einfach die Summe der beteiligten Atome. Sie sagt nichts über den tatsächlichen Aufbau aus.
C2H6 - Ethan
- b) Konstitutionsformel
Die Konstitutionsformel zeigt den einfachen, zweidimensionalen Aufbau der Verknüpfungen von Kohlenwasserstoffen.
- c) Strukturformel
In der Regel entspricht sie der Konstitutionsformel. Sie kann (bei einfachen Molekülen) auch dreidimensional gezeichnet sein (gestrichelte Linien ragen nach hinten, dicke Dreieckslinien ragen nach vorn - aus der Ebene hinaus).
- d) Halbstrukturformel (Kettenschreibweise)
- Propan: CH3-CH2-CH3
- Iso-Butan: CH3-CH(CH3)-CH3
- e) Strichschreibweise
Bei dieser Schreibweise werden Wasserstoffe nicht gezeichnet. Die Kohlenstoffatome befinden sich an den Winkeln bzw. Schnittpunkten.
- Weitere Möglichkeiten der dreidimensionalen Abbildung für die K12
Wiederholungsaufgaben
[Bearbeiten]- Was versteht man unter einer Atombindung? Zeichne die Atombindung zwei Sauerstoffatome.
- Zeichne die folgenden Verbindungen als Valenzstrichformel: H2, O2, N2, Cl2, HCl, CO, H2O, CH4, CO2
- Was ist die homologe Reihe der Alkane? Wie unterscheiden sich Alkane, Alkene und Alkine? Nenne je ein Beispiel sowie die allgemeine Formel.
- Welchen Zusammenhang siehst du zwischen der Länge der Kohlenstoffkette und dem Litergewicht sowie der Siedetemperatur der homologen Reihe der Alkane?
- a) Welche Summenformel haben Cyclo-Alkane b) Alkene mit zwei Doppelbindungen)?
- Erkläre den Begriff „Isomer“. Zeichne dann alle Isomere von Hexan.
- Wie erklärst Du Dir die Vielfalt der organischen Verbindungen?
- Nenne 10 Stoffe in denen Kohlenstoff enthalten ist
- Wie kann man Kohlenstoff chemisch nachweisen? Beschreibe ein Experiment mit Aufbau.
- Welche Gefahr geht von den Dämpfen kohlenstoffhaltiger Lösungsmittel (z.B. Benzin oder Alkohol) aus?
- Kohlenstoff steht in der 4. HG. Wie viel Atombindungen kann ein Element der 4. HG nur haben?
- Stelle die Valenzstrichformeln der folgenden Verbindungen auf: a) alle Dir bekannten Säurenb) Methan, Heptan, C2H6, C6H14, C4H10, C9H20, C2H4, C6H12, C6H6
- Wiederhole die Regeln der Genfer Nomenklatur.
- Zeichne: 2,2 Dimethyl Propan; 2,3,4 Trimethyl-Penten; 4,4, Dimethyl Heptan
- Unter welchen Bedingungen konnten sich Erdgas und Erdöl bilden. Beschreibe den Vorgang.
- Norddeutsches Erdgas enthält auch Schwefelwasserstoff. Welche Gefahren würden auftreten, wenn dieser Bestandteil nicht vor der Verbrennung heraus gewaschen würde? Begründe mit einer Reaktionsgleichung!
- Woran liegt es, dass die Zusammensetzung des Erdöls aus verschiedenen Ländern unterschiedlich ist?
- Erkläre den Begriff „Isomer“ und stelle alle Isomere von Hexan auf
- Gib die Strukturformeln und Namen von 4 isomeren Alkoholen der Summenformel C4H11OH an!
- Zeichne die folgenden Strukturformeln und benenne die Substanzen:a) CH3-CHCl2 b) C2H5OH c) CH3-CH4O d) C2H3Br e) C3H8Cl f) C6H6 g) C3H8 h) C3H5Cl i) C3H4COOH j) C3H3O k) Butanal l) (CH3)3CCH3 m) CH2=C(CH3)CH2F n) H3C-CH2-Br o) 1,5-Diiodpenta-1,4-dien p) 2-Fluor-3,4-dimethylhex-3-en q) 4,4, Dimethyl Heptan r) 2,3,4 Trimethyl Penten s) H3C-CH2-CH2-CH2-CH2 t) H3C-CH=CH-CH=CH-CH3 u) 2,2 Dimethyl Propan
- Begründe, warum es in der organischen Chemie eine theoretisch unendliche Anzahl an Verbindungen gibt.
- Warum ist Kohlenstoff immer vierbindig und warum darf Wasserstoff nur eine Bindung haben? Wie viele Bindungen hat Stickstoff? Wie sehen die typisch gebunden Sauerstoffe aus?
- Nenne 10 Stoffe in denen Kohlenstoff enthalten ist. Wie kann man Kohlenstoff in ihnen chemisch nachweisen? Beschreibe ein Experiment. (Wie kann man Halogene in Kohlenwasserstoffen nachweisen?)
- Vervollständige die Tabelle:
| Stoffklasse | funktionelle Gruppe | Endung | Beispiel |
|---|---|---|---|
| Alkan | C-C | ||
| Alken | |||
| Alkin | |||
| Alkohol | |||
| Carbonsäure | |||
| Halogenalkane |
- Erstelle eine Übersicht über die drei Dir nun bekannten Reaktionsmechanismen. Erkläre jeden Mechanismus schrittgenau. und nenne jeweils mögliche Ausgangstoffe (=Edukte) und mögliche Produkte.
- Benenne die folgenden Verbindungen: