Schilddrüse: Therapie
Zurück zur Schilddrüse
Therapie (Behandlung) von Schilddrüsenkrankheiten
Therapie Übersicht
[Bearbeiten]- oft ist keine Therapie notwendig, sondern nur Kontrolluntersuchungen
- beispielsweise bei harmlosen Schilddrüsenknoten
- Jodsalz,
- Jodtabletten
- bei Jodmangel und zur Kropfvorbeugung
- Thyroxin (T4)
- zur Behandlung der Unterfunktion und teilweise auch zur Kropfrückbildung
- Levothyroxin kann auch abends eingenommen werden
- Triiodthyronin (T3)
- zur Behandlung spezieller Unterfunktionserkrankungen
- Medikamente die die Schilddrüsenfunktion reduzieren
- Thiamazol
- Carbimazol
- Propylthiouracil
- Perchlorat = Irenat)
- bei Überfunktion
- Betablocker (Propanolol, Bisoprolol, Metoprolol, ....)
- bei Überfunktion
- Alkoholbehandlung von heißen Schilddrüsenknoten
- Radiojodbehandlung
- bei Überfunktion und Schilddrüsenkrebs
- Operation der Schilddrüse
- Begrenzte Schilddrüsen Operation
- Subtotale Schilddrüsen Operation
- Radikale Schilddrüsen Entfernung
- Schilddrüsen Operation + Lymphknotenausräumung am Hals
- Sonstige Therapie der Schilddrüse
- Pharmafirmen mit Schilddrüsenpräparaten
- Henning Berlin
- Merck Darmstadt
- ....
Medikamentenliste der wichtigen Schilddrüsenwirkstoffe
[Bearbeiten]Verschiedene Namen für den gleichen Wirkstoff
Jodpräparate
[Bearbeiten]- Jodetten Henning
- Jodid Beta
- Jodid Dura
- Jodid Hexal
- Jodid ratiopharm
- Jodid Verla
- Kalium Jodatum
- Kaliumiodid
- Mono-Jod
- Strumedical
- Strumex
- ....
T4-Thyroxin-Monopräparate
[Bearbeiten]- Berlthyrox (50, 100, 150 Berlin-Chemie)
- Eferox (25, 50, 75, 100, 125, 150 Lindopharm)
- Euthyrox (25, 50, 75, 100, 125, 150, 175, 200 Merck KGaA)
- Lixin liquid (Henning Berlin)
- L-Thyrox (25, 50, 75, 100, 125, 150, 175, 200 Hexal)
- L-Thyroxin beta (25, 50, 75, 100, 125, 150, 175, 200 betapharm)
- L-Thyroxin Henning (25, 50, 75, 100, 125, 150, 175, 200 Henning-Berlin)
- Thevier (50, 100 Glaxo Smith Kline)
- ....
Thyreostatika Überfunktionsbremser
[Bearbeiten]Wirkstoff Thiamazol:
[Bearbeiten]- Favistan
- Methizol
- Thyrozol
Wirkstoff Carbimazol:
[Bearbeiten]- Carbimazol
- Carbistad
- Neo-Thyreostat
Wirkstoff Propylthiouracil:
[Bearbeiten]- Propycil
- Prothiucil
- Thyreostat
Wirkstoff Natriumperchlorat:
[Bearbeiten]Betablocker
[Bearbeiten]Propranolol
[Bearbeiten]Bisoprolol
[Bearbeiten]......
[Bearbeiten]Schilddrüsenmedikamente im Einzelnen
[Bearbeiten]Iodbedarf in Mikrogramm pro Tag
[Bearbeiten]Säuglinge 50 – 80 Kleinkinder 100 – 120 Schulkinder 140 – 200 Jugendliche 200 Erwachsene bis 35 Jahre 200 Erwachsene über 35 Jahre 180 Schwangere und Stillende 230 – 260
Links
[Bearbeiten]- http://www.iod-fuer-zwei.de/
- Iodbehandlung in der Schwangerschaft
Jod Salz
[Bearbeiten]Jod Tabletten
[Bearbeiten]Anwendung:
[Bearbeiten]- Vorbeugung eines Jodmangels, zur Vorbeugung eines Kropfes in Jodmangelgebieten und nach Entfernung eines Jodmangelkropfes,
- Behandlung eines Kropfes bei Neugeborenen, Kindern, Jugendlichen, Erwachsenen und Schwangeren.
Gegenanzeigen
[Bearbeiten]- Autoimmunerkrankungen der Schilddrüse (Morbus Basedow, Hashimoto Thyreoiditis)
- Manifeste Schilddrüsenüberfunktion.
- Latente Schilddrüsenüberfunktion
- Diffuse und fokale Autonomien (autonome Adenome).
Präparate:
[Bearbeiten]- Jodetten ® 100 Henning enthält 130,8µg Kaliumjodid, entspricht 100µg Jod
- Jodetten ® 200 Henning enthält 261,6µg Kaliumjodid, entspricht 200µg Jod
- Jodetten ® depot Henning enthält 2mg Kaliumjodid, entspricht 1,53mg Jod
- Strumedical 400 Henning®
- Strumex®
- Jodid®
- Jodid ratiopharm®
- Jodid Verla®
- Kaliumiodid BC 200®
- Kalium Jodatum 0,1g®
- Mono-Jod®
siehe auch http://www.madeasy.de/6/jodid.htm
Thyroxin (Schilddrüsenhormon)
[Bearbeiten]siehe http://www.madeasy.de/6/euthyrox.htm
Anwendung
[Bearbeiten]- Schilddrüsenunterfunktion (SD-Hormonmangel)
- Ausgleich eines angeborenen oder erworbenen Schilddrüsenhormonmangels
- nach einer operativen Entfernung der Schilddrüse
- nach einer Radiojodtherapie mit folgendem Schilddrüsenhormonmangel
- nach einer Erkrankung der Schilddrüse und Untergang von Schilddrüsengewebe.
- chronische Autoimmunthyreoiditis Hashimoto (im Anfangsstadium umstritten, in jedem Fall in der Endphase)
Wirkstoff Thyroxin (T4) ist enthalten in
[Bearbeiten]( Wirkstärken meist in mikrogramm )
- Euthyrox® 25/-50/-75/-88/-100/-112/-125/-137/-150/-175/-200 Mikrogramm Tabletten
- L-Thyroxin® Henning 25 /50 /75 /100 /150 /175 /200 /300
- L-Thyrox® HEXAL® 25/-50/-75/-88/-100/-112/-125/-150/-175/-200 mikrog
- Berlthyrox® 50 /100 /150
- Eferox® 25 /50 /75 /100 /125 /150 /175
- L-Thyroxin® Henning depot 1mg
- Thevier® 50/ Thevier 100
- L-Thyroxin HF® 50 /75 /100 /125
Kombinationspräparate Jod + T4
- Jodthyrox®
- Thyreocomb N®
- Thyronajod®
Kombinationspräparate T4 + T3
- Novothyral® 75µg + 15µg / 100µg + 20µg
T4 und T3 intravenös
[Bearbeiten]Schilddrüsenhormone müssen manchmal auch intravenös verabreicht werden. Dafür gibt es 2 Präparate in Deutschland:
- L-Thyroxin Henning® inject.
- L-Thyroxin Henning® inject. Durchstechflasche mit Trockensubstanz und Lösungsmittel
- Thyrotardin®-inject.
- Thyrotardin®-inject. Durchstechflasche mit Trockensubstanz und Lösungsmittel (Mono)
Das erste Präparat hat eine relativ hohe Dosis von 500 mikrog T4 und hat nur die Zulassung zur Therapie des hypothreoten Comas. Das zweite Präparat hat eine Dosis von 100 mikrog T3 und wird deswegen auch bei Patienten verwendet, die einen Hormonersatz brauchen, aber nicht schlucken können.
L-Thyroxin Henning® inject. 500
[Bearbeiten]- Zusammensetzung
- 1 Durchstechflasche enthält Levothyroxin-Natrium 514,1 μg (entspr. 0,5 mg Levothyroxin).
- Weitere Bestandteile:
- Natriummonohydrogenphosphat
- 2H2O,
- Mannitol,
- Natriumchlorid,
- Wasser f. Inj.-zwecke,
- zur pH-Einstellung:
- Phosphorsäure,
- Natriumhydroxid.
- Kosten
- 1 Durchstechfl. (N1) Trockensubstanz u. Lsgm. (AP) Circa 50 Euro
Anwendung
- Notfalltherapie bei hypothyreotem Koma.
- Dosierung
- i.v. Infusion von 0,3-0,5 mg gemäß Gebrauchsanweisung.
Gegenanzeigen
- Unbehandelte Hyperthyreose.
- Frischer Myokardinfarkt,
- Myokarditis,
- Pankarditis,
- unbehandelte hypophysäre oder Nebennierenrinden-Insuffizienz.
In Notfallsituationen individuell abwägen.
- Anwendungsbeschränkung:
- Patienten bei welchen sich unter einer lang andauernden Hypothyreose bereits eine Coronar- oder Herzinsuffizienz ausgebildet hat oder eine Hypophysenvorderlppen-Insuffizienz besteht (Infusion unter EKG-Kontr. zusätzliche Glucocorticoid-Gabe).
- Hypertonie,
- Angina Pectoris,
- tachykarde Herzrhythmusstörungen
- Nebenwirkungen
- Hyperthyreose
- Bei Überdosierung (insbesondere bei zu schneller Steigerung der Dossis zu Beginn der Behandlung):
Hyperthyreotische Erscheinungen (z. B. Fingertremor, Tachykardie, Hyperhidrosis, Diarrhö, Gewichtsabnahme, innere Unruhe) Bei zu hoher Anfangsdosis kann bei besonders empfindlichen Patienten Vorhof- bzw. Kammerflimmern ausgelöst werden.
- Toxizität
- Hyperthyreose
- Tachykardie,
- Heißhunger,
- Herzpalpitation,
- vermehrtes Schwitzen
- Hitzegefühl, Wärmeintoleranz,
- Unruhe,
- Fingertremor,
- lebhaft gesteigerte Reflexe,
- Diarrhöen,
- Fieber,
- Blutdruckabfall,
- pektanginöse Beschwerden.
- Hyperthyreose
Eine thyreotoxische Krise ist bei Überdosierung von Schilddrüsenhormonpräparaten bisher nicht beschrieben worden, und es ist zweifelhaft, ob sie überhaupt auftreten kann.
Therapie der Überdosierung:
- Sedierende Mittel,
- v. a. Reserpin,
- Schlafmittel,
- Betarezeptorenblocker,
- Corticoide, ggf. Digitalis.
- Bei thyreotoxischer Krise: u. U.
- künstliche Hibernation,
- Peritonealdialyse,
- Hämoperfusion über Kohle od. Austauscherharze.
Thyrotardin®-inject 100 mikrog T3
[Bearbeiten]Zusammensetzung
- 1 Durchstechflasche enthält Liothyronin = T3 0,1 mg.
Weitere Bestandteile: Natriummonohydrogenphosphat 2H2O, Mannitol, Natriumchlorid, Wasser f. Inj.-zwecke, zur pH-Einstellung: Phosphorsäure, Natriumhydroxid.
Kosten
- 1 Durchstechflasche (N1) Trockensubstanz und Lösungsmittel circa 50 €
Anwendung
- Notfalltherapie bei hypothyreotem Koma,
- zur Substitution, wenn eine orale Applikation nicht möglich ist.
Dosierung: i.v. Infusion von 0,1 mg gemäß Gebrauchsanweisung.
Gegenanzeigen
- Unbehandelte Hyperthyreose.
- Frischer Myokardinfarkt,
- Myokarditis,
- Pankarditis,
- unbehandelte hypophysäre oder Nebennierenrinden-Insuffizienz.
In Notfallsituationen individuell abwägen.
- Anwendungsbeschränkung:
- Patienten bei welchen sich unter einer lang andauernden Hypothyreose bereits eine Coronar- oder Herzinsuffizienz ausgebildet hat oder eine Hypophysenvorderlppen-Insuffizienz besteht (Infusion unter EKG-Kontr. zusätzliche Glucocorticoid-Gabe).
- Hypertonie,
- Angina Pectoris,
- tachykarde Herzrhythmusstörungen
- Nebenwirkungen
- Hyperthyreose
- Bei Überdosierung (insbesondere bei zu schneller Steigerung der Dossis zu Beginn der Behandlung):
Bei zu hoher Anfangsdosis kann bei besonders empfindlichen Patienten Vorhof- bzw. Kammerflimmern ausgelöst werden.
Hyperthyreotische Erscheinungen (z. B. Fingertremor, Tachykardie, Hyperhidrosis, Diarrhö, Gewichtsabnahme, innere Unruhe)
- Toxizität
- Hyperthyreose
- Tachykardie,
- Heißhunger,
- Herzpalpitation,
- vermehrtes Schwitzen
- Hitzegefühl, Wärmeintoleranz,
- Unruhe,
- Fingertremor,
- lebhaft gesteigerte Reflexe,
- Diarrhöen,
- Fieber,
- Blutdruckabfall,
- pektanginöse Beschwerden.
- Hyperthyreose
Eine thyreotoxische Krise ist bei Überdosierung von Schilddrüsenhormonpräparaten bisher nicht beschrieben worden, und es ist zweifelhaft, ob sie überhaupt auftreten kann.
Therapie der Überdosierung:
- Sedierende Mittel,
- v. a. Reserpin,
- Schlafmittel,
- Betarezeptorenblocker,
- Corticoide, ggf. Digitalis.
- Bei thyreotoxischer Krise: u. U.
- künstliche Hibernation,
- Peritonealdialyse,
- Hämoperfusion über Kohle od. Austauscherharze.
Schilddrüsenbremser
[Bearbeiten]Anwendung
- manifeste oder latente Schilddrüsenüberfunktionen
- bei gutartigen, hormonbildenden Knoten oder unkontrolliert hormonbildenden Bezirken
- Morbus Basedow
Thiamazol
[Bearbeiten]Wirkstoff Thiamazol
- Methizol® = 1 Tbl. enthält 5mg Thiamazol
- Favistan® = 1 Tbl. enthält 20mg Thiamazol
- Thyrozol® 5/10/20 = 1 Tbl. enthält 5/10/20mg Thiamazol
Thiamazol iv,im,sc (Favistan)
[Bearbeiten]Anwendung:
- Thyreotoxische Krise,
- Basedow-Koma.
Zusammensetzung:
- 1 ml enthält Thiamazol 40 mg.
Weitere Bestandteile:
- Wasser für Injektionszwecke,
- Stickstoff als Schutzgas
Kosten
10 Amp. (N1) 1 ml 16,40 Euro
Gegenanzeigen:
- Schwere vorausgegangene Überempfindlichkeitsreaktionen (z. B. Agranulozytose)
- Leberschäden durch das anzuwendende Thyreostatikum in der Vorgeschichte
Wechselwirkungen:
- Jodmangel verstärkt das Ansprechen auf Thiamazol.
Hinweise:
- Es wurde wiederholt über Kinder von mit Thiamazol behandelten Müttern berichtet, die mit einer Aplasia cutis im Kopfbereich geboren wurden, die nach einigen Wochen spontan abheilte.
Dosierung: Injektions-Lösung:
- 3-4 mal täglich 1 ml i.v.,
- in schweren Fällen bis zu 3mal täglich 2 ml.
- Bei eingeschränkter Leberfunktion individuelle Dosisanpassung.
Es ist zu unterscheiden zwischen der Behandlung im akuten Stadium und der Dauerbehandlung nach Erreichen der euthyreoten Stoffwechsellage.
Carbimazol
[Bearbeiten]- Wirkstoff Carbimazol
- Carbimazol® 5mg/ 10mg
- Neo-Thyreostat® = 1 Tbl. enthält Carbimazol 10mg
Propylthiouracil
[Bearbeiten]
- Propycil 50® = 1 Tbl. enthält 50mg PTU
- Thyreostat II/ 50mg® = 1 Tbl. enthält 25mg /50mg PTU
Perchlorat (Irenat)
[Bearbeiten]Natriumperchlorat ist das Natriumsalz der Perchlorsäure. Es besitzt die Summenformel NaClO4. Natriumperchlorat (Handelsname Irenat®) hemmt kompetitiv die Aufnahme von Iod und Technetium in die Schilddrüse. Es wurde daher früher häufig zur Behandlung der Hyperthyreose eingesetzt. Heute wird es fast nur noch zur Blockade der Schilddrüse bei Verabreichung iodhaltiger Kontrastmittel oder schilddrüsengängiger Radiopharmaka (123I, 131I, 99mTc) verwendet. Letzeres geschieht, um die Strahlenbelastung der Schilddrüse gering zu halten, es sei denn, es soll die Schilddrüse selbst dargestellt werden.
Zusammensetzung
[Bearbeiten]1 ml Irenat entsprechend ca. 15 Tropfen enthält 344,2 mg Natriumperchlorat 1H2O Weitere Bestandteile sind Ammoniumchlorid, Magnesiumchlorid, Calciumchlorid, Wasser.
Dosierung
[Bearbeiten]Perchlorat wird als Tropfen verabreicht.
Substanz Handelsname Verabreichung Anfangsdosis Erhaltungsdosis --------------------------------------------------------------------------------- Perchlorat Irenat Tropfen (15 Tropfen = 300 mg) 1200 mg/die 400 mg/die
Einnahme auf 4 mal pro Tag verteilen !
Irenat Tropfen werden mit Wasser verdünnt eingenommen. Irenat Tropfen werden auf 4-6 Einzeldosen verteilt. Anfangsdosis 40-50 Tropfen täglich, in Ausnahmefällen 75 Tropfen täglich.
Erhaltungsdosis 20 Tropfen täglich Hirnszintigraphie 10-20 Tr., in Einzelf. 50 Tr. Perchlorat Discharge-Test einmalig 30-50 Tr.
Kosten
[Bearbeiten]40 ml (N2) 17,16 Euro
Anwendung
[Bearbeiten]- Hyperthyreose
- Blockade der Schilddrüse bei szintigraphischen Untersuchungen anderer Organe mit radioaktiv markiertem Iod
- Hirnszintigraphie)
- Immunszintigraphien
- Tumorsuche mit Radioiod-markierten Anitikörpern
- Perchlorattest
Gegenanzeigen
[Bearbeiten]- Retrosternale Struma.
- Plummerung zur Operationsvorbereitung.
- Bereits früher unter Perchlorat-Gabe aufgetretene Blutbildveränderungen.
- Schwangerschaft
- Stillzeit
Nebenwirkungen
[Bearbeiten]- Gelegentlich.:
- flüchtiges Exanthem,
- Übelkeit oder Brechreiz,
- Mundtrockenheit,
- Reizungen im Rachenbereich,
- Lymphadenopathie,
- Leukopenie,
- Purpura,
- fieberhafte Gelenkschmerzen,
- Arzneimittelfieber.
- Selten:
- anfängl. Durchfall,
- leichte Muskelkrämpfe,
- Brennen in den Füßen,
- Schwere im Kopf,
- Eosinophilie,
- Juckreiz,
- Ikterus.
- Agranulozytose.
- In Einzelfällen:
- Thrombozytopenie,
- aplastische Anämie,
- Agranulozytose mit tödlichem Ausgang
- Albuminurie,
- nephrotisches Syndrom,
- Haarausfall,
- Akne,
- Dermatitis,
- Urtikaria,
- Leberschädigung mit akutem Leberversagen,
- Erythema nodosum mit Fieberschüben,
- antinukleären und antierythrozytären Antikörpern und Eosinophilie.
- Durchbruch eines Zwölffingerdarmgeschwüres.
Wechselwirkungen
[Bearbeiten]Die Radiojod- bzw. 99m Tc-Pertechnetat-Aufnahme wird dosisabhängig durch Perchlorat gehemmt. Die TSH-Stimulierbarkeit der Radiojodaufnahme wird durch Perchlorat nicht beeinflußt. Wirkungsverstärkung durch Propylthiouracil, Thiamazol, Carbimazol. Eine gleichzeitige Thiamazolgabe verursacht einen positiven Perchlorat Discharge-Test. Eine gleichzeitige Jodgabe vermindert die Irenat Tropfen-Wirkung.
Hinweise
[Bearbeiten]Bei Langzeitanwendung von Irenat Tropfen sind regelmäßige Blutbildkontrollen und Kontrollen der Schilddrüsenfunktion erforderlich.
Literatur
[Bearbeiten]- Wolff J: Perchlorate and the thyroid gland. Pharmacol Rev 1998; 50: 33–8.
Betablocker (Propranolol, Bisoprolol, Metoprolol)
[Bearbeiten]Betablocker schützen das Herz und andere Organe bei einer Schilddrüsenüberfunktion vor der Wirkung der erhöhten und dann auch gefährlichen Schilddrüsenhormone. Betablocker sind im allgemeinen gut verträglich. Bei Asthma, Diabetes und Durchblutungsstörungen der Beine muß man mit der Gabe von Betablockern zurückhaltend sein. Ob es echte Vorteile in der herzschützenden Wirkung der verschiedenen Betablocker gibt, ist umstritten. Bei Schilddrüsenüberfunktion wird meistens mit Propranolol behandelt. Bisoprolol ist wahrscheinlich genauso gut wirksam und hat den Vorteil, daß man es nur einmal am Tag nehmen muß. Die Dosis des Bisoprolol liegt zwischen 2,5 und 10 mg. Sie wird als Einmalgabe morgens eingenommen( 1-0-0) .
siehe Schilddrüse: Bisoprolol
Selen
[Bearbeiten]Bei Hashimotothyreoditis läßt sich die Höhe der Antikörper Titer durch die Gabe von Selen reduzieren, auch fühlen sich die Patienten wohler. ( täglich Gabe von 200 mikrog Natrium selenit zb Cefasel, selen-loges) Ob die Einnahme von Selen auch die Ausbildung einer Hypothyreose verhindert ist noch unklar. Der Einsatz beim Basedow und der Endokrionen Orbitopathie ist auch noch nicht sauber geklärt.
Literatur
[Bearbeiten]Ultraschalltherapie von Schilddrüsenknoten
[Bearbeiten]Man kann Schilddrüsenknoten auch mit einem fokusierten starken Ultraschallstrahl behandeln. Die Behandlung ähnelt der Steinzertrümmerung von Nierensteinen mit Ultraschall ( Lithotrypsie ). Sie kann nur bei gutartigen Knoten angewendet werden und wird teilweise noch nicht von den Krankenkassen bezahlt.
Adressen in Deutschland für die Ultraschallknotenbehandlung
- Nuklearmedizin Reumontstraße 35, 33102 Paderborn – Deutschland
- 0 52 51 41 77 9 – 10
- kontakt(at)nm-pb.de
- Webseite : www.nuklearmedizin-pb.de
- 0 52 51 41 77 9 – 10
- Borad
- Neustraße 17a – 46236 Bottrop – Deutschland
- 02041.1840-150
- info(at)borad.de
- www.borad.de/standorte/bottrop/
Schilddrüsenoperation
[Bearbeiten]Vorbemerkungen
[Bearbeiten]Durch eine regelmäßige Untersuchung lassen sich viele Operationen der Schilddrüse vermeiden. In Deutschland werden im Vergleich zur Schweiz etwa 5 mal mehr Schilddrüsenoperationen / 1 Million Einwohner durchgeführt. In einem Jahr sind das etwa 120 000 Eingriffen. Der entscheidende Grund dafür ist der nach wie vor bestehende Jodmangel in Deutschland.
Vor allem die diffuse Vergrößerung der Schilddrüse, die Knotenbildung in der Schilddrüse und ein Teil der Fälle mit Überfunktion ließe sich mit einer ausreichenden Jodversorgung stark reduzieren. Betroffen vom Jodmangel sind dabei vor allem Frauen. Ihr Anteil bei den Schilddrüsenoperationen liegt etwa bei 75 %.
Statistik der Schilddrüsenoperationen
[Bearbeiten]Mit der Studie Papillon 2007 liegt eine retrospektive Untersuchung von 56.300 Patienten vor, die in Deutschland an der Schilddrüse operiert wurden.
Grund zur Operation -------------------------------------- Knotenkropf 65 % Struma diffusa 15 % andere Schilddrüsenerkrankungen 20 % Komplikationen der Operation -------------------------------------- Rekurrenzparese 2 % Hypoparathyreoidismus 3,6 % Rezidivkropf 20 %
40 Prozent der Patienten, die an der Schilddrüsen operiert wurden, hatten vor ihrer Operation keine Schilddrüsentabletten bekommen.
Wann ist eine Operation unvermeidlich ?
[Bearbeiten]Der Hauptgrund für eine Schilddrüsenoperation ist der Verdacht auf eine bösartige Schilddrüsenkrankheit. Weitere OP-Indikationen sind:
- Mechanische oder mechanisch-kosmetische Veränderungen
- Hormonüberproduktion
Notwendige Voruntersuchungen
[Bearbeiten]- Allgemeine Voruntersuchungen mit der Frage der Opfähigkeit
je nach Alter und Vorerkrankungen können folgende Untersuchungen notwendig sein:
- Röntgen Thoraxaufnahme
- EKG und Echokardiografie
- Laboruntersuchungen insbesondere Blutbild, Gerinnung
- Lungenfunktion
- eventuell Belastungs-EKG
- Spezielle Voruntersuchungen der Schilddrüse
- Schilddrüsenultraschall und eventuell ein Szintigramm, CT oder NMR der Schilddrüse
- aktueller Hormonbefund
- Prüfen der Stimmbandfunktion
- Vorbesprechung des operativen Eingriffes ambulant beim verantwortlichen Chirurgen
- Schriftliche Einverständnis zur Operation
Wann ist eine Operation nicht möglich oder nicht sinnvoll?
[Bearbeiten]- wenn der Patient aus internistischer Sicht nicht opfähig ist
- Schwere Herzerkrankung
- Schwere Lungenerkrankung
- Schwere Lebererkrankung
- Schwere Nierenerkrankung
- Schwere Bluterkrankung
- notwendig ist ein Hb > 10
- Schlechte Gerinnungswerte
- (notwendig ist ein Quick > 50 %, Thrombos > 50000 PTT < 50 sek)
- Schwere Infektionskrankheit
- Schwere Tumorkrankheit
- Andere schwere Krankheit die den Operationserfolg beinträchtigt
- wenn der Patient nicht mit der Operation einverstanden ist
- wenn ein deutlicher positiver Effekt durch die Operation nicht zu erwarten ist
Risiken einer Schilddrüsen Operation
[Bearbeiten]Das Operationsrisiko hängt entscheidend von den Begleiterkrankungen des betroffenen Patienten ab. Außerdem ist die Erfahrungs des Operationsteams sehr wichtig. Eine Mindestzahl von 40 - 50 Schilddrüsenoperation / Jahr ist zu fordern. Es gibt allerdings Zentren die pro Jahr mehr als 500 Schilddrüsen OPs durchführen und damit vor allem für Problemfälle empfehlenswert sind.
Circa 24 Stunden lang ist nach der Operation eine intensivmedizinische Überwachung empfehlenswert, um eine bedrohliche Nachblutung mit Luftröhrenkompression oder sonstige Komplikationen sofort erkennen zu können.
- allgemeine Operationsrisiken
- Typische Risiken einer Schilddrüsenoperation
- Nachblutung in den Hals mit Kompression der Luftröhre
- Wundinfektion am Hals
- Verletzung des Stimmbandnerves
- Entfernung der Nebenschilddrüse mit nachfolgender Unterfunktion der Nebenschilddrüse
(Hypoparathyreodismus mit tetanischen Krämpfen)
Ablauf einer Schilddrüsenoperation
[Bearbeiten]( Vorsicht! Der folgende Abschnitts ist m.E.überarbeitungsbedürftig Benutzer:Rho)
Die Schilddrüsenchirurgie ist eine nahezu jahrhundertealte, bewährte Methode zur Behandlung von Schilddrüsenerkrankungen. In erster Linie werden drei Erkrankungsformen der Schilddrüse operativ erfaßt:
bösartige (Struma maligna), entzündliche (Thyreoiditis) Erkrankungen und die stoffwechsel störenden(funktionelle,hormonelle)Veränderungen.
Allen Operationsmethoden gemein ist die Verkleinerung oder die Entfernung des ganzen Organs mit dem Ziel das veränderte Gewebe aus dem Körper zu eliminieren oder die schädigenden Stoffwechsel produkte (Hormone) zu reduzieren.
Ein gänzliches Fehlen von Schilddrüsenhormonen ist mit dem Leben nicht vereinbar.Zu keinem Lebensalter. Ein Grundsatz, der niemals außer acht gelassen werden darf.
Genauso bedeutet ein Überangebot an Schilddrüsenhormon eine ernste Gefahr für dessen Träger:alle Organfunktioen arbeiten auf einem erhöhten Energielevel, d.h. die Reserven werden leichter erschöpft,was zu anhaltenden Organstörungen führen kann (!! Herzversagen !!).
Bis in die 70er Jahre wurde die Schilddrüsenchirurgie in Lokaler Betäubung vorgenommen,was für den Operateur gewisse Vorteile bot (geringeres Risiko einer Nervenverletzung) andererseits aber für den Patienten gelegentlich eine unerträgliche Qual darstellte, wenn z.B. die Masse der Schilddrüse zu voluminös war und operationstechnische Schwierigkeiten auftraten. Die Vollnarkose durch einen Narkosearzt ist daher obligat und vereinfacht das Verfahren erheblich.
Kurz umrissen sollen die Ziele der Operation bei den drei großen Schilddrüsenerkrankungen genannt sein:
- Schilddrüsenkrebs:
- möglichst totale Entfernung des erkrankten Organs. Bei Befall von ortsständigen Lymphknoten deren radikale Entfernung und bei Einbruch in Nachbarorgane deren Beseitigung (neck dissection)
- Schilddrüsenentzündung:
- totale Entfernung des gesamten Organs. Da dieses meist im Zuge einer sog.Autoimmunerkrankung miterkrankt (Hashimoto-,Riedel -Thyreoiditis) und das Organ ohnehin durch den Entzündungsprozess ausbrennt. Bakterielle Schilddrüsenentzündungen sind heutzutage nahezu ausgestorben.
- Hormonelle Schilddrüsenerkrankungen:
- hier werden über- oder unteraktiver Knoten ("heiß" oder "kalt) aus dem Gewebe entfernt. Die Schilddrüse ganz oder zum Teil entfernt.
Stets muss nach allen Operationen Schilddrüsenhormon in angemessener Dosis (nach dem Körpergewicht und Alter) eingenommen werden.
Mit dem Kocherschen Zugang werden am Hals und nach hinten abgeknickten Kopf ca 4-6 cm vom oberen Brustbeinende Haut- und Muskelplatte (Platysma) durchtrennt.
In allen Operationsschritten ist von nun an auf subtilste Blutstillung zu achten ,da die Schilddrüse extrem gut durchblutet ist. Möglichst stumpf d.h. ohne Einsatz von Skalpell und Schere werden die kurzen Halsmuskeln von der Schilddrüse abgeschoben und die spiegelnde Kapsel zur Darstellung gebracht.
Mit dem Zeigefinger kann man, nach Freilegung, das Organ umfahren und damit vorsichtig aus seiner Umgebung lösen. Doch: bietet sich dem Finger irgendeinen Widerstand: sofort denselben in seinem Tatendrang bremsen. Denn es finden sich massenhaft feiner Venen, die ekelig bluten und die man selten wiederfindet.
Mit großen runden Nadeln durchsticht man ein oder mehrmals die beiden Seiten-Lappen. Und legt damit sog. Haltefäden an, mit denen man einfach die Schilddrüsenlappen aus ihrer Loge mobilisieren kann.
Im nächsten Schritt werden die sog. oberen Polgefäße unterbunden (Aa.thyr.supp) und abgetrennt. Anschließend der Steg zwischen den beiden Seitenlappen (Isthmus). Nun folgt eine Sissyphus - Arbeit: das Aufsuchen und Unterbinden der unterschiedlich vorhandenen dicken oder dünnen, vielen oder wenigen, dick- oder dünnwandigen Seitenvenen. Dann werden die unteren Polgefäße dargestellt, unterbunden und durchtrennt. Ein nicht ganz leichter Akt,den im Gegensatz zu den oberen Polgefäßen teilen sich die unten oft schon vor der Schilddrüse oder sind nicht dort anzutreffn, wo man sie erwartet,weil sie aus einem tieferliegenden Blutgefäß entspringen als die oberen. Hier droht auch die erste Nervenverletzung (N.recurrens. Früher verzichtete man oft auf diesen nicht ungefährlichen Operationsschritt und versorgte die Blutung bei der späteren Kapselnaht. Ist die Versorgung der unteren Polgefäße geglückt, folgt die Schilddrüsen Resektion, d.h. die Verkleinerung oder Entfernung des Drüsenkörpers.
Hierbei muss immer der Nervus recurrens dargestellt werden. Seine Lähmung hat immer eine Katastrophe für den Operierten zur Folge:
Stimmbandlähmung! Er kann nicht mehr beschwerdefrei atmen, nicht mehr laut sprechen,nie wieder einen Ton singen ! Trotz sorgfältigster Unterbindung der zu und abführenden Blutgefässe ist stets mit einer mehr oder minder ausgeprägten Blutung bei der eigentlichen Resektion zu rechnen,was daran liegt, dass dieses höchststoffwechselaktive Organ auch noch aus vielen kleinen Gefässen mit versorgt wird. Es folgt die Kapselnaht,d.h. das Restgewebe wird mit einer fortlaufenden Naht zusammengezogen,um die Blutung zu beenden. Der N. wird fortgesetzt streng beachtet und nicht verletzt!
Es werden heiße Mullstreifen in die entstandnen Logen der Schilddrüsenlappen eingebracht und mit Haken festgehalten und einige Minuten abgewartet. Abschließend werden diese wieder hinausgelöst und die Bluttrochkenheit kontrolliert. Zwei Saugdrainagen werden eingebracht und die Halsmuskulatur kulissenartig vor die Schilddrüsenlogen gebracht bzw., nach Durchtrennung, wieder vernäht. Im letzten Schritt wird der Kopf des Operierten wieder nach vorne gebeugt und nur die Haut geklammert (Kölner Sparklammern) oder intracutan genäht. Beendet wird der Eingriff mit einem sterilen Wundverband.Die Muskelplatte (Platysma) darf nicht genäht werden :Narbenbildung.
Präparat zur Histologie
Im Aufwachraum läßt der Operateur den Patienten nacht Entfernen des Tubus "Amerika" sagen. Das geht nur, wenn der Nerv heil geblieben ist.
OP-Verfahren
[Bearbeiten]
- Solitäres autonomes Adenom:
- Knotenresektion
- Nur der heiße Knoten wird entfernt , die restliche gesunde Schilddrüse wird belassen
- Knotenresektion
- Euthyreote Struma
- subtotale Resektion. bds
- Entfernung der Schilddrüse beidseits bis auf einen kleinen Rest
- subtotale Resektion. bds
- Multifokale Adenome:
- funktionsorientierte Resektion bis zur subtotalen Resektion bds.
- Entfernung der knotigen Schilddrüseanteile beidseits
- funktionsorientierte Resektion bis zur subtotalen Resektion bds.
- Neckdissection
- Entfernung aller Lymphknoten am Hals bei Schilddrüsenkrebs mit Lymphknotenbefall oder Kehlkropfkrebs
- Die radikale Neckdissektion wird nur selten durchgeführt. Man macht häufiger die modifizierte Neckdiessektion. Dabei bleibt der M. sternocleidomasteoideus, die V. Jugularis interna, der N. vagus und der N. accessorius erhalten.
- Entfernung aller Lymphknoten am Hals bei Schilddrüsenkrebs mit Lymphknotenbefall oder Kehlkropfkrebs

OP-Technik
[Bearbeiten]Subtotale Resektion:
- Lagerung:
- halbsitzende Position mit Reklination des Kopfes
- Unterpolsterung der Fersen und Knie mit einem Polster.
- Halbrolle unter die Oberschenkel
Ablauf:
- Kocherscher Kragenschnitt: Haut, Subkutis und Platysma
- Durchtrennung der Faszie und Präparation der Faszienvenen die ligiert und durchtrennt werden
- Längsspaltung der geraden Halsmuskulatur, bei großen Strumen wird die Muskulatur quer durchtrennt
- Stumpfes Freilegen des Strumalappens
- Durchtrennen des Isthmuses und Freilegen der Trachea
- Hervorluxieren des SD-Lappens
- Eventuell Darstellung des N. laryngeus recurrens
- Ligatur der unteren SD-Arterie
- Ligatur und Durchtrennung der Gefäße am oberen Pol
- Entwicklung des unteren Poles
- Resektion der SD-Seite, über Kocherklemmen oder unter schneller Blutstillung
- Durchgreifende Kapselnaht mit Maxon
- Gleiches Vorgehen auf der anderen Seite
- Je eine Redondrainage 12 Charrier in die Wundhöhle
- Schichtweiser Wundverschluß
- Verband
Postoperative Nachsorge
[Bearbeiten]Statistik
[Bearbeiten]Alle medizinischen Operationen und aufwendigeren diagnostischen Methoden werden mittels eines Ziffernkataloges OPS-301 verschlüsselt. Die die OPS Nummern für Schilddrüsenoperationen sind im folgenden augelistet.
- Kapitel: 5
- OPERATIONEN
- (5-01...5-99)
- Operationen an endokrinen Drüsen
- (5-06...5-07)
- OPERATIONEN
Hinw.: Die Anwendung mikrochirurgischer Technik ist, sofern nicht als eigener Kode angegeben, zusätzlich zu kodieren ( 5-984 )
Die Anwendung von Lasertechnik ist, sofern nicht als eigener Kode angegeben, zusätzlich zu kodieren ( 5-985 )
Die Durchführung der Operation im Rahmen der Versorgung einer Mehrfachverletzung ist zusätzlich zu kodieren ( 5-981 )
Die Durchführung der Operation im Rahmen der Versorgung eines Polytraumas ist zusätzlich zu kodieren ( 5-982 )
Die Durchführung einer Reoperation ist, sofern nicht als eigener Kode angegeben, zusätzlich zu kodieren ( 5-983 )
Der vorzeitige Abbruch einer Operation ist zusätzlich zu kodieren ( 5-995 )
5-06 Operationen an Schilddrüse und Nebenschilddrüse
[Bearbeiten]Hinw.: Bei fehlender Seitenangabe ist die Operation als einseitiger Eingriff zu kodieren
Eine durchgeführte Neck dissection ist gesondert zu kodieren ( 5-403 )
- 5-060 Inzision im Gebiet der Schilddrüse
- 5-060.0 Ohne weitere Maßnahmen
- 5-060.1 Drainage
- 5-060.2 Exploration
- Inkl.: Biopsie der Schilddrüse
- 5-060.3 Revision der Operationswunde
- 5-060.x Sonstige
- 5-060.y N.n.bez.
- 5-061 Hemithyreoidektomie
- Hinw.: Eine durchgeführte Neck dissection ist gesondert zu kodieren ( 5-403 )
- 5-061.0 Ohne Parathyreoidektomie, ohne Monitoring des N. recurrens
- 5-061.1 Ohne Parathyreoidektomie, mit Monitoring des N. recurrens
- 5-061.2 Mit Parathyreoidektomie, ohne Monitoring des N. recurrens
- 5-061.3 Mit Parathyreoidektomie, mit Monitoring des N. recurrens
- 5-061.x Sonstige
- 5-061.y N.n.bez.
- 5-062 Andere partielle Schilddrüsenresektion
- 5-062.0 Exzision von erkranktem Gewebe
- 5-062.1 Exzision eines Knotens
- 5-062.2 Subtotale Resektion, einseitig
- 5-062.3 Subtotale Resektion, beidseitig
- 5-062.4 Subtotale Resektion, einseitig mit Exzision eines Knotens der Gegenseite
- 5-062.5 Subtotale Resektion, einseitig mit Hemithyreoidektomie der Gegenseite
- 5-062.6 Reexploration mit partieller Resektion
- 5-062.7 Resektion des Isthmus
- 5-062.x Sonstige
- 5-062.y N.n.bez.
- 5-063 Thyreoidektomie
- Hinw.: Eine durchgeführte Neck dissection ist gesondert zu kodieren ( 5-403 )
- 5-063.0 Ohne Parathyreoidektomie, ohne Monitoring des N. recurrens
- 5-063.1 Ohne Parathyreoidektomie, mit Monitoring des N. recurrens
- 5-063.2 Mit Parathyreoidektomie, ohne Monitoring des N. recurrens
- 5-063.3 Mit Parathyreoidektomie, mit Monitoring des N. recurrens
- 5-063.4 Reexploration mit Thyreoidektomie, ohne Monitoring des N. recurrens
- 5-063.5 Reexploration mit Thyreoidektomie, mit Monitoring des N. recurrens
- 5-063.x Sonstige
- 5-063.y N.n.bez.
- 5-064 Operationen an der Schilddrüse durch Sternotomie
- Hinw.: Eine durchgeführte Neck dissection ist gesondert zu kodieren ( 5-403 )
- 5-064.0 Exzision von erkranktem Gewebe
- 5-064.1 Subtotale Resektion
- 5-064.2 Hemithyreoidektomie
- 5-064.3 Thyreoidektomie
- 5-064.x Sonstige
- 5-064.y N.n.bez.
- 5-065 Exzision des Ductus thyreoglossus
- 5-065.0 Exzision einer medianen Halszyste, ohne Resektion des medialen Zungenbeines
- 5-065.1 Exzision einer medianen Halszyste, mit Resektion des medialen Zungenbeines
- 5-065.2 Exzision einer medianen Halsfistel, ohne Resektion des medialen Zungenbeines
- 5-065.3 Exzision einer medianen Halsfistel, mit Resektion des medialen Zungenbeines
- 5-065.4 Sekundärer Eingriff, ohne Resektion des medialen Zungenbeines
- 5-065.5 Sekundärer Eingriff, mit Resektion des medialen Zungenbeines
- 5-065.x Sonstige
- 5-065.y N.n.bez.
- 5-066 Partielle Nebenschilddrüsenresektion
- 5-066.0 Exzision von erkranktem Gewebe
- 5-066.1 Reexploration mit partieller Resektion
- 5-066.x Sonstige
- 5-066.y N.n.bez.
- 5-067 Parathyreoidektomie
- 5-067.0 Ohne Replantation
- 5-067.1 Mit Replantation (Autotransplantation)
- 5-067.x Sonstige
- 5-067.y N.n.bez.
- 5-068 Operationen an der Nebenschilddrüse durch Sternotomie
- 5-068.0 Exzision von erkranktem Gewebe
- 5-068.1 Parathyreoidektomie ohne Replantation
- 5-068.2 Parathyreoidektomie mit Replantation (Autotransplantation)
- 5-068.x Sonstige
- 5-068.y N.n.bez.
- 5-069 Andere Operationen an Schilddrüse und Nebenschilddrüsen
- 5-069.0 Naht (nach Verletzung)
- .00 Schilddrüse
- .01 Nebenschilddrüse
- 5-069.1 Plastische Rekonstruktion
- .10 Schilddrüse
- .11 Nebenschilddrüse
- 5-069.2 Exzision einer Zungengrundschilddrüse
- .20 Transoral
- .21 Transzervikal, ohne Resektion des medialen Zungenbeines
- .22 Transzervikal, mit Resektion des medialen Zungenbeines
- .2x Sonstige
- .2y N.n.bez.
- 5-069.x Sonstige
- 5-069.y N.n.bez.
- 5-069.0 Naht (nach Verletzung)
Adressen
[Bearbeiten]Literatur
[Bearbeiten]- Eva Nicole Seidel-Schneider
- DISSERTATION Die Risikofaktoren und Komplikationen in der chirurgischen Strumatherapie
- vorgelegt der Medizinischen Fakultät der Humboldt-Universität zu Berlin
- DISSERTATION Die Risikofaktoren und Komplikationen in der chirurgischen Strumatherapie
- Chirurgische Therapie bei beidseitiger benigner Struma nodosa: Abwägung zwischen Radikalität und Komplikationen
- Dtsch Arztebl Int 2014; 111(10): 171-8; DOI: 10.3238/arztebl.2014.0171
- Rayes, Nada; Seehofer, Daniel; Neuhaus, Peter
- Dtsch Arztebl Int 2014; 111(10): 171-8; DOI: 10.3238/arztebl.2014.0171
Links
[Bearbeiten]- http://www.schilddruesenguide.de/jaehne_beuleke.html
- Gut verständliche Angaben zur Schilddrüsen Operation
- http://www.aok.de/bund/tools/medicity/therapie.php?icd=57
- Allgemein verständliche Angaben zur Schilddrüsen Operation
- http://www.kueterscheck.de/folge_2.htm
- http://edoc.hu-berlin.de/dissertationen/seidel-schneider-eva-nicole-2004-04-30/PDF/Seidel-Schneider.pdf
Radiojodtherapie
[Bearbeiten]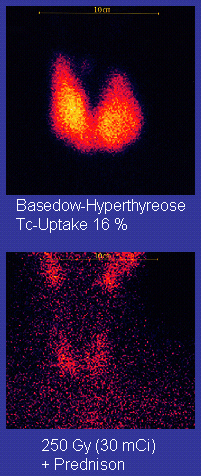
Allgemeines
[Bearbeiten]Die Radioiodtherapie (RIT, auch Radiojodtherapie, RJT) ist ein bewährtes, gut wirksames nuklearmedizinisches Therapieverfahren zur Behandlung der Schilddrüsenautonomie, der Basedow-Krankheit, der Schilddrüsenvergrößerung und bestimmter Formen des Schilddrüsenkrebses. Eingesetzt wird das radioaktive Iod-Isotop 131Iod, das ein überwiegender Beta-Strahler mit einer Halbwertszeit von acht Tagen ist und im menschlichen Körper nur in Schilddrüsenzellen gespeichert wird.
Die RIT unterliegt in vielen Ländern bestimmten gesetzlichen Voraussetzungen und kann in Deutschland nur stationär durchgeführt werden. Die Therapieform wird seit den 1940er Jahren angewendet und ist nebenwirkungsarm und auch in der langjährigen Verlaufsbeobachtung weitgehend sicher. In Deutschland existieren etwa 150 Therapieeinrichtungen, in denen etwa 60.000 bis 70.000 Behandlungen jährlich durchgeführt werden.
Grünwald">F. Grünwald, C. Menzel. Radioiodtherapie. In: T. Kuwert, F. Grünwald, U. Haberkorn, T. Krause. Nuklearmedizin. Stuttgart, New York 2008 ISBN 978-3-13-118504-4
Anwendungsgebiete
[Bearbeiten]Die Radioiodtherapie ist ein nuklearmedizinisches Therapieverfahren, das bei verschiedenen Erkrankungen der Schilddrüse durchgeführt wird. Die häufigsten Grüne für die Behandlung sind
- die autonomen Funktionsstörungen der Schilddrüse (Autonomes Adenom, multifokale Autonomie),
- die Basedow-Krankheit (Morbus Basedow) und
- diejenigen Formen des Schilddrüsenkrebses (Schilddrüsen-Karzinom), die Iod speichern:
- das papilläre und das follikuläre Schilddrüsenkarzinom.
Auch eine Schilddrüsenvergrößerung (Struma) ohne Funktionsstörung kann mittels Radioiodtherapie behandelt werden.
Eine Schwangerschaft gilt als absolute Kontraindikation für die Radioiodtherapie bei gutartigen Schilddrüsenerkrankungen. Aus allgemeinen strahlenbiologischen Erwägungen wird empfohlen, bis zu 6 Monate nach der RIT eine Schwangerschaft zu vermeiden. Tritt in dieser Zeit doch eine Schwangerschaft ein, so ist dies aber kein ausreichender Grund für einen Schwangerschaftsabbruch. Es wird jedoch empfohlen, eine genetische Beratung in Anspruch zu nehmen. Für die Radioiodtherapie beim Schilddrüsenkrebs in der Schwangerschaft gilt, dass zwar die theoretische Wahrscheinlichkeit für das Auftreten einer genetischen Schädigung berechenbar ist, solche Schäden in der Realität aber bisher nicht aufgetreten sind.
Alternative Behandlungsverfahren sind für die Funktionsstörungen die verschiedenen Formen der Schilddrüsenoperation. Der Morbus Basedow kann in einem Teil der Fälle unter der medikamentösen Behandlung mit Thyreostatika vorübergehend oder dauerhaft in seiner Aktivität nachlassen, als endgültige („definitive“) Therapie kommt neben der RIT auch die Operation in Frage. Bei den Schilddrüsen-Karzinomen kann nur beim papillären Karzinom im Frühstadium pT1a nach der Operation auf die Radioiodtherapie verzichtet werden. Zur Behandlung der gutartigen Schilddrüsenvergrößerung werden die medikamentöse Therapie, Operation und RIT eingesetzt.
Wenn die Wahl zwischen Operation und Radioiodtherapie besteht, sprechen folgende Argumente für die RIT:
- Wenn die Schilddrüse bereits operiert worden war oder bereits eine (einseitige) Lähmung des Stimmbandnervens (Rekurrensparese) vorliegt,
- bei Patienten in höherem Lebensalter oder mit schweren Begleiterkrankungen,
- wenn die Schilddrüse relativ klein ist oder
- der Patient unter Operationsangst leidet.
Jugendliches Alter gilt nicht mehr als Kontraindikation.
Folgende Argumente sprechen dagegen für die Operation:
- Verdacht auf Bösartigkeit,
- durch Iod verursachte Schilddrüsenüberfunktion (Hyperthyreose),
- Schwangerschaft und Stillzeit,
- floride Augenbeteiligung bei Morbus Basedow (endokrine Orbitopathie),
- Zeichen einer Einengung (Kompression) der Nachbarstrukturen
- Luftröhre: Stridor,
- Speiseröhre: ausgeprägte Schluckstörung,
- Halsgefäße: obere Einflussstauung
- Strahlenangst oder
- größere kalte Gebiete der Schilddrüse.
Gesetzliche Voraussetzungen
[Bearbeiten]In den meisten Ländern unterliegt die Durchführung der Radioiodtherapie bestimmten gesetzlichen und quasi-gesetzlichen Regelungen. In vielen Ländern kann die Radioiodtherapie ambulant durchgeführt werden. Deutschland hat dabei ziemlich strenge Regeln, in andern Ländern sind die Bestimmungen weitaus großzügiger, so daß oft ambulante Behandlungen durchgeführt werden.
In Deutschland regeln die Strahlenschutzverordnung und die vom Länderausschuss für Atomkernenergie herausgegebene Richtlinie „Strahlenschutz in der Medizin“ die Durchführung der Radioiodtherapie. Sie legen fest, dass die Therapie nur auf einer nuklearmedizinischen Therapiestation durchgeführt werden darf. Der durchführende Arzt muss eine entsprechende Umgangsgenehmigung haben, deren Erteilung unter anderem an die Fach- und Sachkunde auf dem Gebiet der Anwendung radioaktiver Stoffe in der Diagnostik und Therapie geknüpft ist. Die Anwesenheit eines Medizinphysikexperten ist notwendig. Den Erfordernissen des Strahlenschutzes ist in Bezug auf bauliche und personelle Aspekte Rechnung zu tragen. Insbesondere muss eine geeignete Abklinganlage für radioaktiv kontaminierte Abwässer vorhanden sein. Das betreuende Personal muss regelmäßig im Strahlenschutz unterwiesen werden.
Ambulante Therapien sind in Österreich möglich. Die Grenzaktivitäten sind auch hier gesetzlich festgelegt. Auch in Österreich ist die Anwesenheit eines Medizinphysikexperten vorgeschrieben.
In der Schweiz dürfen Radioiodtherapien mit einer applizierten Aktivität bis 200 MBq ambulant durchgeführt werden.
In den USA dürfen Radioiodtherapien bis zu einer Aktivität von 1110 MBq ambulant durchgeführt werden. Die Mehrzahl der Therapien bei gutartigen Schilddrüsenerkrankungen kann damit ambulant vorgenommen werden.
Therapieprinzip und physikalische Grundlagen
[Bearbeiten]
Das verwendete radioaktive Iod-Isotop 131Iod steht in Kapselform und flüssig zur Verfügung. Es wird in der Regel oral verabreicht, kann in Ausnahmefällen (zum Beispiel bei ausgeprägten Schluckstörungen) auch intravenös appliziert werden. Bei peroraler Aufnahme wird das Iod rasch über die Magenschleimhaut aufgenommen und an das Blut abgegeben. Über den Natrium-Iodid-Symporte gelangt das Iod in die Schilddrüsenzelle und wird letztlich im Schilddrüsenfollikel gespeichert. Unter der Wirkung von TSH oder TRAK (TSH-Rezeptor-Autoantikörpern) ist die Aufnahme von Iod in die Schilddrüsenzellen erhöht. Autonome Anteile der Schilddrüse nehmen Iod unabhängig vom TSH auf.
Die besondere Eleganz der Radioiodtherapie liegt darin begründet, dass nur Schilddrüsenzellen Iod – und damit auch Radioiod – aufnehmen, andere Organe speichern kein Iod. Das nicht in der Schilddrüse gespeicherte Iod wird innerhalb kurzer Zeit über die Nieren und die Harnblase aus dem Körper ausgeschieden. Geringe Mengen werden von den Schweißdrüsen und über den Darm ausgeschieden. In geringem Maße wird Iod zwar von den Speicheldrüsen und der Magenschleimhaut ausgeschieden, über den Magen-Darm-Trakt aber wieder aufgenommen. Wegen dieser besonderen Eigenschaften des Iod-Stoffwechsels ist es möglich, sehr große Strahlendosen im Zielgewebe zur erreichen, während die übrigen Gewebe nur eine geringe Strahlenexposition haben.
131Iod ist ein in Kernreakto]en hergestelltes Nuklid und hat eine Halbwertszeit von 8,02 Tagen. Bei seinem Zerfall zu stabilem Xenon wird ein Beta-Strahl mit der maximalen Energie von 0,61 MeV und einer mittleren Reichweite von 0,5 mm frei. Diese Strahlung ist für die therapeutische Wirkung verantwortlich. Darüber hinaus wird auch Gammastrahlung mit dem Hauptpeak bei 364 keV frei, die die Schilddrüse verlassen kann und daher einerseits für die unerwünschte Strahlenexposition des Patienten und der Umgebung verantwortlich ist, andererseits aber auch für die Bildgebung und den Radioiodtest verwendet werden kann.
Die Betastrahlen bewirken in der Umgebung der Schilddrüsenzellen Schäden in der Desoxyribonukleinsäure(DNA), insbesondere Doppelstrangbrüche, die letztlich zur Einleitung des programmierten Zelltods führen.
Die Radioiodtherapie bei gutartigen Schilddrüsenerkrankungen
[Bearbeiten]Vorbereitung
[Bearbeiten]Iodkarenz
[Bearbeiten]
Um eine optimale Aufnahme des Iods in die Schilddrüse zu erreichen, sollen vor dem Radioiodtest und der Therapie mit radioaktivem Iod zusätzliche Iodquellen gemieden werden (Iodkarenz). Solche Iodquellen sind insbesondere iodhaltige Kontrastmittel, das Antiarrhythmikum Amiodaron und bestimmte iodhaltige Desinfektionsmittel. Bei wasserlöslichen Kontrastmittel reicht eine Karenzzeit von 6 Wochen. Nach der Anwendung fettlöslicher Kontrastmitteln oder des ebenfalls fettlöslichen Amiodaron kann die Schilddrüse für viele Monate blockiert sein.
Iod in nennenswerten Mengen ist in vielen Multivitaminpräparaten und Nahrungsergänzungsmitteln enthalten, sowie in Seefisch, Meeresfrüchten und bestimmten Produkten aus Algen. Diese Iodquellen sollen für etwa eine Woche vor Iodtest und Therapie vermieden werden. Die Einnahme von Iod aus iodiertem Speisesalz und mit diesem zubereiteten, industriell gefertigten Lebensmitteln ist praktisch nicht vollständig zu vermeiden.
Stoffwechseleinstellung
[Bearbeiten]
Die Radioiodtherapie soll möglichst nicht bei manifest hyperthyreoter Stoffwechsellage durchgeführt werden, da die Überfunktion durch Freisetzung der Schilddrüsenhormone Thyroxin (T4) und Trijodthyronin (T3) verstärkt werden kann. Daher sollen mit der niedrigsten möglichen Dosis von Thyreostatika in den Wochen vor der RIT normale Werte für T4 und T3 eingestellt werden. Allerdings vermindern Thyreostatika die Iodaufnahme in die Schilddrüse, so dass empfohlen wird, diese wenigstens ein bis zwei Tage vor der Radioiodherapie abzusetzen.
Bei der Schilddrüsenautonomie soll der TSH-Wert supprimiert sein, um über den thyreotropen Regelkreis die Iodaufnahme in nicht-autonome Anteile der Schilddrüse zu minimieren. Gegebenenfalls müssen hierfür zur Vorbereitung Schilddrüsenhormone gegeben werden. Bei der euthyreoten Struma wird die Therapie in der Regel ohne begleitende Schilddrüsen-gerichtete Medikamente durchgeführt.
Ermittlung der geeigneten Therapie-Aktivität
[Bearbeiten]Die deutsche Richtlinie „Strahlenschutz in der Medizin“ schreibt vor: Bei der Planung einer nuklearmedizinischen Behandlung ist die Dosis für die zu behandelnden Organe oder Gewebe [...] im voraus zu ermitteln und die danach zu verabreichende Aktivität zu bemessen. Soweit patientenspezifische Parameter benötigt werden, sind hierfür individuelle Messungen und Daten heranzuziehen.
Referenz: Richtlinie "Strahlenschutz in der Medizin" (zur StrlSchV)[1]
Bei der Ermittlung der zur Therapie notwendigen Aktivität ist in Deutschland und in Österreich neben dem Nuklearmediziner auch ein Medizinphysikexperte hinzuzuziehen. In die Berechnung gehen die Zieldosis, das Zielvolumen und das Integral der Aktivität in der Schilddrüse über die Zeit ein.
Das Zielvolumen der Radioiodtherapie und die im Zielvolumen angestrebte Energiedosis richten sich nach der zu behandelnden Erkrankung. Beim Morbus Basedow, bei der Schilddrüsenvergrößerung ohne Autonomie und bei der disseminierten Autonomie wird das sonografisch bestimmte Gesamtvolumen der Schilddrüse als Zielvolumen angenommen, bei der unifokalen und multifokalen Autonomie nur das Volumen der Adenome. Die angestrebten Zieldosen laut Leitlinie der Deutschen Gesellschaft für Nuklearmedizin zur Radioiodtherapie bei benignen Schilddrüsenerkrankungen sind in folgender Tabelle angegeben.
| Unifokale Autonomie | etwa 300 bis 400 Gy | 4,8 Tage | 4,2 Tage |
| Multifokale Autonomie | etwa 150 Gy | 5,5 Tage | 4,8 Tage |
| Disseminierte Autonomie | etwa 150 Gy | 5,5 Tage | 4,8 Tage |
| Morbus Basedow | 4,2 Tage | ||
| Ablatives Konzept | etwa 200 bis 300 Gy | ||
| Funktionsoptimiertes Konzept | etwa 150 Gy | ||
| Struma zur Verkleinerung | etwa 120 bis 150 Gy | 5,5 Tage | |
Das Aktivitäts-Zeit-Integral kann mit dem Radioiodtest ermittelt werden. Hierzu wird eine geringe Menge Radioiod verabreicht (meist peroral): etwa 1 bis 5 MBq 131Iod oder – seltener – 5 bis 10 MBq 123Iod. Zu bestimmten Zeitpunkten wird die Aktivität über der Schilddrüse gemessen und ins Verhältnis zur Ausgangsaktivität und ihrem natürlichen Zerfall gesetzt. Zu bestimmen sind die maximale Aufnahme (uptake) in Prozent und die effektive Halbwertszeit in Tagen. Je mehr Messpunkte vorliegen, desto genauer kann die Fläche unter der Kurve bestimmt werden. Aus Gründen der praktischen (ambulanten) Durchführbarkeit wird meist nur nach 24 und 48 Stunden gemessen, unter Umständen auch nur nach 24 Stunden. Beim Morbus Basedow wird wegen des beschleunigten Iodumsatzes eine erste Messung bereits nach vier bis acht Stunden gefordert. Zur genauen Bestimmung der effektiven Halbwertszeit wird eine weitere Messung nach vier bis acht Tagen notwendig. Wegen nur geringer Unterschiede der effektiven Halbwertszeit zwischen den einzelnen Patienten mit gleicher Erkrankung und gleicher Stoffwechsellage, kann die effektive Halbwertszeit auch als empirisch ermittelter Wert angenommen werden (siehe Tabelle).
Die anzuwendende Therapie-Aktivität kann dann nach der Marinelli-Formel berechnet werden.
Marinelli LD, Quinby EH, Hine GJ. Dosage determination with radioactive isotopes. Practical considerations in therapy and protection. Am J Röntgenol 1948; 59:260 - 81
Hierbei ist A die zu errechnende Aktivität, HD die angestrebte Herddosis, V das bestimmte Zielvolumen, K eine empirisch ermittelte Konstante von 24,67, Umax der maximale uptake und t0,5 eff die effektive Halbwertszeit.
Cortison-Vorbehandlung bei endokriner Orbitopathie
[Bearbeiten]Eine endokrine Orbitopathie (eO) bei Morbus Basedow kann sich unter der Radioiodtherapie verschlechtern oder erstmals auftreten. Bei vorbestehender eO wird daher ab dem Tag der RIT oder dem Tag zuvor eine Behandlung mit Glucocorticoiden (Cortison) empfohlen, die Dosierung richtet sich nach dem Schweregrad der Augenerkrankung. Beim Morbus Basedow ohne endokrine Orbitopathie ist die prophylaktische Gabe von Glucocorticoiden umstritten. Die möglichen Nebenwirkungen und Kontraindikationen der Cortison-Therapie (Diabetes mellitus, Magengeschwüre und Elektrolytstörungen) sind zu beachten.
Aufklärung
[Bearbeiten]Vor Beginn von Radioiodtest und Radioiodtherapie erfolgt eine Aufklärung. In dieser wird der Patient auf den Ablauf von Test und Therapie hingewiesen. Neben den Risiken und Nebenwirkungen der RIT ist in den Ländern, in denen die RIT nur stationär durchgeführt werden kann, insbesondere die Tatsache, dass nach Gabe der Therapieaktivität der Patient die Therapiestation nicht verlassen darf, Gegenstand des Aufklärungsgespräches. Der Patient wird außerdem darauf hingewiesen, dass regelmäßige Nachuntersuchungen medizinisch geboten und gesetzlich vorgeschrieben sind (siehe → Abschnitt Nachsorge).
Durchführung
[Bearbeiten]Nach der meist peroralen – in Ausnahmefällen intravenösen – Gabe des 131Iod muss in Deutschland der Patient mindestens 48 Stunden auf der Therapiestation verbleiben. Es wird empfohlen, etwa eine Stunde nach peroraler Einnahme nüchtern zu bleiben, bis das Radioiod weitgehend resorbiert ist.[2]
Üblicherweise erfolgen dann regelmäßige Messungen der Strahlung, diese lassen Rückschlüsse auf die im gesamten Körper des Patienten beziehungsweise in der Schilddrüse verbliebene Aktivität. Erstere ist wichtig für den Zeitpunkt der Entlassung nach der Therapie, letztere im Maximalwert und im zeitlichen Verlauf zur Kontrolle des Therapieerfolges. Es lassen sich nämlich der tatsächlich erreichte maximale Uptake (Umax) und die tatsächlich erzielte effektive Halbwertszeit (t0,5 eff) ermitteln und durch Umstellung der Marinelli-Formel (siehe oben) die tatsächlich erzielte Herddosis (HD) bestimmen. Das Zielvolumen V und die empirisch ermittelte Konstante K sind unverändert.
Sollte die Herddosis vom geplanten Wert wesentlich nach oben abweichen, so ist mit höherer Wahrscheinlichkeit mit der Entwicklung einer Schilddrüsen-Unterfunktion nach der Therapie zu rechnen und die Nachsorge entsprechend zu planen.
Sollte die Herddosis dagegen wesentlich nach unten abweichen, kann noch während des stationären Therapie-Aufenthaltes eine zusätzliche Gabe von Radioiod erfolgen, um die erwünschte Zieldosis noch zu erreichen und den Therapieerfolg zu sichern. Dabei ist zu beachten, dass aufgrund der Frühwirkung der Radioiodtherapie („stunning“) der Uptake der zweiten Dosis regelmäßig niedriger liegt, als der der ersten.
Durch die Gabe geringer Mengen nicht-radioaktiven Iods oder von Lithium nach der Gabe des Radioiods lässt sich das Verbleiben des Radioiods in der Schilddrüse und damit die effektive Halbwertszeit t0,5 eff verlängern und eine um bis zu 30 % höhere Herddosis erzielen. Hierbei sind insbesondere beim Lithium Risiken und Nebenwirkungen sowie die geringe therapeutische Breite zu beachten.[2]
Risiken und Nebenwirkungen
[Bearbeiten]Strahlenexposition
[Bearbeiten]Aufgrund der biologischen Eigenschaften von Iod und der physikalischen Eigenschaften von 131Iod verursacht die Radioiodtherapie nur eine geringe Strahlenexposition der Organe, die kein Radioiod aufnehmen. Die Strahlenexposition ist in den der Schilddrüse benachbarten Strukturen wie dem Kehlkopf oder den Nebenschilddrüsen gering – bedingt durch die geringe Reichweite der Betastrahlung aus der Schilddrüse. Einige Gewebe, die den Natrium-Iodid-Symporter exprimieren, darunter die Speicheldrüsen, Magen und die Weibliche Brust, reichern vorübergehend Iod an. Nieren, Harnblase und Darm sind an der Ausscheidung des Anteils Radioiod, der nicht in der Schilddrüse gespeichert wird, beteiligt. In allen diesen Geweben liegt ein geringes Aktivitäts-Zeit-Integral vor, die Strahlenexposition ist entsprechend gering. Sie wird bei einem Uptake des Radioiods in die Schilddrüse von 25 % für die Magenwand mit 0,46 mGy/MBq angegeben, für die Ovarien mit 0,04 mGy/MBq, das rote Knochenmark 0,07 mGy/MBq, die Leber 0,035 mGy/MBq und die Hoden mit 0,028 mGy/MBq.[3] Im Zielgewebe Schilddrüse liegt dagegen die (erwünschte) Strahlendosis um vier bis fünf Zehnerpotenzen höher: bei einem Uptake von 25 % bei 350 mGy/MBq.[3]
Die Kohortenstudien von Hall 1992 mit über 45.000 Patineten[4] und Ron 1998 mit über 35.000 Patienten[5] haben keine erhöhte Krebsmortalität der mit radioaktivem Iod behandelten Patienten festgestellt. Die American Thyroid Association (amerikanische Schilddrüsengesellschaft) weist auf eine mögliche, minimal erhöhte Inzidenz von Schilddrüsen-Karzinomen nach einer Behandlung hin.[6]
Akute Nebenwirkungen
[Bearbeiten]Nur in wenigen Fällen kommt es zu akuten Nebenwirkungen, diese sind meist harmlos. Am häufigsten ist die Radiothyreoiditis, eine schmerzhafte Entzündungsreaktion der Schilddrüse bedingt durch die akute Strahlenwirkung, die etwa drei bis fünf Tage nach Einnahme des Radioiods auftreten kann. Durch Kühlung und entzündungshemmende Medikamente wie nichtsteroidale Antirheumatika oder Glucocorticoide lassen sich die Beschwerden, die innerhalb weniger Tage abklingen, meistens gut bessern. Die die Entzündung der Schilddrüse begleitende Schwellung kann lediglich bei vorbestehender Verengung der Luftröhre (Trachealstenose) zu ernsthaften Problemen wie Luftnot führen, so dass in diesen Fällen eine vorbeugende entzündungshemmende Behandlung empfoheln wird.
Entzündliche Schwellungen der Speicheldrüsen kommen meist nur bei höheren Therapie-Aktivitäten vor.
Bei vorbestehender Schilddrüsenüberfunktion kann sich diese etwa sieben bis zehn Tage nach Beginn der Behandlung verschlechtern, bedingt durch den beginnenden Zellzerfall und die damit verbundenene Freisetzung von Hormonen, die in der Schilddrüse gespeichert waren. Diese Komplikation kann durch eine gute Einstellung einer normalen Stoffwechsellage vor der Behandlung vermieden werden.
Eine seltene Nebenwirkung nach Radioiodtherapie wegen einer Schilddrüsenautonomie (zum Beispiel Autonomes Adenom) ist das zusätzliche Auftreten einer immunogenen Hyperthyreose wenige Wochen später. Dieses Phänomen wird Marine-Lenhart-Syndrom genannt und limitiert sich meistens selbst. Die Häufigkeit wird mit 0,5 bis 1 % angegeben. In einem Teil der Fälle muss aber wegen der neu aufgetreten Überfunktion eine zweite Radioiodtherapie durchgeführt werden.
Entlassung nach der Therapie
[Bearbeiten]In Deutschland beträgt die Mindest-Aufenthaltsdauer auf der Therapiestation 48 Stunden. Die Entlassung hängt von der im Körper verbliebenen Restaktivität ab. 1999 wurde der Grenzwert für die Restaktivität erhöht: die Dosisleistung darf in 2 Meter Abstand vom Patienten 3,5 µSv/h nicht überschreiten, wodurch innerhalb eines Jahres bei einem Abstand von 2 Metern eine Strahlenexposition von 1,0 mSv nicht überschritten wird. Dies entspricht einer Restaktivität von etwa 250 MBq. Ähnliche Regelungen gelten für Österreich. In der Schweiz sind 5 mSv in 1 Meter Abstand zulässig, wodurch eine höhere Restaktivität bei Entlassung möglich ist.
In Deutschland beträgt die mittlere Verweildauer noch etwa drei bis fünf Tage und hängt im Wesentlichen vom Zielvolumen ab. Bei sehr großen Strumen kann die Aufenthaltsdauer auch zehn Tage erreichen.[2]
Bei Entlassung wird der Patient auf eventuell nach Entlassung noch zu beachtende Strahlenschutzmaßnahmen hingewiesen. Diese betreffen insbesondere den Umgang mit kleinen Kindern und Schwangeren. Auf mögliche Probleme mit Radioaktivitätsmessungen – an Flughäfen, Kernkraftwerken, Abfallbeseitigung – ist der Patient hinzuweisen, gegebenenfalls wird dem Patienten eine entsprechende Bescheinigung mitgegeben.
In besonderen Fällen – zum Beispiel eine akute Erkrankung des Patienten, die eine Untersuchung und Behandlung des Patienten außerhalb der Therapiestation notwendig machen – ist in Deutschland eine vorzeitige Entlassung möglich. Diese muss bis zu einer Dosisleistung von 17,5 µSv/h der Aufsichtsbehörde angezeigt werden, ab 17,5 µSv/h muss eine Genehmigung eingeholt werden. Bei Verlegung des Patienten auf eine andere Station muss der zuständige Strahlenschutzbeauftragte dafür sorgen, dass dort geeignete Maßnahmen zum Strahlenschutz ergriffen werden, zum Beispiel vorübergehend ein Kontrollbereich eingerichtet wird.
Nachsorge und Erfolge
[Bearbeiten]In Deutschland ist der Arzt, der die Radioiodtherapie durchgeführt hat, auch für die Nachbetreuung verantwortlich. Es hat der für die Durchführung der Behandlung verantwortliche, fachkundige Arzt die Wirkung und die Nebenwirkungen der nuklearmedizinischen Behandlung durch geeignete, in angemessenen Zeitabständen erfolgende, Nachuntersuchungen zu erfassen und zu dokumentieren; ggf. hat er eine Behandlung einzuleiten. Der Nuklearmediziner kann Teile der Nachsorge an einen fachlich geeigneten Arzt übergeben, der diesem die Ergebnisse der Nachsorge mitzuteilen hat. Das enthebt den Nuklearmediziner aber nicht von seiner Verantwortung für die Nachsorge.[1]
Je nach behandelter Erkrankung der Schilddrüse und Stoffwechsellage beziehungsweise medikamentöser Vorbehandlung werden die ersten Kontrollen der Schilddrüsen-Laborwerte nach vier bis sechs Wochen durchgeführt, beim Morbus Basedow gegebenenfalls auch eher, um die Entwicklung einer Schilddrüsenunterfunktion rechtzeitig zu erkennen. Insbesondere bei vorbestehender endokriner Orbitopathie kann eine Unterfunktion ungünstige Auswirkungen haben und muss daher frühzeitig behandelt werden.
In den meisten Fällen tritt die vollständige Wirkung der Radioiodtherapie in den ersten drei bis sechs Monaten ein, so dass nach diesem Zeitraum eine abschließende Untersuchung zur Beurteilung des Therapieeffektes und -erfolges ansteht. Diese Umfasst üblicherweise neben der Bestimmung der Schilddrüsenhormone auch ein Schilddrüsen-Sonogramm und ein -Szintigramm. Da in einem Teil der Fälle auch nach sechs Monaten noch eine gewisse Spätwirkung der Radioiodtherapie zu erwarten ist, soll die Indikation zu einer Wiederholung der Behandlung nicht zu früh gestellt werden.
Für die verschiedenen Indikationen zur Radioiodtherapie gelten unterschiedliche Therapieziele und Erfolgsquoten. Für die Autonomie der Schilddrüse ist das Ziel die Ausschaltung der autonomen Anteile der Schilddrüse. Es wird bei einer angestrebten Herddosis von 300 bis 400 Gy eine Erfolgsquote von über 90 % angegeben. Etwa 10 % der Patienten müssen wegen einer Schilddrüsenunterfunktion nach der Therapie dauerhaft mit Schilddrüsenhormonen behandelt werden („Substitution“). Bei der fokalen Autonomie kann mit einer Abnahme des Volumens der autonomen Gebiete um etwa 80 % gerechnet werden, Die Abnahme des Volumens der Gesamtschildrüse liegt bei 20 bis 50 %.
Beim Morbus Basedow ist das Ziel die dauerhafte Beseitigung der Überfunktion. Beim ablativen Therapiekonzept mit angestrebter Herddosis von 200 bis 300 Gray liegt die Erfolgsquote bei über 90 %. Allerdings sind anschließend 80 bis 90 % der Patienten dauerhaft von einer Substitution mit Schilddrüsenhormonen abhängig. Beim sogenannten funktionsoptimierten Konzept mit einer angestrebten Herddosis von etwa 150 Gray liegt die Rate an behandlungsbedürftigen Unterfunktionen zwar nur bei 40 %, allerdings die Erfolgsquote auch nur bei etwa 70 %. Insbesondere bei schwierigen Verläufen mit medikamentös nur schwer einstellbarer Überfunktion, Augenbeteiligung (endokrine Orbitopathie) oder wiederholten Rückfällen ist diese niedrige Erfolgsquote nicht akzeptabel, so dass inzwischen überwiegend das ablative Therapiekonzept angewendetet wird. Für das alternative Therapieverfahren zur RIT, die Strumaresektion, ist ebenfalls regelhaft mit einer behandlungsbedürftigen Unterfunktion zu rechnen.
Das Therapieziel bei der Struma ohne Überfunktion ist vor allem eine Verminderung der Schilddrüsengröße und die Beseitigung eventuell durch die Größe verursachter Beschwerden. Bei einem Ausgangsvolumen von 50 bis 100 ml ist mit einer Größenreduktion um etwa die Hälfte zu rechnen, bei sehr großer Struma mit einem Volumen von über 250 ml nur mit einer Reduktion um etwa 30 bis 40 %. In insgesamt über 80 % der Fälle wird eine Besserung der Beschwerden erreicht.
Die Radioiodtherapie bei bösartigen Schilddrüsenerkrankungen
[Bearbeiten]
Grundlagen
[Bearbeiten]Die Karzinome der Schilddrüse, nämlich die häufigsten Untertypen papilläres Karzinom (etwa 70 %) und follikuläres Karzinom (etwa 20 %), und ihre Absiedlungen (Metastasen) haben noch ausgeprägte Ähnlichkeiten mit ihrem Ursprungsgewebe. Zum Einen exprimieren sie den Natrium-Iodid-Symporter und haben daher die Fähigkeit zur Iodspeicherung, zum Anderen produzieren sie Thyreoglobulin, das daher als Tumormarker dienen kann. Schilddrüsenkarzinome werden nicht selten als kalte Knoten auffällig, das heißt die Neigung zur Iodspeicherung ist geringer ausgeprägt als bei gesundem Schilddrüsengewebe. Unter der Stimulation mit hohen Spiegeln von TSH besteht aber auch bei bösartigen Schilddrüsenzellen eine Aufnahme von Iod.
Anwendung
[Bearbeiten]Zu unterscheiden sind die Radioiodtherapie zur Entfernung eventuell vorhandener Reste gesunden Schilddrüsengewebes im Sinne einer unterstützenden und die Nachsorge vereinfachenden (adjuvanten) Therapie von der Behandlung eventuell vorhandener Tumorreste oder -absiedlungen (Metastasen) unter einem Anspruch auf Heilung (kurative Therapie) oder zumindest auf Lebensverlängerung und Linderung der Beschwerden (palliative Therapie).
Eine Indikation zur ablativen Radioiodtherapie besteht bei fast allen Fällen der epithelialen Schilddrüsenkarzinome. Lediglich beim papillären Mikrokarzinom (Größe kleiner als 1 cm, mit der TNM-Klassifikation pT1 N0 M0, kann unter Umständen auf eine ablative RIT verzichtet werden.[7]
Keine Indikation zur Radioiodtherapie besteht meist beim medullären und beim anaplastischen Schilddrüsenkarzinom, da diese Tumoren in der Regel kein Iod speichern. Schwangerschaft und Stillzeit gelten als absolute Kontraindikation.[7]
Vorbereitung
[Bearbeiten]Operation
[Bearbeiten]Vor der Radioiodtherapie beim epithelialen Schilddrüsenkarzinom steht grundsätzlich die Schilddrüsenoperation.Sie wird meist als komplette Schilddrüsenentfernung durchgeführt. Ein kleiner Rest von gutartigem Schilddrüsengewebe verbleibt dabei trotzdem fast immer. Bei operationstechnisch schwierigen Verhältnissen – zum Beispiel bei sehr großer Struma oder voroperierten Patienten – kann dieser Rest auch größer ausfallen, was für die weitere Behandlung der Patienten und ihre Überlebensaussichten aber keinen Nachteil bedeutet. Daher wird nicht empfohlen eine absolut vollständige Entfernung der Schilddrüse anzustreben, um eine Schädigung des hinter der Schilddrüse verlaufenden Nervus laryngeus recurrensmzu vermeiden.
Wenn Tumorreste verblieben sind, bereits Absiedlungen bestehen oder ein lokaler Rückfall ( ein Rezidiv) vorliegt, soll zunächst operativ versucht werden, die Menge an bösartigem Gewebe so weit wie möglich zu reduzieren.
Iodkarenz
[Bearbeiten]Mehr noch als bei der Radioiodtherapie gutartiger Schilddrüsenerkrankungen muss in der Phase vor der RIT des Schilddrüsenkarzinoms darauf geachtet werden, dem Patienten kein zusätzliches Iod zukommen zu lassen.
Stimulation des Schilddrüsengewebes und Iodtest
[Bearbeiten]Um für die ablative Therapie die Aufnahme (uptake) des Radioiods in den Schilddrüsenrest zu erhöhen, beziehungsweise für die kurative oder palliative Therapie überhaupt eine nennenswerte Aufnahme zu erreichen, müssen die verbliebenen Schilddrüsenzellen mit einem hohen Spiegel an TSH stimuliert werden. Der TSH-Wert soll über 30 µU/l liegen[7], normal sind (je nach Labor) etwa 0,4 bis 4 µU/l. Dieser hohe Wert wird üblicherweise dadurch erreicht, dass der Patient zunächst nach der Operation nicht mit Schilddrüsenhormonen behandelt, wie es sonst nach einer vollständigen (Thyreoidektomie) oder weitgehenden Schilddrüsenentfernung (subtotale Strumaresektion) bei gutartigen Schilddrüsenerkrankungen üblich ist. Etwa drei bis vier Wochen nach der Operation befindet sich der Patient dann in einer Schilddrüsenunterfunktion (Hypothyreose). Häufig besteht durch die Unterfunktion eine Arbeitsunfähigkeit und die Patienten sind darauf hinzuweisen, in dieser Phase wegen der verminderten Reaktionsfähigkeit kein Kraftfahrzeug zu führen und keine gefährlichen Maschinen zu steuern.
Vor der ablativen Radioiodtherapie soll ein (verkürzter) Radioiodtest von 24 Stunden durchgeführt werden. Bei einem hohen uptake wird die Therapie mit verminderter Aktivität durchgeführt, bei sehr hohem uptake ist eine Zweitoperation zur Verminderung des Schilddrüsengewebes zu erwägen.
Als Alternative zur Unterfunktion steht seit einigen Jahren gentechnisch hergestelltes, rekombinantes, humanes TSH (rhTSH) zur Verfügung, das intramuskulär gegeben werden kann und mit dem sich durch Injektionen an zwei aufeinander folgenden Tagen TSH-Spiegel am dritten und vierten Tag von meist deutlich über 30 µU/l erreichen lassen.
Als mögliche Vorteile der Anwendung von rhTSH gegenüber der Hypothyreose können gelten: besseres Allgemeinbefinden; erhaltene Arbeitsfähigkeit; Fehlen eines anhaltenden Wachstumsreizes auf eventuell noch vorhandene Krebszellen durch mehrwöchig erhöhtes TSH; niedrigere Konzentration des 131Iod im Serum und damit geringere Strahlenexposition. Die Erfolgsraten der ablativen Radioiodtherapie sind in Unterfunktion und mit rhTSH gleich hoch.[7]
Als mögliche Nachteile sind zu erwähnen: deutlich verkürzte effektive Halbwertszeit, erhöhte Mengen an nicht-radioaktivem Iod im Körper des Patienten durch die fortgesetzte Gabe der (iodhaltigen) Schilddrüsenhormone; fehlender Nachweis einer Gleichwertigkeit bei der Behandlung von Metastasen; fehlende Möglichkeit, an eine Diagnostik mit Radioiod eine Therapie anzuschließen, da der TSH-Spiegel innerhalb von wenigen Tagen wieder abfällt; hohe Kosten.
Durchführung
[Bearbeiten]Die Standardaktivität für die ablative Radioiodtherapie beträgt 3,7 GBq. Wenn nach der Operation und vor der ersten (ablativen) Radioiodtherapie nennenswerte Reste von Schilddrüsengewebe verblieben sind, wird üblicherweise eine geringere Aktivität von 1,1 bis 1,85 GBq (entsprechend 30 bis 50 mCi) eingesetzt, um eine strahlenbedingte Entzündung benachbarter Gewebe zu vermeiden.
Wenn – auch nach Ausschöpfen der operativen Möglichkeiten – noch anzunehmen ist dass bösartiges Gewebe im Körper des Patienten verblieben ist, also ein Resttumor, ein Lokalrezidiv oder Metastasen vorliegen, werden höhere Aktivitäten angewendet. Diese liegen meist im Bereich von 3,7 bis 11,1 GBq, in Einzelfällen auch deutlich darüber.
Nach der Therapie wird ein Ganzkörperszintigramm angefertigt. Die Therapie wird in etwa dreimonatigen Abständen wiederholt, bis weder das Szintigramm, das Ultraschallbild der Halsregion, noch der Tumormarker Thyreoglobulin einen Hinweis auf verbliebenes Schilddrüsengewebe (gutartig oder bösartig) geben. Eine Gesamt-Aktivität über alle durchgeführten Radioiodbehandlungen von bis zu 74 GBq wird bei sonst gesunden Patienten meist problemlos vertragen. Darüber ist mit einem erhöten Risiko für eine dauerhafte Schädigung des Knochenmarks als blutbildendes Organ zu rechnen.
Bezüglich der Entlassung nach der Therapie gelten die gleichen Fristen und Grenzwerte, wie bei der Therapie gutartiger Schilddrüsenerkrankungen.
Risiken und Nebenwirkungen
[Bearbeiten]Bei den unerwünschten Effekten der Radioiodtherapie sind die kurzfristig und akut auftretenden von den langfristig und chronisch auftretenden Nebenwirkungen zu unterscheiden und ihre jeweiligen Häufigkeiten und Tragweiten zu beachten.
Im Vergleich zur Therapie gutartiger Schilddrüsenerkrankungen werden beim Schilddrüsen-Karzinom zum Teil wesentlich höhere Aktivitäten eingesetzt. Mit der erwünschten höheren Strahlendosis im Zielgewebe sind damit auch höhere Strahlendosen in anderen Geweben verbunden.
Relativ häufig treten während der Therapie Appetitverlust, Veränderung der Geschmacksempfindung, Übelkeit und Speicheldrüsenreizung auf; selten finden sich Nackenschmerz oder - schwellung, Kopfschmerz oder vorübergehende Veränderungen des Blutbildes.[8]
Schwerwiegende Langzeitauswirkungen sind selten und betreffen meist Speichel- und Tränendrüsen (vor allem verminderte Tränen- bzw Speichelproduktion), Knochenmar] (sehr selten bei Patienten >45 Jahren Knochenmarksdepression oder myeloische Leukämie), Lungen (sehr selten strahleninduzierte Lungenentzündung, besonders Verschlechterung bei vorbestehender Pneumonie, bzw. Neuauftreten bei diffusen Lungenmetastasen) und Ovarien (vorübergehend fehlender Eisprung, gering erhöhte Mißbildungsrate bei Schwangerschaft innerhalb des ersten Jahres nach Therapie) bzw. Hoden (Azoospermie] - selten dauerhaft).[9] Der Nutzen der Radioiodtherapie übersteigt die Nebenwirkungsrate um das 4 - 40 fache. Die zu erwartende Inzidenz von Zweitkarzinomen oder Leukämie ist dosisabhängig. Eine minimale Zunahme von Zweitkarzinomen fand sich in den Organen (Speicheldrüsen, Dickdarm und Blase), in denen sich während der Therapie vorübergehend auch Iod123 in nennenswerter Menge ansammelt.[8] In einer englischen Studie an 7417 Patienten zeigte sich eine statistisch signifikante Abnahme des Auftretens von Krebs der Luftwege (Bronchien und Luftröhre).[8]
Nachsorge: Radioioddiagnostik
[Bearbeiten]Erst nach vollständiger Entfernung des nach der Operation verbliebenen Restes (Ablation) ist Thyreoglobulin als Tumormarker zu verwenden.
Geschichte
[Bearbeiten]Im Vorfeld des Einsatzes der Radioiodtherapie wurde beim Schilddrüsenkarzinom postoperativ eine Nachbestrahlung (mit Röntgenstrahlen) allgemein eingesetzt und als effektiv angesehen.
Smith A.M.: Virginia M. Monthly, 69:318-324. 1942; zuletzt eingesehen am 10. März 2008
Leddy, E. T. [Mayo Clinic, Rochester, Minn. M. Clin. North Amerika, 25:973-1009. 1941; zuletzt eingesehen am 10. März 2008]
Die Diagnose des Schilddrüsenkarzinoms bereitete jedoch noch Mitte des letzten Jahrhunderts große Probleme,
[http://cancerres.aacrjournals.org/cgi/reprint/3/5/344.pdf Bonne, C.: Over Maligne Schildkliergezwellen, (Malignant tumors of the thyroid), South African M, J., 15:1477-152, 1941; zuletzt eingesehen am 10. März 2008
sodass Begriffsüberschneidungen in der Literatur dieser Zeit wahrscheinlich sind.
1939 und 1940 veröffentlichte Joseph G. Hamilton Arbeiten über den Iodmetabolismus der Schilddrüse, wobei er radioaktives Iod bei gesunden Probanden und solchen mit Strumen unterschiedlicher Ursache einsetzte.
- Joseph G. Hamilton and Mayo H. Soley: Studies in iodine metabolism of the thyroid gland in situ by the use of radio-iodine in normal subjects and in patients with various types of goiter, Am J Physiol -- Legacy Content, Oct 1940; 131: 135 - 143.
- Joseph G. Hamilton and Mayo H. Soley: Studies in iodine metabolism by the use of a new radioactive isotope of iodine, Am J Physiol -- Legacy Content, Sep 1939; 127: 557 - 572.
Bereits in den Vorjahren hatte er zur Wirkung von Radioaktivität auf den menschlichen Körper geforscht.
- Joseph G. Hamilton and Gordon A. Alles: The physiological action of natural and artificial radioactivity, Am J Physiol -- Legacy Content, Jan 1939; 125: 410 - 413.
- Joseph G. Hamilton: The rates of absorption of the radioactive isotopes of sodium, potassium, chlorine, bromine, and iodine in normal human subjects, Am J Physiol -- Legacy Content, Nov 1938; 124: 667 - 678.
1942 wendeten S. Hertz und A. Roberts erstmals die Radioiodtherapie beim Morbus Basedow an.
- Hertz, S., Roberts, A.: Application of radioactive iodine in therapy of Grave´s disease, J div 21 (624) (1942) zuletzt eingesehen am 10. März 2008
Im selben Jahr beschrieben A.S. Keston e.a. in einer Kasuistik die aus therapeutischen und diagnostischen Zwecken durchgeführte Anwendung radioaktiven Iodes bei einer im Oberschenkelknochen sitzenden Metastase eines Schilddrüsenkarzinoms, das auf die damals übliche Therapie mit Röntgenstrahlen nicht angesprochen hatte.
Eine andere Kasuistik aus dem Jahr 1942 zeigt, dass es sich dabei noch keineswegs um ein Routinevorgehen beim Schilddrüsenkarzinom handelte.
Noch 1949 veröffentlichte Henry A. Sloviter ein Tierexperiment, in dem er die lebensverlängernde Wirkung von Iod131 beim Schilddrüsenkarzinom darstellte.
Als Erfinder der Radioiodtherapie gilt Joseph Hamilton, Neurologe aus Berkeley. Während des Manhattan-Projekts untersuchte Hamilton die Wirkung der Falloutprodukte auf den Menschen. Die erste Anwendung von 131I beim Menschen führte er 1942 durch.
Literatur und Quellen
[Bearbeiten]- F. Grünwald, C. Menzel. Radioiodtherapie. In: T. Kuwert, F. Grünwald, U. Haberkorn, T. Krause. Nuklearmedizin. Stuttgart, New York 2008 ISBN 978-3-13-118504-4
- Leitlinie der Deutschen Gesellschaft für Nuklearmedizin (DGN): Radioiodtherapie (RIT) bei benignen Schilddrüsenerkrankungen online
- Leitlinie der DGN: Verfahrensanweisung zur Radioiodtherapie (RIT) beim differenzierten Schilddrüsenkarzinom online
- Bell, Eberhard; Grünwald, Frank:
- Radiojodtherapie.Bei benignen und malignen Schilddrüsenerkrankungen. 1999. X, 142 S. m. 51 z.
- Tl. farb. Abb. 24 cm. Gebunden. 412gr. ISBN 3-540-65913-7, -SPRINGER, BERLIN-49.95 EUR
- Radiojodtherapie.Bei benignen und malignen Schilddrüsenerkrankungen. 1999. X, 142 S. m. 51 z.
Einzelnachweise
[Bearbeiten]Einzelnachweise [Bearbeiten]↑ a b c d e f g h i j k l F. Grünwald, C. Menzel. Radioiodtherapie. In: T. Kuwert, F. Grünwald, U. Haberkorn, T. Krause. Nuklearmedizin. Stuttgart, New York 2008 ISBN 978-3-13-118504-4 ↑ a b Richtlinie "Strahlenschutz in der Medizin" (zur StrlSchV) PDF (1,74 MB) ↑ Leitlinie der Deutschen Gesellschaft für Nuklearmedizin (DGN): Radioiodtherapie (RIT) bei benignen Schilddrüsenerkrankungen ↑ Marinelli LD, Quinby EH, Hine GJ. Dosage determination with radioactive isotopes. Practical considerations in therapy and protection. Am J Röntgenol 1948; 59:260 - 81 ↑ a b Robertson IS. Dosimetry of radionuclides. In: Falk S (Hrsg.). Thyroid disease. New York: Raven 1997. Zitiert nach: F. Grünwald, C. Menzel. Radioiodtherapie. In: T. Kuwert, F. Grünwald, U. Haberkorn, T. Krause. Nuklearmedizin. Stuttgart, New York 2008 ISBN 978-3-13-118504-4 ↑ Hall P, Boice JD Jr, Berg G, Bjelkengren G, Ericsson UB, Hallquist A, Lidberg M, Lundell G, Mattsson A, Tennvall J, et al. Leukaemia incidence after iodine-131 exposure. Lancet. 1992 Jul 4;340(8810):1-4. PMID 1351599 ↑ Ron E, Doody MM, Becker DV, Brill AB, Curtis RE, Goldman MB, Harris BS 3rd, Hoffman DA, McConahey WM, Maxon HR, Preston-Martin S, Warshauer ME, Wong FL, Boice JD Jr. Cancer mortality following treatment for adult hyperthyroidism. Cooperative Thyrotoxicosis Therapy Follow-up Study Group. JAMA. 1998 Jul 22-29;280(4):347-55. PMID 9686552 ↑ Homepage der American Thyroid Association; zuletzt eingesehen am 13. März 2008 ↑ a b c d Verfahrensanweisung zur Radioiodtherapie (RIT) beim differenzierten Schilddrüsenkarzinom ↑ a b c Chow S.M.: Side effects of high-dose radioactive iodine for ablation or treatment of differenciated thyroidcarcinoma, Hong Kong College Radiologist, 2005, (:127 - 135; zuletzt eingesehen am 13. März 2008 ↑ Handelman D.J., e.a.: Azoospermia after iodine-131 treatment for thyroid carcinoma, British Medical Journal, 1980, 281:1527; zuletzt eingesehen am 13. März 2008 ↑ Smith A.M.: Virginia M. Monthly, 69:318-324. 1942; zuletzt eingesehen am 10. März 2008 ↑ Leddy, E. T. [Mayo Clinic, Rochester, Minn. M. Clin. North Amerika, 25:973-1009. 1941; zuletzt eingesehen am 10. März 2008] ↑ Bonne, C.: Over Maligne Schildkliergezwellen, (Malignant tumors of the thyroid), South African M, J., 15:1477-152, 1941; zuletzt eingesehen am 10. März 2008 ↑ Joseph G. Hamilton and Mayo H. Soley: Studies in iodine metabolism of the thyroid gland in situ by the use of radio-iodine in normal subjects and in patients with various types of goiter, Am J Physiol -- Legacy Content, Oct 1940; 131: 135 - 143. ↑ Joseph G. Hamilton and Mayo H. Soley: Studies in iodine metabolism by the use of a new radioactive isotope of iodine, Am J Physiol -- Legacy Content, Sep 1939; 127: 557 - 572. ↑ Joseph G. Hamilton and Gordon A. Alles: The physiological action of natural and artificial radioactivity, Am J Physiol -- Legacy Content, Jan 1939; 125: 410 - 413. ↑ Joseph G. Hamilton: The rates of absorption of the radioactive isotopes of sodium, potassium, chlorine, bromine, and iodine in normal human subjects, Am J Physiol -- Legacy Content, Nov 1938; 124: 667 - 678. ↑ Hertz, S., Roberts, A.: Application of radioactive iodine in therapy of Grave´s disease, J div 21 (624) (1942) zuletzt eingesehen am 10. März 2008 ↑ Paschke, R. e.a.: Therapie der uni- oder multifokalen Schilddrüsenautonomie, Dtsch Arztebl 2000; zuletzt eingesehen am 10. März 2008 ↑ Keston, A. S., Ball, R. P., Frantz, V. X., and Palmer, W. W.: Storage of radioactive iodine in a metastasis from thyroid carcinoma. Science, 95:362-363. 1942; zuletzt eingesehen am 10. März 2008 ↑ Wikle, H. T., and Ritzmann, A. J.: The course of carcinoma of the thyroid gland. Report of an unusual case. Am.JL SurE., 5 6 : 507-512, 1942; zuletzt eingesehen am 10. März 2008 ↑ Sloviter H.A.: The distribution and action of a radioactive oxaxine dye in tumor-bearing mice, Cancer Research, 9:677-80, 1949; zuletzt eingesehen am 10. März 2008
Weblinks
[Bearbeiten]- Suchmaske der DGN für Radioiodtherapiezentren in Deutschland
- Informationsseite der Uni-Klinik Hamburg
- Informationsseite des Therapiezentrums für Schilddrüsenerkrankungen
- Informationsseite der Uniklinik Würzburg
- Informationsseite der TU München
- Informationsseite der Uniklinik Düsseldorf
- http://www1.us.elsevierhealth.com/THB/chapter_M016.php
Liste der selten gebrauchten Schilddrüsenwirkstoffe
[Bearbeiten]T3-Monopräparate
[Bearbeiten]- Thybon
- Trijodthyronin
Auch nach einer kompletten Entfernung der Schilddrüse reicht die Dejodase in den Organen außerhalb der Schilddrüse völlig aus, um genügend T3 aus dem T4 zu bilden. Somit ist eine alleinige T4 Therapie völlig ausreichend und für eine T3 Therapie ergibt sich nur in den seltensten Fällen eine echte Indikation.
T3-/T4-Kombinationspräparate
[Bearbeiten]- Novothyral (Verhältnis 1 : 5)
- Prothyrid (Verhältnis 1 : 10)
- Thyreotom (Verhältnis 1 : 4)
- Thyroxin-T3 Henning (Verhältnis 1 : 5)
Jod-/T4-Kombinationspräparate
[Bearbeiten]- Eferox Jod (100 µg Jod / 100 µg T4)
- Jodthyrox (100µg Jod / 100 µg T4)
- L-Thyrox Jod (150 µg Jod / T4 variabel)
- Thyreocomb (115 µg Jod / 70 µg T4)
- Thyronajod (150 µg Jod / T4 variabel)
Natürliche SD-Hormonpräparate (Schweinethyroxin)
[Bearbeiten](Von Schulmediziner nicht empfohlen !)
- Armour Thyroid (Forest Pharmaceuticals)
- Nature Thyroid (Western Research Labs)
- Westthyroid (Western Research Labs)
- ....
Liste der unwirksamen Schilddrüsenwirkstoffe
[Bearbeiten]Pflanzliche Thyreostatika
[Bearbeiten]Achtung, Von Schulmediziner nicht empfohlen !
- Lycoaktin (Steigerwald)
- Mutellon (Klein)
- Prothyrysat (Bürger, Ysatfabrik)
- Thyreogutt (Schwabe, Willmar)
- Thyreo-loges (Dr. Loges)
Homöopathische Mittel
[Bearbeiten]Achtung, Von Schulmediziner nicht empfohlen, da unwirksam !
- Hewethyreon (Hevert)
- Presselin Thyro plus (Combustin)
- Strumeel (Heel)
- Thyreoidinum (DHU)
- Thyreoidea comp (Wala)
- Thyreo Pasc N (Pascoe)
- Thyreo EM (Kairos Remedia)
- Thyreo Gastreu (Reckeweg)
- Thyreo Cyl (Liebermann)
Referenzen
[Bearbeiten]- ↑ 1,0 1,1 Richtlinie „Strahlenschutz in der Medizin“ (zur StrlSchV) bmub.bund.de, bmu.de (PDF; 841 kB)
- ↑ 2,0 2,1 2,2 F. Grünwald, C. Menzel: Radioiodtherapie. In: T. Kuwert, F. Grünwald, U. Haberkorn, T. Krause: Nuklearmedizin. Stuttgart / New York 2008, ISBN 978-3-13-118504-4.
- ↑ 3,0 3,1 Robertson IS. Dosimetry of radionuclides. In: Falk S (Hrsg.). Thyroid disease. New York: Raven 1997. Zitiert nach: F. Grünwald, C. Menzel. Radioiodtherapie. In: T. Kuwert, F. Grünwald, U. Haberkorn, T. Krause. Nuklearmedizin. Stuttgart, New York 2008 ISBN 978-3-13-118504-4
- ↑ Hall P, Boice JD Jr, Berg G, Bjelkengren G, Ericsson UB, Hallquist A, Lidberg M, Lundell G, Mattsson A, Tennvall J, et al. Leukaemia incidence after iodine-131 exposure. Lancet. 1992 Jul 4;340(8810):1-4. PMID 1351599
- ↑ Ron E, Doody MM, Becker DV, Brill AB, Curtis RE, Goldman MB, Harris BS 3rd, Hoffman DA, McConahey WM, Maxon HR, Preston-Martin S, Warshauer ME, Wong FL, Boice JD Jr. Cancer mortality following treatment for adult hyperthyroidism. Cooperative Thyrotoxicosis Therapy Follow-up Study Group. JAMA. 1998 Jul 22-29;280(4):347-55. PMID 9686552
- ↑ Homepage der American Thyroid Association; zuletzt eingesehen am 13. März 2008
- ↑ 7,0 7,1 7,2 7,3 Verfahrensanweisung zur Radioiodtherapie (RIT) beim differenzierten Schilddrüsenkarzinom
- ↑ 8,0 8,1 8,2 Chow S.M.: Side effects of high-dose radioactive iodine for ablation or treatment of differenciated thyroidcarcinoma, Hong Kong College Radiologist, 2005, (:127 - 135; zuletzt eingesehen am 13. März 2008
- ↑ Handelman D.J., e.a.: Azoospermia after iodine-131 treatment for thyroid carcinoma, British Medical Journal, 1980, 281:1527; zuletzt eingesehen am 13. März 2008


