Biochemie und Pathobiochemie: Enzyme
Allgemeines
[Bearbeiten]
Enzyme katalysieren chemische Reaktionen, indem sie die Aktivierungsenergie herabsetzen. D.h. sie stabilisieren den energetisch ungünstigen Übergangszustand. Erst so können die chemischen Reaktionen auch bei Körpertemperatur in der notwendigen Geschwindigkeit ablaufen. Die endgültige Gleichgewichtslage bleibt davon jedoch unbeeinflusst, denn die hängt nur von der freien Reaktionsenthalpie (ΔG) ab.
Die katalysierte Reaktion kann prinzipiell in beide Richtung ablaufen. Weitere Eigenschaften sind die meist hohe Substratspezifität (Schlüssel-Schloss-Prinzip) und Reaktionsspezifität der Enzyme.
Enzyme werden nach den Reaktionen, die sie katalysieren, klassifiziert:
- Oxidoreduktasen katalysieren Redoxreaktionen.
- Transferasen übertragen funktionelle Gruppen von einem Substrat auf ein anderes.
- Hydrolasen spalten Bindungen unter Aufnahme von Wasser.
- Lyasen (Synthasen) spalten komplexere Produkte zu bzw. bilden sie aus einfacheren Substraten ohne Spaltung von ATP.
- Isomerasen katalysieren isomerische Umwandlungen.
- Ligasen (Synthetasen) spalten komplexere Produkte zu bzw. bilden sie aus einfacheren Substraten mit Spaltung von ATP.
Manche Enzyme zeigen eine größere Bandbreite an katalysierten Reaktionen und können mehreren Enzymklassen zugeordnet werden.
Mechanismen der enzymatischen Katalyse
[Bearbeiten]- Säure-Basen-Katalyse
- Kovalente Katalyse
- Metallionen-Katalyse
Cofaktoren
[Bearbeiten]- Metallionen
- Magnesium (Mg) - Magnesium wird typischerweise von Kinasen genutzt (Mg-ATP als Substrat).
- Eisen (Fe) - Häm-gebundenes Eisen ist an Elektronentransportvorgängen (Enzyme der mitochondrialen Atmungskette) sowie an verschiedenen Redoxreaktionen beteiligt (Cytochrom P450, Cyclooxygenase).
- Kupfer (Cu) - Bestandteil der zytoplasmatischen Kupfer,Zink-Superoxiddismutase (SOD).
- Zink (Zn) - Bestandteil der zytoplasmatischen Kupfer,Zink-Superoxiddismutase (SOD), der Carboanhydrase, der Carboxypeptidase, der alkalischen Phosphatase und von Steroidhormon-Rezeptoren.
- Mangan (Mn) - Bestandteil der mitochondrialen Mangan-Superoxiddismutase (SOD)
- Organische Verbindungen wie z.B. Vitamine, Biopterin.
Michaelis-Menten-Kinetik
[Bearbeiten]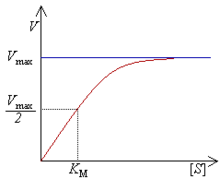
Die Geschwindigkeit v des Substratumsatzes steigt zuerst linear mit der Substratkonzentration [S] und flacht dann zunehmend ab, bis das Enzym gesättigt und die Maximalgeschwindigkeit vmax erreicht ist. vmax hängt dann nur noch von der Enzymkonzentration [E] und der Wechselzahl des Enzyms kcat ab. Die Substratkonzentration in mmol/l, bei der das Enzym mit halbmaximaler Geschwindigkeit läuft nennt man Michaelis-Konstante Km. Je niedriger die Km, desto effizienter arbeitet das Enzym. Graphisch ergibt sich eine hyperbolische Sättigungskurve.
| mit Vmax = kcat x [E] |
Lineweaver-Burk-Auftragung
[Bearbeiten]
Die Konstanten der Michaelis-Menten-Kinetik können durch doppelt reziproke Auftragung von Reaktionsgeschwindigkeit 1/V und Substratkonzentration 1/[S] ermittelt werden. Diese Darstellung wird Lineweaver-Burke-Diagramm genannt und ergibt eine Gerade. vmax kann aus dem y-Achsenabschnitt und Km aus der Steigung der Geradengleichung berechnet oder aus dem x-Achsenabschnitt abgelesen werden.
- y = Steigung mal x + y-Achsenabschnitt
Kooperativität
[Bearbeiten]
Manche Enzyme zeigen eine sigmoide Sättigungskurve. Beschrieben wurde diese Kinetik erstmals beim Sauerstoffbindungsverhalten des Hämoglobins. Ein Hämoglobin-Molekül besteht aus 4 Untereinheiten. Hat eine dieser Untereinheiten Sauerstoff gebunden, so ändert sich die räumliche Konformation und die restlichen Untereinheiten binden Sauerstoff leichter. Bezogen auf ein Enzym mit mehreren Bindungsstellen heißt das, dass die Affinität eines Enzyms für ein Substrat im Falle einer positiven Kooperativität mit der Zahl der besetzten Substrat-Bindungsstellen zunimmt.
Allosterie
[Bearbeiten]Ein allosterisch regulierbares Enzym besitzt zusätzlich zu der/den Substratbindungsstelle(n) weitere Bindungsstellen für andere Effektoren, die die Enzymaktivität modulieren können. Ein Beispiel dafür ist die Phosphofructokinase (Glycolyse), die durch den allosterischen Regulator Fructose-2,6-bisphosphat aktiviert wird.
Allosterische Liganden vom V-Typ senken die vmax. Allosterische Liganden vom K-Typ beeinflussen die Substratkonzentration, bei der 1/2 vmax erreicht wird, d.h. die Km.
Enzyminhibition
[Bearbeiten]
- Kompetitive Hemmung - Der dem Substrat strukturell ähnelnde Inhibitor konkurriert mit dem Substrat am aktiven Zentrum des Enzyms. Die Kinetik-Kurve wird nach rechts verschoben und die Km wird größer. Eine höhere Substratkonzentration kann die Hemmung durchbrechen.
- Nicht-kompetitive reversible Hemmung - Der Inhibitor bindet außerhalb des aktiven Zentrums am Enzym oder am Enzym-Substrat-Komplex. Gesenkt wird v.a. die vmax.
- Nicht-kompetitive irreversible Hemmung - Der Inhibitor bindet irreversibel und blockiert das Enzym. Die Hemmung ist mit einer höheren Substratkonzentration nicht zu durchbrechen.
- Suizidinhibitoren - Suizidinhibitoren werden im aktiven Zentrum des Enzym umgesetzt, lösen sich dann aber nicht von diesem ab. Das Enzym ist dauerhaft blockiert.
-
a) normale Umsetzung
b) kompetitive Hemmung -
a) normale Umsetzung
b) nicht-kompetitive Hemmung
Weitere Einflüsse auf die Enzymaktivität
[Bearbeiten]- Temperatur (Faustregel: Verdopplung der Geschwindigkeit bei einer Temperaturerhöhung um 10°C).
- pH - Enzyme haben bei einem bestimmten pH ihr Aktivitätsmaximum.
- Redoxgleichgewicht - Oxidations- und Reduktionsmittel können die Enzymaktivität beeinflussen.
Regulation im Organismus
[Bearbeiten]Kurzfristig:
- Änderungen der Substrat- und Produktkonzentrationen
- Allosterische Regulation z.B. in Form einer Aktivierung durch die Edukte oder als Rückkopplungshemmung (Feedback-Hemmung) durch die Produkte. Oder durch eigens gebildete Zwischenprodukte.
Mittelfristig:
- Interkonversion - Reversible kovalente Modifikation. Bsp.: Phosphorylierung des Enzyms durch spezifische Kinasen und Dephosphorylierung durch spezifische Phosphatasen.
- Lokalisation des Enzyms und Kompartimentierung der Enzymaktivitäten.
- Regulation der Halbwertszeit der mRNA (Translation) oder des Proteins (Enzym-Abbau durch Ubiquitinilierung).
- Limitierte Proteolyse - Aktivierung durch Abspaltung von bestimmten Peptidstücken am Pro-Enzym (Zymogen). Bsp.: Das Pankreasenzym Trypsinogen wird erst im Darm durch die Enteropeptidase in das aktive eiweißspaltende Trypsin umgewandelt.
Längerfristig:
- Regulation auf Ebene der DNA (Genexpression) - Repression oder Induktion der Enzyme durch Trankriptionsfaktoren.
Da Stoffwechselwege meist in Form von längeren Reaktionsketten, -kaskaden oder -zyklen organisiert sind können komplexe Stoffwechselprozesse effektiv über einzelnen Enzyme gesteuert werden, die häufig am Anfang des Stoffwechselwegs liegen und die Kaskade starten. Diese „Schrittmacherenzyme“ werden meist allosterisch oder durch Interkonversion reguliert.
Haben Ihnen die Informationen in diesem Kapitel nicht weitergeholfen?
Dann hinterlassen Sie doch einfach eine Mitteilung auf der Diskussionsseite und helfen Sie somit das Buch zu verbessern.

![{\displaystyle v={V_{max}\times [S] \over K_{m}+[S]}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/930ae4b532a3858fc08e7c3dc0bfa5597e7a4a6f)
![{\displaystyle {\frac {1}{V}}={\frac {K_{m}+[S]}{V_{max}\times [S]}}={\frac {K_{m}}{V_{\max }}}\cdot {\frac {1}{[S]}}+{\frac {1}{V_{\max }}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/7214ee9511b68400bb7eadcca115ca5c82e704a8)

