Biochemie und Pathobiochemie: Glycolyse
Allgemeines
[Bearbeiten]Die Glycolyse (Embden-Meyerhof-Parnas-Weg, E.M.P.) wurde 1929 von Gustav Embden, Otto Meyerhof und Jakub Parnas aufgeklärt. Der Stoffwechselweg ist der wichtigste Weg des Glucoseabbaus. Glucose wird darin unter Energiegewinn in zwei kleinere Bruchstücke zerlegt. Die Glycolyse nimmt im Stoffwechsel durch die Verknüpfung mit vielen anderen anabolen und katabolen Wegen eine zentrale Stellung ein.
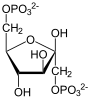
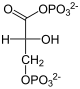
Teil 1: Spaltung von Glucose in Glycerinaldehyd-3-phosphat und Dihydroxyacetonphosphat
[Bearbeiten]| Tr. | All. | ⇓ | Subst. | ( ⇑ ) | Co. | Enzym | EC | EG | Erkr. | |||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
|
||||||||||||||
| + Insulin (HK2) | - G6P | ATP
ADP |
|
2.7.1.1 | Tr | HK1-Def. | ||||||||
| + Insulin | - GKRP | Glucokinase (Hexokinase IV) | 2.7.1.2 | MODY2, PNDM, HHF3 | ||||||||||
|
||||||||||||||
| 6-Phospho- gluconat |
|
5.3.1.9 | Iso | GPI-Def. | ||||||||||
|
||||||||||||||
|
+ Insulin |
+ ADP, AMP, F-2,6-BP |
ATP
ADP |
|
2.7.1.11 | Tr | GSD7 (Tarui) | ||||||||
|
||||||||||||||
| Zn |
|
4.1.2.13 | Ly | GSD12, Hered. Fructoseintoleranz | ||||||||||
|
|
5.3.1.1 | Iso | TPI1-Def. | ||||||||||
Im ersten Teil wird ein C6-Körper in zwei einander ähnliche C3-Körper gespalten. Dafür muss das Kohlenhydrat zuerst mit 2 Phosphat-Resten präpariert werden, wofür 2 ATP investiert werden.
Teil 2: Abbau von Glycerinaldehyd-3-phosphat zu Pyruvat
[Bearbeiten]| Tr. | Kov. | All. | ⇓ | Subst. | ( ⇑ ) | Co. | Enzym | EC | EG | Erkr. | |||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
|
|||||||||||||
| Pi + NAD+ | Pi + NAD+ |
|
1.2.1.12 | Ox | |||||||||
|
|||||||||||||
| ADP
ATP |
ADP
ATP |
|
2.7.2.3 | Tr | PGK1-Def. | ||||||||
|
|||||||||||||
|
5.4.2.1 | Iso | GSD10 | ||||||||||
|
|||||||||||||
|
H2O |
H2O |
Mg |
|
4.2.1.11 | Ly | ENO1-Def., GSD13 | |||||||
|
|||||||||||||
| + Insulin - cAMP |
- Phosph. | + F1,6BP - Alanin, ATP |
ADP
ATP |
|
2.7.1.40 | Tr | PKLR-Def., ATP-Erh. in RBC | ||||||
|
|||||||||||||
| NADH/H+ | NADH/H+ | L-Lactat-Dehydrogenase | 1.1.1.27 | Ox | GSD11, LDHB-Def. | ||||||||
|
|||||||||||||
Im 2. Teil der Glycolyse werden insgesamt 4 ATP (aus 2 Glycerinaldehyd-3-phosphat) zurückgewonnen.
Die Glycolyse
[Bearbeiten]Die Glycolyse ist die wichtigste Stoffwechselreaktionskette überhaupt. Sie findet im Zytosol statt und spaltet ein Glucosemolekül (C6) in zwei Pyruvat (C3) mit einem Nettogewinn von 2 ATP und 2 NADH/H+. Hefepilze und manche Bakterien setzen Pyruvat auch zu Ethanol um (alkoholische Gärung: Decarboxylierung von Pyruvat durch die Pyruvatdecarboxylase (EC 4.1.1.1) zu Acetaldehyd, dann NADH/H+-abhängige Reduktion zum Alkohol durch die Alkoholdehydrogenase). Der ebenfalls anaerobe Abbau zum Lactat durch die Lactatdehydrogenase entspricht der bakteriellen Milchsäuregärung z.B. durch Milchsäurebakterien. Anaerob bezieht sich hier auf die Tatsache, dass die Endprodukte Lactat oder Alkohol nicht weiter unter Sauerstoff-Verbrauch abgebaut werden, d.h. über Citratzyklus und Atmungskette.
Beim anaeroben Abbau bis zum Alkohol oder Lactat wird der vorher (in der Glycerinaldehyd-3-phosphat-Dehydrogenase-Reaktion) entzogene Wasserstoff, der als reduzierendes NADH/H+ zwischengespeichert wurde, wieder auf die Endprodukte übertragen. So wird NAD+ regeneriert und das wichtige Redoxgleichgewicht neutral gehalten. Würde die Glycolyse unter anaeroben Bedingungen (bei anaeroben Bakterien oder beim Sauerstoffdefizit im Muskel) auf Pyruvat enden, so würde die Glycolyse wegen NAD+-Mangel sehr schnell zum Stillstand kommen.
Beim in der menschlichen Zelle üblicheren Abbau bis zum Pyruvat (der ebenfalls keinen Sauerstoff benötigt) entstehen zusätzlich zu den 2 ATP noch 2 NADH/H+. Diese können für Reduktionen (Elektronenübertragungen) verwendet werden oder wie die anderen Reduktionsäquivalente z.B. aus dem Citratzyklus zur ATP-Bildung in der Atmungskette genutzt werden. Letzteres setzt jedoch ein ausreichendes Sauerstoffangebot voraus, da die Elektronen (bzw. der Wasserstoff, der sich aus je einem Elektron und einem Proton zusammensetzt) am Ende der Atmungskette auf Sauerstoff übertragen werden müssen.
Die Reaktionen im Detail
[Bearbeiten]Die Glycolyse lässt sich in zwei Teile gliedern. Im ersten Teil wird Glucose in zwei ähnliche Moleküle gespalten und es müssen pro Glucosemolekül 2 ATP investiert werden. Ähnlichkeit ist deswegen sinnvoll, damit der weitere Abbau gemeinsam stattfinden kann und nicht zwei separate Abbauwege unterhalten werden müssen. Im zweiten Teil werden 4 ATP (und 2 NADH/H+) zurückgewonnen.
Im Einzelnen laufen folgende Reaktionen ab:
- Die intrazelluläre Glucosekonzentration steht mit der extrazellulären im Diffusionsgleichgewicht. Damit die Zelle Glucose im Zytosol anreichern kann wandelt sie es mit Hilfe einer Hexokinase unter ATP-Verbrauch in Glucose-6-phosphat (G6P) um. So kann neue Glucose nachströmen. G6P kann die Zelle auch nicht mehr verlassen, da kein Transportmechanismus für G6P vorhanden ist. So werden mit der Hexokinase-Reaktion zwei Fliegen mit einer Klappe geschlagen.
- G6P kann nun in verschiedene Stoffwechselwege fließen, z.B. in die Glycogen-Synthese (Leber, Muskel) oder in den HMP-Weg. Soll G6P jedoch abgebaut werden, dann muss nun die Spaltung in zwei ähnliche Teile vorbereitet werden. G6P wird daher von der G6P-Isomerase zu Fructose-6-phosphat (F6P) isomerisiert und noch einmal von der Phosphofructokinase 1 ATP-abhängig phosphoryliert. Fructose-1-6-bisphosphat (F-1,6-BP) ist entstanden.
- F-1,6-BP wird nun von der F-1,6-BP-Aldolase in Glycerinaldehyd-3-phosphat (GAP) und Dihydroxyacetonphosphat (DHAP) gespalten. Bei den zwei C3-Körpern handelt es sich um Konstitutionsisomere. Sie können von der Triosephosphat-Isomerase leicht ineinander überführt werden und damit gemeinsam weiterverstoffwechselt werden. Der erste Teil der Glycolyse ist damit abgeschlossen und es folgt die Pay-off-Phase, beginnend mit (zwei) GAP.
- Die Oxidation der Aldehydgruppe des GAP zur Carbonylgruppe mit Hilfe der GAP-Dehydrogenase liefert 1,3-Bisphosphoglycerat (BPG). Diese Reaktion ist ausgesprochen exergon und das wird voll genutzt. Erstens wird dabei ein Reduktionsäquivalent (NADH/H+) gewonnen, zweitens ist noch genug Energie übrig, um auch noch ein anorganisches Phosphat an die neu entstandene Carboxyl-Gruppe zu heften. Letzteres macht sich in der nächsten Reaktion bezahlt.
- Die Phosphoglycerat-Kinase überträgt die Phosphatgruppe vom BPG nun auf ADP, so dass ein ATP gewonnen wird. Dies nennt man Substratkettenphosphorylierung. 3-Phosphoglycerat (3PG) ist das Endprodukt.
- Nun ist noch eine zweite Phosphatgruppe vorhanden, die gewinnbringend eingesetzt werden kann. Dafür wird 3PG zu 2PG isomerisiert (Phosphoglycerat-Mutase) und Wasser abgespalten (Enolase). Dabei kommt Phosphoenolpyruvat (PEP) heraus. PEP kann aufgrund seines hohen Gruppenübertragungspotentials als nächstes in einer zweiten Substratkettenphosphorylierung sein Phosphat auf ADP übertragen und ein weiteres ATP erzeugen. Übrig bleibt Pyruvat, das verschiedentlich weiterverstoffwechselt werden kann oder das bei Sauerstoffdefizit zum Lactat reduziert wird.
Energiebilanz
[Bearbeiten]Es werden 2 ATP investiert und über die Substratkettenphosphorylierung 4 zurückgewonnen. D.h. der anaerobe Glucoseabbau bis zum Pyruvat liefert 2 ATP. Beim Abbau bis zum Lactat bleiben zusätzlich noch 2 NADH/H+ übrig, die bei der vollständigen Oxidation über Citrazyklus und Atmungskette ca. 32 ATP liefern, also 16 mal mehr als der anaerobe Abbau der Glucose. Dafür setzt der aerobe Abbau aber auch ein ausreichendes Sauerstoffangebot und die entsprechenden Enzyme voraus, sowie beim Eukaryonten das Vorhandensein von Mitochondrien.
Regulation
[Bearbeiten]Die Transkription der Schlüssel- oder Schrittmacherenzyme wird durch Glucose und Insulin gefördert und durch cAMP gehemmt.
Der erste und durch Insulin geförderte Schritt, die Umwandlung von Glucose in Glucose-6-phosphat durch das 1. Schlüsselenzym, die Hexokinase dient der Fixierung von Glucose in der Zelle, nachdem es aus dem Blut aufgenommen wurde. Glucose-6-phosphat kann die Zelle nicht mehr verlassen. Dadurch, dass Glucose aus dem Diffusionsgleichgewicht entfernt wird, kann vermehrt neue Glucose nachströmen. Unterstützt wird dieser Prozess durch die Translokation des Glucosetransporters GLUT4 in die Plasmamembran, die ebenfalls von Insulin gefördert wird. Glucose-6-phosphat steht dann intrazellulär für zahlreiche Stoffwechselwege zu Verfügung. Darunter die Glycolyse, der Hexosemonophosphatweg, der Inositolphosphat-Stoffwechsel und nach Umwandlung in UDP-Glucose können die C6-Körper in die Glycogensynthese, die Biosynthese der Uronsäuren und den Galactose-Stoffwechsel fließen.
Das 2. Schlüsselenzym, die 6-Phosphofruktokinase katalysiert die Bildung von Fructose-1,6-bisphosphat, welches im nächsten Schritt gespalten wird. Damit ist die Phosphofruktokinase für die Einleitung des endgültigen Glucoseabbaus verantwortlich und das wichtigste Stellglied der Glycolyse. Reguliert wird das Enzym durch den wichtigsten allosterischen Regulator, das D-Fructose-2,6-bisphosphat. Fructose-2,6-bisphosphat schaltet die Phosphofruktokinase und damit die Glycolyse an und gleichzeitig die Fructose-1,6-Bisphosphatase, das komplementäre Enzym der Gluconeogenese ab.
Das 3. Schlüsselenzym ist die Pyruvatkinase. Dieses Enzym katalysiert den letzten Schritt der Glycolyse und sorgt insbesondere für den Nettogewinn von 2 ATP pro Glucosemolekül. Gehemmt wird das Enzym allosterisch von Alanin und ATP. Diese Moleküle signalisieren dem Enzym ein ausreichendes Energieangebot.
Bedeutung der anaeroben Glycolyse
[Bearbeiten]| Cori- und Glucose-Alanin-Zyklus | ||||||||||||
| ||||||||||||
| Farbcode: Stickstoffaufnahme/-transport/-abgabe |
Der anaerobe Abbau von Glucose ist die einzige Möglichkeit, wie Zellen und Gewebe auch unter Sauerstoffmangel Energie erzeugen können, wenn auch vergleichsweise ineffizient (2 ATP gegenüber maximal 32 ATP bei vollständiger Oxidation der Glucose über Citratzyklus und Atmungskette). Das entstehende Lactat wird in die Umgebung resp. das Blut abgegeben. Netto kann der Gesamtorganismus anaerob keine Energie gewinnen, da das Lactat in der Leber wieder unter hohem Aufwand (6 ATP) zur Glucose aufgebaut werden muss. Anders als bei Bakterien, die Lactat in die Umgebung abgeben, akkumuliert das Produkt rasch im Körper und muss daher wegen seiner Azidogenität (pKs = 3,86) beseitigt werden, zweitens muss die Glucose regeneriert werden, da die Vorräte sonst rasch erschöpft sind.
Der anaerobe Glucoseabbau zur Energiegewinnung spielt für den Skelettmuskel unter erhöhter Belastung eine große Rolle, wenn mehr Lactat entsteht als oxidativ in den Mitochondrien weiterverarbeitet werden kann. Das entstehende Lactat wird über den Blutweg zur Leber transportiert, dort wieder zur Glucose aufgebaut und dann zum Muskel zurücktransportiert (Cori-Zyklus). Der Abbau bis zum Lactat hat den Vorteil, dass die NADH-Bilanz neutral bleibt und damit auch das Redoxgleichgewicht in der Muskel- und Leberzelle.
Die zweite Möglichkeit besteht darin, Pyruvat durch Stickstoffübertragung in Alanin umzuwandeln (Transaminierung durch GPT bzw. AL(A)T und Pyridoxalphosphat), dieses zur Leber zu transportieren, dort wieder zu Pyruvat zu deaminieren (das frei werdende Ammoniak kann in der Leber zu Harnstoff entgiftet und über die Niere ausgeschieden werden) und wieder Glucose zu bilden. Der letztgenannte Weg, der Glucose-Alanin-Zyklus, ist wichtig, da hiermit auch der Stickstoff (-> giftiges Ammoniak) aus dem Muskel zur Leber geschafft wird, der durch die gesteigerte Proteolyse (Desaminierung glucogener Aminosäuren) vermehrt freigesetzt wird.
Erythrozyten nutzen den anaeroben Abbau von Glucose, da sie keine Mitochondrien haben. Bei lokalem Sauerstoffmangel greifen alle betroffenen Zellen auf dieses „Notstromaggregat“ zurück, um zu überleben.
Verbindungen zu anderen Stoffwechselwegen
[Bearbeiten]Siehe dazu die Stoffwechsel-Übersicht.
Glucose wird in die Zelle aufgenommen und (wenn es nicht für die Fructose-Bildung (v.a. in den Samenblasen) genutzt wird) in Glucose-6-phosphat umgewandelt, so dass es die Zelle nicht mehr verlassen kann. Glucose-6-phosphat kann dann in der Glycolyse zu Pyruvat abgebaut werden oder je nach Organ und Bedarf für die Bildung von Glycogen (Leber, Skelettmuskel), Galactose (u.a. Milchdrüse), Glucuronsäure (v.a. Leber) oder Inositolphosphate verwendet werden sowie in den Pentosephosphatweg fließen. Umgekehrt ist Glucose-6-phosphat das Endprodukt des Abbaus von Glycogen (Leber, Muskel) und Galactose.
Die nächste Station ist Fructose-6-phosphat. Hier mündet bereits wieder ein Teil des Substrats des Pentosephosphat-Shunts ein (bzw. fließt dorthin ab). F6P stellt weiterhin die Verbindung zum Mannose- und Fucose-Stoffwechsel sowie zum Aminozucker-Stoffwechsel her.
Die isomeren Spaltprodukte von Fructose-1,6-Bisphosphat - Glycerinaldehyd-3-phosphat und Dihydroxyacetonphosphat - liefern das Glycerin für die Biosynthese der Neutralfette und Phosphoglyceride. Umgekehrt kann das Glycerin aus der Lipolyse hier in die Glycolyse/Gluconeogenese einmünden. Der Abbau von Fructose liefert ebenfalls DHAP und Glycerin und das 2. Endprodukt (bzw. Edukt für die Gegenrichtung) des Pentosephosphatwegs ist Glycerinaldehyd-3-phosphat. Die Verbindungen sind hier nocheinmal dargestellt.
3-Phosphoglycerat ist der Startpunkt der Serin- und Glycin-Biosynthese.
Phosphoenolpyruvat (PEP) wird für die Synthese von N-Acetylneuraminsäure (NANA) benötigt.
Pyruvat kann durch Transaminierung in Alanin umgewandelt werden und durch Reduktion in Lactat sowie vice versa. Pyruvat ist weiterhin der Ausgangpunkt der Gluconeogenese und die mögliche Endstrecke des Abbaus von Cholin und einigen glucogenen Aminosäuren wie dem genannten Alanin, Tryptophan (über Alanin), Threonin, Serin, Glycin und Cystein (über Serin). Pyruvat kann weiterhin aus dem Citratzyklus bezogen werden (Decarboxylierung von Malat) und zu guter letzt zur Energiegewinnung oder zur Biosynthese von Fettsäuren oder Cholesterin durch dehydrierende Decarboxylierung zu Acetyl-CoA umgesetzt werden.
Transport der Reduktionsäquivalente ins Mitochondrium zur Atmungskette
[Bearbeiten]NADH (+ H+) kann die die innere Mitochondrienmembran nicht durchdringen. Die in der Glycolyse erzeugten Reduktionsäquivalente müssen jedoch irgendwie vom Zytosol ins Mitochondrium zur Atmungskette gelangen. Zur Lösung dieses Problems gibt es verschiedene Möglichkeiten.
Das Malat-Aspartat-Shuttle
[Bearbeiten]| ⇓ | Subst. | ⇑ | Co. | Enzym | EC | EG | Erkr. | |||
|---|---|---|---|---|---|---|---|---|---|---|
|
||||||||||
| NAD+ | 2. |
NAD+ | Malat-Dehydrogenase | 1.1.1.37 | Ox | |||||
|
||||||||||
| L-Glutamat | 3. |
L-Glutamat | Pyridoxal- phosphat | Aspartat-Transaminase (AST, ASAT, GOT) |
2.6.1.1 | Tr | ||||
|
||||||||||

Eine geschickte Lösung bietet die Übertragung der Elektronen auf ein Transportmolekül, in diesem Falle auf Oxalacetat, das dadurch zum Malat reduziert wird (1.). Malat wird nun in die Matrix geschafft, wo die Malat-Dehydrogenase die entsprechende Rückreaktion katalysiert, so dass die Elektronen wieder auf NAD+ übertragen werden (2.).
Nun wird der Rückweg ins Zytosol dadurch verkompliziert, dass Oxalacetat die innere Mitochondrienmembran ebenfalls nicht permeieren kann. Deswegen muss Oxalacetat in eine Form gebracht werden, für die ein Membrantransporter vorhanden ist. Oxalacetat wird also von der Aspartat-Transaminase (AST, GOT) PALP-abhängig zu Aspartat transaminiert (3). Die Aminogruppe stammt dabei von Glutamat, das durch die Transaminierung zum α-Ketoglutarat wird. Aspartat und α-Ketoglutarat gelangen nun über die entsprechenden Membrantransporter zurück ins Zytosol, die Aspartat-Transaminase sorgt noch einmal für die Rückreaktion (4.) und es entsteht wieder Oxalacetat für den nächsten Transportzyklus, sowie Glutamat, das wieder in die Matrix transportiert wird und dort für die nächste Transaminierung bereitsteht.
Das Zusammenspiel aus Umwandlungs- und Transportprozessen ergibt eine pfiffige Choreographie, die in der Abbildung rechts noch einmal schematisch dargestellt ist.
Die beteiligten Reaktionspartner Oxalacetat, Malat und α-Ketoglutarat sind (unter anderem) Intermediate des Citratzyklus.
Das Glycerin-3-Phosphat-Shuttle
[Bearbeiten]| ⇓ | Subst. | ⇑ | Co. | Enzym | EC | EG | Erkr. | |||
|---|---|---|---|---|---|---|---|---|---|---|
|
||||||||||
| NADH/H+ | 1. |
FADH2 | 1) Glycerin-3-phosphat-Dehydrogenase | 1.1.1.8 | Ox | |||||
| 2) ? | ? | Ox | ||||||||
|
||||||||||
Eine Alternative stellt das Glycerin-3-phosphat-Shuttle dar. Das Glycolyse-Intermediat DHAP wird dabei zu Glycerin-3-phosphat reduziert (1.) und überträgt sie an der inneren Mitochondrienmembran auf FAD (2.). FADH2 gibt die Elektronen an Ubichinon (Q) weiter. Das Glycerin-3-phosphat-Shuttle ist etwas schneller als das Malat-Aspartat-Shuttle, hat jedoch durch die Umgehung der NADH-Dehydrogenase (Komplex I der Atmungskette) eine etwas geringere Energieausbeute. Man findet dieses Shuttle z.B. im Gehirn und im Skelettmuskel.
In einem Nebenweg der Glycolyse entsteht 2,3-Bisphosphoglycerat
[Bearbeiten]| ⇓ | Subst. | ( ⇑ ) | Co. | Enzym | EC | EG | Erkr. | |||
|---|---|---|---|---|---|---|---|---|---|---|
|
||||||||||
|
5.4.2.4 | Iso | BPGM-Def. | |||||||
|
||||||||||
| H2O
Pi |
|
3.1.3.13 | Hyd | |||||||
|
||||||||||
1,3-Bisphosphoglycerat und 3-Phosphoglycerat sind Intermediate der Glycolyse, wobei das letzteres aus ersterem unter ATP-Gewinn und katalysiert von der Phosphoglycerat-Kinase gebildet wird (s.o.).
1,3-Bisphosphoglycerat kann jedoch auch von der Bisphosphoglycerat-Mutase zu 2,3-Bisphosphoglycerat (2,3-BPG) isomerisiert werden. Dies spielt insbesondere in Erythrozyten eine wichtige Rolle. Dort verschiebt 2,3-BPG die Sauerstoffbindungskurve des Hämoglobins durch Stabilisierung des Desoxyhämoglobins nach rechts und erleichtert so die Sauerstoffabgabe im Gewebe.
Durch die Bisphosphoglycerat-Phosphatase-Reaktion kann 2,3-BPG es zu 3-Phosphoglycerat dephosphoryliert und damit wieder der Glycolyse zugeführt werden. Die Reaktionen laufen auch unter der Bezeichnung Rapoport-Luebering-Zyklus.
Im Gegensatz zur Phosphoglycerat-Kinase-Reaktion kann hierbei kein ATP gewonnen werden.
Pathobiochemie
[Bearbeiten]Enzymdefekte der Glycolyse (bzw. Gluconeogenese) äußern sich häufig in hämolytischen Anämien, Myopathien und Neurodegeneration. Dies hat damit zu tun, dass Erythrozyten (keine Mitochondrien!) und Nervenzellen ihren Energiebedarf fast ausschließlich über Glucose decken, ebenso wie der Skelettmuskel unter anaeroben Bedingungen.
Klinische Chemie und Laboratoriumsmedizin
[Bearbeiten]Die Umschaltung des Skelettmuskels auf den anaeroben Glucoseabbau zur Energiegewinnung unter Belastung, die sog. „anaerobe Schwelle“, ist als Lactat-Anstieg im Blut messbar. Für den Sport wird allgemein aerobes Training empfohlen. Ein erhöhtes Lactat ist auch bei schweren Allgemeinerkrankungen und ischämischen Zuständen feststellbar, wenn die Sauerstoffversorgung des Organismus oder einzelner Gewebe insuffizient wird, z.B. im Schock oder bei einer Darmischämie. Die sog. metabolische Laktatazidose geht mit einer lebensbedrohlichen Übersäuerung des Körpers einher und kann verschiedenste Ursachen haben, z.B. eine Vergiftung.
Die Serum-Konzentration der Lactat-Dehydrogenase (LDH) steigt bei einem erhöhten Zellzerfall und kann daher als Parameter für z.B. Gewebsschädigungen oder Tumorerkrankungen (hoher Zellumsatz) dienen. Eine unsachgemäße Blutentnahme (Hämolyse) kann dergleichen vortäuschen. Neben der LDH können auch erhöhte Harnsäure- (Endprodukt des Purin-Stoffwechsels (DNA, RNA)) und Kalium-Spiegel (normalerweise vorwiegend intrazellulär) auf Zelluntergänge hindeuten, wenn sie nicht durch andere Störungen (Niereninsuffizienz, Gicht, Medikamente) bedingt sind.
Weblinks
[Bearbeiten]- KEGG: Glycolysis / Gluconeogenesis - Homo sapiens (human)
- RCSB PDB: Glycolytic Enzymes
- The chemical logic behind... Glycolysis von Prof. Doutor Pedro Silva.
- Glycolysis in animation (von John Kyrk)
- Glycolysis (von Donald Nicholson)
- The Biochemists' Songbook MP3 Files: In Praise of E. M. P. (Tune: "The British Grenadiers")
| Allgemeine Hintergrundfarbe für Substrate | Hintergrundfarbe Reaktionspfeile | „Schlüsselenzyme“ | |
| Energiereiche Phosphate Reduktionsäquivalente | CO2 / HCO3− C1-Reste Stickstoff |
Abk.: Tr.: Transkriptionelle Regulation, Tl.: Regulation der Translation, Lok.: Regulation über die Enzymlokalisation, Kov.: Regulation durch kovalente Modifikation, All.: Allosterische Regulation, Koop.: Kooperativer Effekt, Co.: Cofaktoren, EC: Enzymklassifikation, EG: Enzymgruppe (Oxidoreductase, Transferase, Hydrolase, Lyase, Isomerase, Ligase), Erkr.: Assoziierte Erkrankungen.
Haben Ihnen die Informationen in diesem Kapitel nicht weitergeholfen?
Dann hinterlassen Sie doch einfach eine Mitteilung auf der Diskussionsseite und helfen Sie somit das Buch zu verbessern.