Biochemie und Pathobiochemie: Phosphoglycerid-Stoffwechsel
Allgemeines
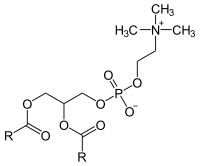
[Bearbeiten]Phospholipide bilden den Hauptteil der Lipidphase biologischer (Doppel-)Membranen. Sie bestehen aus einer hydrophilen Phosphatgruppe und meist zwei hydrophoben Fettsäuren, die über ein Glycerin verbunden sind. Man unterscheidet zwei Gruppen, Phosphoglyceride und Sphingomyeline (die Sphingomyeline gehören sowohl zu den Phospholipiden als auch zu den Sphingolipiden, denen ein eigenes Kapitel gewidmet ist).
Wichtige Phosphoglyceride, die am Aufbau von Biomembranen beteiligt sind, sind Phosphatidylethanolamin, Phosphatidylserin, sowie das mengenmäßig am häufigsten vorkommende Phosphoglycerid, das Phosphatidylcholin (Lecithin) und die Phosphatidyl-Inositole, die eine wichtige Rolle in intrazellulären Signaltransduktionskaskaden spielen.
Biosynthese von Phosphatidat (1,2-Diacylglycerin-3-phosphat)
[Bearbeiten]| ⇓ | Subst. | ( ⇑ ) | Co. | Enzym | EC | EG | Erkr. | |||
|---|---|---|---|---|---|---|---|---|---|---|
|
||||||||||
| NADH/H+ | NADH/H+ | Glycerin-3-phosphat-Dehydrogenase 1 löslich | 1.1.1.8 | Ox | ||||||
|
Ox. Akz. |
oder |
Ox. Akz. |
Flavin | oder
Glycerol-3-phosphat-Dehydrogenase 2 mitochondrial |
1.1.99.5 | |||||
|
||||||||||
| Acyl-CoA | Glycerol-3-phosphat-Acyltransferase mitochondrial | 2.3.1.15 | Tr | |||||||
|
||||||||||
| Acyl-CoA | 1-Acylglycerol-3-phosphat- O-Acyltransferase | 2.3.1.51 | Tr | |||||||
|
||||||||||
Die aufgeführten Schritte zur Biosynthese von 1,2-Diacylglycerin-3-phosphat (Phosphatidsäure bzw. Phosphatidat) sind mit den ersten Schritten der Triacylglycerinbiosynthese identisch. Phosphatidat kann auch durch Phosphorylierung von 1,2-Diacylglycerin (aus dem Triacylglycerin-Abbau) gewonnen werden (Diacylglycerinkinase, 2.7.1.107).
Phosphatidat ist der Ausgangspunkt für die Biosynthese der verschiedenen Phosphoglyceride. Phosphadidat selbst findet sich im Gewebe nur in geringen Mengen.
Biosynthese von 1-Phosphatidyl-D-myo-Inositol
[Bearbeiten]| ⇓ | Subst. | ( ⇑ ) | Co. | Enzym | EC | EG | Erkr. | |||
|---|---|---|---|---|---|---|---|---|---|---|
|
||||||||||
| CTP
PPi |
CDP-Diacylglycerol-Synthase (Phosphatidat-Cytidylyltransferase) | 2.7.7.41 | Tr | |||||||
|
||||||||||
| myo-Inositol | CDP-Diacylglycerol--Inositol-3-Phosphatidyltransferase | 2.7.8.11 | Tr | |||||||
|
||||||||||
Den weiteren Stoffwechsel der Inositolphosphate finden Sie im Kapitel Inositolphosphat-Stoffwechsel. 1-Phosphatidyl-D-myo-Inositol ist auch der Startpunkt der Biosynthese von Glycosylphosphatidylinositol-Ankern (GPI-Anker).
Biosynthese von Cardiolipin
[Bearbeiten]| ⇓ | Subst. | ( ⇑ ) | Co. | Enzym | EC | EG | Erkr. | |||
|---|---|---|---|---|---|---|---|---|---|---|
|
||||||||||
| CTP
PPi |
CDP-Diacylglycerol-Synthase (Phosphatidat-Cytidylyltransferase) | 2.7.7.41 | Tr | |||||||
|
||||||||||
| Glycerin-3-phosphat | CDP-Diacylglycerol--Glycerol- 3-phosphat-3-Phosphatidyltransferase | 2.7.8.5 | Tr | |||||||
|
||||||||||
| H2O
Pi |
Phosphatidylglycerophosphatase | 3.1.3.27 | Hyd | |||||||
|
||||||||||
| CDP-Diacylglycerin | Cardiolipin-Synthase 1 | ? | ||||||||
|
||||||||||
Cardiolipin (Diphosphatidylglycerin) findet sich in hoher Konzentration in der inneren Membran von Mitochondrien und damit auch vermehrt in Mitochondrien-reichen Geweben wie Herz und Muskel.
Klinik: Bei der Syphilis (und vielen anderen Erkrankungen, die mit Gewebsschäden einhergehen) treten Autoantikörper gegen das mitochondriale Cardiolipin (Cl) auf. Diese können mit dem sog. VDRL-Test (Veneral-Disease-Research-Laboratories-Test) in einer Agglutinationsreaktion nachgewiesen und zur Verlaufskontrolle der Syphillis genutzt werden.
Eine erbliche Erkrankung, die mit dem Cardiolipin-Stoffwechsel assoziiert ist das Barth-Syndrom.
Stoffwechsel von Phosphatidylcholin (Lecithin)
[Bearbeiten]Ausgangspunkt ist 1,2-Diacylglycerin. Dieses stammt aus dem Triacylglycerin-Abbau oder aus Phosphatidat (1,2-Diacylglycerin-3-phosphat) (s.o. und Triacylglycerinbiosynthese).
| ⇓ | Subst. | ( ⇑ ) | Co. | Enzym | EC | EG | Erkr. | |||
|---|---|---|---|---|---|---|---|---|---|---|
|
||||||||||
| H2O
Pi |
Phosphatidat-Phosphatase | 3.1.3.4 | Hyd | |||||||
|
||||||||||
| CDP-Cholin | Diacylglycerol-Cholinphosphotransferase | 2.7.8.2 | Tr | |||||||
|
||||||||||
| Sterol
Sterol-Fettsäureester |
Lecithin--Cholesterol-Acyltransferase (LCAT) | 2.3.1.43 | Tr | Fischaugenkrankheit, Norum-Krankheit | ||||||
|
|
oder | Ca | oder
Phospholipase A2 |
3.1.1.4 | Hyd | |||||
|
||||||||||
| H2O | Lysophospholipase | 3.1.1.5 | Hyd | |||||||
|
||||||||||
Spaltung von Phosphatidylcholin zu Cholin und Phosphatidat:
| ⇓ | Subst. | ( ⇑ ) | Co. | Enzym | EC | EG | Erkr. | |||
|---|---|---|---|---|---|---|---|---|---|---|
|
||||||||||
| H2O | Phospholipase D | 3.1.4.4 | Hyd | |||||||
|
||||||||||
Stoffwechsel von Phosphatidylserin und Phosphatidylethanolamin
[Bearbeiten]Biosynthese von Phosphatidylserin und Phosphatidylethanolamin aus Lecithin und sukzessive Abspaltung der Fettsäuren:
| ⇓ | Subst. | ( ⇑ ) | Co. | Enzym | EC | EG | Erkr. | |||
|---|---|---|---|---|---|---|---|---|---|---|
|
||||||||||
| L-Serin | Phosphatidylserin-Synthase | 2.7.8.- | Tr | |||||||
|
||||||||||
|
|
1. |
Ethanolamin | Pyridoxal- phosphat od. Pyruvat | 1) Phosphatidylserin- Decarboxylase | 4.1.1.65 | Ly | ||||
| 2) Phosphatidylserin- Synthase 2 | 2.7.8.- | Tr | ||||||||
|
||||||||||
| H2O | Ca | Phospholipase A2 | 3.1.1.4 | Hyd | ||||||
|
||||||||||
| H2O | Lysophospholipase | 3.1.1.5 | Hyd | |||||||
|
||||||||||
Spaltung von Phosphatidylethanolamin zu Ethanolamin und Phosphatidat:
| ⇓ | Subst. | ( ⇑ ) | Co. | Enzym | EC | EG | Erkr. | |||
|---|---|---|---|---|---|---|---|---|---|---|
|
||||||||||
| H2O
Ethanolamin |
Phospholipase D | 3.1.4.4 | Hyd | |||||||
|
||||||||||
Phosphatidylethanolamin und Phosphatidylcholin (Lecithin) besitzen eine negativ geladene Phosphat-Gruppe (Anion) und ein positiv geladenes Stickstoff-Atom (Kation), d.h. sie sind insgesamt neutral geladen. Phosphatidylserin trägt zusätzlich eine negative geladene Carboxyl-Gruppe und ist deswegen im physiologischen Milieu negativ geladen.
Weblinks
[Bearbeiten]
| Allgemeine Hintergrundfarbe für Substrate | Hintergrundfarbe Reaktionspfeile | „Schlüsselenzyme“ | |
| Energiereiche Phosphate Reduktionsäquivalente | CO2 / HCO3− C1-Reste Stickstoff |
Abk.: Tr.: Transkriptionelle Regulation, Tl.: Regulation der Translation, Lok.: Regulation über die Enzymlokalisation, Kov.: Regulation durch kovalente Modifikation, All.: Allosterische Regulation, Koop.: Kooperativer Effekt, Co.: Cofaktoren, EC: Enzymklassifikation, EG: Enzymgruppe (Oxidoreductase, Transferase, Hydrolase, Lyase, Isomerase, Ligase), Erkr.: Assoziierte Erkrankungen.
Haben Ihnen die Informationen in diesem Kapitel nicht weitergeholfen?
Dann hinterlassen Sie doch einfach eine Mitteilung auf der Diskussionsseite und helfen Sie somit das Buch zu verbessern.