Lehrbuch der Biochemie: Biomoleküle: Enzyme
Was sind Enzyme
[Bearbeiten]
Enzyme sind Proteine, die als Biokatalysatoren wirken. Sie beschleunigen biochemische Reaktionen in Lebewesen (solche Vorgänge werden als in vivo bezeichnet) und in nicht natürlicher Umgebung (in vitro, sozusagen im Reagenzglas). So ermöglichen Enzyme erst die Existenz der meisten heutigen Lebewesen, da der Großteil der Reaktionen ohne Katalyse viel zu langsam ablaufen würde.
Auch biotechnologisch haben Enzyme eine enorme Bedeutung als Reaktionsbeschleuniger in Fermentationsreaktoren.
Die Stoffe, die durch enzymatische Wirkung miteinander reagieren, nennt man Substrate.
Einteilung der Enzyme
[Bearbeiten]Je nach Art der Reaktion, die Enzyme durchführen, können Sie laut IUPAC und IUBM in 6 Gruppen eingeteilt werden:
| Gruppe | Art der Reaktion | Beispiele |
| 1. Oxidoreduktasen | Katalysieren Redoxreaktionen | Alkoholdehydrogenase, Pyruvatdehydrogenase |
| 2. Transferasen | Übertragen funktionelle Gruppen zwischen einzelnen Substraten | Pyruvatkinase |
| 3. Hydrolasen | Spalten Bindungen unter Einsatz von Wasser | Glycosidasen, Peptidasen, Esterasen |
| 4. Synthasen | Katalysieren Spaltung komplexer Substrate in einfache oder Synthese komplexer Substrate aus einfachen - ohne Mitwirkung von ATP; nichthydrolytische Addition oder Eliminierung von Molkülgruppen | Fumarase |
| 5. Isomerasen | Beschleunigen die Umwandlung von chemischen Isomeren | Epimerase |
| 6. Synthetasen oder Ligasen | Wie die Synthasen, nur werden hierbei ATP verbraucht | Pyruvatcarboxylase |
Enzymkatalysierte Reaktionen
[Bearbeiten]Reaktionsprinzip
[Bearbeiten]
Aktive Zentren
[Bearbeiten]Enzyme haben meist hochkomplexe räumliche Gestalten. Daraus ergeben sich mancherorts „Einstülpungen“ oder allgemein Plätze, die für genau ein oder ein paar wenige Substrate spezifisch Platz bieten. Durch Diffusion (z.B. im Cytoplasma) gelangt also ein Substrat an ein Enzym, wo es an einer Stelle Platz findet, also an ein aktives Zentrum gebunden wird. Aktive Zentren sind nur kleine Stellen im Enzym, meist Spalten oder Höhlungen. Das Substrat wird dabei durch mehrere schwache Wechselwirkungen im Zentrum gebunden. Durch die hohe Spezifität der Substrate, die an ein Enzym binden können, spricht man auch von Induced fit (früher: „Schlüssel und Schloss-Prinzip“).
Die Reaktion
[Bearbeiten]Mit einem Substrat ist es aber nicht getan. Ziel ist es, das bereits gebundene Substrat mit einem anderen Substrat reagieren zu lassen/zu verbinden. Das Enzym „wartet“ also, bis wieder durch Diffusion ein zweites Substrat im Zentrum bindet. Durch die Tatsache, dass die beiden an das Enzym gebundenen Substrate nun räumlich nahe beieinander sind, können die beiden Substrate letztendlich zu einem Produkt reagieren. Das ist das Geheimnis der Enzymreaktion. (Umgekehrt gilt das natürlich für ein „großes“ Substrat, das durch ein Enzym in zwei „kleine“ Produkte gespaltet wird).
Durch diesen Mechanismus erhöht man die Reaktionsgeschwindigkeit um mehrere Größenordnungen, teilweise um das 107-fache.
Substrate können sich manchmal nur in einzelnen Atomgruppen voneinander unterscheiden. Enzyme sind oft nicht selektiv genug, um zwei sehr ähnliche Substrate auseinander zu halten. Bindet eine Verindung sehr gut im aktiven Zentrum des Enzyms, so blockiert es dieses und die eigentliche Reaktion kann nicht durchgeführt werden. Es gibt Gifte, die genau das machen, und dadurch Enzymaktivitäten vermindern. Dieser Vorgang dient andererseits aber auch zur (absichtlichen und gewollten) Regulation von Enzymaktivität. Man nennt dies Inhibition von Enzymen.
Thermodynamisch bedeutet das…
[Bearbeiten]- Enzyme setzen (durch räumliche Näherbringung der Substrate bzw. Unterstützung der Spaltung von Substraten) die Aktivierungsenergie von Reaktionen herab
- Enzyme verändern die Reaktionsgleichgewichte nicht
- Sie beschleunigen lediglich die Einstellung des Gleichgewichtszustandes
Michaelis Menten Kinetik
[Bearbeiten]Im Geiste der Wissenschaft werden wir den oben beschriebenen Reaktionsmechanismus nun mathematisch und chemisch etwas genauer ausformulieren. Dabei werden wir wichtige enzymabhängige Konstanten kennenlernen.
Die Reaktionen
[Bearbeiten]Ein Substrat (S) bindet an ein Enzym (E) und es entsteht ein Enzym-Substrat-Komplex (ES). Im Normalfall handelt es sich hierbei um eine Gleichgewichtsreaktion. Inhibitoren können jedoch, wie oben bereits erwähnt, irreversibel an ein Enzym binden. Dies ignorieren wir zunächst. Die Hinreaktion wird über die Geschwindigkeitskonstante , die Rückreaktion mit charakterisiert.
Der Enzym-Substrat-Komplex reagiert dann weiter und es steht ein Produkt (Gleichgewichtskonstante ).
Die Michaelis-Konstante
[Bearbeiten]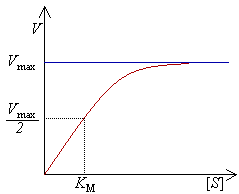
Im stationären Zustand (steady State-Prinzip) bleibt die Konzentration von ES konstant. Bildungsgeschwindigkeit und Zerfall von ES sind also gleich schnell, die Rückreaktion der Produkte zu ES kann vernachlässigt werden.
Umgeformt ergibt das die Michaelis-Menten-Konstante :
Aussage
[Bearbeiten]- ist jene Substratkonzentration, bei der die Hälfte der aktiven Zentren besetzt sind. Sie ist abhängig von pH-Wert, Temperatur und Ionenstärke.
- liegt zwischen und M
- Wenn , dann ist gleich der Dissoziationskonstante des ES-Komplexes.
Regulation der Enzymaktivität
[Bearbeiten]Organismen haben im Laufe der Evolution eine Vielfalt von Regualtionsmechanismen bezüglich der Enzymaktivität entwickelt. Manchmal sollen Enzyme daran gehindert werden, Reaktionen zu katalysieren - etwa wenn eines der Endprodukte der Reaktion momentan im Organismus nicht gebraucht wird. Wir gehen hier auf die wichtigsten Regulationsmethoden ein:
Allosterische Effekte
[Bearbeiten]Enzyme sind hochkomplexe Moleküle. Es kann passieren, dass an einer Stelle eines Enzyms ein Substrat bindet und als Folge darauf eine räumliche Umstrukturierung zum Beispiel am aktiven Zentrum einsetzt. So gibt es manche Enzyme, die nur funktionieren, wenn eine Phosphogruppe an eine bestimmte Stelle ihrer Struktur gebunden wird und so das aktive Zentrum für das Substrat räumlich passend verändert wird. Mit diesem Effekt (Phosphorilierung und Dephosphorilierung) können Organismen gezielt einzelne Enzyme ein- und ausschalten.
Inhibitoren
[Bearbeiten]Wie besprochen können Substratähnliche Moleküle an aktive Zentren binden und diese blockieren.
Enzymmenge
[Bearbeiten]Wie viele Enzyme sind an einem gewissen Ort vorhanden?
Substratmenge
[Bearbeiten]Wieviel Substrat ist an einem gewissen Ort vorhanden?
Endproduktmenge
[Bearbeiten]Wird das Endprodukt ständig vom Reaktionsort abgeführt, so stellt sich kein stationäres Gleichgewicht ein. So schaffen es Organismen, nahezu alle Substrate in Produkte zu überführen. Die Reaktionen befinden sich in einem sogenannten Fließgleichgewicht.
Coenzyme
[Bearbeiten]Bedeutung und Funktion
[Bearbeiten]Ein Coenzym ist ein niedermolekulares organisches Molekül (kein Protein) oder ein Metallion, das als Zusatzfaktor zum viel größeren Proteinanteil eines Enzyms wirkt. Das Coenzym geht im allgemeinen (wie das Substrat) verändert aus einer katalytischen Reaktion hervor und wird deshalb auch Cosubstrat genannt. Seine Regeneration geschieht typischerweise in einer nachgeschalteten Reaktion.
Wichtige Coenzyme
[Bearbeiten]NAD(P)H
[Bearbeiten]Nicotinsäure-Amid-Dinucleotid ist ein elektronentransportierendes Coenzym, das an zahlreichen Redoxreaktionen des Stoffwechsels in Lebewesen beteiligt ist. NAD+ wird durch Anlagerung eines Hydridions (H+) zweifach reduziert bzw. durch Abspaltung dessens zweifach oxidiert. So können pro Mol NAD+ 2 Mol Elektronen übertragen werden. Die Redoxreaktion sieht folgendermaßen aus:
Beachten Sie, dass bei jeder Reduktion von NAD+ zu NADH + H+ ein Proton entsteht (=Ansäuerung der Umgebung)!
NADP+ bzw. NADPH besitzen dieselbe Struktur und Funktionsweise wie die eben besprochenen Moleküle, außer dass Sie im Gegensatz zu NAD+ und NADH noch eine Phosphogruppe angelagert haben.
Im Organismus gibt es jedoch eine Klare Trennung, da NADPH beim anabolischen (=aufbauenden) Stoffwechsel gebraucht wird, während NADH beim katabolen (=abbauenden) Stoffwechsel verwendung findet. Ein großer Teil des NADH-Vorrats verbrauchen aerobe Organismen bei der oxydativen Phosphorilierung – der (Zell-)Atmung, unter Bildung von ATP.
Coenzym A
[Bearbeiten]CoA lagert Carbonsäuren in energiereicher Thioesterbindung an und beteiligt sich als Coenzym am Umsatz von Essigsäure, längerkettigen Fettsäuren und anderen Säuren. Mit anderen Worten: CoA aktiviert Fettsäuren, so dass sie weitere Reaktionen eingehen können, und andere Substanzen im Stoffwechsel, indem es mit diesen eine Thioesterbindung bildet. Besonders wichtig sind die Thioester zwischen Acetat und CoA (Acetyl-CoA) sowie zwischen Fettsäure und CoA (Acyl-CoA).
Acetyl-CoA
[Bearbeiten]Acetyl-CoA ist ein aktivierter Essigsäurerest (Acetylgruppe: ). Dieser ist an die SH-Gruppe des Cysteamin-Anteils von Coenzym A gebunden. Als Thioester ist die Verbindung energiereich, sie entsteht bei der beta-Oxidation der Fettsäuren und im Anschluss an die Glykolyse durch oxidative Decarboxylierung von Pyruvat durch den Pyruvatdehydrogenase-Enzymkomplex. Im Startschritt des Citratzyklus entsteht durch Übertragung der Acetylgruppe auf Oxalacetat der namengebende Metabolit Zitrat/Zitronensäure.






![{\displaystyle {\frac {d[\mathrm {ES} ]}{dt}}=k_{1}\mathrm {[E][S]} -k_{2}\mathrm {[ES]} -k_{3}\mathrm {[ES]} =0}](https://wikimedia.org/api/rest_v1/media/math/render/svg/96ee428be2ed77aaca5701472e63e21c9028ed36)

![{\displaystyle {\frac {\mathrm {[E][S]} }{\mathrm {ES} }}={\frac {k_{2}+k_{3}}{k_{1}}}=K_{m}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/f8b3942fb2899c217f3a0617d946c545cf94a953)




