Medizinische Mikrobiologie: Grampositive Kokken
Anaerobe Gram-positive Kokken
[Bearbeiten]Peptostreptococcus spp.
[Bearbeiten]| Peptostreptococcus spp. | ||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Systematik | ||||||||||||||||||||||||
|
Morphologie und Eigenschaften: Peptostreptococcus spp. sind eine Gattung anaerober, Gram-positiver, nicht-sporen-bildender Bakterien. Die Bakterien sind klein, rund und können einzeln, paarweise oder in kurzen Ketten vorliegen. Peptostreptococcus wächst langsam und gewinnt zunehmend Resistenzen gegen Antibiotika.
Vorkommen: Peptostreptokokken leben als Kommensalen der Normalflora im Mund, Darm und Genitaltrakt. Sie kommen weltweit vor.
Krankheitsbilder: Unter opportunen Bedingungen wie Immunsuppression oder Trauma (Wundinfektionen) können sie endogene, eitrige Infektionen der Haut, Weichteile, Gelenke, Knochen, Gehirn und inneren Organe hervorrufen.
Therapie: Die Bakterien sprechen meist auf Penicillin G und Aminopenicilline an, alternativ können Clindamycin (ein Lincosamid), Carbapeneme oder Glycopeptide (Vancomycin) angewendet werden.
Staphylokokken (Katalase-positive Kokken)
[Bearbeiten]Koagulase-positive Staphylokokken
[Bearbeiten]Staphylococcus aureus
[Bearbeiten]Etymologie: Staphylococcus ist der latinisierter Singular des griechischen σταφυλόκοκκος, d.h. „die Traubenkugel“, aus älterem Griechisch σταφυλή, staphylé, „die Weintraube“ und κόκκος, kókkos, „das Kügelchen“, aureus lateinisch „der goldene“.
Morphologie und Eigenschaften: Staphylokokken sind kugelförmige, Gram-positive Bakterien, häufig in Haufen bzw. Trauben angeordnet. Sie sind unbeweglich und bilden keine Sporen. Die Größe des Bakteriums liegt bei 0,8 - 1,2 µm. S. aureus ist fakultativ anaerob, Katalase- und Koagulase-positiv. Auf z.B. Blutagar wachsen gelb-weißliche Kulturen, meist mit β-Hämolyse.
Vorkommen: S. aureus kommt fast ubiquitär in der Natur vor, auch als Kolonisationskeim bei vielen Menschen auf der Haut und in den oberen Atemwegen.
Pathogenitäts- und Virulenzfaktoren:
- Adhäsine wie Clumping Factor A und B, Fibronectin-Bindungsprotein A und B sowie ein Kollagen-Bindungsprotein
- Polysaccharidkapsel mit Protein A -> Phagozytoseschutz
- Protein A bindet Fc-Teile von Ak -> Ak-Inaktiverung (statt Fab bindet Fc)
- Koagulase (Coa, bildet mit Prothrombin Staphthrombin) und Clumping Faktor (Clf, ein Fibrinogenbindungsprotein) -> Fibrinwall -> Schutz vor Immunsystem des Wirts
- Fibrinolysin zur Auflösung des Fibrinwalls bei Vermehrung
- Invasine: Hyaloronidase, DNAasen, Lipasen, Hämolysin, Exfoliatine A und B (5% der Staph. aureus) -> Eindringen ins Gewebe
- Leukocidin -> Abwehr gegen Granulozyten und Makrophagen
- TSST-1 (Toxic Shock Syndrome Toxine 1)
- PVL (Panton Valentin Leukocidin) ist ein Toxin welches von einer neuen und aggressiven Variante des Methicillin-resistenten S. aureus, dem cMRSA (community-associated MRSA) produziert wird.
Krankheitsbilder:
- Pyogene Infektionen, z.B. Furunkel, Karbunkel, Osteomyelitis, Pneumonie, Endokarditis, Abszesse, Empyeme, Sepsis
- Intoxikation (Lebensmittelvergiftung): Hitzebeständige Enterotoxine (Superantigene) führen nach kurzer Inkubationszeit zu Brechdurchfall (Toxinbedingte Fernwirkung).
- Exfoliatine A und B (5 % der Staph. aureus):
- Impetigo contagiosa - Blasenbildung am Ort der Infektion, bei immunkompetenten Patienten mit Antikörpern gegen Exfoliatine.
- Staphylococcal Scalded Skin Syndrome (Morbus Ritter von Rittershain, Pemphigus neonatorum, Syndrom der verbrühten Haut) - Blasenbildung im Bereich der Haut, Rötung, Juckreiz, Lethargie, Fieber oder Hypothermie, Schleimhäute nicht mitbetroffen (im Gegensatz zum Lyell-Syndrom), Blasen ohne Erreger, hauptsächlich bei Kleinkindern und immunsupprimierten Erwachsenen über 60 Jahre. Das Toxin stammt aus lokalen Infektionen (Toxinbedingte Fernwirkung). Therapie: symptomatisch, Flüssigkeit, Haut wie bei Brandverletzten (ITS), Clindamycin als Antibiotikum der Wahl
 |
 |
 |
 |
 |
- Toxic Shock Syndrome - Toxinbedingte Fernwirkung. Früher bei Frauen aufgetreten, die eine neue Langzeittamponsorte verwendet hatte. Heutige Tampons sind sicher. Das Toxin wirkt als Superantigen (massive T-Zellaktivierung). Klinisch äußert sich das TSS durch Fieber über 38,5°C, diffuses makuläres Exanthem, Blutdruckabfall und nach ein bis zwei Wochen Hautschuppung. Zusätzlich sind definitionsgemäß drei weitere Organsysteme betroffen z.B. als Erbrechen/Diarrhoe, Anstieg der Retentions- und Leberwerte, Thrombozytopenie, psychiatrisch-neurologische Störungen und hyperämische Schleimhaut.
Staphylococcus aureus zählt zu den wichtigsten Erregern nosokomialer Infektionen. Der Erreger ist äußerst widerstandsfähig gegen Einflüsse wie Austrocknung und kann eine Reihe von Resistenzen gegenüber Antibiotika aufweisen.
Therapie: Häufig β-Lactamase-Bildung, zunehmend Mehrfach- und Multiresistenzen. Penicillin G oder Amoxicillin plus β-Lactamase-Hemmer (BLI). Bei Penicillinresistenz Isoxazolylpenicilline ("Staphylokokkenpenicillin") oder parenterale Cephalosporine der 1. (und 2.) Generation. Bei MRSA siehe unten.
Epidemiologie: Staphylokokken verursachen in den Industrieländern ca. 20 % der ambulant und 40% der nosokomial erworbenen Infektionen. In den USA verursacht S.aureus pro Jahr mehr als 1 Million invasive Infektionen, davon sind etwa 170.000 lebensbedrohlich und mehr als 30.000 enden tödlich.
MRSA und Antibiotika-Resistenzen:
MRSA ist die Abkürzung für Methicillin-resistenter Staphylococcus aureus. Methicillin ist ein β-Lactam-Antibiotikum und ein Indikatorantibiotikum für die Antibiotika-Sensitivität von Bakterien. Methicillinresistenz ist gleichbedeutend mit Resistenz gegenüber allen β-Lactam-Antibiotika. MRSA wird oft auch als multiresistenter S. aureus übersetzt. Synonym wird ORSA verwendet mit O für Oxacillin.
Resistenzmechanismen:
- Resistenzgen mecA, das für ein modifiziertes Penicillin-Bindungsprotein (PBP2a, syn. PBP2´) kodiert - Dieses PBP, die bakterielle Transpeptidase, ist für die Verknüpfung der Bausteine der Zellwand (Murein) verantwortlich und Zielmolekül der β-Lactam-Antibiotika. Das modifizierte PBP bindet keine β-Lactam-Antibiotika und bedingt die Resistenz. Charakteristisch für MRSA war bis vor kurzem, dass sie auch gegen weitere Antibiotikaklassen (beispielsweise Tetracycline, Aminoglykoside, Makrolide) Resistenzen erworben haben und damit eine Multiresistenz aufweisen. Seit wenigen Jahren beobachtet man zusätzlich eine neue Gruppe von MRSA, die diese Multiresistenz nicht aufweisen und als sog. community-acquired MRSA (auch community onset MRSA) bezeichnet werden.
- β-Lactamasen - Penicillinabbauende bakterielle Enzyme.
Entstehung, Vorkommen und Häufigkeit von MRSA:
Entstehung und Verbreitung durch klassische Selektion im evolutionsbiologischen Sinn in Bereichen mit hohem Antibiotikaeinsatz wie z.B. Krankenhäusern, bes. auf Intensivstationen. MRSA werden zunehmend auch außerhalb des Krankenhauses gefunden. Im englischen Schriftgut werden diese Keime als Community-associated methicillin-resistant Staphylococcus aureus bezeichnet. Darunter gibt es Keime mit besonders aggressiven Verhalten, die den sogenannten Panton-Valentine Leukozidin Faktor aufweisen.
Häufigkeit: In Deutschland liegt die MRSA-Rate in Krankenhäusern derzeit bei etwa 20% mit starken lokalen Unterschieden.
cMRSA: cMRSA (CA-MRSA, community-associated MRSA) ist eine neue und aggressive Variante des Methicillin-resistenten S. aureus. Die Variante infiziert auch gesunde Menschen und führt zu einer nekrotisierenden Pneumonie, die binnen weniger Tage letal enden kann. Neben Adhäsionssteigernden Proteinen soll für die Virulenz insbesondere das porenbildende Toxin PVL (Panton Valentin Leukocidin) verantwortlich sein, das die Zellmembranen von Epithelzellen und Immunozyten durchlöchert und eine hyperinflammatorische Immunreaktion induziert. Der Erreger scheint noch auf die meisten Antibiotika (außer Methicillin) anzusprechen, allerdings ist die Zeit für eine erfolgreiche Behandlung kurz. [1]
Therapie: Reserveantibiotika wie Linezolid (Empfehlungswert) Fosfomycin, Vancomycin und Streptogramine (i.v.) nach Antibiogramm.
Prophylaxe: Rationaler Einsatz von Antibiotika, hygienische Maßnahmen (bes. Händehygiene!), Isolierung bei Keimnachweis (Wirksamkeit umstritten).
Weblinks:
Koagulase-negative Staphylokokken (CONS)
[Bearbeiten]Beispiele für CONS: S. capitis, S. cohnii, S. epidermidis, S. haemolyticus, S. hominis, S. lugdunensis, S. saprophyticus, S. schleiferi, S. simulans, S. warneri
Staphylococcus epidermidis
[Bearbeiten]| Staphylococcus epidermidis | ||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
 | ||||||||||||||
| Systematik | ||||||||||||||
|
Morphologie und Eigenschaften: Kugelförmige, Gram-positive Bakterien, unbeweglich und keine Sporenbildung. S. epidermidis ist aerob, Katalase-positiv und Koagulase-negativ.
Vorkommen: Physiologischer Hautkeim
Pathogenitätsfaktoren:
- Adhäsine
- Biofilmbildung (Polysaccharide) -> Schutz vor Immunsystem des Wirts und Antibiotika
Krankheitsbilder:
- Generalisierte opportunistische und neonatale Infektionen (Sepsis)
- Fremdkörper-assoziierte Infektionen (z.B. an künstlichen Herzklappen, Kathetern, Shunts, Endoprothesen usw.)
Therapie: Penicillin G, bei Penicillin-Resistenz Isoxazolylpenicilline, ORSE: Vancomycin.
Staphylococcus saprophyticus
[Bearbeiten]Krankheitsbilder: Harnwegsinfekte bei jungen Frauen
Streptokokken (Katalase-negative Kokken)
[Bearbeiten]Morphologie und Eigenschaften: Streptokokken sind unbewegliche, kugelig bis oval geformte, Gram-positive Bakterien von etwa 0,5-1,5 µm Größe, die oft in Paaren oder Ketten gelagert sind. Sie lassen sich nach Hämolyseverhalten, Lancefield-Gruppierung und M-Fimbrienprotein einteilen:
- Hämolyseverhalten auf Blutagar:
- α-Hämolyse = Vergrünung durch unvollständige Hämolyse auf Blutagar mit Bildung grünlicher Zwischenprodukte (Methämoglobinbildung aus Hämoglobin)
- β-Hämolyse = Vollständige Hämolyse
- Lancefield-Gruppierung: Erfolgt anhand von Polysaccharid-Antigenen der Zellwand, gebräuchlich bei β-hämolysierenden Streptokokken (Gruppe A, B,...)
- M-Fimbrienprotein (über 80 Varianten): Wichtiger Adhärenz- und antiphagozytotischer Faktor bei β-A-Streptokokken.
β-hämolysierende Streptokokken
[Bearbeiten]| Streptococcus pyogenes | ||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
 | ||||||||||||||||
| Systematik | ||||||||||||||||
|
Streptococcus pyogenes
[Bearbeiten]
Morphologie und Eigenschaften: Streptococcus pyogenes gehört zu den β-hämolysierenden Streptokokken der Gruppe A (GAS) und ist ein Gram-positives, Katalase-negatives und kettenbildendes, fakultativ-anaerobes Bakterium. Es ist unbeweglich und bildet keine Sporen. Die einzelne Zelle ist rundlich und hat eine Größe von 0,6 bis 1 µm. Auf Blutagar wächst es in grauweißlichen schleimigen Kolonien. Zudem ist es Bacitracin-empfindlich.
Pathogenitäts- und Virulenzfaktoren:
- Das M-Protein vermittelt sowohl die Adhärenz an Blut und Interzellularbestandteile als auch den Phagozytoseschutz durch Kreuzreaktivität mit Wirtsantigenen.
- Die Fibronectin-bindenden Proteine F1 und SfbI dienen dem Bakterium zum Anheften an die Endothelzellen.
- Streptolysin O und S
- C-Polysaccharidschicht der Zellwand: direkt gewebetoxisch
- Invasine wie DNase, Hyaluronidase, Streptokinase, Proteinase
- Scharlachtoxine (Bakteriophagen-kodiert): Erythrogene Toxine A, B und C
Krankheitsbilder:
- Tonsillitis, Pharyngitis, Sinusitis, Otitis media
- Scharlach - Infektion mit einem der drei toxinbildendenden Stämmen (lysogene Bakteriophagen).
- Klinik: Maximal eine Woche nach Infektion beginnt die Erkrankung akut mit Fieber, Erbrechen und zervikaler Lymphadenopathie. Typisch sind das feinfleckige Scharlachexanthem mit perioraler Blässe und die im Verlauf (nach Abschuppung der Beläge im Mund) auftretende "Himbeerzunge", sowie die abschuppende Haut im Bereich der Handinnenflächen. Nach fünf bis sechs Tagen kommt es zur Entfieberung mit Eosinophilie und Schuppung der vom Exanthem betroffenen Hautareale.
- Epidemiologie: In Deutschland erkranken ca. 30.000 Menschen pro Jahr, v.a. Kinder.
- Therapie: Antibiotika sind obligat wegen den drohenden Komplikationen (Rheumatisches Fieber, Nierenbeteiligung).
- Impetigo contagiosa (Kleinblasige Form)
- Erysipel (Entzündung der Lymphspalten)
- Fasciitis necrotisans (Zellulitis, Fourniersche Gangrän): Tiefe, rasch sich ausbreitende Kolliquationsnekrose der Faszie und Unterhaut mit einer Letalität um die 30-50 %. (Boulvardpresse: „Fleischfressende Bakterien“) Die Diagnose wird durch Probeexzision (Kolliquationsnekrose) und MRT gesichert. Therapeutisch ist ein radikales Debridement, oft auch die Amputation unausweichlich, um das Leben des Patienten zu retten.
- Sepsis
- Folgeerkrankungen:
- Rheumatisches Fieber durch kreuzreagierende Antikörper (Anti-Streptolysin O, ASL): Karditis und Polyarthritis zwei bis drei Wochen nach Streptokokkeninfekt.
- Glomerulonephritis durch Ablagerung von Immunkomplexen ein bis zwei Wochen nach Infektion.
Epidemiologie: Die Trägerquote ist im Kindesalter am höchsten (15 bis 20 %).
Diagnose: Klinik, Schnelltest bei Angina, Kultur, serologischer Nachweis von Anti-Streptolysin O (ASL) und Anti-DNase B.
Therapie: Indikation ist hauptsächlich die Prophylaxe von Folgeerkrankungen. Geeignete Antibiotika sind Penicillin G und V, Cephalosporine der 1. und 2. Generation und Makrolide.
Weblinks: RKI - Scharlach
| Streptococcus agalactiae | ||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Systematik | ||||||||||||||||
|
Streptococcus agalactiae
[Bearbeiten]Morphologie und Eigenschaften: Streptococcus agalactiae gehört zu den β-hämolysierenden Streptokokken der Gruppe B. Das rundliche Bakterium ist aerob, katalase-negativ, unbeweglich und bildet keine Sporen.
Vorkommen: Besiedelung des Gastrointestinal- und Genitaltrakts (sexuelle Übertragung).
Krankheitsbilder: Sepsis und Meningitis beim Neugeborenen (Häufigkeit: 1/1.000 Geburten)
Therapie: Penicillin G, Cephalosporine 3. Generation, Erythromycin.
Prophylaxe: Empfohlenes Schwangerenscreening in der 35. bis 37. SSW (Selbstzahlerleistung).
α-hämolysierende Streptokokken (Vergrünende Streptokokken)
[Bearbeiten]
Viridans-Gruppe
[Bearbeiten]
Vorkommen: Physiologisch im Mundrachenraum (über 20 Spezies)
Krankheitsbilder:
- Karies - S. mutans, S. sangius, S. mitis
- Endokarditis lenta (50 bis 70 % der bakteriellen Endokarditiden, v.a. bei Herzfehlern, künstlichen Herzklappen, chronischen Infektionsherden im Mundrachenraum)
Prophylaxe der Endokarditis: Bei bekannten Herzfehlern (außer ASD), künstlichen Herzklappen usw. sollte vor medizinischen und zahnärztlichen Eingriffen eine Antibiotikaprophylaxe durchgeführt werden. Generell sind gesunde Zähne und Zahnfleisch von Vorteil (Zahnpflege, regelmäßige zahnärztliche Kontrolle.)
Endokarditisprophylaxe: Bsp.:
- Amoxicillin p.o.: 3g 1h vor und 1,5g 6h nach dem Eingriff
- Clarithromycin p.o.: 1g 2h vor und 0,5g 6h nach dem Eingriff
- Ampicillin i.v.: 2g 0,5h vor und 1g 6h nach dem Eingriff
- Clindamycin i.v.: 0,3g 0,5h und 0,15g 6h nach dem Eingriff
Therapie: 1.Wahl: Penicillin G und V, Amoxicillin, 2.Wahl: Cephalosporine der 1. und 2. Generation, Makrolide, Clindamycin, Vancomycin.
Streptococcus pneumoniae
[Bearbeiten]| Streptococcus pneumoniae | ||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
 | ||||||||||||||||
| Systematik | ||||||||||||||||
|
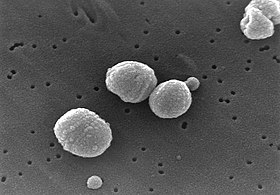
Morphologie und Eigenschaften: Pneumokokken sind Gram-positive bis Gram-labile oft bekapselte Diplokokken. Sie sind rundlich, unbeweglich, bilden keine Sporen, sind Optochin-empfindlich sowie Katalase-negativ. Auf Blutagar wachsen sie in α-hämolysierenden, grüngelben und eingedellten, bei Bekapselung in schleimigen Kolonien.
Epidemiologie: Oft asymptomatische Besiedlung des Nasenrachenraumes. Etwa 30% der jungen Erwachsenen und etwa 60% der Vorschulkinder sind asymptomatisch besiedelt. Mit zunehmendem Alter nimmt die Trägerrate ab. Pneumokokken sind der häufigste Erreger der ambulant erworbenen Pneumonie und ein häufiger Erreger der Meningitis bei Erwachsenen.Schätzungen zufolge sterben 4.000 bis 8.000 Menschen in Deutschland pro Jahr an invasiven Pneumokokkeninfektionen.
Infektionsweg: Übertragung durch Tröpfcheninfektion, Infektionen sind meist endogener Natur.
Pathogenitäts- und Virulenzfaktoren:
- Polysaccharidkapsel -> Phagozytoseschutz
- Pneumolysin O
- Resistenzen gegen Penicillin bzw. β-Lactam-Antibiotika durch verändertes PBP (Deutschland: ca. 10 %).
Faktoren zur Überwindung der Bluthirnschranke (Meningitis)[2]:
- H202 und Pneumolysin -> Apoptoseinduktion in den Endothelzellen, die die BHS aufbauen (unabhängig von TLR2 und TLR4).
- Zellwandbestandteile -> Apoptoseinduktion über den klassischen Caspase-Weg (TLR2-abhängig).
Krankheitsbilder: Pneumonie und Atemwegsinfekte, akute Otitis media, akute Sinusitis, Konjunktivitis, Meningitis (zweithäufigste Ursache für bakterielle Menigitiden bei Kindern unter fünf Jahren). Gefährdet sind v.a. Kleinkinder, Alte und Immunkompromitierte sowie Splenektomierte. Meist handelt es sich um endogene Infektionen.
Diagnose: Abgrenzung gegen andere α-hämolysierende Streptokokken mit Optochin-Test oder Gallelöslichkeit, serologischer Nachweis von Antikörpern gegen Kapselantigen.
Therapie: Penicillin G und V, Amoxicillin, bei Penicillinase-Bildern: Cephalosporine der 1. und 2. Generation, Vancomycin, Makrolide oder Clindamycin.
Prophylaxe: Schutz vor Pneumokokken bieten zwei Impfstoffe: Ein 23-valenter Polysaccharid-Impfstoff (Kapselantigen), der 90% der Pneumokokkentypen abdeckt steht seit vielen Jahren für ältere Kinder und Erwachsene zur Verfügung. Ein 7-valenter Konjugat-Impfstoff wurde im Februar 2001 zugelassen und ist für Säuglinge und Kleinkinder bestimmt.
Weblinks: RKI - Pneumokokkeninfektionen
Enterokokken
[Bearbeiten]| Enterococcus spp. | ||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
 | ||||||||||||||||
| Systematik | ||||||||||||||||
|
Morphologie und Eigenschaften: Enterokokken (Enterococcus spp.) werden zu den Milchsäurebakterien gerechnet. Es handelt sich um grampositive, teilweise in kürzeren Ketten, gepaart oder einzeln gelagerte, Katalase-negative und fakultativ-anaerobe Kokken mit variablem Hämolyseverhalten. Enterokokken zeichnen sich durch ihre hohe Umweltresistenz aus. So vermehren sie sich auch in 10-prozentiger Kochsalzlösung und sind Galle-resistent (Esculin-Test). Darüberhinaus exprimieren Enterokokken das Lancefield-D-Antigen weshalb sie früher auch als "Streptokokken der Gruppe D" bezeichnet wurden.
Vorkommen und Epidemiologie: Enterokokken gehören zur normalen Darmflora von Menschen, Säugetieren, Vögeln und Insekten. Als Umweltkeime können sie z.B. in Bodenproben oder (Ab-)Wasserproben nachgewiesen werden. Enterokokken gelten als opportunistische Infektionserreger und bedingen ca. 10 % der nosokomialen Infektionen. Infektionskrankheiten beim Menschen werden vor allem durch die beiden Spezies E.faecium und E.faecalis verursacht. Während bis vor wenigen Jahrzehnten das Verhältnis E.faecalis zu E.faecium bei 10:1 lag, verschiebt sich das Verhältnis derzeit insbesondere bei nosokomialen Infektionen zunehmend in Richtung E.faecium.
Krankheitsbilder: Opportunistische Infektionen (nosokomiale Infektionen): Zweithäufigster Erreger von Harnwegs- und chirurgischen Infektionen, dritthäufigster Erreger der Sepsis beim Erwachsenen, 5-15 % der Endokarditiden.
Diagnostik: Biochemie (Sherman-Kriterien)
Therapie: Die Therapie von Enterokkeninfektionen ist aufgrund zahlreicher intrinsischer und erworbener Resistenzen äußerst schwierig. Während E.faecalis in der Regel sensibel gegenüber Aminopenicillen ist, zeigen sich klinische Isolate von E.faecium in der Regel resistent gegenüber dieser Substanzklasse. Enterokokken sind grundsätzlich resistent gegenüber Cephalosporinen, man spricht deshalb auch von der "Enterokokkenlücke" der Cephalosporine. Häufig stellen Reserveantibiotika wie Vancomycin oder Linezolid die einzige Therapieoption bei Enterokokken dar. Insbesondere bei Endokarditiden oder anderen Blustroinfektionen wird häufig eine Kombination aus Aminopenicillinen oder Vancomycin mit einem Aminoglykosid (Synergismus)eingesetzt.
Literatur und Weblinks:
- Constanze Wendt, Henning Rüden, Michael Edmond: Vancomycin-resistente Enterokokken: Epidemiologie, Risikofaktoren und Prävention. Deutsches Ärzteblatt (Köln) 95(25), S. A1604 - A1611 (1998), ISSN 0012-1207
- M. Kolbert, P.M. Shah: Multiresistente Enterokokken: Epidemiologie, Risikofaktoren, Therapieoptionen. Arzneimitteltherapie 17(4), S. 133 ff. (1999), ISSN 0723-6913
- G. Schulze, W. Schott, G. Hildebrandt: Vancomycin-resistente Enterokokken - Krankenhausküche als Vektor? Bundesgesundheitsblatt 44(7), 732 – 737 (2001), ISSN 0007-5914
- A. Simon, N. Gröger, S. Engelhart, G. Molitor, M. Exner, U.Bode, G. Fleischhack: Vancomycin-resistente Enterokokken (VRE) - Übersicht zu Bedeutung, Prävention und Management in der Pädiatrie. Hygiene und Medizin 29(7/8), S. 259 ff. (2004), ISSN 0172-3790
Quellen
[Bearbeiten]- ↑ Labandeira-Rey M et al. “Staphylococcus aureus Panton Valentine Leukocidin Causes Necrotizing Pneumonia”. Science, Epub: Jan 18 2007. DOI:10.1126/science.1137165. PMID:17234914
- ↑ Bermpohl D et al. “Bacterial programmed cell death of cerebral endothelial cells involves dual death pathways”. J Clin Invest, 115(6):1607-15, Jun 2005 Epub: May 2 2005. DOI:10.1172/JCI23223. PMID:15902310

