Organische Chemie für Schüler/ Alkohole
Alkohol
Allgemeine Informationen
- Neben Nikotin ist Alkohol die die häufigste Droge in Deutschland. (Volksdroge Nummer 1)
- Er ist fast immer präsent: beim Essen, Fernsehen, Arbeiten, Reisen, Unterhalten, Sport.
- Das Wort „Alkohol“ kommt aus dem Arabischen „Ar-kul“ = das Feinste
- seit 3000 Jahren bekannt
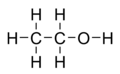
- Umgangssprachlich wird unter Alkohol vor allem der Alkohol Ethanol (früher Äthanol oder noch früher Ethylalkohol, auch Weingeist) verstanden. Es gibt natürlich zu jedem Alkan entsprechende Alkohole und mehrfach Alkohole! Zur Unterscheidung werden sie deshalb auch Alkanole genannt.
- In Deutschland starben im Jahr 2005 ca.17.000 Menschen durch Alkohol-Missbrauch. 2005 starben alleine in Russland 36000 Menschen nur durch Alkoholvergiftungen!
- Konsum: In Deutschland wurden 2001 pro Kopf getrunken (120 L Bier, 16 L Wein, 6 L Spirituosen, 6 L Sekt. Das entspricht 153 L alkoholischer Getränke im Vergleich zu 507 L nicht alkoholische Getränke) also einer Menge von 10,5 Litern reinem Alkohol pro Einwohner.
Wirkung
- Berauschende Wirkung
- Die Blutgefäße werden geweitet, → stärkere Durchblutung (rote Haut, Nase)
- Hautporen öffnen sich → trotz anfänglichem Wärmegefühl erfolgt ein Wärmeverlust für den Körper → Gefahr der Unterkühlung
- Die Niere scheidet Alkohol mit viel Wasser aus
- hoher Wasserverlust durch Urinausscheidung
- Nachdurst
- Alkohol enthaltende Getränke (mit Angabe des Alkoholgehaltes in Volumenprozent)
- reifer Kefir: bis ca. 3%
- Leichtbiere: 1-2,5%
- Vollbiere: ca 3-5%
- Starkbiere: 6-12%
- Weine: 10-15%
- Met: 5-14%
- Liköre: 15-75%, oft ~ 30%
- Spirituosen: ca. 30-96%
- Im Handel ist noch eine andere Form erhältlich
Spiritus enthält meist 96% Ethanol und 4% Wasser sowie einen geringen Anteil an Vergällungsmittel, welcher den Alkohol ungenießbar machen soll. Solcher vergällter Alkohol ist für Menschen ungenießbar und somit von der Genussmittelsteuer befreit.
Spiritus ist ein gutes Reinigungsmittel für Fette, Lösungsmittel und beispielsweise Nikotinflecken
Chemische Hintergründe, Aufnahme und Abbau
Die Aufnahme des Alkohols (=Resorption) in das Blut findet vor allem in Magen und Darm statt. Sie dauert (je nach Getränk) ca. 30-60 Minuten. Ein geringer Teil des Alkohols wird allerdings schon von der Mundschleimhaut aufgenommen, so dass der aufgenommene Alkohol direkt ins Blut gelangt und sich dann über den gesamten Körper verteilt. Er wirkt dabei besonders auf Gehirn und Nervenzellen.
Alkohol wird mit dem Blut in die Leber transportiert, welche ihn dann letztlich durch enzymatische Vorgänge abbaut (pro Stunde und pro Kilogramm Körpergewicht ca. 0,1g Alkohol)[1].
Da vor allem bei destillierten (gebrannten) Produkten die volle Wirkung des Getränks erst nach ca. 30min einsetzt, kann diese erst nach einiger Zeit eingeschätzt werden. Keinesfalls schon sofort nach dem Genuss! Dies bemerken vor allem sehr junge Jugendliche, die erstmalig Alkohol trinken, anfänglich keine Wirkung spüren und dann weiter trinken. Nach einer halben Stunde haben sie dann schon zu große Mengen getrunken → Alkoholvergiftung.
Die Alkoholaufnahme wird bei die Durchblutung steigernden Faktoren beschleunigt:
- Sport
- Wärme (Irish Coffee, Grog)
- Zucker (Likör)
- Kohlenstoffdioxid (als Kohlensäure z.B. im Sekt)
Die Alkoholaufnahme wird durch Fette verlangsamt:
- Dies führt aber nicht zu einer niedrigeren Aufnahme des Alkohols insgesamt, sondern nur zu einer zeitlichen Streckung.
Abbau des Ethanols im menschlichen Körper
Der Alkoholabbau wird im Körper durch gespeicherte Leberenzyme durchgeführt.
- Ethanol → Ethanal → Ethansäure (=Essigsäure) → Kohlenstoffdioxid
- Das Zwischenprodukt Ethanal sowie ein oft einhergehender kurzzeitiger Magnesiummangel (bedingt durch eine hohe Affinität von Ethanol zu Magnesium) ist für den so genannten Kater verantwortlich.
- Der Abbau des Ethanols wird durch Zucker gehemmt → Bei süßen Getränken bleibt der Alkohol länger im Blut und seine Abbauprodukt Ethanal entsteht später und über ein längeren Zeitraum. Die Konsequenz ist eine verstärkte Katerwirkung bei süßen alkoholischen Getränken wie Bowlen und Likören.
- Der Abbau des Ethanols im menschliche Körper ist bei Frauen und Männern nicht genau gleich. minimale genetische Unterschiede beschleunigen den Alkoholabbau bei Männern im Magen durch die „gastrische“ Alkoholdehydrogenase. Männer bauen Alkohol also etwas schneller ab als Frauen. Hinzu kommt eine bei Männern in der Regel größere Körpermasse, welche den Abbau ebenfalls beschleunigt.
- Durch häufigen Alkoholkonsum wird die Abbaurate übrigens nicht erhöht. Der Trainingseffekt bei regelmäßigem Konsum ist vor allem auf eine Vorratsspeicherung von Alkoholdehydrogenase in der Leber sowie eine Gewöhnung des Nervensystems an die höhere Ethanolmenge zurückzuführen.
- Berechnung des Alkoholspiegels: C Alkohol (in Promille ‰) = [Getrunkener Alkohol (in Gramm)] : [Körpergewicht (in Kilogramm) ] · 0,7
Alkoholkonsum
| ‰ (Promille) | Wirkung |
|---|---|
| 0,2 | Entspannung, Wärmegefühl, Persönlichkeitsveränderungen wie z.B.: Fröhlichkeit, Gesprächigkeit, Risikobereitschaft, Volkstänze oder sich sonst irgendwie zum Deppen machen *g* |
| 0,5 | Aggressionen steigen, Leistungsfähigkeit sinkt, Selbstüberschätzung nimmt zu („klar kann ich noch fahren“) |
| 0,6 | Sehleistung bereits vermindert (leichter Tunnelblick), Konzentrationsverlust |
| 0,8 | Sehfähigkeit lässt um etwa 30% nach, Reaktionszeit ist etwa 35% länger. Motorik bereits grob |
| 1-2 | Rausch, Sprach- und Gleichgewichtsstörungen, Verlust der Selbstkontrolle, Absterben von Gehirnzellen (reicht deutlich aus für ein „nie wieder Alkohol“ am nächsten Morgen *g*) |
| 2-3 | Betäubungsstadium: Erinnerungslücken (Filmriss), Verwirrung, Erbrechen, vermehrte Anzeichen von Atemschwierigkeiten |
| 3-4 | komplette Desorientierung/Halluzinationen, Lähmungen, Tiefschlaf |
| 4-5 | Atmungsmuskel wird gelähmt → Tod |
- (Leichte) Symptome des Dauerkonsums
Magenschleimhautentzündungen, Magengeschwüre, Verminderung der Sexualfunktion, geringere körperliche Leistungsfähigkeit, teilweise Verwahrlosung
- (Schwerwiegende) Symptome des Dauerkonsums
Abhängigkeit (bereits ab 2 Bier pro Tag möglich!), erst Fettleber, später Schrumpfleber (=Leberzirrhose), Organbeeinträchtigungen, Organversagen, soziale Ausgrenzung.
- Nebenwirkungen
- Alkohol ist ein gutes Lösungsmittel für viele Substanzen. Dies ist problematisch, wenn Alkohol zusammen mit Medikamenten oder anderen Drogen konsumiert wird. Vielfältige Wechselwirkungen, welche die Einzelwirkungen noch verstärken sind üblich.
- jedes Jahr sterben tausende weltweit durch den für Menschen giftigen Alkohol Methanol, welcher bei der Herstellung von Ethanol als Nebenprodukt entstehen kann. (2006 alleine 300 in Russland)
- Aufgaben
- Berechne, wie viel Promille Alkohol Du schon bei einem Glas der folgenden Alkoholika im Blut hättest:
- Ein Glas Bier (0,3l) enthält 14,4g reinen Alkohol
- Ein Glas Wein (0,2l) enthält 19,2g reinen Alkohol
- Ein Glas Schnaps (Korn) (0,02l) enthält 7,8g reinen Alkohol
- Warum reagieren Männer und Frauen unterschiedlich stark auf dieselbe Menge Alkohol? Ergibt sich dadurch eine Konsequenz für eine mögliche Sucht Gefährdung?
- 10% aller Verkehrsunfälle werden durch Alkohol verursacht. Jährlich sterben dadurch mehr als 2000 Menschen[2], mehr als 55000 werden dabei verletzt. Ein Viertel der „Alkoholtäter“ sind nach Polizeiangaben jünger als 25 Jahre. Versuche Ursachen und Erklärungen für diese Aussagen zu finden.
- Zusatzinformationen
Ethanolherstellung
Herstellung durch alkoholische Gärung
Alkohol entsteht u.a. bei der Vergärung von zucker- oder stärkehaltigen Substanzen durch Hefen oder Bakterien. So entsteht zum Beispiel Wein aus Weintrauben oder Bier (aus Malz und Hopfen).
Durch Destillation kann der Alkoholgehalt noch erhöht bzw. fast reiner Alkohol (=Azeotropes Gemisch) gewonnen werden. Solche Getränke bezeichnet man als Spirituosen (z.B. Whiskey, Kognak, Schnaps, Wodka oder Rum). Liköre sind Spirituosen, denen Zucker und Aromen zugesetzt werden.
Als Nebenprodukt kann beim Destillieren Methanol (früher auch Methylalkohol genannt) entstehen. Dieser ist so giftig, dass jedes Jahr Hunderte daran sterben!
Zur Wiederholung aus der Biologie: Hefezellen betreiben Zellatmung, aber bei Sauerstoffmangel (=anaerobe Bedingungen) führen sie die alkoholische Gärung durch!
- C6H12O6 → 2 C2H5OH + 2 CO2 + E
Die maximal erzielbare Alkoholkonzentration durch Gärung beträgt dabei ca. 15% Vol., danach sterben die Hefepilze.
Herstellung durch elektrophile Addition von Wasser an ein Alken
(1) Kurzzeitige Dipole beim Wasser sorgen für eine Anziehung zwischen dem elektropositiveren Wasserstoff des Wassers und der Doppelbindung.
(2) Als Folge wird das Wasser heterolytisch gespalten (in H+ und OH-). Das Wasserstoffion wird von der Doppelbindung angezogen
(3) Es bildet sich ein Übergangskomplex von H+ mit dem Ethen. Die Doppelbindung wird dabei aufgespalten.
(4) Es bildet sich eine feste Bindung zwischen Kohlenstoff und Wasserstoff, da die Doppelbindung sozusagen wie ein Fensterladen „aufklappt“. In der Folge ist das obere C-Atom allerdings nur noch dreibindig und somit positiv geladen (=Carbeniumion).
(5) Die positive Ladung des Carbeniumions sorgt für eine Anziehung und eine anschließende Verbindung mit dem negativen Hydroxid. Es ist Ethanol entstanden.
Nomenklatur
- Alkohole heißen Alkanole, Endung –ol (bzw. bei komplexen Verbindungen auch „-Hydroxy“)
- Kohlenstoffkette, die die funktionelle Gruppe trägt gibt der Verbindung den Namen
- Alkyl- und Halogensubstituenten werden dem Namen vorangestellt
-
1-Brom-2-Butanol
-
1-Brom-4-Butanol
-
3-Brom-2-Methyl-1-Propanol
-
3-Brom-2-methylbutan-2-ol
- Man kann die Alkohole in primäre, sekundäre und tertiäre Alkohole unterscheiden, indem man je nach Anzahl der Kohlenstoffnachbarn des OH-Gruppe gebundenen C-Atoms zählt.
- Primärer Alkohol: Das C-Atom mit der OH-Gruppe hat ein weiteres C-Atom gebunden (z.B. bei Ethanol) - siehe auch Beispiel 1.
- Sekundärer Alkohol: Das C-Atom mit der OH-Gruppe hat zwei weitere C-Atome gebunden - siehe auch Beispiel 2.
- Tertiärer Alkohol: Das C-Atom mit der OH-Gruppe hat drei weitere C-Atome gebunden (Beispiel 3)
Auch eine Unterscheidung nach der Anzahl in einem Molekül vorhanden OH-Gruppen in einwertige, zweiwertige, dreiwertige usw... (also mehrwertige) Alkohole ist möglich. Mehrwertige Alkohole enthalten also zwei oder mehr OH-Gruppen.
Eigenschaften primärer Alkanole
Alkanole leiten sich von den Alkanen ab und sind gesättigte Alkohole mit der Summenformel CnH2n+1+OH. Ein entständiges Wasserstoffatom der Kohlenstoffkette ist durch eine Hydroxidgruppe ersetzt. Früher wurden diese Alkohole auch mit der Endung „-yl“ versehen, z.b. Methylalkohol scheint als Wort unausrottbar in den Köpfen der Menschheit fest gebrannt - die korrekte Bezeichnung lautet Methanol).
Die Isomerie kommt hier genauso vor, wie bei den Alkanen auch, so dass es mit steigender Kettenlänge und Verzweigung der Kohlenstoffkette eine zunehmende Anzahl an Isomeren gibt.
Schmelz- und Siedepunkte liegen höher als die der entsprechenden Alkane - Ursache ist die Hydroxidgruppe, welche Wasserstoffbrückenbindungen (WBBs) ausbildet. So kommt es zu einem stärkerem Zusammenhalt der Moleküle. Dadurch ist mehr Energie notwendig, sie aus ihrem jeweiligem Verband zu lösen und in den nächsten Aggregatzustand zu überführen.
| Systematischer Name | Summenformel | Dichte (g/cm3) | Siedepunkt (°C) | Siedepunkt der entsprechenden Alkane (°C) |
|---|---|---|---|---|
| Methanol | CH3OH | 0,812 | 66 | -161 |
| Ethanol | C2H5OH | 0,806 | 78 | -88 |
| Propanol | C3H7OH | 0,817 | 96,5 | -42 |
| Iso-Propanol | C3H7OH | 0,789 | 81 | -0,5 |
| Butanol | C4H9OH | 0,823 | 116,7 | 36 |
| Pentanol | C5H11OH | 0,829 | 137 | 69 |
| Hexanol | C6H13OH | 0,833 | 157 | 98 |
| Heptanol | C7H15OH | 0,836 | 175 | 126 |
| Octanol | C8H17OH | 0,839 | 194,5 | 151 |
| Nonanol | C9H19OH | 0,842 | 213 | 174 |
Typische Vertreter der Alkohole
| Typische primäre Alkohole | |
|---|---|
| Methanol | H3C-OH
|
| Ethanol |
|
| Eigenschaften sekundärer Alkanole | |
| Isopropanol (2-Propanol) |
|
| Eigenschaften zwei- und mehrwertiger Alkohole | |
| Auch als Polyalkohole bezeichnet, enthalten mehrwertige Alkohole mehrere Hydoxidgruppen. | |
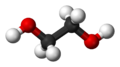
| Ethandiol (Glykol) | zweiwertiger Alkohol (Glycol)
|
| Glycerin (Propantriol) | dreiwertiger Alkohol (Glycerin)
|
| Pentaerythrit(ol) |
|
| Eigenschaften aromatischer Alkohole | |
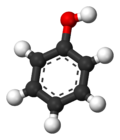
| Phenol (Hydroxybenzol) |
|
Die funktionelle Gruppe der Alkohole -OH
Funktionelle Gruppen sind Gruppen, welche an Alkanen und Alkenen eine besondere Funktion erfüllen. Sie sind in der Regel stark für den Charakter der jeweiligen Verbindung bestimmend. So ist die funktionelle Gruppe der Alkanole, die auch Alkohole genannt werden die Hydroxylgruppe (OH) die funktionelle Gruppe. Sie kennzeichnet die Gruppe der Alkohole, welche auch Alkanole genannt wird.
- Beispiele für natürlich vorkommende Alkohole
- Ethanol ist ein Produkt der alkoholischen Gärung von Hefen.
- Glycerin findet man in Membranfetten, Fetten und Ölen. Es gibt auch einen Frosch, der im Winter eingefroren in Eis überlebt, da er Glycerin im Blut hat, welches vor Kristallisation schützt.
- Zucker, Stärke und Zellulose enthalten viele Hydroxylgruppen
- Verwendung
- Kurzkettige Alkohole sind meist recht passable Lösungsmittel für wasserlösliche also hydrophile Stoffe. Aber auch unpolare (lipophile) Stoffe lassen sich teilweise Lösen. Alkohol hat als Lösungsmittel damit eine Doppelrolle.
- als Genussmittel
- Rohstoff der Kosmetik und Parfumindustrie
- Lösungsmittel und Ausgangstoff für Synthesen in der chemischen Industrie
- zur Sprengstoffherstellung bei der Synthese von Nitroglyzerin
- Alkohole sind Ausgangstoffe für die Produktion von Alkansäuren durch Oxidation
Der Vorgang ist umkehrbar, d.h., durch eine Reduktion von Ethansäure lässt sich Ethanol herstellen.
- Zusatzinformationen
Oxidierbarkeit von Alkoholen (Unterschied primäre und sekundäre Alkohole)
Primäre Alkohole werden über das entsprechende Aldehyd zur Carbonsäure oxidiert.
Sekundäre Alkohole können nur zum Keton oxidiert werden. Eine weitere Oxidation ist mangels Angriffspunkt für einen zweiten Sauerstoff nicht möglich. Nur die endgültige Oxidation zum Kohlenstoffdioxid ist immer möglich.
Tertiäre Alkohole nur zum Kohlenstoffdioxid oxidiert werden.
→ Unterscheidbarkeit isomerer Alkohole
Dem Alkohol verwand: Die Ether
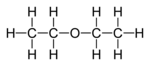
Ether sind Verbindungen, welche nach dem Schema R1 − O − R2 aufgebaut sind (R steht dabei für beliebige Alkylreste). Sie kommen sowohl in der Natur (z.B. die Aromastoffe Anisol und Vanillin), als auch in künstlich hergestellten Formen vor. Der bekannteste Ether ist der Di-Ethyl-Ether:
Diethylether ist eine gutes Lösungsmittel für apolare Stoffe und hat einen scharfen Geruch nach Desinfektionsmittel, bzw. Zahnarzt. Es wurde früher als Narkosemittel benutzt.
- Halbstrukturformel Diethylether: CH3-CH2-O-CH2-CH3
- Smp. / Sdp.: -116,3°C, 34,4°C
Die Bindungsverhältnisse der Ether sind denen der Alkohole ähnlich - auch wenn es formal keine Alkohole sind!
Es gibt sowohl unverzweigte, verzweigte und zyklische Ether.
Die meisten Ether sind nicht sehr reaktionsfreudig.
Säurekatalysierte Kondensation von zwei Alkoholen zu Ether
Durch Säure können zwei Alkoholmoleküle zu einem Ether kondensieren:

- R = beliebiger Alkylrest
- wird bei der Herstellung nur eine Alkoholart verwendet, entstehen symetrische Ether
Zusatzinformationen:
Wiederholungsaufgaben zu Alkoholen
- Gibt es eine eindeutige homologe Reihe der Alkohole?
- Wie kann man Ethanol gewinnen. Nenne 2 Möglichkeiten.
- Zeichne alle und benenne (nur 10) Alkohole mit 5 Kohlenstoffatomen. Ordne anschließend in primäre, sekundäre und tertiäre Alkohole.
- Welche Alkohole sind dabei Spiegelbildisomere?
- Je höher die Anzahl an Kohlenstoffatomen, desto viskoser werden sie. Erkläre.
- Warum haben Alkohole im Vergleich zu Alkanen gleicher Kettelänge höhere Smp. und Sdp.?
- Zeichne 1-Propanol und Propantriol und treffe Aussagen bezüglich der Smp., Sdp. und der Viskosität.
- Ordne die folgenden Substanzen hinsichtlich ihrer Löslichkeit in Wasser: CO2, Methan, Methanol, Pentanol. Begründe.
- Ordne die folgenden Substanzen hinsichtlich ihres Vermögens Kochsalz zu lösen: Methanol, Wasser, Benzin, Tetrachlormethan.
- Ordne nach zunehmenden Siedepunkten: 1,2 Propandiol, Glycerin, 2 Propanol, Propan.
- Vergleiche Ethanol und (Diethyl-)Ether (H3C-CH2-O-CH2-CH3) hinsichtlich ihrer Siedepunkte.
- Formuliere die Reaktionsgleichung des Ethanolations mit Wasser. Was wird man beobachten können, wenn man Universalindikator hinzufügt.
- In Gegenwart von Natronlauge reagiert Ethanol nicht als Säure. Bei der Reaktion mit Natrium gibt es allerdings schon ein Proton ab. Ist Ethanol damit doch eine Säure?
Weblinks
- http://wiki.zum.de/Lernzirkel_Alkohole - Lehrmaterial zur Gruppenarbeit
- ↑ Das Enzym Alkoholdehydrogenase baut Ethanol zu Ethanal (H3C-CHO) ab, das weiter zu Ethansäure (=Essigsäure) oxidiert wird. Die Ethansäure wird über den Citratzyklus und die Atmungskette in allen Zellen des Körpers unter Energiegewinnung zu CO2 veratmet.
- ↑ Insgesamt ca. 60 000 Alkoholtote in Deutschland