Organische Chemie für Schüler/ Aromatische Kohlenwasserstoffe
Die Aromaten sind eine besondere Verbindungsklasse der OC. Ihr Hauptmerkmal ist ihre besondere Bindungsstruktur (konjugierten Doppelbindungen[1]) in Ringform. Sie unterscheiden sich in der Regel deutlich in ihren Eigenschaften von den kettenförmigen Kohlenwasserstoffverbindungen (auch aliphatische Kohlenwasserstoffe genannt).
Geschichte
[Bearbeiten]Der erste Aromat den man entdeckte war das Benzol (C6H6). Von seinem Geruch stammt die Bezeichnung Aromat (Griechisch: Aroma = Duft).
Bald fand man auch Stoffe mit ähnlichen Eigenschaften, welche einen anderen Aufbau zeigten. Man bemerkte schnell, dass diese Verbindungen trotz Doppelbindungen nicht leicht zu Additionsreaktionen zu bewegen waren.
Gemeinsame Eigenschaften
[Bearbeiten]- mehrfach ungesättigt (also mehrere Doppelbindungen)
- zyklische, fast immer planare (!) Moleküle
- alle Atome des Rings sind sp2-hybridisiert (nur LK)
- gegenüber der Addition an der Doppelbindung relativ reaktionsträge
- neigen stattdessen zu einer Substitution an der Doppelbindung
- das Bindungssystem aus konjugieren Doppelbindungen ist für eine hohe Stabilität des Moleküls verantwortlich. Um die Bindungen aufzubrechen ist vergleichsweise viel Energie notwendig.
Hückel-Regel: Die Zahl der delokalisierten π-Elektronen muss bei Aromaten der Formel 4n+2 entsprechen. (z.B. 2, 6, 10, 14)
Der bekannteste Vertreter der Aromaten ist das Benzol. (nach der Hückel-Regel besitzt Benzol 6π-Elektronen.)Reaktionen von Aromaten
[Bearbeiten]Additionsreaktionen am Aromaten sind aufgrund der festen Bindungsstruktur schwierig. Aromaten reagieren überwiegend nach dem Mechanismus der elektrophilen aromatischen Substitution (z.B. Sulfonierung, Nitrierung). Nucleophile aromatische Substitution sind selten.
Aromaten lassen sich mehrfach substituieren. Dafür gelten dann besondere Regeln.
Zusatzinformationen
Benzol (C6H6)
[Bearbeiten]Eigenschaften und aromatische Struktur
[Bearbeiten]Das erste Mal, dass Wissenschaftler auf Benzol aufmerksam wurden, war beim Prozess des Entgasens von Steinkohle. Dies führte man im 19. Jahrhundert durch, um beispielsweise Gas für Straßenlaternen zu gewinnen. Als Nebenprodukt fand man eine bei Raumtemperatur farblose Flüssigkeit, welche besonders aromatisch riecht. Liebig nannte sie Benzol.
Benzol ist besonders dünnflüssig und verbrennt an der Luft mit oranger und rußender Flamme. Schon bei Raumtemperatur ist es allerdings leicht flüchtig, so das seine Dämpfe besonders feuergefährlich sind.
Den Umgang damit sollte man meiden, da es über die Haut in den Körper eindringt und über die Lunge eingeatmet wird und im Körper als Zellgift wirkt. Es schädigt das Knochenmark, die Leber und die Nieren sowie die Bildung der roten Blutkörperchen. Schon geringe Mengen führen beim Einatmen zu Schwindel und Erbrechen. Bewusstlosigkeit schließt sich an.
Des Weiteren ist es krebserregend (cancerogen).
Benzol ist apolar und mischt sich demzufolge nicht mit Wasser. Es ist aufgrund seines apolaren Charakters ein gutes Lösungsmittel für apolare Stoffe und somit ein wichtiger Rohstoff der chemischen Industrie.
Vorkommen und Verwendung
[Bearbeiten]Man findet Benzol in Steinkohle und Erdöl. Bei der Verbrennung von Benzin und Diesel wird es demzufolge freigesetzt. Auch wenn der Anteil im Laufe der letzten Jahre in Treibstoffen stetig abgenommen hat, so werden immer noch 75% der Emissionen durch den Verkehr freigesetzt.
Es entsteht ebenfalls beim Verbrennen von Tabak. (10-100 µg pro Zigarette). Auch durch Vulkanausbrüchen oder unvollständigen Bränden (Schwelbränden) kann es entstehen und freigesetzt werden.
Lebensmittel die an Tankstellen verkauft werden waren in den letzten Jahren immer wieder durch verhältnismäßig hohe Benzolbelastung aufgefallen. Mittlerweile sind die Tankstellenmärkte mit Überdruck gefüllt, damit beim Öffnen der Tür nur Luft nach draußen gelangt und keine Benzingase hinein.
Viele Substanzen, welche Benzol enthielten sind heutzutage in Deutschland verboten. (Außer den Treibstoffen, wo es z.B. die Klopffestigkeit von Benzin erhöht (Zumischung 1 bis 5%!). In den USA ist diese Praxis schon lange verboten.
In der chemischen Industrie wird es als Lösungsmittel sowie als Ausgangsstoff für die Synthese vieler organischer Verbindungen (v.a. von Kunststoffen) verwendet (z.B. Anilin, Styrol, Nylon, Synthesekautschuk, Kunststoffe, waschaktive Stoffe, Insektizide, Farbstoffe usw.)
Mehrringige Aromaten sowie Aromaten mit Substituenten werden ebenfalls aus Benzol gewonnen (Phenol, Nitrobenzol, Anilin, Chlorbenzol, Hydrochinon und Pikrinsäure usw.).
Geschichte der Strukturaufklärung des Benzols
[Bearbeiten]Der Chemiker August Kekulé (1829-1896) erforscht die Strukturformel des Benzols. Er hatte an dieser harten Nuss lange zu „knabbern“. Aus den Messungen von 1845 des Chemikers Mitscherlich wusste er, dass alle 6 Atome des Benzols gleichwertig sind und das es reaktionsträge wie ein Alkan ist. Additionen, wie die der Alkene waren bei Benzol aber nicht möglich.
Mit den üblichen Alkanformeln war aber dieses Rätsel nicht zu lösen, bis ihm eines Nachts im Traum die Verbindung in Form einer Schlange erschien, die den eigenen Schwanz erfasste. So schloss Kekulé auf die Ringstruktur des Benzols.
Mesomerie
[Bearbeiten]Kekulé nahm an, dass die Doppelbindungen des Benzols nicht einen festen Platz haben, sondern dass sie vielmehr ständig den Platz wechseln.
-
Strukturformel Benzol
-
mesomere Grenzformeln
Heute weiß man, dass die 6 pz-Elektronen des Benzols über und unter der Ebene des Rings liegen. Es bildet sich ein ringförmiges π-Elektronensystem aus, welches durch die ständige Bewegung der Elektronen delokalisiert ist.
Durch diese Form der Mesomerie ist das Benzolmolekül energetisch besonders stabilisiert und demzufolge reaktionsträge. Deshalb ist ein wichtiges Erkennungsmerkmal der Aromaten auch das Ausbleiben der Additionsreaktion mit beispielsweise Bromwasserstoffsäure oder Bromwasser.
Ein Beweis für die Delokalisierung und die demzufolge besondere Art der Bindung sind die Bindungslängen zwischen den Kohlenstoffatomen. Eine C-C Einfachbindung ist 154pm und eine C=C Doppelbindung ist 134pm[2] lang. Beim Benzol liegt bei allen Kohlenstoffen eine Bindungslänge von 139pm vor.
Zusatzinformationen:
Mesomeriestabilisierung des Benzol
[Bearbeiten]
Die Senkrecht stehenden p-Orbitale (Elektronenwolken) überlappen und bilden so über und unterhalb des Benzolrings einen gemeinsamen Bereich. Dieser wird π-Orbital genannt.
Dies ist der tatsächliche Zustand der Elektronen im Benzol. Mesomere Grenzstrukturen können diese exakt Darstellung nicht liefern - vermitteln aber immerhin ein Idee davon!
- Merkmale der Bindungen
- Planarer Aufbau des gesamten Moleküls
- Die Bindungslänge zwischen allen Kohlenstoffatomen beträgt 139pm
- Jedes Kohlenstoffatom besitzt ein p-Orbital (auch sp2-Hybridisierung genannt). Die Folge ist eine Delokalisierung der Elektronen ober- und unterhalb des Rings.
Verschiedene Aromaten
[Bearbeiten]a) Fünfringige Aromaten
[Bearbeiten]-
Furan
-
Benzofuran
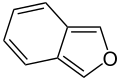
-
Isobenzofuran
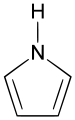
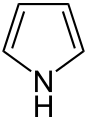
-
Pyrrol
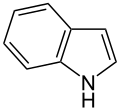
-
Indol
-
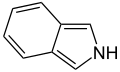
Isoindol
-
Thiophen
-
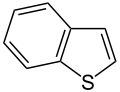
Benzothiophen
-
Benzo[c]thiophen
-
Imidazol
-
Benzimidazol
-
Purin
-
Pyrazol
-
Indazol
-
Oxazol
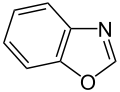
-
Benzoxazol
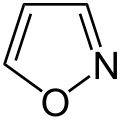
-
Isoxazol
-
Benzisoxazol
-
Thiazol
-
Benzothiazol
b) Sechsringige Aromaten
[Bearbeiten]-
Benzol
-
Naphthalin
-
Anthracen
-
Pyridin
-
Chinolin
-
Isochinolin
-
Pyrazin
-
Chinoxalin
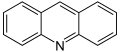
-
Acridin
-
Pyrimidin
-
Chinazolin
-
Pyridazin
-
Cinnolin
Freiarbeit Aromaten: 1. Was sind Aromaten?
[Bearbeiten]- Sind Aromaten mit 3 Kohlenstoffatomen möglich?
- Zeichne Aromaten mit 6 bzw. 9 oder 10 Kohlenstoffatomen
- Zeichne in die folgenden Strukturformeln die Doppelbindungen ein und bestimmen dann, ob Aromaten vorliegen:
- Zeichne alle drei mesomeren Grenzformen für Naphthalin. C10H8
- Ist die Verbindung [10]-Annulen ein Aromat, oder nicht?
- Ist Cycloheptatrien ein Aromat?
- Kannst Du jetzt definieren, was der aromatische Zustand ist?
Zusatzinformationen: Hückel-Regel Naphthalin
Freiarbeit Aromaten: 2. Nomenklatur der Aromaten
[Bearbeiten]- Zeichne: a) Benzaldehyd, b) Benzylalkohol, c) Toluol, d) Phenol e) Benzoesäure
- Zeichne: a) 1,3,5-Trimethylbenzol, b) 2,6-Dibrom-4-chlortoluol, c) Phenylcyclohexan
- Heteroaromaten sind durch Atome im Ringsystem gekennzeichnet, die nicht aus Kohlenstoff bestehen. Sind sie wirklich Aromaten?
- Bei welchen der oben genannten Aromaten gilt sie nicht?
- Entsprechen die folgenden polycyklischen Aromaten der Hückelregel?
- Wähle zwei beliebige Verbindungen dieser Seite und male jeweils zwei mesomere Grenzstrukturen
Zusatzinformationen: Polyzyklische aromatische Kohlenwasserstoffe
Freiarbeit Aromaten: 3. Die elektrophile aromatische Substitution
[Bearbeiten]
- Erkläre mit Deinen Worten den Ablauf und die Reaktionsschritte der katalytischen Sulfonierung von Benzol. Beachte dabei die drei mesomeren Grenzstrukturen in der Klammer. Damit die Reaktion abläuft, verwendet man übrigens frisch konzentrierte Schwefelsäure, welche immer auch etwas Schwefeltrioxid (SO3) enthält. Dieses verbindet sich mit Protonen der Schwefelsäure zu (HSO3)+.
- Suche aus zwei verschiedenen Chemiebüchern (oder aus dem Internet) den Ablauf einer Halogenierung eines Aromaten (z.B. der Bromierung von Benzol). Schau genau hin und suche Gemeinsamkeiten und Unterschiede. Erstelle dann eine eigene Zeichnung für deine Unterlagen.
- Zeichne ein Energiediagramm unter deine Version der aromatischen, Eelektrophilen Substitution und ordne dem Energiediagramm dann die passenden Substanzen zu.
- Wie würde das Energiediagramm aussehen, wenn stattdessen eine Addition von Brom am Aromaten stattfinden würde?
Freiarbeit Aromaten: 4. Phenol und seine Besonderheiten
[Bearbeiten]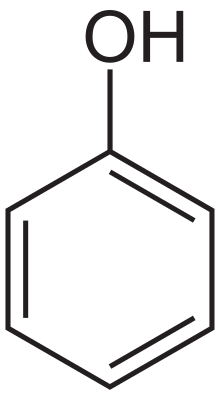

- Lies in Deinem Buch über Phenol und seine Eigenschaften nach und erstelle dann einen Kurzsteckbrief (Vorkommen, Eigenschaften, Verwendung). Beantworte dann, ob es eher ein Alkohol, eine Lauge, eine Base oder eine Säure ist.
- Wenn Phenol ein Proton abgibt, liegt das einfach negative Phenolation vor. Zeichne es und finde insgesamt 5 mesomere Grenzstrukturen. (Tipp: die Ladung ist nicht immer am Sauerstoff!)
- Wie interpretierst Du die folgende Regel: „Je mehr mesomere Grenzstrukturen vorliegen, desto stabilisierter ist ein Ion und somit ist seine Existenz wahrscheinlicher“
- Erstelle die Protolysegleichung der Reaktion von Phenol mit Wasser sowie die Reaktionsgleichungen der Reaktion mit Natrium und Natronlauge. Kennzeichne dann das Natriumphenolation.
- Wozu wird Phenol verwendet?
- Phenol als Substituent an Kohlenstoffketten oder anderen aromatischen Ringen wird Phenyl genannt. Wie ist eigentlich die Summenformel von Phenyl?
- Zur Erfreuung des Chemikerherzens. Konjugierte π-Elektronensysteme sind ab einer gewissen Länge farbig. Phenolphtalein hat ein solches umfangreiches konjugiertes π-Elektronensystem. a) Warum entfärbt es sich bei Säurezugabe? Für Nomenklaturmasochisten: benenne es korrekt!
Zusatzinformationen:
Freiarbeit Aromaten: 5. Anilin - ist keine Lauge, aber eine Base
[Bearbeiten]- Lies in Deinem Buch über Anilin und seine Eigenschaften nach und erstelle dann einen Kurzsteckbrief (Vorkommen, Eigenschaften, Verwendung). Beantworte dann, ob es eher eine Lauge, eine Säure oder eine Base ist.
- Erstelle die Reaktionsgleichung der Säure-Base-Reaktion von Anilin mit Salpetersäure.
- Wiederhole die Säure und Base Definitionen nach Brönstedt. Kennzeichne dann jeweils das korrespondierende Säure-Base-Paar der Reaktion aus der vorherigen Aufgabe.
- Weltweit werden ca. 1 Mrd. kg Anilin benötigt. Wozu wird es eigentlich verwendet?
- Welches wäre der korrekte IUPAC-Name von Anilin?
- Wie sieht im Vergleich Nitrobenzol aus?
Zusatzinformationen: Anilin
Freiarbeit Aromaten: 6. Toluol und andere Benzol Derivate
[Bearbeiten]- Lies in Deinem Buch über Toluol, Benzoesäure, Xylol und Styrol nach und erstelle dann jeweils Kurzsteckbriefe (Vorkommen, Eigenschaften, Verwendung).
- Di-Methylbenzol (=Xylol) liegt in insgesamt drei Isomeren vor. Zeichne sie. Sie werden als ortho-, meta bzw para-Xylol bezeichnet.
- Formuliere die Reaktionsgleichung für die Kern- bzw. Seitenkettenbromierung von Toluol.[4]
- Zeichne die drei Isomeren Trimethylbenzole.
- Formuliere die Reaktion von Benzoesäure mit Kalilauge.
- Zeichne 2,4,6-Trinitromethylbenzen (=TNT). (Nitro- als Substituent bezeichnet Nitrit (ohne Ladung), also NO2)
- Wie müssen die Zwischenstufen der oxidativen Herstellung von Benzoesäure aus Toluol aussehen? Zeichne und benenne sie:
Zusatzinformationen:






![Benzo[c]thiophen](http://upload.wikimedia.org/wikipedia/commons/thumb/9/95/Benzo_c_thiophen.svg/120px-Benzo_c_thiophen.svg.png)