Topographische Anatomie: Peritonealhöhle: Pankreas
< Topographische Anatomie | Peritonealhöhle
Einführung
[Bearbeiten]Lernziele:
- Lage und topographische Beziehungen des Pankreas beschreiben können.
- Die Blutversorgung des Pankreas grob beschreiben können.
- Die Funktion des Pankreas erklären können.
- Erklären können, wie es dazu gekommen ist, dass die verschiedenen Anteile des Pankreas an ihrem jeweiligen Ort liegen.
Zum Vorverständnis:
- Das Pankreas ist die Drüse des Körpers, die einerseits Verdauungsenzyme ins Duodenum abgibt und andererseits mittels der Hormone Insulin und Glucagon die Zucker-Homöostase des Körpers regelt. Es hat also einen exokrinen und einen endokrinen Anteil. Im Pankreas sind gewissermaßen zwei Organe in einem vereinigt.
- Das Pankreas entsteht aus zwei Anlagen, die im Laufe der Embryonalentwicklung verschmelzen und dann hinter dem Bauchfell zu liegen kommen.
- Das Pankreas liegt quer im Bauch und schmiegt sich ans Duodenum. Blut erhält es von benachbarten Arterien, und zwar von einer oberen und einer unteren.
Das Pankreas besitzt drei Teile und liegt sekundär retroperitoneal in der Duodenalkrümmung mit Beziehungen zu Gefäßen und anderen Organen
[Bearbeiten]
Gliederung des Pankreas
[Bearbeiten]Das Pankreas ist 80-120 g schwer und ca. 20 cm lang.
Es gliedert sich in drei Teile:
- Kopf (Caput pancreatis): er liegt an der Pars descendens duodeni; kaudal besitzt er einen hakenförmigen Fortsatz (Processus uncinatus), der bis zur Pars horizontalis duodeni heranreicht.
- Körper (Corpus pancreatis): er verläuft auf Höhe von L1/L2.
- Schwanz (Cauda pancreatis): er endet kurz vor dem Milz-Hilum im Ligamentum splenorenale (Verbindung zwischen Milz und dorsalem Peritoneum parietale).
| Merke Das Pankreas gliedert sich in Kopf (mit Processus uncinatus), Körper und Schwanz. Der Schwanz "leckt am Milz-Hilum". |
Topographische Beziehungen
[Bearbeiten]In einer Lücke zwischen Pankreaskopf und -schwanz, der Incisura pancreatis, treten die Arteria und Vena mesenterica superior sowie der Truncus intestinalis (Lymphgefäß) hervor, wobei der Processus uncinatus des Pankreaskopfs hinter diesen Gefäßen liegt. Kranial des Pankreaskopfs tritt der Truncus coeliacus aus der Aorta aus; einer seiner Abgänge, die Arteria splencia, begleitet den Pankreaskörper und -schwanz nach links.
Das Pankreas liegt sekundär retroperitoneal in der Krümmung des Duodenums und bildet somit einen Teil der Rückwand der Bursa omentalis. Da das Pankreas in seinem Verlauf die großen Gefäße des Bauchraums überquert (Aorta und Vena cava inferior), wölbt es sich zusammen mit dem Peritoneum parietale nach ventral (Tuber omentale). Vor dem Pankreas liegt der Magen, wobei die dazwischenliegende Bursa omentalis als Verschiebespalt dient.
Operativ gelangt man zum Pankreas über folgende Zugangswege:
- Foramen omentale der Bursa omentalis,
- Omentum minus,
- Ligamentum gastrocolicum.
- Mesocolon transversum.
| Merke Zwischen Pankreaskopf und -körper verlaufen Gefäße. Weil das Pankreas über deren Stammgefäße hinwegläuft, wird es nach ventral gewölbt (Tuber omentale). |
Arterielle Versorgung und venöser Abfluss erfolgen unterschiedlich für Pankreaskopf und für Pankreaskörper und -schwanz
[Bearbeiten]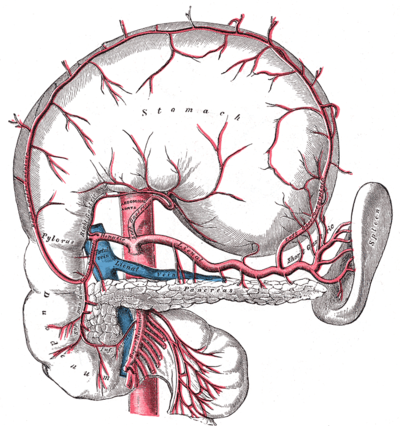
Arterielle Versorgung
[Bearbeiten]Das Pankreas wird von vier Arterien versorgt:
- Arteria pancreatica dorsalis aus der Arteria splenica: sie verlässt die Arteria splenica proximal und zieht nach kaudal.
- Rami pancreatici aus der Arteria splenica: verlassen die Arteria splenica auf deren Weg zur Milz, nachdem die Arteria pancreatica dorsalis ausgetreten ist.
- Arteria pancreaticoduodenalis superior aus der Arteria gastroduodenalis: die Arteria gastroduodenalis wiederum entspringt aus der Arteria hepatica communis, zieht nach kaudal und gibt zuerst die Arteria gastroomentalis dextra nach links ab, anschließend Rami duodenales nach rechts und endet schließlich als Arteria pancreaticoduodenalis superior; diese spaltet sich in einen vorderen (Arteria pancreaticoduodenalis superior anterior) und einen hinteren Ast (Arteria pancreaticoduodenalis superior posterior), welche vor und hinter dem Pankreas nach kaudal laufen, um sich mit den vorderen und hinteren Ästen der Arteria pancreaticoduodenalis inferior zu vereinigen.
- Arteria pancreaticoduodenalis inferior aus der Arteria mesenterica superior: sie teilt sich in die Rami anterior und posterior, die vor und hinter dem Pankreas nach kranial ziehen und sich mit den Arteriae pancreaticoduodenales superiores anterior und posterior zu einem Kranz vereinigen.
- Die Rami pancreatici versorgen somit einen Großteil des Pankreaskörpers und den Pankreasschwanz (also Bereiche des Pankreas links von der Aorta), die Arteria pancreaticoduodenales versorgen den Pankreaskopf und den restlichen Teil des Pankreaskörpers (also Bereiche des Pankreas rechts von der Aorta).
Folgende Besonderheiten gilt es außerdem zu beachten:
- Die Verbindung zwischen den Arteriae pancreaticoduodenales superiores anterior und posterior einerseits und den aus der Arteria pancreaticoduodenalis inferior abgehenden Rami anterior und posterior andererseits bildet eine wichtige Anastomose zwischen Truncus coeliacus und Arteria mesenterica superior.
- Die Arteria pancreatica inferior ist ein zusätzliches Gefäß, das einen Teil des Pankreaskörpers und den Pankreasschwanz versorgt. Sie wird gespeist aus den Abgängen der Arteria splenica (Arteria pancreatica dorsalis und Rami pancreatici) sowie aus den dorsalen Arterien der Arteriae pancreaticoduodenales, und zwar über die Arteria pancreatica transversa, die dabei als Querverbindung dient; ist diese Querverbindung der Hauptzufluss, nennt sich die Arteria pancreatica inferior "Arteria pancreatica major".
| Merke Das Pankreas erhält arterielles Blut über ein linksseitiges Versorgungsgebiet (Arterien aus der Arteria splenica) und ein rechtsseitiges Versorgungsgebiet (oberer Teil: Arteria pancreaticoduodenalis superior; unterer Teil: Arteria pancreaticoduodenalis inferior), dessen Arterien einen Kranz um den Pankreaskopf bilden (Anastomose zwischen Truncus coeliacus und Arteria mesenterica superior). Die Arteria pancreatica inferior wird aus den übrigen Pankreas-Arterien gespeist. |
Venöser Abfluss
[Bearbeiten]Wie sämtliche Venen der unpaaren Bauchorgane münden auch die Venen des Pankreas letztlich in die Vena portae hepatis. Es gibt zwei Abflusswege:
- Venen aus Pankreasschwanz und -körper münden in die Vena splenica (analog zur arteriellen Versorgung),
- Venen aus dem Pankreaskopf münden entweder in die Vena mesenterica superior oder direkt in die Vena portae hepatis.
Die Vena splenica nimmt die Vena mesenterica inferior auf und vereinigt sich anschließend mit der Vena mesenterica superior zur Vena portae hepatis. Wegen der Nähe des Pankreaskopfs zu diesen Venen können Tumoren des Pankreaskopfs zu Stauungen und folglich zu einem Aszites führen.
Lymphabfluss
[Bearbeiten]Der Lymphabfluss erfolgt aus drei Gebieten, wobei die kranialen Gebiete nach kranial drainieren und die kaudalen Gebiete nach kaudal:
- entlang der Arteria pancreaticoduodenalis superior zu den Nodi coeliaci,
- entlang den Rami pancreatici ebenfalls zu den Nodi coeliaci,
- entlang der Arteria pancreaticoduodenalis inferior zu den Nodi mesenterici superiores,
Nervale Versorgung
[Bearbeiten]Die nervale Versorgung des Pankreas erfolgt aus zwei Gebieten: von kranial und von kaudal.
- Von kranial: sympathische und parasympathische Fasern aus dem Plexus coeliacus erreichen das Pankreas über den Plexus pancreaticus.
- Von kaudal: vom Ganglion mesentericum superius gelangen ausschließlich sympathische Fasern zum Pankreas.
Klinik (Innere Medizin): Pankreatitis
|
Das exokrine Pankreas bildet den Pankreassaft, das endokrine Pankreas verschiedene Hormone
[Bearbeiten]Physiologie des Pankreas
[Bearbeiten]Funktionell besteht das Pankreas aus zwei unterschiedlichen Organen: aus einem exokrinen und einem endokrinen Anteil.
- Der exokrine Anteil bildet ein alkalisches Sekret ("Pankreassaft"; Tagesproduktion ca. 2 Liter, pH-Wert ca. 8) mit Verdauungsenzymen und Bikarbonat und gibt es über die Papilla duodeni major ins Lumen des Duodenums ab, wo die Verdauung und Resorption des Nahrungsbreis stattfindet.
- Der endokrine Anteil produziert Hormone wie Insulin und Glucagon, die den Stoffwechsel beeinflussen.
Physiologie des exokrinen Pankreas
Das exokrine Pankreas bildet Bikarbonat sowie Verdauungsenzyme und wird durch verschiedene Hormone reguliert.
- Die Bildung von Bikarbonat und Verdauungsenzymen findet an unterschiedlichen Orten des Pankreasparenchyms statt:
- Die Bikarbonat-Bildung erfolgt in den Gangepithelzellen; sie entziehen dabei dem von den Azinuszellen produzierten Primärsekret Chlorid im Austausch gegen Bikarbonat. Bikarbonat ist erforderlich, zum einen um im Duodenum den durch den Magensaft angesäuerten Speisebrei zu neutralisieren und ihn somit für eine Passage durch den Darm vorzubereiten, zum anderen um den pH-Wert im Duodenum an das pH-Optimum der Verdauungsenzyme anzugleichen und dadurch eine effektive Zersetzung des Speisebreis zu ermöglichen.
- Synthese und Exozytose von Verdauungsenzymen und -proenzymen leisten die Azinuszellen. Zu den Verdauungsenzymen zählen Kohlenhydrat-spaltende Enzyme (Amylase, Maltase), Fett-spaltende Enzyme (Lipasen, Cholesterinesterase), Nucleinsäuren-spaltende Enzyme (Ribonuclease, Desoxyribonuclease) sowie Aminosäure-spaltende Enzyme (Peptidasen wie Trypsin, Chymotrypsin, Elastase, Carboxypeptidasen; bilden den Hauptanteil der Verdauungsenzyme). Wie viele andere Enzyme gelangen die Peptidasen als inaktive Vorstufen ins Duodenum (Trypsinogen, Chymotrypsinogen, Proelastase, Procarboxypeptidasen); dort wird Trypsinogen von der in der Duodenum-Mukosa lokalisierten Enteropeptidase zu Trypsin aktiviert, Trypsin seinerseits aktiviert alle übrigen Vorstufen zu aktiven Peptidasen. Trypsin vermag also eine Kettenreaktion in Gang zu setzen; um eine Selbstverdauung des Pankreas zu verhindern, enthält der Pankreassaft daher einen Trypsin-Inhibitor als Sicherung. Ein zusätzliches Protein namens Lithostatin schützt die zahlreichen Calcium-Ionen des Pankreassafts vor der Kristallisation.
- Die Sekretionstätigkeit des exokrinen Pankreas wird reguliert hauptsächlich von den Hormonen Sekretin und Cholecystokinin (CCK), außerdem vom Nervus vagus.
- Sekretin wird von S-Zellen (lokalisiert in Duodenum und Jejunum) ausgeschüttet, und zwar sowohl bei Übertritt von sauerem Magensaft (pH < 4,5) oder von Gallensäuren ins Duodenum. Vermittelt über eine Adenylatzyklase-Kaskade stimuliert es daraufhin die Bikarbonat-Sekretion, während es zugleich die Magensaft-Sekretion hemmt. Der Sekretin-Regelkreis sorgt somit für einen konstant neutralen pH-Wert im Duodenum.
- CCK wird von I-Zellen (lokalisiert in Duodenum und Jejunum) sowie von Nervenendigungen sezerniert, und zwar sowohl bei Übertritt von Nahrungsstoffen (langkettige Fettsäuren, Peptide und Aminosäuren, Calcium) ins Duodenum als auch stimuliert durch Gastrin; Trypsin hingegen hemmt die CCK-Sekretion. Vermittelt über eine Phosphoinositid-Kaskade steigert CCK die Sekretion von Verdauungsenzymen und bewirkt zudem eine Kontraktion der Gallenblase mit nachfolgendem Gallensäure-Fluss ins Duodenum. Der CCK-Regelkreis sorgt somit für einen geringen Gehalt von zu verdauenden Nahrungsstoffen im Duodenum.
- Acetylcholin aus dem Nervus vagus erhöht die Sekretion sowohl von Bikarbonat als auch von Verdauungsenzymen. Dies spielt v. a. in der kephalen und gastralen Phase eine Rolle.
| Merke Gangepithel → Sekretion von Bikarbonat (hebt den pH-Wert im Duodenum); Azinuszellen → Sekretion von Verdauungsenzymen (zersetzen die im Nahrungsbrei enthaltenen Nahrungsstoffe und bereiten dadurch deren Resorption vor). Sekretin reguliert den Duodenums-pH über die Bikarbonat-Sekretion, CCK den Gehalt an Nahrungsstoffen im Duodenum über die Verdauungsenzym-Sekretion und Gallenblasen-Kontraktion. |
Physiologie des endokrinen Pankreas
Das endokrine Pankreas besteht aus den Langerhans-Inseln. Diese setzen sich aus vier Zelltypen zusammen, die jeweils spezifische Hormone sezernieren:
- α-Zellen (ca. 14 %): sie bilden Glucagon, ein Hormon das bei erniedrigter Blutglucose-Konzentration (< 5 mM) ausgeschüttet wird und katabole Wirkungen entfaltet, ähnlich dem Adrenalin oder Noradrenalin. Glucagon wirkt an seinen Zielzellen über einen 7-Transmembrandomänen-Rezeptor mit nachgeschalteter Adenylatzyklase-Kaskade.
- Glucagon wirkt diabetogen (d. h. die Blutglucose-Konzentration steigernd), indem es in der Leber die Schlüsselenzyme von Glycogenolyse und Gluconeogenese aktiviert sowie die Expression der Glucogenese-Enzyme steigert.
- Glucagon wirkt lipolytisch und erhöht aufgrund des dadurch gesteigerten Acetyl-CoA-Angebots die Ketonkörper-Konzentration im Blut.
- β-Zellen (ca. 80 %): sie bilden Insulin, ein Hormon, das bei erhöhter Blutglucose-Konzentration (> 5,6 mM) ausgeschüttet wird und anabole Wirkungen entfaltet. Als Signal für die Freisetzung des Insulins aus den Speichervesikeln dient der erhöhte Glucose-Spiegel in der β-Zelle: bei erhöhtem Glucose-Angebot gelangt Glucose durch konstitutiv in die Membran eingebaute Kanäle (GLUT-2) in die β-Zelle und durchläuft die Glycolyse; dabei entsteht ATP, das zu ATP-abhängigen Kalium-Kanälen in der Zellmembran diffundiert und deren Schließung induziert. Dadurch kommt es zur Depolarisation, die eine Öffnung von Calcium-Kanälen bewirkt; das einströmende Calcium schließlich triggert die Exozytose der Insulin-haltigen Vesikel. Insulin selbst wirkt über eine Tyrosinkinase-Rezeptor, der die Phosphorylierung von Proteinen (Insulin-Rezeptor-Substrate) bewirkt; unter anderem verringert sich dadurch der intrazelluläre cAMP-Spiegel, und es treten je nach Zelltyp verschiedene Effekte ein.
- Insulin wirkt antidiabetogen:
- Es fördert die Glucose-Aufnahme in Skelett- und Muskelzellen (Translokation von Glucose-Transportern [GLUT-4] in die Zellmembran).
- Es stimuliert die Glucose-Verwertung innerhalb der Zelle (Induktion oder Stimulation von Schlüsselenzymen der Glycolyse: Hexokinase, Glucokinase, Phosphofructokinase, Pyruvatkinase) und sorgt somit für eine Auffüllung der Glycogen-Speicher.
- Es verhindert die Herstellung von Glucose aus Nicht-Kohlenhydraten wie Lactat, Aminosäuren oder Glycerin (Repression von Schlüsselenzymen der Gluconeogenese: Pyruvatcarboxylase, Phosphoenolpyruvat-Carboxykinase, Fructose-1,6-Bisphosphatase, Glucose-6-Phosphatase) und reprimiert die Bereitstellung von Glucose aus Glycogen-Speichern.
- Insulin wirkt antilipolytisch, indem es die Lipoproteinlipase induziert und dadurch eine Umverteilung von Fettsäuren von Chylomikronen und VLDL in Adipozyten bewirkt; in den Adipozyten entstehen aus den Fettsäuren Triacylglycerine, die anschließend gespeichert werden.
- Zudem fördert es die Kalium-Aufnahme in die Zelle, indem es indirekt die Natrium-Kalium-ATPase stimuliert.
- Insulin und Glucagon sind direkte Gegenspieler.
- Insulin wirkt antidiabetogen:
- δ-Zellen (ca. 5 %): sie bilden Somatostatin, ein Hormon, das auf verschiedene Zielzellen v. a. hemmend wirkt. So inhibiert es die Sekretion von Insulin, Glucagon aus den α- und β-Zellen, außerdem die Sekretion anderer gastrointestinaler Hormone (Gastrin, Sekretin), hypophysiärer Hormone (TSH, ACTH, Prolaktin); außerdem hemmt es Wachstumsprozesse und bildet somit den Gegenspieler des somatotropen Hormons (STH, GH, Wachstumshormon).
- PP-Zellen (ca. 1 %): sie bilden das Pankreatische Polypeptid, ein Hormon, das die Sekretionstätigkeit des exokrinen Pankreas hemmt und somit einen Gegenspieler des CCK darstellt.
| Merke Insulin: antidiabetogen, antilipolytisch, anabol, zudem Förderung der Kalium-Aufnahme; Glucagon: diabetogen, lipolytisch, katabol; Somatostatin: entfaltet diverse v. a. hemmende Wirkungen auf verschiedene Zelltypen; PP: hemmt das exokrine Pankreas. |
Klinik (Innere Medizin): Tumore des Pankreas
|
Histologie des Pankreas
[Bearbeiten]Makroskopisch besteht das Pankreas aus Läppchen, die durch Bindegewebe separiert sind.
Mikroskopisch sind exokrine und endokrine Anteile des Pankreas differenzierbar:
- Die exokrinen Anteile bilden die Gangepithelien mit den serösen Drüsenendstücken (tubuloazinäre Endstücke, Acini). Die Ausführungsgänge münden in den zentral durch das Pankreas verlaufenden Ductus pancreaticus. Histologisch ist dabei Folgendes auffällig:
- Die distalen Gangepithelzellen stülpen sich gewissermaßen in die Acini hinein (zentroacinäre Zellen).
- Die Ausführungsgänge sind kurz, es existieren keine Streifenstücke - ein wichtiges histologisches Differenzierungskriterium gegenüber beispielsweise Speicheldrüse.
- Die endokrinen Anteile bilden die etwa zwei Millionen Langerhansinseln, die in die exokrinen Funktionsbereiche unregelmäßig eingestreut sind.
Embryonalentwicklung des Pankreas
[Bearbeiten]Das Pankreas (Bauchspeicheldrüse) entsteht aus einer dorsalen und ventralen Pankreas-Anlage:
- Zunächst bildet sich die dorsale Pankreas-Anlage aus der Duodenum-Anlage,
- wenig später (28. Tag) entsteht die ventrale Pankreas-Anlage zwischen Duodenum-Anlage und Gallenblasen-Anlage; sie besitzt eine rechte und eine linke Knospe.
- Beide Anlagen stehen in der Sagittalebene.
- Durch Wachstum des Mesogastrium dorsale und Magendrehung drehen sich auch die Pankreas-Anlagen um 90° und stehen schließlich in der Frontalebene.
- Die rechte Knospe der ventralen Pankreas-Anlage wandert zusammen mit dem proximalen Ductus choledochus nach dorsal und kommt hinter dem Duodenum zu liegen, und zwar hinter und unter der dorsalen Pankreas-Anlage; die linke Knospe der ventralen Pankreas-Anlage bildet sich dagegen zurück.
- Beide Pankreas-Anlagen sowie ihre Ausführungsgänge verschmelzen miteinander, schließlich entstehen im Normalfall zwei Gänge:
- Ductus pancreaticus (Wirsung) für die ventrale Anlage: vereinigt sich zumeist mit dem Ductus choledochus in einer Erweiterung (Ampulla hepatopancreatica) und mündet dann in der Papilla duodeni major ins Duodenum;
- Ductus pancreaticus accessorius (Santorini) für die dorsale Anlage: mündet in der Papilla duodeni minor, die über der Papilla duodeni major liegt, ins Duodenum.
- Dabei können auch Varianten entstehen:
- fehlender Ductus pancreaticus accessorius,
- Ductus pancreaticus accessorius als Hauptausführungsgang,
- septierte Ampulla hepatopancreatica oder Doppelmündung von Ductus pancreaticus und Ductus choledochus,
- fehlende Ampulla hepatopancreatica.
- Auch bei Doppelmündung von Ductus pancreaticus und Ductus choledochus sind Gallenwege und Pankreaswege weiterhin miteinander verbunden, und zwar über zahlreiche kleine Pankreasgänge, die in die in den Ductus choledochs einmünden.
- Dabei können auch Varianten entstehen:
- Ab der siebten Woche differenziert sich das Pankreas, indem es sich die Epithelstränge unter dem Einfluss von Wachstumsfaktoren verzweigen und sich ab der zwölften Woche Drüsenendstücke (Acini) ausbilden; bald entstehen auch endokrine Pankreaszellen.
- Durch weitere Umlagerungsprozesse erreicht das Pankreas schließlich seinen definitiven Ort: sekundär retroperitoneal in der Krümmung des Duodenums.
| Merke Das Pankreas entsteht aus zwei Anlagen, wobei die ventrale Anlage nach dorsal wandert und unter der dorsalen Anlage zu liegen kommt. An diesen Vorgang erinnern die beiden Ausführungsgänge mit je eigener Mündung ins Duodenum: Ductus pancreaticus für die ventrale Anlage, Ductus pancreaticus accessorius für die dorsale Anlage. |
Klinik (Innere Medizin): Fehlbildungen des Pankreas
|
Zusammenfassung
[Bearbeiten]Das Pankreas ist einerseits für die Produktion von Verdauungssekreten und andererseits für die Stoffwechsel-Homöostase entscheidend. Es besteht aus Kopf, Körper und Schwanz, liegt sekundär retroperitoneal im C des Duodenums und verläuft über die großen Gefäße des Bauchraums hinweg zur Milz. Arteria und Vena mesenterica superior erscheinen zwischen Pankreaskopf und -körper.
Arteriellen Zufluss erhält das Pankreas sowohl aus der Arteria splenica, welche die linken Anteile (Pankreaskörper, -schwanz) versorgt, als auch aus dem Truncus coeliacus und der Arteria mesenterica superior, welche die rechten Anteile (Pankreaskopf, -körper) versorgen und sich dabei zu einem anastomosierenden Kranz um den Pankreaskopf vereinigen. Der venöse Abfluss erfolgt auf analoge Weise, die Lymphe fließt entlang den Arterien nach kranial oder kaudal.
Funktionell unterscheidet man das exokrine und das endokrine Pankreas. Das exokrine Pankreas bildet sowohl eine Vielzahl von Verdauungsenzymen zur Zersetzung der verschiedenen Bestandteile des Nahrungsbreis als auch Bikarbonat-Ionen, die den Magensaft neutralisieren und ein alkalisches Milieu im Duodenum schaffen; es wird einerseits endokrin über intestinale Hormone (CCK, Sekretin), andererseits nerval über den Nervus vagus reguliert. Das endokrine Pankreas produziert Hormone wie Insulin, Glucagon, die für die Glucose-Homöostase von Bedeutung sind und zahlreiche metabolische Wirkungen zeitigen.
Das Pankreas entsteht aus einer ventralen und einer dorsalen Anlage, wobei die dorsale Anlage ortsständig bleibt, während die ventrale Anlage zusammen mit dem Ductus choledochus nach dorsal wandert und sich mit der dorsalen Anlage vereinigt. Meist besitzt das Duodenum daher zwei Papillen - eine große für die ventrale Anlage und eine kleine, über der großen Papille einmündende für die dorsale Anlage.
Fragen und Aufgaben
[Bearbeiten]- Beschreiben Sie Lage und Verlauf des Pankreas!
- Wodurch entsteht das Tuber omentale?
- Wie gelangt man operativ zum Pankreas?
- Beschreiben Sie die arterielle Versorgung des Pankreaskopfs!
- Warum haben Tumoren des Pankreaskopfs oftmals Stauungen zur Folge?
- Was produziert das exokrine Pankreas und wohin werden diese Produkte abgegeben?
- Was produziert das endokrine Pankreas und wohin werden diese Produkte abgegeben?
- Zu welcher Pankreasanlage gehört die Papilla duodeni minor?
Antworten zu den Fragen finden Sie an entsprechenden Stellen im Kapitel. Haben Sie die Lernziele erreicht?

