Werkstoffkunde Metall/ Innerer Aufbau/ Legierung
|
Unter einer Legierung versteht man ein Stoffgemisch mit metallischem Charakter. Dazu muss zwischen den Komponenten die metallische Bindung bestehen, d.h. freier Austausch der Valenzelektronen. Als Komponenten kommen in Frage:
In dem folgenden Kapitel soll (noch) nicht auf spezielle Legierungen eingegangen werden. Die erwähnten Metalle dienen nur als Beispiel für die allgemeinen Vorgänge in Legierungen. |
Zustands- oder Phasendiagramme
[Bearbeiten]In der Thermodynamik wird häufig mit Temperatur-Druck-Zustandsdiagrammen gearbeitet, in denen die Phasenübergänge eines bestimmten Stoffes (mit bestimmter Zusammensetzung) verzeichnet sind. In der Werkstoffkunde arbeiten wir dagegen mit Zustandsdiagrammen, die den Existenzbereich einer Phase in Abhängigkeit von Temperatur und Zusammensetzung aufzeigen – bei konstantem Druck.
Wie gesagt, bestehen Legierungen aus mindestens zwei Komponenten, im folgenden Basismetall und Legierungselement(e) genannt. Weit verbreitet sind Zustandsdiagramme von Legierungen mit zwei Komponenten (Zweistoff- oder Binäre Systeme). Die meisten Legierungen bestehen aber aus dem Basismetall mit zwei, drei oder mehr Legierungselementen, die einen erheblichen Einfluss haben, so dass die Zweistoff-Phasendiagramme nur begrenzte Gültigkeit haben. Daher gibt es Diagramme von Dreistoffsystemen. Eine Abhandlung über die ternären Diagramme würde aber den Rahmen diese Ks sprengen. Später werden wir uns deshalb darauf beschränken, bei zusätzlichen Legierungselementen deren Wirkung als „Verschiebung des Existenzbereichs einer Phase in eine bestimmte Richtung“ zu beschreiben.
Im schmelzflüssigem Zustand lassen sich fast alle Metalle sehr gut miteinander vermischen. Schwierigkeiten treten nur bei extremen Unterschieden beim Schmelzpunkt oder der Dichte auf. Im festen Zustand gibt es dagegen große Unterschiede in der Löslichkeit. Die Komponenten lassen sich entweder vollständig, überhaupt nicht, oder in Abhängigkeit von der Temperatur miteinander vermischen – entsprechend werden wir nun drei grundlegend verschiedene Typen von Zweistoff-Diagrammen kennen lernen.
Zweistoffsysteme mit vollständiger Löslichkeit
[Bearbeiten]Bei vollständiger Löslichkeit im festen Zustand bilden sich in jeder Zusammensetzung Mischkristalle. Diese sind entweder Einlagerungs- oder Substitutionsmischkristalle.
Typische Substitutions-MK-Bilder sind die Legierungen Eisen-Chrom, Eisen-Nickel, Gold-Kupfer, Gold-Silber und Kupfer-Nickel.
Ein wichtiger Einlagerungs-Mischkristalle ist Austenit (γ-Eisen-Kohlenstoff).
Durch die Mischkristallbildung wird auch bei noch so großer Ähnlichkeit der Legierungselemente immer das Kristallgitter verzerrt, da die verschiedenen Elemente auch verschiedene Atomdurchmesser besitzen. Dadurch entstehen Spannungen, welche die Versetzungsbewegungen und damit die Verformungen des Materials erschweren. Die Gitterverzerrung erhöht also Härte und Festigkeit.
Ein beliebtes Beispiel für eine Legierung mit vollkommener Löslichkeit im festen Zustand ist das Zweistoffsystem Cu-Ni.

|
|
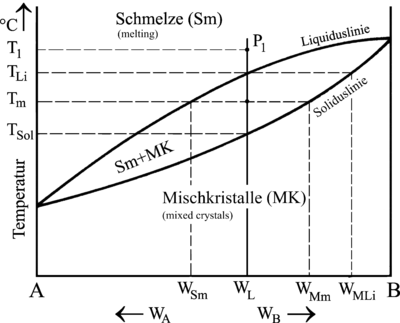
| Abkühlkurven und Zustandsschaubild einer Legierung verschiedener Zusammensetzung mit Mischkristallbildung | |
Die Legierungen (Kurven 2-5) erstarren im Gegensatz zu den Basismetallen (Kurven 1,6) nicht bei einer festen Temperatur, sondern in einem Haltebereich. Die Temperatur bleibt also nicht konstant, sondern sinkt langsam. Die Haltebereiche verschiedener Zusammensetzungen einer Legierung liegen jedoch immer zwischen den jeweiligen Erstarrungstemperaturen ihrer reinen Komponenten.
Ursache dafür ist die „Behinderung“ der Kristallisation in einer Legierung durch Komponente A (Kurve 1), die, wenn sie könnte, bei noch tieferer Temperatur erstarren würde. Komponente B dagegen „drängt“ auf Erstarrung, die eigentlich schon eher hätte beginnen müssen.
Ablesen lassen sich diese Zusammensetzungen am Zustandsschaubild, indem man durch jeden beliebigen Punkt an der ausgewählten Legierung (Bild WL) eine Waagerechte zur Soliduslinie zieht. Bei der Liquidustemperatur TLi (Beginn der Erstarrung) besitzen die ersten Kristalle also eine Zusammensetzung von WMLi. Auch die jeweilige Zusammensetzung der Restschmelze lässt sich auf diese Weise ermitteln, indem man zum Beispiel bei Tm die Waagerechte bis zur Liquiduslinie durchzieht. Die Schmelze hätte also an diesem Punkt die Zusammensetzung WSm und die Mischkristalle die Zusammensetzung WMm.
Mit Hilfe des Zustandsschaubildes lässt sich auch berechnen, wie hoch bei jeder Zwischentemperatur der Anteil an Schmelze bzw. der Anteil an Mischkristallen ist:
| MS · WSm + MMK · WMm = 1 · WL MS + MMK = 1 |
MS = Anteil Schmelze WSm = Zusammensetzung Schmelze (bei Tm) |
Während der Kristallisation ändert sich also die Zusammensetzung des Materials, das mit Kristall aus der Schmelze hinzugefügt wird. Die Folge sind Konzentrationsunterschiede zwischen dem Korninneren und den Korngrenzen. Diese gleichen sich selbst nach vollständiger Erstarrung der Schmelze durch Diffusion aus – abhängig von der Abkühlungsgeschwindigkeit findet der Stoffausgleich aber nur teilweise statt, so das gewisse Konzentrationsunterschiede erhalten bleiben – in diesem Fall entstehen Kristallseigerungen.
Zweistoffsysteme mit vollständiger Unlöslichkeit
[Bearbeiten]Legierungen dieser Art sind zwar in der Schmelze ineinander gelöst, entmischen sich jedoch während der Kristallisation vollständig. Es entsteht ein Kristallgemisch aus zwei Phasen, wobei jede Phase nur aus einer Komponente besteht und völlig frei ist von der anderen Komponente.

|

|
| Abkühlkurven und Zustandsschaubild einer Legierung verschiedener Zusammensetzung bei getrennter Kristallbildung | |
Zweistoffsysteme, die ineinander vollständiger unlöslich sind, weisen ein Eutektikum auf. Bei diesem besonderen Mischungsverhältnis erstarrt die Schmelze bei einer besonders niedrigen Temperatur, dem eutektischen Punkt, der weit unter der Schmelztemperatur der reinen Komponenten liegt. Die Abkühlungskurve einer eutektischen Legierung zeichnet sich durch einen Haltepunkt aus – während das System bei allen anderen Mischungsverhältnissen in einem Haltebereich erstarrt.
Nachdem die Liquidustemperatur unterschritten ist, beginnt die jeweils dominierende Komponente zu kristallisieren. Links des Eutektikums (= untereutektisch) besteht die Legierung aus wachsenden Primär-Kristallen der Komponente A und der Restschmelze. Während die Komponente A kristallisiert, reduziert sich ihr Anteil an der Restschmelze, bis deren Zusammensetzung der des Eutektikums entspricht. Zu diesem Zeitpunkt hat die Temperatur der Legierung die Soliduslinie erreicht und verharrt wie ein Reinstoff in einem Haltepunkt, bis die Erstarrung vollständig abgeschlossen ist. Dominiert die Komponente B in der Legierung (rechts des Eutektikums = übereutektisch) wird sie entsprechend zuerst kristallisieren. Der Anteil an Primärkristallen in einer Legierung lässt sich mithilfe des Zustandsschaubildes errechnen. Die Berechnung setzt dabei am Punkt TEu an, also an der Stelle, an der die Restschmelze gerade eben die eutektische Zusammensetzung erreicht:
|
MEu = Anteil Restschmelze eutektischer Zusammensetzung = Anteil des Eutektikums MPr = Anteil Primärkristalle |
Der Grund für dieses Verhalten liegt in der starken, gegenseitigen Behinderung der beiden Komponenten, die sich während der Kristallisation entmischen, um Kristalle der eigenen Art bilden zu können. Das Maximum an gegenseitiger Störung liegt demnach bei Legierung 3, bei der sich im Erstarrungspunkt gleichzeitig Kristalle der Komponenten A und B bilden. Bedingt durch die anhaltende, gegenseitige Behinderung beim Entmischen und der tiefen Temperatur sind die Wege der Atome allerdings sehr klein und das Kristallgemisch daher sehr feinkörnig.
Dieser Besonderheit wegen erhält Legierung 3 den Namen Eutektische Legierung (= Das Feine ; Das Wohlgebaute). Die allen Legierungen gemeinsame Soliduslinie wird entsprechend Eutektikale genannt und die dazu gehörige Temperatur eutektische Temperatur (TEu).
Eine besondere Bedeutung hat das Eutektikum bei Gusslegierungen und bei Lötzinn – durch die niedrige Schmelztemperatur ist der Energieaufwand beim Schmelzen gering.
| Name | System | Mischungsverhältnis | Schmelztemp. |
|---|---|---|---|
| Lötzinn | Sn-Pb | 62 / 38 | 183°C |
| Roses Metall | Bi-Pb-Sn | 50 / 25 / 25 | 98°C |
| Woodsches Metall | Bi-Pb-Cd-Sn | 50 / 25 / 12,5 / 12,5 | 70°C |
| Galinstan | Ga-In-Sn | 68,5 / 21,5 / 10 | -19°C (!) |
Des Weiteren existieren binäre Systeme vollständiger Unlöslichkeit, bei denen kein Eutektikum entsteht, sondern nach dem Abkühlen die eine Komponente auf der anderen liegt. Bringt man beispielsweise Eisen und Blei in eine Schmelze, so wird das Eisen auf dem Blei (wie Öl auf Wasser) schwimmen. Kühlt die Schmelze ab und härtet aus, wird erst das feste Eisen auf dem flüssigen Blei schwimmen (da es eine geringere Dichte hat) bis dieses am Grund des Tiegels aushärtet.
Zweistoffsysteme mit begrenzter Löslichkeit
[Bearbeiten]Legierungen dieser Art können, wie der Titel schon andeutet, zwar Mischkristalle bilden, jedoch nicht in jeder Zusammensetzung. Im Gegensatz zu Legierungen mit vollkommener Löslichkeit unterscheiden sich hier die Atomgrößen stärker, was bedeutet, dass die Gitterverzerrungen ab einer gewissen Zusammensetzung unerträglich werden. Auch das Kristallsystem kann ein Hindernis sein, wenn sich die Legierungselemente im Kristallsystem zwar ähnlich, aber nicht gleich sind.
So kann zum Beispiel jede Komponente in der Legierung Blei (kubisch-flächenzentriert) - Zinn (tetragonal-raumzentriert) mit der anderen in begrenztem Maße Austausch-Mischkristalle bilden.
Typische MK-Bildner begrenzter Löslichkeit:
- Aluminium-Magnesium
- Blei-Zinn
- Kupfer-Aluminium
- Kupfer-Zink
- Kupfer-Zinn
- Zink-Aluminium
Begrenzte Löslichkeit im festen Zustand heißt aber nicht nur, dass die eine Komponente beim Kristallisieren bis zu einem gewissen Prozentsatz Atome der anderen Komponente aufnehmen kann, sondern auch, dass die Löslichkeit bei sinkender Temperatur abnimmt. Da die Bewegungsenergie der Atome geringer wird, schrumpft natürlich auch entsprechend die Gitterkonstante des vorliegenden Kristallsystems, und es bietet Fremdatomen weniger Platz. Die Folge davon ist, dass die Mischkristalle ab der Übergangstemperatur TÜ beginnen, sich zu entmischen.
Genau diese Eigenschaft - teilweise Entmischung der Komponenten durch abnehmende Löslichkeit bei tieferen Temperaturen - wird zur Festigkeitssteigerung einer solchen Legierung ausgenutzt. Man spricht hierbei auch von Ausscheidungshärtung.
|
|
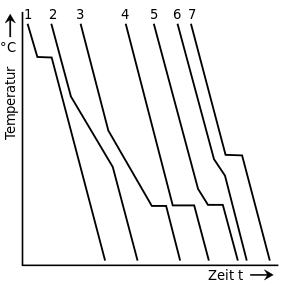
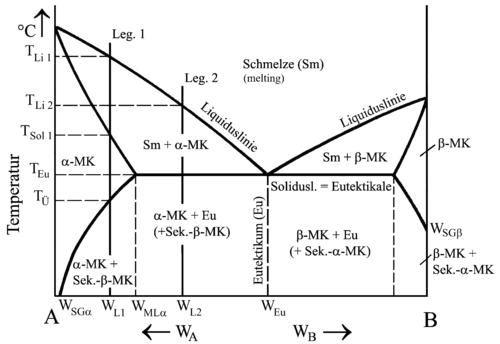
| Abkühlkurven und Zustandsschaubild einer Legierung verschiedener Zusammensetzung mit Mischkristallbildung begrenzter Löslichkeit im festen Zustand | |
Legierung 1 erstarrt somit zwischen TLi 1 und TSol 1 und bildet Mischkristallen mit dem Kristallsystem von A, genannt α-Kristalle. Dessen homogener Zustand bleibt bis TÜ erhalten. An diesem Punkt sind die Mischkristalle gesättigt, was bedeutet, dass die Komponente A die maximalen Löslichkeit für die Komponente B bei dieser Zusammensetzung erreicht hat.
Sinkt die Temperatur weiter ab, sind die Mischkristalle übersättigt – die maximale Löslichkeit von B in der Komponente A ist überschritten
Bei TÜ wandern die Atome von B entsprechend der maximalen Löslichkeit für diese Temperatur zu den Korngrenzen und bilden dort Sekundär-Mischkristalle mit dem Kristallsystem von B, genannt β-Mischkristalle. Zum Ausgleich diffundieren entsprechend A-Atome ins Korninnere.
Der Anteil der Sekundär-Mischkristalle lässt sich nach folgender Formel berechnen:
|
MSβ = Anteil Sekundär-β-Mischkristalle WL = Zusammensetzung Legierung |
Legierung 2 kristallisiert zunächst genau wie Legierung 1. Bei Erreichen der Eutektikalen erstarrt die Restschmelze jedoch in einem Haltepunkt und es bildet sich ein feinkörniges Gemisch aus α- und β-Mischkristallen, welches, wie bei getrennter Kristallbildung, Eutektikum genannt wird. Die zuvor entstandenen α-Mischkristalle entsprechen den Primärkristallen.
Unterhalb der Eutektikalen scheiden auch bei dieser Legierung aus den Primär-α-Mischkristallen B-Atome aus. Um hier den Anteil der Sekundär-β-Mischkristalle aus den Primär-Kristallen berechnen zu können, muss zuerst der Anteil an Primärkristallen an der Gesamtlegierung berechnet werden. Die Berechnung entspricht derjenigen bei getrennter Kristallisation. Anschließend wird der Anteil Sekundär-β-Mischkristalle aus den Primärkristallen berechnet und mit dem Anteil der Primärkristalle multipliziert :
| 1) 2) |
MPr = Anteil Primärkristalle in % WEu = Zusammensetzung des Eutektikums |
Intermetallische Kristalle
[Bearbeiten]Eine weitere Möglichkeit zur Legierungsbildung besteht darin, dass die beteiligten Elemente zwar einen gemeinsamen Kristall bilden, dieser jedoch keinem Kristallsystem der Basiselemente ähnelt. Es entsteht ein eigenes Kristallsystem, das im Gegensatz zu denen von reinen Metallen sehr kompliziert aufgebaut ist. Solche Verbindungen sind zudem sehr hart und spröde.
Beispiele für intermetallische Kristallisation sind:
- Al2Cu
- Mg2Si
- Cu4Sn
Die Kristallisationsformel ist gleich der Formel für die chemisch Verbindungen. Die Kristalle erfordern ein festes Atomzahlenverhältnis, denn die vorliegenden Verbindungsart ist nicht die (rein) metallische, sondern jene, die zwischen der metallischen einerseits und der ionischen bzw. konvalenten Bindung andererseits steht. Solch eine Legierung, deren Legierungselemente ausschließlich Metalle sind, nennt man deshalb intermetallische Verbindung oder auch intermetallische Phase.
Intermediäre Kristalle
[Bearbeiten]Gleiches gilt für „Legierungen“ zwischen Metallen und Nicht-Metallen, z.B.:
- Fe3C (Zementit)
- WC (Wolframcarbid) und
- BN (Bornitrid)
- TiN u. TiC (Titannitrid und Titancarbid)
Diese bezeichnet man als Intermediäre Phasen. Zementit ist ein wesentlicher Bestandteil in Stahl und Gusseisen. Wolframcarbid und Bornitrit sind extrem harte und verschleißfeste Verbindungen, die z.B. als Schneidwerkstoffe Anwendung finden und dem Diamant in seiner Schneidleistung nur wenig nachstehen.
Diffusion
[Bearbeiten]Unter Diffusion versteht man die Bewegung von Teilchen wie Atomen, Molekülen und Ionen innerhalb einer Substanz. Sie beruht NICHT auf äußeren Kräften, die auf das Material einwirken, sondern ist rein thermisch bedingt (Brown´sche Molekularbewegung). Wir wissen, dass Teilchen temperaturabhängig in regelloser Bewegung sind. Der Motor für eine gerichtete Bewegung dieser Teilchen sind Konzentrationsunterschiede. Folge der Diffusion ist also der Ausgleich dieser Unterschiede. Der Prozess kann innerhalb einer Phase stattfinden, oder zwischen zwei Phasen über die Phasengrenze hinweg.
Wahrscheinlichkeit und Entropie
[Bearbeiten]
- Angenommen innerhalb einer Lösung sind 90 Teile eines Stoffen in der rechten Hälfe und nur zehn in der linken Hälfte. Jedes Teilchen bewegt sich durch die Brownsche Molekularbewegung in eine völlig zufällige Richtung – und zu 50% auch über die Mitte hinweg, auf die andere Hälfte. Damit ist es neunmal wahrscheinlicher, dass eines der 90 Teilchen zufälligerweise von rechts nach linke springt, als dass eines der 10 Teilchen von links nach rechts springt. Unterm Strich und nach ausreichend langer Zeit werden im Durchschnitt 50 Teilchen links und 50 Teilchen rechts landen. Nach der Statistischen Normalverteilung ist jedes davon abweichende Ergebnis umso unwahrscheinlicher, je weiter es vom Mittelwert abweicht.
– So viel zur Wahrscheinlichkeit.
Für sich genommen hat sich jedes Teilchen – rein zufällig – für links oder rechts entschieden. Im Ganzen betrachtet hat aber ein Stofftransport stattgefunden - die Diffusion. Ihr Motor ist das Streben des Systems nach maximaler Entropie. Doch muss diese kinetisch auch möglich sein, d.h. die Beweglichkeit der Teilchen muss groß genug sein.
Diffusionskoeffizient und -geschwindigkeit
[Bearbeiten]Die Geschwindigkeit der Diffusion,
- sinkt proportional zum Abstand zwischen den Konzentrationsunterschieden und,
- steigt proportional zum Niveau zwischen ihnen.
Die Diffusion verlangsamt sich also mit ihrem Fortschritt – eine völlige Durchmischung kann also nur bei unendlich lange anhaltender Diffusion erfolgen – in der Praxis wird sie aber irgendwann als ausreichend und damit als gegeben angesehen.
Diffusionskoeffizienten in Feststoffen[1] sind i. d. R. mehrere tausend Mal kleiner als Diffusionskoeffizienten in Flüssigkeiten.
Für die Diffusion in Festkörpern sind Sprünge zwischen verschiedenen Gitterplätzen erforderlich. Dazu müssen die Teilchen erst die Aktivierungsenergie QD, was bei höherer Temperatur leichter möglich ist als bei niedrigerer. Dies wird durch den Zusammenhang[2]:
|
Da die Diffusion ein Teilchen- oder Massestrom ist, wird sie als Fluss F gemessen; d.h. die transportierte Masse oder die Anzahl der Teilchen pro Fläche und Zeiteinheit.
beschrieben. D0 lässt sich näherungsweise berechnen mit:
|
|
Allerdings empfiehlt es sich insbesondere bei Diffusionskoeffizienten in Feststoffen, diese experimentell zu bestimmen.
Diffusionspfade und -mechanismen
[Bearbeiten]Generell kann der Stofftransport nach folgenden Mechanismen erfolgen:
- Leerstellen-Diffusion
- Teilchen von beliebiger Größe nutzen vorhandene Leerstellen im Kristallgitter und springen von einer Leerstelle zur nächsten. Aus einem anderen Blickwinkel wandern die Leerstellen in die entgegengesetzte Richtung, wenn Teilchen (A) von Leerstelle (1) nach (2) springt und Teilchen (B) ihm folgt.
- Da Leerstellen thermisch bedingt sind (ihre Anzahl steigt exponentiell zur Temperatur), ist dieser Mechanismus stark Temperatur abhängig.
- Nicht nur wurde dieser Mechanismus mit dem Kirkendall-Effekt experimentell nachgewiesen, mit seinen Experimenten begründete Dr. Ernest Kirkendall überhaupt die Vorstellung von Leerstellen im Kristallgitter.
- Zwischengitterplatz-Diffusion
- Der Weg kleinerer Atome (z.B. Wasserstoff, Kohlenstoff, Stickstoff) führt über freie Zwischengitterplätze des Kristallgitters. Geschwindigkeit und Reichweite dieser Diffusionsart liegen um Größenordnungen über der Leerstellen-Diffusion, ist aber auf kleine Atomdurchmesser beschränkt.
- Der Diffusionskoeffizient ist von der Größe der wandernden Atome abhängig,
- sowie von der Größe der vorhandenen Zwischengitterplätze,
- und damit von Temperatur und Kristallsystem des Materials
- Platzwechsel- und Ringtausch
- Dieser Mechanismus ist hypothetisch und experimentell nicht nachgewiesen. Jedoch deuten einige Fakten auf seine Existenz hin.
- Beim Platzwechsel „tauschen“ zwei Atome ihre Plätze
- Beim Ringtausch wechselt eine ringförmige Gruppe von Atomen ihre Plätze reihum.
Dafür ist eine hohe Beweglichkeit der Teilchen (= sehr hohe Temperatur), sowie ein großer Freiraum für die Bewegung nötig (zu finden im störungsreichem Bereich der Krongrenzen). Naturgemäß kann dieser Mechanismus keine große Reichweite haben, er mag aber großen Einfluss beim Stoffübergang zwischen zwei Phasen haben.
- Pfade bevorzugter Diffusion
- Bisher sind wir von einem ungestörten Gitter mit konstanter Aktivierungsenergie für den Platzwechsel ausgegangen. Diese Energie enthält nicht nur die nötige Kraft um die Atome in Bewegung zu versetzen, schließlich muss gleichzeitig auch eine neue Leerstelle gebildet werden. Auf diese Energiebilanz haben Gitterstörungen wie Versetzungen, Korngrenzen und Phasengrenzflächen einen erheblichen Einfluss. Diese Störungen stellen also Pfade bevorzugter Diffusion dar. Hier ist die Aktivierungsenergie für den Platzwechsel um den Faktor 2 bis 4 niedriger als im ungestörten Gitter. Mit sinkender Temperatur nimmt die Differenz sogar noch zu.
Der Kirkendall-Effekt
[Bearbeiten]1942 führte der Chemiker und Metallurg Ernest Kirkendall Experimente durch, bei denen er Proben aus Kupfer und Messing (bekanntlich eine Kupfer-Zink-Legierung) bei etwa 780°C glühte. Er stellte fest, dass sich die Grenzfläche zwischen den Probenteilen nach dem Glühen verschoben hat. Die Veröffentlichung dieses Ergebnisses löste in der Fachwelt eine heftige Diskussion um die Mechanismen der Diffusion aus.
Bis zu diesem Zeitpunkt wurde die Existenz von Leerstellen im Kristallgitter kaum in Betracht gezogen. Lediglich Walter Schottky und wenige andere postulierten diese. Für die Mechanismen der Diffusion galten Platzwechsel- und Ringtausch als am wahrscheinlichsten – ohne die Existenz von Leerstellen erforderte diese aber gleiche Diffusionskoeffizienten der unterschiedlichen Elemente. Der einzige zu jener Zeit diskutierte Mechanismus, der unterschiedlich Diffusionskoeffizienten zuließ, war der über Zwischengitterplätze. Dieser ist jedoch nur auf kleinere Atome anwendbar und nicht für in etwa gleich große Atome wie Kupfer und Zink.
1947 setzten daher Kirkendall und seine Mitarbeiterin Alice Smigelskas die Arbeit fort, um zu belegen, dass Zink tatsächlich schneller diffundieren würde als Kupfer.

- Dazu umhüllten sie eine Probe aus Messing auf elektrolytischem Wege mit Kupfer.
- Vor dem Verkupfern wurden Molybdändrähte am Messingblock befestigt, so dass diese später die Grenzfläche zwischen den Probenteilen kennzeichneten.
- Die Probe wurde mit Unterbrechungen über mehrere Tage bei 785°C geglüht.
- Während der Pausen wurde jeweils ein Längsschnitt der Probe hergestellt.
- Bei der Auswertung zeigte sich, dass die Molybdändrähte nach außen „gewandert“ sind, der Messingkern ist also geschrumpft.
- Die Volumenänderung der Probenteile konnte nur als Ausgleichsreaktion für eine schnellere Diffusionsrate des Zinks gedeutet werden.

In den folgenden Jahren führten zahlreiche Wissenschaftler Experimente zur Bestätigung des Kirkendall-Effekts in weiteren Metallsystemen durch. Dabei wurden weitere Phänomene entdeckt, die im Zusammenhang mit dem Kirkendall-Effekt stehen:
- Der verlängerte Teil der Proben wies eine Querdehnung auf.
- Im verkürzte Teil fand eine Einschnürung statt.
- Außerdem zeigte sich im reduzierten Volumen nahe der Grenzfläche ein Porensaum. Diese Poren werden Kirkendall-Löcher genannt.
Insbesondere aus letzterem lässt sich schließen, dass während der Diffusion das schnellere Zink in die Leerstellen des (reinen) Kupferblocks gewandert ist. Dabei wurde nicht nur das (äußere) Volumen des Messings reduziert, auch seine Leerstellenkonzentration hat sich erhöht. Im weiteren Verlauf haben sich die Leerstellen dann zu Poren vereint.
Der Kirkendall-Effekt gilt damit als Nachweis der Existenz von Leerstellen mit Kristallgitter.
Quellen
[Bearbeiten]- ↑ E. L. Cussler: Diffusion - Mass Transfer in Fluid Systems. Cambridge University Press, Cambridge, New York, 1997, ISBN 0-521-56477-8
- ↑ W. Jost: Diffusion in solids, liquids and gases. Academic Press Inc., New York, 1960













