Biochemie und Pathobiochemie: Arachidonsäure-Stoffwechsel
Allgemeines
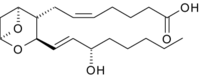
[Bearbeiten]Die 4fach ungesättigte Fettsäure Arachidonsäure (5,8,11,14-Eicosatetraensäure) ist der Ausgangspunkt für die Biosynthese der sog. Eikosanoide, zu denen die Prostaglandine und Leukotriene gehören.
Prostaglandinbiosynthese
[Bearbeiten]Biosynthese von Prostaglandin G2 und H2
[Bearbeiten]| ⇓ | Subst. | ( ⇑ ) | Co. | Enzym | EC | EG | Erkr. | ||
|---|---|---|---|---|---|---|---|---|---|
|
|||||||||
| H2O
Monoacylphosphoglycerin |
Ca | Phospholipase A2 | 3.1.1.4 | Hyd | |||||
| 2 O2
|
Häm | Prostaglandin-Endoperoxid-Synthase (Cyclooxygenase-Aktivität) | 1.14.99.1 | Ox | |||||
| AH2
H2O, A |
Häm | Prostaglandin-Endoperoxid-Synthase (Peroxidase-Aktivität) | 1.14.99.1 | Ox | |||||
Aus PGH2 werden die anderen Prostaglandine gebildet. Durch Isomerisierung entsteht TxA2, PGI2 (Prostacyclin), PGD2 oder PGE2. Die Synthese von PGF2α und 11-epi-PGF2α erfordert zusätzlich noch eine Reduktion.
Biosynthese von Thromboxan A2
[Bearbeiten]| ⇓ | Subst. | ( ⇑ ) | Co. | Enzym | EC | EG | Erkr. |
|---|---|---|---|---|---|---|---|
| Häm-Thiolat | Thromboxan-A-Synthase (CYP5A1) | 5.3.99.5 | Iso | Ghosal haemato-diaphyseal dysplasia | |||
Biologische Wirkung: Thrombozytenaggregation, Vasokonstriktion. TxA2 wird v.a. von Thrombozyten gebildet (COX1).
Biosynthese von Prostacyclin (Prostaglandin I2)
[Bearbeiten]| ⇓ | Subst. | ( ⇑ ) | Co. | Enzym | EC | EG | Erkr. |
|---|---|---|---|---|---|---|---|
| Häm-Thiolat | Prostacyclin-Synthase | 5.3.99.4 | Iso | ||||
Biologische Wirkung: Vasodilatation, Hemmung der Plättchenaggregation. Prostacyclin ist der Gegenspieler des TxA2 und wird vom Endothel gebildet (COX2).
Biosynthese von Prostaglandin D2
[Bearbeiten]| ⇓ | Subst. | ( ⇑ ) | Co. | Enzym | EC | EG | Erkr. |
|---|---|---|---|---|---|---|---|
| Glutathion | PGD-Synthase | 5.3.99.2 | Iso | ||||
| NADPH/H+ | PGF-Synthase | 1.1.1.188 | Ox | ||||
Biologische Wirkung: PGD2 fungiert im ZNS als Neuromodulator und trophischer Faktor, beeinflusst den Tonus der glatten Muskulatur und hemmt die Plättchenaggregation. Weiterhin ist es evtl. in den Ablauf des Non-REM-Schlafs involviert.
Biosynthese von Prostaglandin E2 und F2α
[Bearbeiten]| ⇓ | Subst. | ( ⇑ ) | Co. | Enzym | EC | EG | Erkr. |
|---|---|---|---|---|---|---|---|
| Glutathion | PGE-Synthase | 5.3.99.3 | Iso | ||||
| NADPH/H+ | Carbonyl-Reduktase (NADPH) | 1.1.1.184 | Ox | ||||
| PGE2- 9-Reduktase | 1.1.1.189 | ||||||
Biologische Wirkung:
- PGE2 wird durch den Entzündungsmediator Interleukin-1β (IL1β) und das Tumorsuppressorprotein TP53 induziert. Es ist u.a. beteiligt am Entzündungsschmerz. PGE2 ist weiterhin für die Erzeugung von Fieber verantwortlich: Bakterienbestandteile und IL-1 stimulieren das Epithel des Organum vasculosum laminae terminalis (OVLT) -> Expression von COX-2↑ -> PGE2-Synthese↑ -> Stimulation des Temperaturregulationszentrums im Nucleus preopticus medianus des Hypothalamus über EP3-Rezeptoren -> Erhöhung des Temperatur-Sollwertes und Aktivierung der Wärmeproduktion (Kältegefühl, Muskelzittern, erhöhte Stoffwechselaktivität). Im Magen wirkt PGE2 schleimhautprotektiv und hemmt die Bildung der Magensäure. Am Uterus führt es zu Kontraktionen.
- PGF2α wirkt luteolytisch und ist an der Regulation des Augeninnendrucks beteiligt und an der Uteruskontraktion.
Leukotrienbiosynthese
[Bearbeiten]Biosynthese der Leukotriene A4 und B4
[Bearbeiten]| ⇓ | Subst. | ( ⇑ ) | Co. | Enzym | EC | EG | Erkr. | |||
|---|---|---|---|---|---|---|---|---|---|---|
|
||||||||||
| H2O
Monoacylphosphoglycerin |
Ca | Phospholipase A2 | 3.1.1.4 | Hyd | ||||||
| O2
|
Fe | Arachidonat-5-Lipoxygenase | 1.13.11.34 | Ox | ||||||
|
||||||||||
|
|
Fe | Arachidonat-5-Lipoxygenase | 1.13.11.34 | Ox | ||||||
| H2O
|
Zn | LTA4-Hydrolase | 3.3.2.6 | Hyd | ||||||
Biologische Wirkung: LTB4-Rezeptoren finden sich v.a. im lymphatischen Gewebe und weisen auf eine immunmodulatorische Rolle hin.
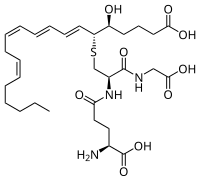
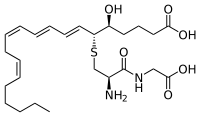
Biosynthese der Leukotriene C4, D4 und E4 aus Leukotrien A4
[Bearbeiten]| ⇓ | Subst. | ( ⇑ ) | Co. | Enzym | EC | EG | Erkr. |
|---|---|---|---|---|---|---|---|
| Glutathion
|
LTC4-Synthase | 4.4.1.20 | Ly | LTC4-Synthase-Def. | |||
| Aminosäure
γ-Glutamyl-Aminosäure |
γ-Glutamyltransferase | 2.3.2.2 | Tr | Glutathionurie | |||
| H2O | Dipeptidase 2 | 3.4.13.19 | Hy | ||||
 |
Biologische Wirkung: Leukotriene wirken stark proinflammatorisch. Die Leukotriene C4, D4 und E4 wirken konstriktorisch an der glatten Muskulatur, z.B. an der Bronchialmuskulatur und an den Hautgefäßen.
Allgemeines zu den Eikosanoiden
[Bearbeiten]Prostaglandine und Leukotriene sind wichtige Mediatoren im lokalen Gewebsstoffwechsel und vermitteln u.a. Entzündungsvorgänge. Sie werden aus der 4fach ungesättigten Fettsäure Arachidonsäure (5,8,11,14-Eicosatetraensäure) gebildet, die durch die Phospholipase A2 von Phospholipiden der Zellmembran, z.B. dem Phosphatidylcholin (Lecithin), abgespalten wird. Arachidonsäure ist essentiell bzw. kann begrenzt aus der essentiellen ω-6-Fettsäure Linolsäure gebildet werden.
Pharmakologie
[Bearbeiten]Mit Cyclooxygenase-Hemmern wie Acetylsalicylsäure (ASS) lässt sich die Prostaglandinsynthese unterbinden, was die schmerzlindernde, entzündungshemmende und fiebersenkende Wirkung erklärt. ASS hemmt v.a. das Isoenzym COX1 in den Thrombozyten durch irreversible Acetylierung, die das thrombogene TxA2 bildet. Die Wirkung auf die COX2, die im Endothel v.a. das antithrombogene Prostacyclin (PGI2) produziert, ist geringer. Zudem kann das Endothel das Enzym rasch regenerieren, was den kernlosen Thrombozyten nicht möglich ist. Das Gleichgewicht zwischen TxA2 und PGI2 wird dadurch zum antithrombogenen PGI2 hin verschoben und prädestiniert ASS als Medikament zur Prophylaxe von akuten Gefässverschlüssen, die durch Aufbrechen und Thrombosierung von Atheroskleroseplaques entstehen. Eine häufige Anwendung ist z.B. die Rezidivprophylaxe nach einem Herzinfarkt. Kortikosteroide wie Cortison hemmen die Kaskade an einem früheren Punkt (Hemmung der Phospholipase A2 durch Lipocortin, das von Kortikoiden induziert wird) und unterbrechen damit sowohl die Prostaglandin- als auch die Leukotrien-Biosynthese. Dies - und die Wirkung an vielen anderen Schalthebeln im Organismus - erklärt ihren stärkeren antientzündlichen und immunsuppressiven Effekt. Der Leukotrien D4-Rezeptor-Antagonist Montelukast wird bei Asthma bronchiale angewendet. Das Prostazyklin-Analogon Iloprost findet bei der pulmonalen Hypertonie eine Anwendung. Das vasoaktive Prostaglandin E1 (Alprostadil, Prostavasin) ist parenteral bei schwerer AVK und bei erektiler Dysfunktion verwendbar. Das Prostaglandin E1-Analogon Gemeprost wird vaginal angewendet zur Zervixerweiterung und Förderung der Uteruskontration. Ein weiteres PGE1-Analogon ist das Misoprostol, das früher als Magenschleimhautschutz eingesetzt wurde.
Toxikologie
[Bearbeiten]Die Phospholipase A2 ist ein wirksamer Bestandteil verschiedener Tiergifte und z.B. - neben weiteren Toxinen - im Gift der indischen Kobra (Naja naja) enthalten.
Weblinks
[Bearbeiten]
| Allgemeine Hintergrundfarbe für Substrate | Hintergrundfarbe Reaktionspfeile | „Schlüsselenzyme“ | |
| Energiereiche Phosphate Reduktionsäquivalente | CO2 / HCO3− C1-Reste Stickstoff |
Abk.: Tr.: Transkriptionelle Regulation, Tl.: Regulation der Translation, Lok.: Regulation über die Enzymlokalisation, Kov.: Regulation durch kovalente Modifikation, All.: Allosterische Regulation, Koop.: Kooperativer Effekt, Co.: Cofaktoren, EC: Enzymklassifikation, EG: Enzymgruppe (Oxidoreductase, Transferase, Hydrolase, Lyase, Isomerase, Ligase), Erkr.: Assoziierte Erkrankungen.
Haben Ihnen die Informationen in diesem Kapitel nicht weitergeholfen?
Dann hinterlassen Sie doch einfach eine Mitteilung auf der Diskussionsseite und helfen Sie somit das Buch zu verbessern.