Biochemie und Pathobiochemie: Häm
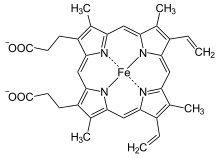
| Häm B | ||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|
 | ||||||||||||
| Steckbrief | ||||||||||||
|
Häm ist als Bestandteil des Hämoglobins für die Sauerstoff-Bindung und die rote Farbe des Blutes verantwortlich. Daneben erfüllt es als Bestandteil zahlreicher Enzyme viele weitere Funktionen bei Redox-Vorgängen (Elektronenübertragungen) im Körper.
Stoffwechselwege
[Bearbeiten]Eigenschaften und Vorkommen
[Bearbeiten]Aufgrund des zentralen Eisenatoms und der konjugierten Doppelbindungen Stabilisierung des oxidierten (Fe3+) und des reduzierten (Fe2+) Zustandes. Gute Sauerstoff-Bindung, Partner von Redoxvorgängen. Im Körper Einbau u.a. in folgende Proteine:
- Hämoglobin
- Myoglobin
- NAD(P)H-Oxidase - ROS-Bildung
- Katalase - siehe unter Atmungskette
- Succinat-Dehydrogenase - Atmungskette (Komplex II)/Citratzyklus
- Cytochrom-c-Reduktase - Atmungskette (Komplex III)
- Cytochrom c - Atmungskette
- Cytochrom-c-Oxidase - Atmungskette (Komplex IV)
- Cytochrom-c-Peroxidase
- Cyclooxygenase (COX) - Arachidonsäure-Stoffwechsel (Hinweis: Eisen bzw. Häm wird weder bei KEGG noch bei EC->PDB als Cofaktor genannt, aber z.B. bei PDB.)
- Lactoperoxidase - Phenylalanin-Abbau
- Thyreoperoxidase - Schilddrüsenhormon-Synthese
- Aldehyd-Oxidase - Serotoninabbauweg
- Tryptophan-2,3-Dioxygenase - Tryptophan-Abbau
- Indolamin-2,3-Dioxygenase - Tryptophan-Abbau
- Sulfit-Oxidase - Schwefel-Stoffwechsel
In Form von Häm-Thiolat findet man das Häm als Cofaktor der Cytochrom P450-Proteine (CYP), die für die Biotransformation Phase I verantwortlich sind. Dazu gehören folgende Enzyme:
- Thromboxan-A-Synthase (CYP5A) - Biosynthese von TXA2
- Unspezifische Monooxygenase (CYP1A1, CYP1A2, CYP1B1, CYP2A, CYP2B, CYP2C, CYP2D, CYP2E, CYP2F, CYP2J, CYP2S, CYP3A, CYP4B, CYP4X, CYP4Z, CYP19A) - Steroidhormon-Stoffwechsel
- Prostacyclin-Synthase (CYP8A) - Biosynthese von Prostacyclin
- Sterol-14-Demethylase (CYP51A) - Cholesterin-Biosynthese
- Calcidiol-1-Monooxygenase (CYP27B) - Calcitriol-Bildung
- Cholesterol-7α-Monooxygenase (CYP7A1) - Gallensäuren-Biosynthese
- Cholestanetriol-26-Monooxygenase (CYP27A) - Gallensäuren-Biosynthese
- Cholesterol-Monooxygenase (20-22-Desmolase, CYP11A) - Steroidhormon-Stoffwechsel
- Steroid-11β-Monooxygenase (11β-Hydroxylase, CYP11B) - Steroidhormon-Stoffwechsel
- Corticosteron-18-Monooxygenase (18-Hydroxylase, CYP11B) - Steroidhormon-Stoffwechsel
- Steroid-17α-Monooxygenase (17α-Hydroxylase, CYP17A) - Steroidhormon-Stoffwechsel
- Steroid-21-Monooxygenase (21-Hydroxylase, CYP21A) - Steroidhormon-Stoffwechsel
Haben Ihnen die Informationen in diesem Kapitel nicht weitergeholfen?
Dann hinterlassen Sie doch einfach eine Mitteilung auf der Diskussionsseite und helfen Sie somit das Buch zu verbessern.
