Schilddrüse/ Druckversion
Hat mein Eisenmangel mit der Schilddrüse zu tun?
Vorwort
[Bearbeiten]Dieser Text soll eine Stoffsammlung für alle sein, die sich mit dem Thema Schilddrüse und Schilddrüsenkrankheiten beschäftigen wollen.
Die Bilder sind nicht immer ganz ernst gemeint. Sie sollen den Text auflockern.
Das Buch soll die schulmedizinisch, naturwissenschaftlich fundierte Medizin darstellen. Alternative Methoden bitte in einem anderen Buch einbringen.
Dieses Buch ist noch in Arbeit
Anregungen,Mitarbeit und Verbesserungen sind jederzeit erwünscht
Ich wünsche allen viel Spaß bei der Weiterentwicklung diese Buches! Einiges stammt von meiner alten Homepage und ist public domain. Vieles wurde aus Wikipedia übernommen und etwas lesbarer gemacht.
R.Ho im Januar 2005 Benutzer:Rho moin
Einleitung
[Bearbeiten]Die Schilddrüse ist das Gaspedal unseres Körpers

Allgemeines
[Bearbeiten]Die Schilddrüse (auch Thyreoidea oder Glandula thyroidea genannt) ist die größte Hormondrüse im menschlichen Körper.
Ihre wichtigsten Aufgaben sind:
- Produktion der Schilddrüsenhormone T3 und T4
- Produktion des Calcitonins
- Speicherung von Schilddrüsenhormonen
Die Schilddrüse kommt auch bei allen anderen Säugetieren und Vögeln vor.
Sie befindet sich am Hals unterhalb des Kehlkopfes vor der Luftröhre und hat die Form eines Schmetterlings.
Der Name leitet sich von der schildartigen Form der Drüse vor der Luftröhre ab.
Funktion
[Bearbeiten]Eine gesunde Schilddrüse ist Voraussetzung für die normale Funktion des ganzen menschlichen Körpers. Ohne Schilddrüsenhormone kann man nicht leben. Die Schilddrüsenhormone haben Einfluss auf viele Stoffwechselvorgänge wie beispielsweise
- Körperwachstum - Körpergewicht
- Haut und Haare
- Muskulatur
- Nervensystem und Psyche
- Hormonsystem
Diagnostik
[Bearbeiten]Die Untersuchungsmethoden der Schilddrüse sind mittlerweile sehr gut geworden. Meist kann man mit geringem Aufwand erkennen, ob und welche Behandlung der Schilddrüse notwendig ist.
Die wichtigsten Methoden zu Untersuchung der Schilddrüse sind
- die Befragung und die körperliche Untersuchung des Patienten
- die Laborwerte aus dem Blut,
- der Ultraschall und
- das Szintigramm.
Seltener angewendet werden die Zytologie, die Biopsie, die Kernspinuntersuchung, das CT und andere Untersuchungsverfahren.
Krankheiten
[Bearbeiten]Jeder dritte Bundesbürger lebt mit krankhaften Veränderungen der Schilddrüse. Schilddrüsenerkrankungen treten gehäuft im Alter auf. Sie können aber auch schon im Kindes- und Jugendalter vorkommen. Vor allem Frauen haben mit einer Häufigkeit von circa 3:1 gegenüber Männern vermehrt Schilddrüsenkrankheiten.
Ein Teil der Krankheiten beruht immer noch auf dem Jodmangel, denn Deutschland ist ein Jod-Mangel-Gebiet. Der andere Teil ist aber durch Entzündungen oder Knoten bedingt, die nicht auf den Jodmangel zurückführbar sind.
Die häufigsten Krankheiten der Schilddrüse sind:
- Jodmangelstruma = Kropf
- ohne Knoten, diffus
- mit Knoten
- Schilddrüsenknoten
- Überfunktion der Schilddrüse
- Morbus Basedow
- Autonome Adenome
- Entzündungen der Schilddrüse
- Unterfunktion der Schilddrüse
- Schilddrüsenkrebs
Daneben gibt es einige seltene Schilddrüsenkrankheiten.
Behandlungsmethoden
[Bearbeiten]Einige Schildrüsenkrankheiten brauchen keine Behandlung, sondern nur regelmässige Kontrolluntersuchungen. Die wichtigsten Behandlungsmethoden bei Schilddrüsenerkrankungen sind:
- Die Tablettenbehandlung
- Jod zur Kropfvorbeugung
- Schilddrüsenhormon bei einer Unterfunktion
- Schilddrüsenhemmer bei einer Überfunktion
- Die lokale Behandlung von heißen Schilddrüsenknoten
- mit Ultraschallstosswellen oder Alkoholinjektion in den Knoten
- wird selten durchgeführt, da die Expertise oder Ausrüstung fehlt.
- Die Radiojodbehandlung
- zur Behandlung einer Überfunktion sowie zur Volumenreduktion
- Die Operation der Schilddrüse
- bei tumorverdächtigen Knoten, bei heißen Knoten, bei sehr großen Strumen
Schilddrüsenmedikamente
[Bearbeiten]Die wichtigsten Schilddrüsenmedikamente sind
- Jodsalz
- Jodtabletten
- Thyroxin (T4) (auch in Kombination mit Jod möglich)
Medikamente bei Schilddrüsenüberfunktion
- Betablocker (Propanolol, Bisoprolol, Metoprolol, ....)
- Thiamazol
- sollte in Rücksprache mit dem behandelnden Arzt
- nicht länger als ein Jahr und
- in angepasster Dosis ingenommen werden,
- da sonst ein Schilddrüsenwachstum begünstigt werden kann)
- veraltet Carbimazol
- sollte in Rücksprache mit dem behandelnden Arzt
- Propylthiouracil
- Perchlorat = Irenat
Medikamente bei Schilddrüsenunterfunktion
- L-Thyroxin (T4) in angepasster und kontrollierter Dosis
- selten T3
Fragen zur Schilddrüse
[Bearbeiten]
Fragen zum Thema Schilddrüse
Hier können Sie Ihre Fragen zum Thema Schilddrüse eingeben:
Mononukleose und Hashimoto Thyreoditis
[Bearbeiten]- Gibt es einen Zusammenhang zwischen der Mononukleose und der Hashimoto Thyreoditis ?
Erhöhter TSH Wert , Was tun ?
[Bearbeiten]Bei mir wurde ein erhöhter TSH-Wert und damit eine Schilddrüsenunterfunktion festgestellt. Die autoimmune Form konnte jedoch anhand der anderen Blutwerte und des Ultraschallbefundes ausgeschlossen werden. Mein Internist hat mir Jodtabletten verschrieben. Reicht das oder muss ich Thyroxin einnehmen?
Antwort: Zur Beantwortung dieser Frage braucht man alle Ihre Schilddrüsenwerte :
TSH wie hoch ? T3 erniedrigt ? T4 erniedrigt ?
Außerdem sollte ein guter Schilddrüsen Ultraschall gemacht werden, mit der Fragestellung, ob eine zu kleine oder zu grosse Schilddrüse vorliegt und ob eine Schilddrüsenentzündung erkennbar ist .
Gibt es gute websites/Informationen über Schilddrüsenkrebs bei Tieren?
[Bearbeiten]Antwort: Recherchieren Sie doch selbst einmal und geben Sie ihre Antwort und gefundenen Links hier ein. Siehe zb http://www.wer-weiss-was.de/tiere/wer-kann-mir-etwas-naeheres-zu-schilddruesenkrebs-be
Welche Funktion hat der N.Laryngeus recurrens ?
[Bearbeiten]Antwort
[Bearbeiten]
Der Nerv versorgt die Stimmbänder. Wenn er geschädigt wird, dann bekommt man eine Stimmbandlähmung. Es resultiert eine Heiserkeit, manchmal auch eine Atemnot. Da der Nerv sehr eng hinter der Schilddrüse verläuft und sehr klein und schlecht zu sehen ist, kann er bei einer Schilddrüsenoperation verletzt werden.
Physiologie
[Bearbeiten]- Gibt es eine circadiane Rhythmik des freien SD-Hormon spiegels T3 oder T4 wie beim Cortison?
Hormonersatz bei der Unterfunktion
[Bearbeiten]- Kann man die Schilddrüsentabletten (Thyroxin) auch am Abend zum Schlafen einnehmen?
- Die Tageszeit der Einnahme ist beliebig, da Thyroxin mit einer Halbwertszeit von 8 Tagen eher als Depot für die Bildung von T3 fungiert. Wichtig ist, dass die Einnahme mindestens 30 Minuten vor bzw. 5 h nach einer Mahlzeit erfolgt, da die Nahrung im Magen eine verminderte Aufnahme des Thyroxin bewirkt. Es sind auch die Wechselwirkungen mit evtl. zum gleichen Zeitpunkt zu nehmenden Medikamenten zu beachten.
ACHTUNG: Dies gilt nur für die Einnahme von Thyroxin, also T4! Bei der Medikation mit T3 oder Kombinationspräparaten T4 / T3 ist durch die schnelle Bioverfügbarkeit des T3-Hormons und dem damit schnell eintretenden Wirkungseintritt eine Einnahme nach dem Aufwachen sinnvoll.
Abnehmen ohne Schilddrüse?
[Bearbeiten]Kann man ohne Schilddrüse abnehmen?
Antwort
[Bearbeiten]Wieso nicht? Man muss nur einen ausreichenden Hormonersatz durchführen. Das muss man aber sowieso, ob man abnehmen will oder nicht. Ohne Schilddrüse kann man nicht leben.
Autonomes Adenom
[Bearbeiten]Mit großem Interesse habe ich den Bericht über die percutane AlkoholInjektion gelesen. Vor etwa 14 Jahren entdeckte man in meinem linken Schilddrüsenlappen eine Zyste. Um die Zyste wuchs in den Jahren ein autonomes Adenom bis auf ca. 4 cm unter ärztlicher Aufsicht an. Die Zyste ist noch die Basis dieses autonomen Adenoms (wurde vor kurzem punktiert). Nun ist der Nuklearmediziner der Meinung, dass man für meine Schilddrüse nichts mehr hormonell tun könne und gab die Indikation zur Operation. Mein Adenom prodoziert mal Hormone und mal nicht. Bislang hatte ich L-Tyroxin eingenommen. Mal habe ich eine Überfunktion und mal eine Unterfunktion. In zwei Kliniken habe ich mich über Risiken und Nutzen der Operation aufklären lassen und bin zum Entschluss gekommen, dass ich mich nicht operieren lassen möchte. Das Risiko der Stimmbandschädigung und sei es auch nur eine vorübergehende Hemiparese würde für mich das berufliche AUS bedeuten und habe auch derzeit nicht die Zeit mich ins Krankenhaus zu legen. Käme für mich die percutane Alkohol Injektion in Frage? Wohin könnte ich mich wenden?
Antwort: Die einfachste Behandlung des Schilddrüsenüberfunktion ist immer noch die Therapie mit Thiamazol. Diese funktioniert auch bei einem oder mehreren autonomem Knoten ganz gut.
Eine Alkoholbehandlung ist vor allem bei einem einzelnen Knoten eine gute Behandlung. Man braucht dazu einen erfahrenen Ultraschalldoktor, der auch gezielte Punktionen vornehmen kann. Wer das in Göttingen kann, weiß ich leider nicht. Auch vor einer Operation braucht man nicht so viel Angst haben, wenn man sich einen Operateur mit mehr als 30 Schilddrüsenoperationen / Jahr heraussucht und mit ihm schriftlich vereinbart, dass er nur den autonomen Knoten > entfernt und die restliche Schilddrüse belässt. Dann ist die Gefahr einer Verletzung der Nervus recurrens oder eine Entfernung der Nebenschilddrüsen sehr gering. Nicht ganz klar, ist mir Ihre bisherige Thyroxinbehandlung. Sie scheint mir unnötig und kontraindiziert.
Hashimotothyreoditis
[Bearbeiten]Welchen Einfluss hat die niedrigdosierte Gabe von T4 ( zB Thyroxin 50 mikrog / Tag ) auf den Verlauf einer beginnenden Hashimotoerkrankung ?
[Bearbeiten]Nicht selten gibt es Patienten mit einer initialen Hashimotoerkrankung. Die AK sind hoch, TSH ist leicht erhöht, T3 und T4 sind aber noch normal. Was soll man tun ? Kann bei so einer Konstellation extern zugeführtes T4 das Fortschreiten zu einer Unterfunktion verzögern oder beschleunigen ?
Hat die Jodversorgung etwas mit der Thyreoiditishäufigkeit insbesondere mit der Häufigkeit der Hashimotothyreoiditis zu tun?
[Bearbeiten]- Gängige Medizinische Lehrmeinung: Die Autoimmunerkrankungen (Basedow und Hashimoto Thyreoiditis) der Schilddrüse haben nichts oder sehr wenig mit der Jodversorgung zu tun. Dazu gibt es eine lange medizinische Diskussion über Jahrzehnte. Die Länder mit Trinkwasserjodierung und einer einigermaßen brauchbaren Häufigkeitsstatistik der Schilddrüsenkrankheiten zeigen, dass es keinen echten Anstieg der Krankheitszahlen nach Einführung der Jodierung gegeben hat. Der Entstehungsmechanismus ist weitgehend unabhängig vom Jod Benutzer:Rho
- Literatur dazu:
- Lit 1: :
- Thyroid. 2003 Feb;13(2):199-203.
- Introduction of iodized salt to severely iodine-deficient children does not provoke thyroid autoimmunity: a one-year prospective trial in northern Morocco.
- Zimmermann MB, Moretti D, Chaouki N, Torresani T.
- The Human Nutrition Laboratory, Swiss Federal Institute of Technology, Zurich, Switzerland. michael.zimmerman@ilw.agrl.ethz.ch
- lit2
- J Clin Endocrinol Metab. 1999 Feb;84(2):561-6.
- The spectrum of thyroid disorders in an iodine-deficient community: the Pescopagano survey.
- Aghini-Lombardi F, Antonangeli L, Martino E, Vitti P, Maccherini D, Leoli F, Rago T, Grasso L, Valeriano R, Balestrieri A, Pinchera A.
- Department of Endocrinology, University of Pisa, Italy.
- Literatur dazu:
- Andere Meinung: Das kann man nicht so apodiktisch sagen. Die Iodversorgung beeinflusst die Häufigkeit von Hashimoto- und Basedow-Erkrankungen nur nicht linear. Vermutlich werden Thyreoiditiden bei zu hoher Iodeinnahme (> 500 ug/d) verursacht. Einige Einzelstudien: siehe lit1 [2] [3] Ausführliche Darstellung: [4]. --w:Benutzer:MBq Disk Bew 17:14, 1. Sep 2006 (CEST)
- lit1:
- N Engl J Med. 2006 Jun 29;354(26):2783-93.
- Comment in: N Engl J Med. 2006 Jun 29;354(26):2819-21.
- Effect of iodine intake on thyroid diseases in China.
- Teng W, Shan Z, Teng X, Guan H, Li Y, Teng D, Jin Y, Yu X, Fan C, Chong W, Yang F, Dai H, Yu Y, Li J, Chen Y, Zhao D, Shi X, Hu F, Mao J, Gu X, Yang R, Tong Y, Wang W, Gao T, Li C.
- Department of Endocrinology
- lit2
- Thyroid. 2003 May;13(5):485-9.
- Comment in: Thyroid. 2003 Dec;13(12):1187; author reply 1188.
- High prevalence of autoimmune thyroiditis in schoolchildren after elimination of iodine deficiency in northwestern Greece.
- Zois C, Stavrou I, Kalogera C, Svarna E, Dimoliatis I, Seferiadis K, Tsatsoulis A. Division of Endocrinology, Department of Medicine, University of Ioannina, Greece.
- lit3
- J Endocrinol Invest. 2003;26(2 Suppl):43-8. Links
- Improvement of iodine deficiency after iodine supplementation in schoolchildren of Azerbaijan was accompanied by hypo and hyperthyrotropinemia and increased title of thyroid autoantibodies.
- Markou KB, Georgopoulos NA, Makri M, Vlasopoulou B, Anastasiou E, Vagenakis GA, Kouloubi K, Theodosopoulos N, Lazarou N, Veizis A, Sakellaropoulos G, Vagenakis AG.
- Department of Medicine, Division of Endocrinology, University of Patras Medical School, University Hospital, Patras, Greece.
- lit4
- lit1:
- Kommentar zur Dosis: Ein Jodeinnahme von > 500 mikrog/ Tag ist viel zu viel und unnötig . Standarddosis sind 100 - 200 mikrog/ Tag in der Kropfvorbeugung Benutzer:Rho
Als Umweltfaktor ist im Wesentlichen die Iodversorgung zu nennen: umso höher die tägliche Iodaufnahme ist, umso häufiger entwickelt sich eine Hashimoto-Thyreoiditis bei erblicher Veranlagung. Stimmt diese Aussage ?
[Bearbeiten]Diese Aussage findet sich auf der Internetseite von Prof. Dr. Karl-Michael Derwahl. Wie ist diese Aussage belegt ?
Wie müsste eine Untersuchung ausschauen die den Zusammenhang zwischen Jodierung und Autoimmunerkrankungen der SD klärt?
[Bearbeiten]Man müsste 1000 Patienten mit einer Struma diffusa, die man mit Jod behandeln möchte randomisieren. Eine Hälfte erhält Plazebo, die andere erhält Jodid. Dann schaut man nach ein oder 2 Jahren nach, ob in der behandelten Gruppe die Zahl des Hashimoto- oder des Basedowfälle angestiegen ist. So eine saubere Arbeit existiert wohl bislang nicht. Interessant sind auch Beobachtungen aus Ländern, in den einen generelle Jodierung eingeführt wurde (Schweden, Schweiz etc). Kam es zum Zeitpunkt der Jodierung zu vermehrten Autoimmunerkrankungen?
Eine recht gute Literaturstelle zum Thema ist folgende:
- Th. Rink, H.-J. Schroth, L.-H. Holle, H. Garth:
- Effekte von Jodid und Schilddrüsenhormonen bei der Induktion und Therapie einer Thyreoiditis Hashimoto.
- Nuklearmedizin 1999; 38:144-9
- Effekte von Jodid und Schilddrüsenhormonen bei der Induktion und Therapie einer Thyreoiditis Hashimoto.
Keine Lust mehr Tabletten einzunehmen
[Bearbeiten]Was passiert, wenn ein Patient, der an einer hochgradigen Schilddrüsenüberfunktion gelitten hat (Basedow bekannt), dessen Schilddrüse auch schon radioaktiv zerstört wurde, seine verordneten Schilddrüsen-Tabletten nicht einnimmt?
Antwort: Er bekommt wahrscheinlich innerhalb einiger Wochen eine Schilddrüsenunterfunktion. Das sollte man vermeiden und deswegen sollte er die Tabletten brav weiter einnehmen. Manchmal passiert auch gar nichts, wenn eine ausreichende Restfunktion der eigenen Schilddrüse vorhanden ist.
SD und Gedächtnis
[Bearbeiten]Gibt es einen Zusammenhang zwischen der Gedächtnisleistung und der Funktion der Schilddrüse?
Bereits bei der Hirnreifung im Kindesalter sind die Schilddrüsenhormone beteiligt. Auch eine Schilddrüsenunterfunktion wirkt sich negativ auf das Gedächtnis aus. Auch eine Überfunktion beeinträchtigt das Gehirn meist im negativen Sinne.
SD und Uran
[Bearbeiten]Was hat das Uran mit der Schilddrüse zu tun. Einige Soldaten die im Balkankrieg im Einsatz waren und mit Uranmunition in Kontakt kamen müssen sich Schilddrüsen Untersuchungen unterziehen. warum? was hat die Schilddrüse mit dem Uran zu tun?
Hashimoto und Nebenschilddrüse
[Bearbeiten]Ist von der Hashimoto-Erkrankung auch die Nebenschilddrüse betroffen? Falls ja, was tun?
Bei der Hashimotokrankheit ist die Nebenschilddrüse nicht betroffen. Es gibt allerdings Patienten die mehrere Autoimmunerkrankungen kombiniert haben. Dabei gibt es dann sicher auch den seltenen Fall einer Autoimmunerkrankung der Schilddrüse und der Nebenschilddrüse.
Den Ausfall der Nebenschilddrüse muss man mit der Gabe von AT 10 Dihydrotachysterol oder Rocaltrol behandeln. Zusätzlich wird die Calciumzufuhr erhöht.
Thyroxin zur Kropftherapie
[Bearbeiten]Frage
[Bearbeiten]Ich bin 19 Jahre alt und vor ca. 4 Jahren wurde bei mir eine leichte Kropfbildung festgestellt. Mir wurde daraufhin Jod verordnet. Vor ca. 3 Jahren hat die Kasse dieses dann nicht mehr bezahlt, sodass mein Arzt mir vorschlug, L-Thyroxin einzunehmen, was noch bezahlt wird. So nehme ich nun schon seit 3 Jahren täglich eine halbe L-Throxin 50 (also 25 µg). Meine Mutter hat nun gehört, dass dieses Medikament Gedächtnisstörungen verursachen kann. Ist das Medikament in meinem Fall überhaupt angebracht oder soll ich nicht lieber die "sanftere", (wenn auch teurere Variante), einer Jod-Ergänzung bevorzugen.
Antwort
[Bearbeiten]Das Verhalten Ihrer Krankenkasse ist kurzsichtig und aus medizinischer Sicht falsch.
Es reicht für Sie wahrscheinlich völlig aus, wenn Sie Jodtabletten einnehmen. Diese kosten nicht viel. Machen Sie doch einfach einen Probekauf bei der Apotheke. Sie brauchen kein Rezept.
Aber auch die Einnahme der geringen Menge Thyroxin, die ihr Arzt Ihnen verordnet hat, ist nicht verkehrt. Thyroxin in dieser Dosis bremst etwas die Kropfbildung, macht aber noch keine Überfunktion. Außerdem enthält das Molekül auch Jod. Nach dem Abbau wird das Jod vom Körper auch noch genutzt.
Nennen Sie doch bitte die Quelle, nach der Thyroxin Gedächtnisstörungen verursachen soll. Diese Quelle ist wahrscheinlich falsch. Außerdem sind die Nebenwirkungen des Thyroxins entscheidend von der Dosis abhängig. In der niedrigen Dosis die Sie einnehmen ist eine Überfunktion sehr unwahrscheinlich.
Wichtig ist für Ihre Frage auch die Höhe ihrer Schilddrüsenwerte im Blut.
Jod und Thyroxin kombiniert Wann sinnvoll?
[Bearbeiten]Wann ist die kombinierte Gabe von Jod und Thyroxin sinnvoll?
Die Kombination beider Stoffe ist eigentlich nur selten notwendig. Man kann es geben, wenn unter alleiniger Jodgabe ein Kropf ohne Knoten nicht ausreichend kleiner wird. Meist reicht die alleinige Jodgabe aus.
Bei einer Unterfunktion der Schilddrüse ist Thyroxin notwendig. Die zusätzliche Jodgabe bringt in der Regel nichts.
Offizielle Anwendungsempfehlung laut gelber Liste:
Euthyreote Struma ohne gleichz. Funktionsstör., wenn neben Schilddrüsenhormon eine zusätzl. Iodgabe angezeigt ist. Rezidivprophylaxe nach operierter od. m. Radioiodid behandelter Schilddrüse.
siehe Diskussion zu dieser Seite
Gesamt T3 , Gesamt T4
[Bearbeiten]Viele Labore bestimmen nur noch das Freie T3 und das Freie T4 und bieten Gesamt T3, T4 nicht mehr an. Gibt es dennoch eine Indikation für die Bestimmung von Gesamt T3,T4?
Sind erhöhte Schilddrüsenantikörper immer ein Zeichen einer Krankheit?
[Bearbeiten]Bei einer Blutuntersuchung wurden folgende Werte festgestellt:
- der tsh-wert ist normal.
- TAK 267 ( normal < 100 )
- TPO-AK über 600. ( normal < 80 )
Was kann man aus diesen Werten schlussfolgern?
Antwort:
[Bearbeiten]Vorhandene Antikörper gegen Thyreoglobulin (TGAK) und Thyreoperoxidase (TPO-AK) bedeuten noch nicht, dass eine Autoimmunerkrankung, die vorrangig die Schilddrüse betrifft, vorliegt.
Allerdings ist der Teil der Gesunden, die Antikörper aufweisen, sehr klein. Gelegentlich finden sich Antikörper auch bei anderen Schilddrüsenerkrankungen.
Die Wahrscheinlichkeit ist dennoch hoch, dass sich eine Autoimmunerkrankung (Hashimoto Thyreoiditis, Morbus Basedow) entwickeln kann. Besonders die Hashimoto Thyreoiditis kann auch seronegativ verlaufen. Es sind dann keine Antikörper bzw. keine erhöhten Antikörper nachweisbar.
Die Antikörper stellen eine Reaktion auf den Zerstörungsprozess der Schilddürse dar und sind selbst nicht pathogen.
Erhöhte, und wie im Beispiel deutlich erhöhte Antikörper, belegen dagegen eine Autoimmunerkrankung!
Die Schilddrüsenwerte selbst müssen in dem Zusammenhang jedoch nicht außerhalb der Norm liegen, Symptome können dennoch auftreten. In jedem Fall empfiehlt sich eine Sonographie.
Bei Morbus Basedow müssen zwingend die TRAK (TSH-Rezeptorantikörper) bestimmt werden. Diese sind als einzige der genannten Antikörper pathogen und wohl mitverantwortlich für die Entstehung einer endokrinen Orbitopathie.
Kann eine große Joddosis eine erloschene Schilddrüse reaktivieren?
[Bearbeiten]Vorgeschichte: Ich nahm täglich 100 Mikrogramm L-Thyroxin, wegen Hashimoto-Erkrankung. Dann, nach zweimaligem Herzkatheter mit Kontrastmittel, war der TSH-Wert nicht mehr messbar. Jetzt, neun Wochen später, benötige ich immer noch Carbimazol. Ich bin unsicher bezüglich der weiteren Vorgehensweise, zumal eine KHK besteht. Welche diagnostischen Maßnahmen wären empfehlenswert? CL, Bobingen
Antwort
[Bearbeiten]Die wichtigste Maßnahme in so einer etwas verworrenen Situation heißt:
Kurzfristige Kontrollen von TSH, T3 und T4 und dem entsprechende Anpassung der Therapie. (Kontrollen beispielsweise alle 2 Wochen). Die Therapieanpassung kann in Form einer Reduktion oder Erhöhung der Dosis von Carbimazol erfolgen. Falls sich langsam wieder eine Hypothyreose einstellt muss Carbimazol wieder komplett abgesetzt werden und die Thyroxinsubstitution muss wieder begonnen werden. Die Therapie sollte wegen des Herzens auch durch einen Betablocker zb Bisoprolol 2,5 oder 5 mg pro Tag ergänzt werden. Statt Carbimazol könnte man auch Thiamazol geben.
Die Erklärung für so einen Zustand ist nicht so einfach:
Offensichtlich war die Schilddrüse eben doch noch nicht völlig erloschen. Denn bei einer späten ausgebrannten Hashimotothyreoiditis findet sich eigentlich nur noch narbiges Restgewebe. Da wäre eine Reaktivierung eigentlich unerklärbar.
Es gibt Mischbilder der Hashimoto- und der Basedowerkrankung. Vielleicht liegt so etwas vor. Außerdem kann es im Verlauf der Hashimotoerkrankung vorübergehend auch zu einer Hyperthyreose kommen, allerdings meist am Anfang der Krankheit. Offensichtlich wurde durch die exszessive Jodgabe durch das Kontrastmittel die Entzündung der Schilddrüse noch einmal verstärkt. Eine letzte Möglichkeit besteht noch darin, dass sich zusätzlich zur Hashimotoerkrankung ein autonomes Adenom in der Schilddrüse befindet, welches durch die Jodgabe dekompensiert ist.
Alle Erklärungsversuche ändern aber zunächst einmal nichts am therapeutischen Vorgehen: Kurzfristige Kontrollen von TSH, T3 und T4 und dem entsprechende Anpassung der Therapie.
Vielleicht können Sie Ihre Befunde und den Verlauf weiter in diesem Buch dokumentieren. Das wäre recht interessant.
Weiterer Verlauf nach 7 Monaten
[Bearbeiten]Nach Gabe von Carbimazol 10 mg /d über ca. 2 Monate jetzt nach 7 Monaten wieder Normalwerte von TSH, T3, T4 und wieder Substitution von 50 mikrog L-Thyroxin / Tag
Wie erfolgt die Hormonversorgung mit Schilddrüsenhormonen bei angeborenere Hypothyreose vor der Geburt?
[Bearbeiten]Ist Jodmangel weltweit die häufigste vermeidbare Ursache für geistige Retardierung?
[Bearbeiten]Dies wird im Herold/Innere Medizin 2008 behauptet. Müsste es nicht vielmehr heißen: Die unbehandelte angeborene Hypothyreose ist weltweit die häufigste vermeidbare Ursache für geistige Retardierung. Der Jodmangel führt eigentlich nur in extremen Fällen zu einer Hypothyreose.
Quelle dazu:
Im Abstract sind allerdings auch keine echten Daten genannt.
Wachstumsdynamik heißer Knoten
[Bearbeiten]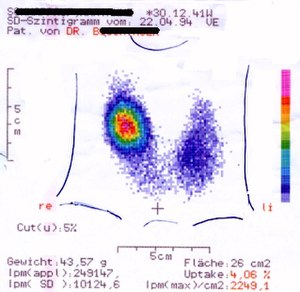
Gibt es heiße Knoten, die unkontrolliert aktiv sind und an Hand des TSH Spiegel noch nicht erkennbar sind ?
Die Frage ist für einen einzelnen heißen Knoten leicht zu beantworten: Es hängt einfach von der Größe und Aktivität des heißen Knotens ab.
Ist der Knoten noch sehr klein ( unter 1 cm ), dann sind die Blutwerte noch normal.
Wird der Knoten langsam größer, dann bremst er die restliche SD und der TSH Spiegel sinkt ab. Die T3 und T4 Werte sind zu diesem Zeitpunkt noch normal. Woher die Hypophyse weiß, dass der Knoten vorhanden ist und die TSH Produktion reduziert, das ist bis heute nicht klar. Wahrscheinlich sind die T3, T4 Spiegel über den ganzen Tag betrachtet, eben doch schon etwas zu hoch.
Wird der Knoten noch größer ( so etwa ab 2 - 3 cm ) , dann kann die Hypophyse Ihre Produktion nicht mehr weiter drosseln , die restliche SD ist fast stillgelegt und der heiße Knoten produziert jetzt auch eindeutig messbar zuviel T3 und T4 . Dann muss man den Knoten auch dringend behandeln.
Der zeitliche Verlauf des Wachstums ist dabei sehr langsam und zieht sich meist über mehrere Jahre hin.
Calcitoninspiegel bei jedem kalten Knoten ?
[Bearbeiten]Soll man bei jedem kalten Knoten der Schilddrüse den Calcitoninspiegel bestimmen ?
Jodinduzierte Hyperthyreose
[Bearbeiten]Kann man durch eine hochdosierte Jodgabe wie z.B. die Gabe eines Röntgenkontrastmittels bei einer primär normalen Schilddrüse eine Hyperthyreose auslösen? Gibt es dazu einen überzeugenden Fallbericht? Wie kann man die Wirkung des Jods dabei erklären?
Bei mir wurde durch Jodkontrastmittel eine Hashimoto ausgelöst.
Das würde mich auch interessieren, insbesondere wie eine Schilddrüsenentzündung behandelte wird, die durch Radoiojod ausgelöst wurde. Nach Herzkathederdiagnostik mit Jodkontrastmittel hatte ich 6 Mon. danach eine Haschimoto und weiß nicht wie die behandelt werden kann. Wer weiss was?
Hashimoto heilbar ?
[Bearbeiten]In welchem Prozentsatz der Fälle heilt eine Hashimotothyreoiditis aus ? Was sind die besten Aktivitätsparameter der Erkrankung ?
Wie kann man die zelluläre Aufnahme von T3 blocken ?
[Bearbeiten]Die molekularen Mechanismen der zellulären Aufnahme des Schilddrüsenhormons L-T3 sind unklar. Dies ist einer der Gründe, warum für die effektive Behandlung einer Schilddrüsenüberfunktion durch spezielle Einflussnahme auf die lokale Schilddrüsenhormonwirkung z.B. am Herzmuskel, bisher kein wirksames und beim Menschen einsetzbares Medikament verfügbar ist. Kann man die Aufnahme mit Calciumantagonisten blocken ?
Thiamazol Therapie, TSH Spiegel bei 6
[Bearbeiten]Bei einem Patienten mit Hyperthyreose, der unter einer Therapie mit 5 mg Thiamazol steht, wird bei einer Kontrolle ein TSH Wert von 6 festgestellt. Welche Konsequenz soll aus dem Wert gezogen werden.
Antwort: Offensichtlich ist Thiamazol leicht überdosiert, hat die Schilddrüse zu stark gebremst und eine leichte Hypothyreose verursacht. Dies ist am leicht erhöhten TSH Spiegel erkennbar. Als Konsequenz des Wertes wird man Thiamazol pausieren oder auf 2,5 mg / Tag reduzieren. Weitere Kontrollen des TSH Wertes sind alle 4 Wochen notwendig.
Spezielle Diät zum Gewichtabnehmen bei Sd-Unterfunktion ?
[Bearbeiten]Bei einer jungen Frau wurde eine Schilddrüsenunterfunktion festgestellt. Trotz Tabletten, Diät und Sport kann sie ihr Übergewicht nicht verlieren ? Gibt es eine spezielle Ernährung oder ein paar hilfreiche Rezepte in diesem Fall ?
Antwort: Das Wichtigste bei einer Schilddrüsenunterfunktion ist die dauerhafte und richtig dosierte Einnahme von Schilddrüsenhormonen.
Eine spezielle Diät gibt es wohl nicht. Auch die Frage, ob man jodarm oder jodreich essen soll, ist wahrscheinlich bis jetzt nicht geklärt. Wahrscheinlich spielt die Jodeinnahme keine große Bedeutung mehr, wenn man genügend Thyroxin schluckt. Es bleibt also nichts anderes übrig als viel Sport zu treiben und möglichst wenig zu essen. Dann klappt das schon mit dem Abnehmen. Außerdem kann man die Thyroxindosis so hoch wählen , daß man knapp an die Überfunktion hinkommt, d.h. Daß der TSH Spiegel an der unteren Grenze liegt. Aufpassen muß man dann aber, daß man keine Herzrhythmusstörungen bekommt oder leicht psychisch überdreht wird.
Versehentliche Überdosierung von Thyroxin
[Bearbeiten]Jemand hat eine leichte Schilddrüsenunterfunktion und wird mit einer niedrigen Dosis Thyroxin behandelt. Durch eine zu hohe Dosis ist er in eine Schilddrüsenüberfunktion gekommen. Thyroxin wurde daraufhin pausiert. Nach sieben Tagen verspürt der Patient immer noch Symptome einer Überfunktion. Wie lange dauert es bis Thyroxin sich abbaut ? Wie eng hängt der Thyroxinspiegel mit den subjektiv empfundenen Symptomen zusammen?
Antwort
[Bearbeiten]Das Thyroxin hat im Körper – an Thyroxin-bindendes Globulin gebunden – eine Halbwertszeit von etwa acht Tag. Es kann also schon ein paar Tage dauern bis die Symptome abklingen. Sie können die Symptome durch Betablocker, ein abendliches Schlafmittel und viel Sport reduzieren. Ausserdem sollten Sie die Überfunktion durch Messung ihres Pulses , ihres Blutdrucks, ihrer Körpertemperatur und ihrer Zittrigkeit zb durch eine Schreibprobe jeden Tag dokumentieren. Das ganze ist nicht lebensbedrohlich und wird bald besser werden. Sie können natürlich ihren T4 Spiegel messen und die Überfunktion auch so objektivieren.
Wie steuert man die Thyroxindosis bei der Hypothyreose ? An welchen Parameter soll man sich halten: TSH, T3, T4. ?
[Bearbeiten]Bei einer älteren Frau wird eine Schilddrüsenunterfunktion mit 150 mikrog Thyroxin / Tag behandelt. Sie wird wegen Luftnot und einer Tachyarrhythmie ins Krankenhaus eingeliefert. Im Labor fällt ein unterdrückter sehr niedriger TSH Spiegel auf . Der T4 Spiegel ist leicht erhöht. Der T3 Spiegel ist leicht erniedrigt.
- Liegt hier eine Hyperthyreose vor ?
- Hängt die Tachyarrhythmie mit der Thyroxintherapie zusammen ?
- Wie steuert man die Thyroxindosis bei der Hypothyreose ?
- An welchen Parameter soll man sich bei der Dosierung von T4 halten: TSH, T3, T4. ?
Antwort
[Bearbeiten]Pathologiefragen Schilddrüsenkrebs
[Bearbeiten]In einer Patho-Klausur wurde folgende Frage gestellt:
Welche Aussage trifft zu?
- Beim Schilddrüsenkarzinom findet man
- A) zytologische Besonderheiten wie Milchglaskerne, indirekte Kerneinschlüsse, dachziegelartige Kernlagerung
- (Milchglaskerne ja, Rest nein, daher falsch?)
- B) praktisch keine Knochenmetastasen
- (falsch)
- C) oft Psammomkörper
- (ja, beim papillären SD-CA)
- D)nicht selten einen hochdifferenzierten, an normales Schilddrüsengewebe oder Adenomgeweben erinnernden histologischen Bau
- (stimmt aber meines Erachtens auch..)
- E)üblicherweise keine Thyreoglobulinsynthese und keine Radiojodspeicherung
- (Radioiod stimmt, aber Thyreoglobulin wird gebildet, oder? also auch falsch ?
- A) zytologische Besonderheiten wie Milchglaskerne, indirekte Kerneinschlüsse, dachziegelartige Kernlagerung
Was sind hier korrekte Antworten ?
Die Fragestellung ist ungenau formuliert. Es gibt verschiedene histologische Typisierungen: - differenzierte SD Ca (follikuläres Ca, Papilläres Ca) - medulläres SD-Ca - undifferenziertes SD-Ca Am häufigsten sind die differenzierten Ca die meistens Thyreoglobulin synthetisieren und eine Radiojodspeicherung aufweisen (deshalb auch die elegante Möglichkeit einer Radiojodszintigraphie und -therapie). Die medullären und undifferenzierten Ca haben keine Radiojodspeicherung und keine Thyreoglobulinsynthese. Histologisch gibt es je nach Typ verschiedene Erscheinungsbilder. Also: richtig sind A, C, D
Adressen
[Bearbeiten]Antwort auf Fragen zu Untersuchung und Behandlung bietet das Forum Schilddrüse an: über
- info@forum-schilddruese.de
- forum-schilddruese.de unter http://schilddruese.de/
- telefonisch zwischen 8.00 und 16.00 Uhr unter der Telefonnummer 069/63803727.
Sehr viele Fragen finden sich auch hier:
Man kann in diesem Gästebuch auch seine Fragen eingeben.
Links
[Bearbeiten]- Siehe auch http://www.jodmangel.de/fragen_und_antworten/
- Siehe auch http://www.schilddruesenselbsthilfe.de/forum/index.html
- Siehe auch http://www.forum-schilddruese.de/fragen_antworten.php
- Siehe auch http://www.schilddruesenforum.at/index.php
- Siehe auch http://www.ht-mb.de
Hallo bei mir wurden die folgenden Schilddrüsenwerte festgestellt (Methode CIMA): TSH - basal 6.3 fT 4 1.01 fT 3 3.09 MAK/Anti TPO 6
Verordnet wurden wurde mir L - Thyroxin 75 Kann mir bitte jemand sagen was diese Werte bzgl. meiner Schilddrüse aussagen denn mein Arzt gab mir ohne weitere Erklärung nur das Rezept für das Schilddrüsenhormon. Vielen Dank!
Aktuelles
[Bearbeiten]
Wo findet man aktuelle Neuigkeiten und Infos über die Schilddrüse ?
[Bearbeiten]- Suchen in den Google News mit dem Stichwort Schilddrüse:
- Suchen im Deutschen Ärzteblatt Archiv mit dem Stichwort Schilddrüse
- Suchen in der Medical Library of North America PubMed mit dem Stichwort thyroid gland
- http://www.ncbi.nlm.nih.gov/entrez/query.fcgi?DB=pubmed
- Suchen in Pubmed Stichwort: thyroid gland deutsche medizinische wochenschrift
- Suchen in Pubmed Stichwort: thyroid gland and new england journal of medicine
- Suchen in Pubmed Stichwort: thyroid gland and lancet
- Suchen in der Medical Tribune mit Stichwort Schilddrüse:
- Englischer Schilddrüsen blog von einem Experten
Neues
[Bearbeiten]Sorafenib bei fortgeschrittenem Schilddrüsenkrebs in USA zugelassen
[Bearbeiten]Am 22. November 2013 hat die amerikanische Gesundheitsbehörde (FDA) Sorafenib zur Behandlung von Patienten mit lokal fortgeschrittenem oder metastasiertem, differenziertem Schilddrüsenkrebs, die auf Radiojod nicht mehr ansprechen, zugelassen. Zulassungsstudie: DECISION-Studie
Dauer des progressionsfreien Überlebens Sorafenibgruppe 10,8 Monate Placebogruppe 5,8 Monate
- Siehe http://www.bayerpharma.com/de/forschung-und-entwicklung/aktuelles/news-page.php/15303/2013-0624
Selen lindert Entzündung bei Hashimoto-Thyreoiditis Mai 2008
[Bearbeiten]Siehe http://www.aerztezeitung.de/medizin/?sid=492795
Neuentwicklungen zum Thema SD an der Charite Berlin
[Bearbeiten]- Thyroxin in Tropfenform etc
Operationen der Schilddrüse mit oder ohne Darstellung des Nervus recurrens
[Bearbeiten]Nach Ansicht des deutschen Bundesgerichtshofes ist es bis heute unsicher, ob Operationen der Schilddrüse unter Darstellung des Nervus recurrens tatsächlich zu weniger Verletzungen dieses Nervs führten als Operationen ohne Darstellung des Nerven. (Beschluss vom 28. März 2008, Az.: VI ZR 57/07) RA Barbara Berner
Iodfalle - Klonierung des Natrium-Jodid-Tansporters der Schilddrüse
[Bearbeiten]Iodfalle = aktive Aufnahme der SD von Iod aus der Blutbahn.
Mit der Klonierung des Natrium-Iodid-Tansporters der Schilddrüse 1996 bei der Ratte wurde eines der letzten wichtigen Proteine der Schilddrüsenzelle charakterisiert. Es handelt sich dabei um ein membranständiges Protein der Schilddrüsenzelle mit vermutlich 12 transmembranösen Regionen.
siehe http://www.uni-leipzig.de/forsch96/49400/49430_p.htm
Thermoablationsverfahren an der Schilddrüse
[Bearbeiten]Mit der Laserinduzierten Thermotherapie (LITT) oder der Radiofrequenzinduzierten Thermotherapie (RFITT) kann man knotige Schilddrüsenveränderungen zunehmend besser auch ohne Operation behandeln.
siehe
Abkürzungen
[Bearbeiten]
Abkürzungen
[Bearbeiten]Wenn man sich mit der Schilddrüse beschäftigt und darüber nachliest, stößt man auf zahlreiche Abkürzungen, die wichtigsten sind hier augelistet:
Abkürzung Bedeutung ---------------------------------------------------------- DJT 3,5 –Dijodtyrosin FT3 freies Trijodthyronin FT4 freies Thyroxin im Blut HCG Humanes Chorion Gonadotropin HVL Hypophysenvorderlappen ICD 10 International Classification of Diseases 10 KeV KiloElektronenVolt µg ein mikro Gramm = ein millionstel Gramm MAK Mikrosomale Antikörper siehe TPO MJT 3 -Monojodtyrosin MW Molekulargewicht NIS Natrium-Iodid Symporter, Blut > Iod > SD PBI Protein-gebundenes Jod rT3 reverses T3 SD Schilddrüse SDH Schilddrüsenhormone T3 Trijodthyronin T4 Tetrajodthyronin = Thyroxin TAK Thyreoglobulin Antikörper TBA Thyroxin- bindendes Albumin TBG Thyroxin bindendes Globulin ( Transportprotein im Blut ) TBPA Thyroxin – bindendes Präalbumin Tc Technetium TRAK TSH-Rezeptor Antikörper TPO Threoidea Peroxidase Antikörper TSH ThyreoideaStimulatingHormone TRH ThyreotropinReleasingHormone 10^-9 ein Milliardstel (1:1 000 000 000) 10^-12 ein Billionstel (1:1 000 000 000 000)
Aufbau der Schilddrüse
[Bearbeiten]
Anatomie (Aufbau) der Schilddrüse
Makroanatomie (Grober Aufbau)
[Bearbeiten]Die Schilddrüse ist in zwei Lappen unterteilt die annähernd gleich groß sind. Beim Erwachsenen ist die rechte Schilddrüse etwa 1,5 - 2 cm breit , 1,5 - 2 cm tief und circa 3,5 bis 4,5 cm lang. Die linke Schilddrüse hat eine identische Größe. Auch bei den meisten Säugetieren besteht die Schilddrüse aus zwei Lappen (Lobus dexter und sinister) seitlich und oberhalb der Luftröhre (Trachea), die durch einen schmalen Streifen (Isthmus) verbunden sind. Bei Vögeln liegen beide Schilddrüsen als kleine Knötchen an der Trachea vor dem Brusteingang, also am anderen Ende des Halses!

Aufbau
[Bearbeiten]- rechter Schilddrüsenlappen
- Isthmus ( Landenge)
- Die schmale Verbindung zwischen dem rechten und linken Schilddrüsenlappen.
- linker Schilddrüsenlappen
- Lobus pyramidalis
- Dieser Lappen ist ein Relikt aus der Embryonalentwicklung und ist im allgemeinen nur noch als bindegewebiger Strang zu finden.
Feinbau der Schilddrüse
[Bearbeiten]
1 Follikel mit Kolloid,
2 Follikelepithelzellen,
3 Endothelzellen der Kapillaren
Schneidet man eine normale Schilddrüse mit dem Messer durch, zeigt sie bis auf einige Gefäße ein sehr gleichmäßiges Gewebsbild. Auch im Ultraschall der Schilddrüse findet man ein homogenes hellgraues Gewebe.
Benutzt man ein Mikroskop und färbt den Schilddrüsenschnitt an, dann erkennt man, daß sich hinter diesem gleichmäßigen Gewebe eine differenzierte Feinstruktur verbirgt.
Mikroskopisch besteht die Schilddrüse aus Follikeln ( = Bläschen), in deren Inneren die Hormone in inaktiver Form als s.g. Kolloid gespeichert werden. Am Rand dieser Bläschen liegen die Follikelepithelzellen. Diese Zellen sind die Produktionsstätten für die Schilddrüsenhormone. Zwischen den Follikelepithelzellen und ihrer Basalmembran liegen die parafollikulären C-Zellen. ( parafollikulär = neben den Bläschen liegend) . In den C-Zellen wird das Calcitonin produziert.
Siehe auch
[Bearbeiten]- Pathologie:_Schilddrüse
- http://www.forpath.org/0201/photos/fullsize/cas7e.jpg
- http://www.kgu.de/zmorph/histopatho/histo4/pub/data/eo/de/002_a.html
- Histologische Bilder der Schilddrüse gut erklärt.
- http://w3.ouhsc.edu/histology/Glass%20slides/42_04.jpg
- Histologisches Bild einer C-Zelle

Zellarten der Schilddrüse:
[Bearbeiten]- Schilddrüsenzellen = Follikelepithelzellen
- parafollikulären C-Zellen.
- Bindegewebszellen
- Gefäßzellen
- Abwehrzellen
Iod und die Schilddrüse
[Bearbeiten]
Allgemeines zum Iod
[Bearbeiten]Iod ist ein für den Menschen wie auch andere Lebewesen essentielles, unverzichtbares Spurenelement. Deswegen wir der Stoff hier ausführlich erklärt, insbesondere was seine Bedeutung für den Menschen und die Schilddrüse betrifft.
Iod ist ein chemisches Element. Es steht im Periodensystem der Elemente in der 17. Gruppe, den sogenannten Halogenen ( Salzbildner). Der Name leitet sich vom altgriechischen Wort „Iodes“ (ιώο-ειδης) für „veilchenfarbig“ ab: Die beim Erhitzen von Iod freigesetzten Dämpfe sind violett.
Während im Deutschen Jod die häufiger gebräuchliche Schreibweise darstellt, bevorzugt die Fachsprache Iod; beide Schreibweisen sind unabhängig von der Rechtschreibreform korrekt. Das Elementsymbol J dagegen ist veraltet und wurde ausnahmslos durch I ersetzt.
Geschichte
[Bearbeiten]Die gesundheitliche Bedeutung iodhaltiger Zubereitungen war schon im Altertum bekannt. So wurden bereits 1500 Jahre vor unserer Zeitrechnung Kropfkranken die iodhaltigen Schilddrüsen von Schafen oder Aschen von Meeresschwämmen verordnet.
Iod wurde im Jahr 1811 durch den Pariser Salpetersieder Bernard Courtois bei der Herstellung von Schießpulver erstmals aus der Asche von Seetang gewonnen. Den elementaren Charakter erforschten jedoch erst ab 1813 die französischen Naturwissenschaftler Nicolas Clément-Désormes und Joseph Louis Gay-Lussac, der ihm ein Jahr später den heutigen Namen verlieh.
Vorkommen
[Bearbeiten]
Iod ist abgesehen von Astat wesentlich seltener als die übrigen Halogene. In der Natur ist es weit verbreitet, jedoch nur in Form seiner Verbindungen, zum Beispiel angereichert (0,02–1 %) im Chilesalpeter, hauptsächlich in Form von Natriumiodat (NaIO3), aber auch Natriumperiodat (NaIO4) und Lautarit (Ca(IO3)2). In geringen Spuren ist es in Böden und Gesteinen nachweisbar. Im Durchschnitt enthält 100 Gramm wasserfreier Feinboden aus dem süddeutschen Raum bis zu 34 Milligramm Iod [1]. Der Iodgehalt des Bodens ist wesentlich für die Versorgung der Bevölkerung mit natürlichem Iod. Als Iodwasserstoff kommt es in geringsten Mengen in vulkanischen Gasen vor.
Lösliche Iodverbindungen wie Alkali- und Erdalkaliiodide werden während der Verwitterung von Gesteinen durch Regenwasser freigesetzt oder zerfallen bei höheren Temperaturen. So gelangen sie schließlich in die Meere und ins Grundwasser. Einige Mineralwässer enthalten Iod. Die Mineralquelle Woodhall Spa in den USA bringt Wasser hervor, das durch Iod braun gefärbt ist. Im Meerwasser liegt die Menge an Iod bei 0,05 Gramm pro Tonne.
Organische Iodverbindungen kann man aus Meeresalgen (19 Gramm Iod pro Kilogramm Trockenmasse), Tangen und Schwämmen (bis zu 14 Gramm Iod pro Kilogramm Trockenmasse) isolieren. Einen wichtigen Speicher für organisch gebundenes Iod stellt die Schilddrüse dar.
Natürlich vorkommendes Iod besteht zu 100 % aus dem Isotop 127I, es ist also ein Reinelement (anisotop).
Gewinnung und Darstellung
[Bearbeiten]Früher gewann man Iod in Form von Iodiden und Iodaten, indem man die durch die Flut an den Strand angeschwemmten Tange einsammelte und verbrannte. Die erhaltene Asche enthielt etwa 0,1–0,5 % Iod. Diese Iodgewinnung hat heute jedoch nur noch lokale Bedeutung und macht ungefähr 2 % der Weltjahresproduktion aus.
Die technische Gewinnung von Iod ist eng mit der Salpetergewinnung verknüpft. Das in den Mutterlaugen enthaltene Iodat wird durch Reduktion in Iod umgewandelt. Im ersten Reaktionsschritt setzt man schwefelige Säure ein, um Iodsäure (Iodat ist das Anion dieser Säure) zu Iodwasserstoff zu reduzieren:
- Iodsäure und schwefelige Säure reagieren zu Iodwasserstoff und [Schwefelsäure
Der Iodwasserstoff wird wiederum in einem zweiten Schritt durch die in der Lösung vorhandene Iodsäure zu Iod oxidiert. Man spricht in diesem Fall von einer Komproportionierung, da Iod in zwei verschiedenen Oxidationsstufen (−1 im Iodwasserstoff und +5 in der Iodsäure) zu elementarem Iod mit der Oxidationsstufe 0 wird.
- Iodsäure und Iodwasserstoff komproportionieren zu Wasser und Iod
Alternativ kann zur Reduktion auch Schwefeldioxid (SO2) den Endlaugen, aus denen der Salpeter bereits auskristallisiert ist, zugesetzt werden.
Bei der Erdöl- und Erdgasförderung fallen bedeutende Mengen an Salzsole an, die einen Iodgehalt zwischen 30 bis über 100 ppm aufweisen. Das in Form von Natriumiodid vorliegende Iod wird durch die Oxidation mit Chlor aus der Sole freigesetzt:
- Natriumiodid und Chlor reagieren zu Natriumchlorid und Iod
Eine weitere Reinigung des gewonnenen Iods wird dadurch erreicht, dass es mit Luft ausgeblasen, anschließend mit Schwefeldioxid in schwefelsaurer Lösung wieder reduziert und zum Schluss mit gasförmigem Chlor zum Iod zurück oxidiert wird.
- Iod wird durch Schwefeldioxid zu Iodwasserstoff reduziert
- Iodwasserstoff und Chlor reagieren zu Chlorwasserstoff und Iod
Chromatographisch kann Iod mittels Adsorption von Polyiodid an Anionenaustauschern angereichert werden. Zur Reinstherstellung setzt man Kaliumiodid und halogenfreies Kupfersulfat ein.
Im Labormaßstab lässt sich Iod durch Einwirken von Schwefelsäure und Mangan(IV)-oxid auf Kaliumiodid herstellen. Die Gewinnung gelingt ebenso aus der iodhaltigen Asche von Meerespflanzen durch Behandlung mit Chlor.
Eigenschaften
[Bearbeiten]
Iod ist unter Normalbedingungen ein Feststoff, der grauschwarze, metallisch glänzende Schuppen bildet, deren Dichte 4940 kg/m³ beträgt. Sie besitzen die Eigenschaften eines Halbleiters. Diese Eigenschaften sind auf das Vorhandensein eines Schichtgitters zurückzuführen, in dem einzelne Ebenen aus I2-Molekülen (Bindungslänge 2,715 Å) bestehen. Der Abstand der Ebenen in einem orthorhombischen Schichtkristall beträgt 4,412 Å und entspricht damit dem van-der-Waals-Abstand zwischen zwei Iod-Atomen (4,30 Å). Das Ergebnis der Messung des kürzesten Abstands zwischen zwei Iod-Molekülen liegt mit 3,496 Å deutlich darunter.
Iod geht beim Schmelzen (Schmelzpunkt 113,70 °C) in eine braune, elektrisch leitfähige Flüssigkeit über. Es siedet bei 184,2 °C unter Bildung eines violetten Dampfes, der aus I2-Molekülen besteht. Iod sublimiert schon bei Zimmertemperatur, so dass ein Schmelzen nur unter rascher und starker Temperaturerhöhung möglich ist.
Iod reagiert weitaus weniger heftig mit anderen Elementen wie Phosphor, Aluminium, Eisen und Quecksilber als Chlor und Brom. Mit Wasserstoff reagiert Iod zu Iodwasserstoff, welcher beim leichten Erwärmen jedoch schnell wieder in die Elemente zerfällt.
- Iod und Wasserstoff stehen mit Iodwasserstoff im Gleichgewicht. Bei erhöhter Temperatur wird dieses nach links verschoben.
Mit Ammoniak findet aufgrund der damit verbundenen Volumenzunahme eine explosionsartige Reaktion statt.
- Ein Mol Iod und zwei Mol Ammoniak reagieren zu sechs Mol Iodwasserstoff und ein Mol Stickstoff.
Eine interessante Eigenschaft des Iods äußert sich darin, Polyiodidverbindungen einzugehen. Dabei verbinden sich gelöste I2-Moleküle jeweils mit einem Iodid-Anion zum einfach negativ geladenen I3−-Anion. Eine Eigenschaft dieser Polyiodidverbindung ist, dass sie sich in Stärke-Helices einlagert. Diese Einlagerungsverbindungen rufen bereits in geringen Konzentrationen eine intensive Blaufärbung hervor (empfindlicher und spezifischer Iod-Stärke-Nachweis).
Iod-Kationen
[Bearbeiten]Vom Iod sind verschiedene Kationen bekannt. So entsteht das blaue Diiod-Kation I2+, wenn Iod durch in Schwefelsäure gelöstes Schwefeltrioxid (65%iges Oleum: H2SO4 • 2SO3) oxidiert wird:
Zur Oxidation kann ebenso Antimon(V)-fluorid bzw. Tantalpentafluorid in flüssigem Schwefeldioxid verwendet werden:
Es gelang jedoch bisher nicht, Verbindungen mit dem unsolvatisierten, das heißt lösungsmittelfreien Monoiod-Kation I+ herzustellen. Selbst in Verbindung mit einer extrem schwachen Lewis-Base wie dem Perchlorat-Anion ClO4− findet man kovalent gebundenes Iod vor. In der Gasphase kann man das I+-Ion bei Abwesenheit eines Gegenions jedoch nachweisen.
Verwendung
[Bearbeiten]Iodtinktur und Iodoform enthalten Iod in elementarer bzw. gebundener Form und dienen als Antimykotikum und Antiseptikum. Es wird vermutet, dass die desinfizierende Wirkung auf der Abspaltung von Sauerstoff aus Wasser beruht. Dieser Sauerstoff ist kurz nach seiner Freisetzung (in statu nascendi) besonders reaktionsfähig:
Dieser Mechanismus wird auch für die anderen Halogene diskutiert. Iod wird aus diesem Grund in einzelnen Fällen auch zur Entkeimung von Wasser in Badeanstalten genutzt. Vorteilhaft ist in diesem Zusammenhang, dass Iod weniger aggressiv ist als Chlor. Allerdings vermag diese Wasserbehandlung nicht Algen abzutöten, so dass zusätzlich ein Algizid zugesetzt werden muss. Der intensive Gebrauch von Iod kann aber zu Hautverfärbungen führen. Auch steht die Gefahr der Allergisierung im Raum. Beides ist durch Einsatz von so genannten Iodophoren, Trägermaterialien, die Iod binden können, vermeidbar.
Kaliumiodat wird in geringen Mengen dem Speisesalz zugesetzt, um Iodmangelerkrankungen vorzubeugen. Der Iodbedarf von Schwangeren muss in der Regel durch die zusätzliche Einnahme von Iodtabletten gedeckt werden.
Die radioaktiven Iod-Isotope 131I und 123I werden als Radiopharmaka in der nuklearmedizinischen Diagnostik und Therapie vorwiegend von Schilddrüsenerkrankungen eingesetzt (vergleiche Radioiodtherapie), wobei 131I heute verstärkt zum Einsatz kommt. Zur Bestimmung des Knochenmineralgehalts wird 125I (Gammastrahlung von γ = 35 keV) herangezogen.
Iod ist ein häufig eingesetzer Katalysator bei chemischen Reaktionen. So verwendet man es bei stereospezifischen Polymerisationen von Butadien. Die Sulfurierung aromatischer Verbindungen sowie die Alkylierung und Kondensation aromatischer Amine sind weitere Einsatzfelder.
Aromatische Iodverbindungen werden als Röntgenkontrastmittel in der Diagnostik eingesetzt.
Natriumiodid wird als Szintillator in Szintillationszählern eingesetzt.
Strahlenschutz
[Bearbeiten]Radioaktive Iod-Isotope sind auch im Fallout (radioaktiver Niederschlag) von Nuklearexplosionen und im Abbrand von Kernkraftwerken enthalten. Bund und Länder bevorraten insgesamt 137 Millionen Kaliumiodid-Tabletten (meist als „Jod-Tabletten“ bezeichnet) in der Umgebung der deutschen Atomkraftwerke für den Fall eines Atomunfalls (vgl. Iodblockade).
Biologische Bedeutung
[Bearbeiten]Schilddrüsenhormone
[Bearbeiten]Iod spielt im Organismus hauptsächlich eine Rolle für die Produktion der Schilddrüsenhormone Thyroxin (T4) und Triiodthyronin (T3), die vier bzw. drei Iodatome enthalten. Der Iodvorrat im menschlichen Körper wird auf 10 bis 30 Milligramm beziffert. Davon sind 99 % in der Schilddrüse gespeichert.
Iodmangel führt zunächst nur zu einer euthyreoten Kropfbildung der Schilddrüse. Erst ein ausgeprägter Iodmangel hat auch eine Unterfunktion der Schilddrüse (Hypothyreose) zur Folge, die sich durch eine Minderproduktion von T4 und T3 auszeichnet. Da die Schilddrüsenhormone wesentliche Funktionen in der Regulation von Stoffwechselprozessen übernehmen, resultieren aus einer Schilddrüsenunterfunktion schwere Stoffwechsel- und Entwicklungsstörungen.
Zur Rolle der Iodversorgung bei Schilddrüsenkrankheiten siehe Iodprophylaxe, Iodunverträglichkeit, Hyperthyreose und Hashimoto-Thyreoiditis.
Sicherheitshinweise
[Bearbeiten]Iod ist von der EU als Gefahrstoff klassifiziert, dessen Freisetzung in die Umwelt zu vermeiden ist. Beim Umgang mit dem Element sind entsprechende Schutzmaßnahmen einzuhalten. Reste von Iod sind mit Natriumthiosulfat-Lösung zu behandeln (→ Reduktion zu Iodid). Vor der Entsorgung ins Abwasser muss der pH-Wert des Reaktionsgemisches mit Natriumhydrogencarbonat neutralisiert werden. Iod darf niemals mit Ammoniak in Verbindung gebracht werden, da sich sonst explosives Stickstofftriiodid bilden kann.
Nachweis
[Bearbeiten]Qualitativ kann Iod als elementares Iod oder als Iodstärke nachgewiesen werden. Bei der Nachweisreaktion über Iodstärke gibt man in die zu untersuchende Lösung wässrige Stärkelösung, die sich bei Anwesenheit von Iod je nach Konzentration blau bis blauschwarz verfärbt. Es lagern sich hierbei Polyiodid-Anionen in die Spiralstruktur der Stärke ein und bilden diesen farbigen Komplex. Freies Iod erkennt man darüber hinaus anhand seines violetten, typisch riechenden Dampfs oder daran, dass sich eine alkoholische Lösung bei Anwesenheit von Iod braun, eine Hexan-Lösung rotviolett färbt.
Iodid-Ionen, zum Beispiel aus Natriumiodid, lassen sich über zahlreiche Fällungsreaktionen nachweisen. So ergeben sie mit Silbernitrat einen gelben Niederschlag von Silberiodid:
Dieser Niederschlag ist in Ammoniak und Natriumthiosulfat praktisch nicht, in Kaliumcyanid-Lösung jedoch leicht löslich.
Quecksilbernitrate können ebenso zum Nachweis herangezogen werden. So fällt Quecksilber(I)-nitrat, wenn es im Überschuss eingesetzt wird, Iodid-Ionen in Form von gelbgrünem Quecksilber(I)-iodid:
Wird dagegen Quecksilber(II)-nitrat verwendet, so erhält man einen roten Niederschlag von Quecksilber(II)-iodid:
Bleiacetat-Lösung lässt einen gelben Niederschlag entstehen.
Chlorwasser vermag Iodid zu elementarem Iod zu oxidieren, das als bräunlicher Niederschlag sichtbar wird. Beim Schütteln einer Iodidlösung mit Chlorwasser und Hexan färbt das Iod die Hexanphase rosaviolett:
Der quantitative Bestimmung von Iod baut auf den oben genannten Reaktionen auf. So ist es möglich, die Iodmenge über Titration mit einer Thiosulfat-Lösung (siehe Iodometrie) zu ermitteln. Für die gravimetrische Bestimmungen bietet sich die Fällung als Silberiodid an. Darüber hinaus kann eine Amperometrie, ein elektrochemisches Bestimmungsverfahren mit Tolidin, in Betracht gezogen werden.
Verbindungen
[Bearbeiten]Als Wasserstoffverbindung ist der Iodwasserstoff, HI, zu nennen, ein farbloses, stechend riechendes Gas. Die davon abgeleiteten Salze sind die Iodide. Eine wässrige Lösung davon bezeichnet man als Iodwasserstoffsäure.
Iod geht mit den anderen Halogenen so genannte Interhalogenverbindungen ein. Diese sind Iodfluorid (IF), Iodtrifluorid (IF3), Iodpentafluorid (IF5), Iodheptafluorid (IF7), Iodchlorid (ICl), Ioddichlorid ((ICl2)2), Iodtrichlorid (ICl3) und Iodbromid (IBr).
Darüber hinaus sind vom Iod verschiedene Sauerstoffsäuren und die dazugehörigen Salze bekannt: hypoiodige Säure (HIO) und Hypoiodite, iodige Säure (HIO2) und die entsprechenden Iodite, Iodsäure (HIO3) und Iodate sowie die Periodsäure (H5IO6) und die dazugehörigen Periodate.
Von den Iodoxiden sind die Verbindungen I2O4, I4O9, I2O5 und I2O6 bekannt, wovon Iodpentaoxid (I2O5) die stabilste Verbindung ist. Vermutlich gibt es noch weitere, wesentlich instabilere Iodoxide.
Quellen und Literatur
[Bearbeiten]- Zur Bedeutung von Iod im Stoffwechsel siehe auch:
- B. J. Füger, R. Dudczak, C. H. Pirich, G. Zettinig: Jodstoffwechsel. In: Journal für Ernährungsmedizin. 4(2), S. 7–9, 2002 (Ausgabe für Österreich), [1] (PDF; 185 KB).
Weblinks
[Bearbeiten]Iod in der Nahrung
[Bearbeiten]Die einfachste Form genügend Iod zu bekommen, ist die Benutzung von iodiertem Salz oder die Einnahme von Iodtabletten, die es rezeptfrei in jeder Apotheke zu kaufen gibt.
Den höchsten Gehalt an Iod haben Fische aus dem Meer: Die Nord- und Ostseefische wie Scholle, Kabeljau und Matjes enthalten bis zu 200 Mikrogramm Iod auf 100 Gramm.
Die Salicorniapflanze wächst an den Meeresküsten. Von dieser iodreichen und salzig schmeckenden Pflanze kann man in der Apotheke getrocknetes Pulver zum Salzen kaufen.
Brokkoli und Feldsalat enthalten bis zu 25 Mikrogramm Jod auf 100 g. Kichererbsen enthalten über 20 Mikrogramm auf 100 g.
Natürliche Mineralwässer weisen teilweise beträchtliche Jodwerte auf. Sie kommen aus Erdtiefen, die von den Auswaschungen der Eiszeit kaum betroffen waren. Einige Mineralwässer enthalten mehr als 250 Mikrogramm Jod auf einen Liter.
Man kann auch Schilddrüsengewebe von Tieren essen. Dieses Gewebe enthält viel Iod und roh gegessen auch viel Schilddrüsenhormon. Dies war historisch gesehen die erste erfolgreiche Behandlungsmöglichkeit der Schilddrüsenunterfunktion. Problem dabei ist die unkontrollierte Höhe der Dosis. Diese Behandlungsform der Unterfunktion ist also nicht mehr empfehlenswert.
Iod im menschlichen Körper
[Bearbeiten]siehe Biochemie Iod
Literatur
[Bearbeiten]- http://edoc.hu-berlin.de/dissertationen/bittermann-heike-1999-10-22/HTML/bittermann.html
- DISSERTATION Jodversorgung deutscher Wehrpflichtiger im Alter von 17,5 bis 21 Jahren
- eingereicht: 05.01.1999
- Die Jodausscheidung wurde in Spontanurinproben gemessen
- eingereicht: 05.01.1999
- DISSERTATION Jodversorgung deutscher Wehrpflichtiger im Alter von 17,5 bis 21 Jahren
Zitat:
Im Rahmen der Verbundstudie Jod-Monitoring 1996 wurde der Jodversorgungszustand von 778 wehrpflichtigen Männern im Alter von 17,5-21 Jahren in 26 zufällig ausgewählten Regionen in Deutschland untersucht. Dabei wurde als Maß zur Beurteilung der alimentären Jodversorgung die Urinjodausscheidung bestimmt sowie anhand eines Fragebogens über die Verzehrshäufigkeit und das Ernährungsverhalten die geschätzte Jodzufuhr berechnet. Der Median der Jodausscheidung im Urin beträgt 57,0 µg/g Kreatinin. Als ausreichend versorgt wird die Bevölkerung nach den Kriterien der Weltgesundheitsorganisation (WHO) erst mit Werten von >100 µg/g Kreatinin eingestuft. Die mittlere Jodzufuhr wurde mit dem Median von 125,2 µg pro Tag errechnet. Nach den Empfehlungen der Deutschen Gesellschaft für Ernährung (DGE) sollte die Jodzufuhr für Jugendliche und Erwachsene 200 µg pro Tag betragen. Gemessen an der Jodausscheidung erreichen nur 12% der Probanden eine ausreichende Jodversorgung, 50,5% weisen einen geringfügigen (Grad I), 33,1% einen mittleren (Grad II), und immerhin 4,4% einen erheblichen Jodmangel (Grad III) auf. Im Gegensatz zu früheren Erhebungen bestehen weder ein Nord-Süd-Gefälle noch signifikante Unterschiede zwischen den alten und neuen Bundesländern.
Zusätzlich wurde der Jodgehalt des Trinkwassers in den Regionen gemessen. Im Median wurde ein Jodgehalt von 2,6 µg/l ermittelt. Es finden sich in Nord höhere Werte (5,9 µg/l) als in Süd (1,55 µg/l). Zwischen den neuen und alten Bundesländern gibt es keine statistischen Unterschiede. Die ermittelten Werte bestätigen, daß das Trinkwasser nicht wesentlich zur täglichen Jodversorgung beiträgt, wenn man von einer täglichen Trinkwasserzufuhr von 2 Litern pro Tag ausgeht.
- http://www.diss.fu-berlin.de/diss/receive/FUDISS_thesis_000000002217
- Monitoring der Urinjodausscheidung Neugeborener als Kriterium für die Wirksamkeit der Jodmangelprophylaxe
- von Eike, Esther
- Monitoring der Urinjodausscheidung Neugeborener als Kriterium für die Wirksamkeit der Jodmangelprophylaxe
Zitat
Die Medianwerte der Urinjodausscheidungen Berliner Neugeborener haben sich vervierfacht: 1991 30,0 µg/l und 2004 123,6 µg/l, im Stadtbezirk Berlin-Lichtenberg zum Vergleich 1991 35,9 µg/l und 2004 130,8 µg/l. Die Hälfte der Neugeborenen zeigten 2004 eine optimale Jodausscheidung (Berlin: 45,5%, Berlin-Lichtenberg 56,2%). In der Auswertung auffallend ist der Anteil der Jodausscheidungs-konzentrationen über 200 µg/l, im Jahr 2001 mit 23% und im Jahr 2004 mit 22%.
Hormone der Schilddrüse
[Bearbeiten]
Auf dieser Seite findet sich nur eine kurze Zusammenfassung über die Hormone, die in der Schilddrüse produziert werden. Da die meisten Mediziner sich auch nicht die komplizierten Namen der Hormone merken können, reicht es völlig aus, wenn man sich die Namen T3 und T4 merkt. Auch den Namen TSH sollte man sich abspeichern, denn TSH ist das Steuerungshormon der Hypophyse für die Schilddrüse (nächsthöhere Instanz).
- Genaueres findet sich im Abschnitt Biochemie und Physiologie der Schilddrüse
- Die Laborwerte finden Sie unter Schilddrüse-Laborwerte
Tabelle der Schilddrüsenhormone und des TSH
[Bearbeiten]--------------------------------------------------------------------------------------
Abkürzung Name Bedeutung
--------------------------------------------------------------------------------------
T3 Triodthyronin eigentlich wirksames Hormon
rT3 reverse T3 inaktives T3
T4 Thyroxin Vorstufe von T3
Calcitonin Senkt den Calciumspiegel
TSH Thyreoideastimulierendes Hypophysenhormon, welches die Schilddrüse anregt
Hormon
---------------------------------------------------------------------------------------
Schilddrüsenhormone T3 rT3 T4
[Bearbeiten]Ohne Schilddrüsenhormone kann man nicht leben. Die Schilddrüsenhormone (Trijodthyronin T3 und Thyroxin T4) sind jodhaltig. Sie werden von den Follikelepithelzellen gebildet.
Die Schilddrüsenhormone T3 und T4 wirken in fast allen Körperzellen und regen dort den Energiestoffwechsel an (allgemeine Wirkung: z.B. Erhöhung des Pulses und Blutdrucks, Gefäßerweiterung, Anstieg der Körpertemperatur), außerdem sind sie für Wachstum und Differenzierung notwendig. Dabei ist T3 etwa zehnfach biologisch wirksamer als T4. T4 kann man als Vorstufe ( Prohormon) von T3 ansehen.
Zur Bedarfsregulation an Schilddrüsenhormonen besteht ein Weg, T4 anstelle zum wirksamen T3 zum unwirksamen rT3 zu konvertieren. Im Labor wird T3 und rT3 gemeinsam gemessen, was zu falsch-hohen Werten führen kann. Einige Labore bieten deshalb auch die Messung von rT3 an.
Die Funktion der Schilddrüse wird durch das Hypophysenhormon TSH (Thyreoidea stimulierendes Hormon) und das Hypothalamushormon TRH (TSH Releasing Hormon) im Rahmen eines Regelkreises gesteuert.
Calcitonin
[Bearbeiten]Die parafollikulären C-Zellen der Schilddrüse bilden das Calcitonin. ( parafollikulär = neben den Schilddrüsenbläschen liegend). Es spielt eine Rolle in der Steuerung des Calciumstoffwechsels. Funktionell sind die Schilddrüsenhormone T3 und T4 und das Calcitonin völlig getrennt zu sehen, da sie verschiedenen Stoffwechselsystemen angehören.
Biochemie und Physiologie der Schilddrüse
[Bearbeiten]
Iod
[Bearbeiten]siehe Schilddrüse: Iod
Iod im menschlichen Körper
[Bearbeiten]Resorption im Dünndarm als Iodid, negatives geladenes Iod-Atom
[Bearbeiten]Iod Transport in die SD-Zelle: Natrium-Iodid Symporter NIS
[Bearbeiten]Der Natrium/Iodid-Symporter (NIS) ist ein langkettiges Eiweiß. Es sitzt in der Membran von Schilddrüsenfollikelzellen und sorgt für den Transport von Iod in die Schilddrüsenzellen. Das Protein des Natrium-Iodid Symporters wurde mittlerweile kloniert. Es besteht aus 643 Aminosäuren. Der NIS bewerkstelligt den aktiven Transport von Iodid in die Schilddrüse, man findet ihn aber auch in einer Reihe extrathyreoidaler Organe, insbesondere in der milchproduzierenden Brustdrüse der Frau.
Der NIS wird
- durch TSH hochreguliert
- durch mäßige Ioddosen offensichtlich herunterreguliert
- durch Perchlorat inhibiert.
Oxidation zu Iod
[Bearbeiten]Synthese von T3 und T4
[Bearbeiten]Übersicht
[Bearbeiten]
Das Thyroxin-Molekül T4 ist an vier Stellen mit Iod besetzt (Tetraiodthyronin = 4-Jod-Schilddrüsenhormon ). T3 ist an 3 Stellen mit Iod besetzt (Triiodthyronin = 3-Jod-Schilddrüsenhormon).
Das Iod wird von der Schilddrüse aus dem Blut abgefangen und konzentriert. Die „Iodierung“ erfolgt stufenweise und stets am Rest der Aminosäure Tyrosin. Über die Vorstufen Monojodtyrosin und Diiodtyrosin (genauer: 3,5-Dijod-L-Tyrosin) entsteht durch Kopplung zweier Moleküle zunächst T4. Daraus wird unter Verlust eines Iodatoms T3 gebildet. Zur Speicherung werden die Hormone an Transporteiweiße, insbesondere w:Thyroxin-bindendes Globulin (TBG), gebunden.
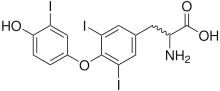
Im Normalfall wird das Iod durch den Abbau der Hormone durch Darm und Niere wieder ausgeschieden. Deswegen ist der gesunde Körper auf ständige, ausreichende Iodzufuhr angewiesen.
Die Ausschüttung von Thyroxin wird verstärkt, wenn der Thyroxinspiegel im Blutplasma zu stark absinkt und umgekehrt. Die Aufrechterhaltung des Schilddrüsenhormonspiegels wird dadurch geregelt.
Siehe auch Wikibuch Biochemie
Tyrosin
[Bearbeiten]
Tyrosin ist in seiner natürlichen L-Form eine nichtessenzielle proteinogene Aminosäure, die in den meisten Proteinen vorkommt, in großen Mengen im Casein. Tyrosin ist Ausgangssubstanz für die Biosynthese von Katecholaminen ( wie zb Adrenalin) , Melanin und Thyroxin.
Vorkommen
[Bearbeiten]Tyrosin kommt im Körper als Zersetzungsprodukt von Proteinen vor. Säugetiere können Tyrosin aus der essentiellen Aminosäure Phenylalanin synthetisieren, welche mit der Nahrung aufgenommen wird.
Funktionen
[Bearbeiten]Im Nebennierenmark werden aus L-Tyrosin die Hormone Adrenalin und Noradrenalin gebildet und bei Bedarf direkt an das Blut abgegeben.
Die Bildung der Schilddrüsenhormone T3 und T4 im Kolloid der Schilddrüse beruht ebenfalls auf Tyrosin-Untereinheiten.
Krankheiten
[Bearbeiten]Auch in Folge einer Phenylketonurie (PKU) kann es zu einem Mangel an Tyrosin kommen. Über Nahrung aufgenommenes Phenylalanin kann nicht korrekt zu Tyrosin synthetisiert werden, welches dem Körper infolgedessen medikamentös zugeführt werden muss, da es ansonsten zu einer Unterproduktion von Melanin (Albinismus) und Thyroxin (Kretinismus) kommt. Ebenso kommt es zu Problemen bei der Herstellung von Katecholaminen.
Literatur
[Bearbeiten]- Biochemie, Berg/Tymoczko/Stryer, 5. Auflage, Spektrum Akademischer Verlag GmbH Heidelberg 2003, ISBN 3827413036
Monoiodtyrosin
[Bearbeiten]Monoiodtyrosin (MIT), veraltet auch Monojodtyrosin (MJT), ist eine nicht-proteinogene Aminosäure, die aus der proteinogenen Aminosäure Tyrosin durch Iodierung entsteht. Es ist im menschlichen Körper die Vorstufe der Schilddrüsenhormone T3 und T4.
Biosynthese (Mensch)
[Bearbeiten]Monoiodtyrosin wird in der Schilddrüse aus L-Tyrosin und Iodid gebildet. Das L-Tyrosin liegt dabei in Form von an Thyreoglobulin gebundenen Tyrosyl-Resten vor und das Iodid wird mit Hilfe des Enzyms Thyreoperoxidase (TPO) an die Tyrosyl-Reste gebunden; durch Bindung eines Iod-Atoms entsteht zunächst Monoiodtyrosin, durch Bindung eines weiteren Iod-Atoms dann Diiodtyrosin (DIT). Da die TPO Häm als prosthetische Gruppe enthält, kann die Synthese von MIT und DIT (und infolgedessen auch die der Schilddrüsenhormone) durch einen Eisenmangel eingeschränkt sein.[2][3][4][5]
Hormonvorstufe (Mensch)
[Bearbeiten]MIT liegt zusammen mit DIT in der Schilddrüse an Thyreoglobuline (TG) gebunden vor. Die Globuline bilden in dieser Form die unmittelbare Vorstufe der in der Schilddrüse produzierten Schilddrüsenhormone. Durch Zusammenlagerung (Koppelung über eine Etherbrücke[6]) im TG-Molekül von einem MIT- und einem DIT-Molekül wird T3 (ca. 11 μg/Tag[5]), durch Zusammenlagerung von zwei DIT-Molekülen T4 (ca. 100 μg/Tag[5]) gebildet. In der Schilddrüse wird T3 sowohl in Form von 3,5,3'-Triiodthyronin (T3, ca. 10 μg/Tag) als auch als inaktives[7] 3,3',5'-Triiodthyronin (rT3, für: reverses Triiodtyronin, ca. 1 μg/Tag) gebildet.[5] Auch bei diesen Koppelungsvorgängen ist wieder die Thyreoperoxidase beteiligt. [2][3][5]
Die entstandenen Hormone werden jedoch nicht frei, sondern in an Transportproteine (Thyroxin-bindendes Globulin|TBG, Transthyretin|TTR, Thyroxin-bindendes Albumin|TBA, Thyroxin-bindendes Präalbumin|TBPA, Sexualhormon-bindendes Globulin|SHBG) gebundener, inaktiver Form in den Blutkreislauf abgegeben. Sie liegen im Blut zu über 99% (T4 zu 99,95%, T3 zu 99,7%[2]) in an Proteine gebundener Form vor und erst bei Bedarf bildet der Körper aus den gebundenen Schilddrüsenhormonen freie, aktive Hormone. Dabei wird freies T4 (fT4) durch einfache Freisetzung des T4 aus seiner Eiweißbindung gebildet. Freies T3 (fT3) und inaktives[7] rT3 wird sowohl unmittelbar durch Freisetzung aus seiner Eiweißbindung, größtenteils aber mittelbar mit Hilfe von Thyroxindeiodasen im Zytoplasma der Zielzelle aus freiem, in die Zelle eingewandertem T4 durch Abspaltung eines Iod-Atoms
- an der 5'-Position (=T3, ca. 25 μg aus den 100 μg tgl. erzeugten T4)[5] oder
- an der 5-Position (=rT3, ca. 35 μg aus den 100 μg tgl. erzeugten T4)[5]
gewonnen. Da die Thyroxindeiodasen selenhaltige Enzyme sind, kann die Synthese von fT3 in den Zielzellen durch einen Selenmangel eingeschränkt sein. [2][3][4][5]
Es ist zu beachten, dass einerseits T4 den Großteil der in der Schilddrüse gebildeten Schilddrüsenhormone ausmacht, andererseits der Großteil des im Körper bzw. in den Zellen freigesetzten fT3 mittelbar aus in die Zielzelle eingewandertem fT4 hergestellt wird.[2][3][5][6] Somit ist MIT lediglich die unmittelbare Vorstufe des in geringen Mengen in der Schilddrüse produzierten T3, hauptsächlich aber mittelbare Vorstufe der aus DIT produzierten Schilddrüsenhormonanteile.
Weblinks
[Bearbeiten]- 3-Iodo-Tyrosine bei DrugBank
- Thyroperoxidase (EC 1.11.1.8) (engl.) bei ExPASy
- Thyroxine 5'-deiodinase (EC 1.97.1.10) (engl.) bei ExPASy
- Thyroxine 5-deiodinase (EC 1.97.1.11) (engl.) bei ExPASy
- Diiodotyrosine transaminase (EC 2.6.1.24) (engl.) bei ExPASy
Diiodtyrosin
[Bearbeiten]
Diiodtyrosin (DIT), veraltet auch Dijodtyrosin (DJT), ist eine nichteiweißbildende Aminosäure, die aus der proteinogenen Aminosäure L-Tyrosin durch Iodierung entsteht. Es ist im menschlichen Körper eine Vorstufe der Schilddrüsenhormone T3 und T4.
Verwendung
[Bearbeiten]Diiodtyrosin wird als Arzneimittel bei Schilddrüsenerkrankungen (Thyreostatikum) eingesetzt.[8] Darüberhinaus ist es ein Anti-Frost-Protein-Hemmer.[9]
Biologische Bedeutung
[Bearbeiten]Biosynthese (Mensch)
[Bearbeiten]Diiodtyrosin wird in der Schilddrüse aus L-Tyrosin und Iodid gebildet. Das L-Tyrosin liegt dabei in Form von an Thyreoglobulin gebundenen Tyrosyl-Resten vor und das Iodid wird mit Hilfe des Enzyms Thyreoperoxidase (TPO) an die Tyrosyl-Reste gebunden; durch Bindung eines Iod-Atoms entsteht zunächst Monoiodtyrosin (MIT), durch Bindung eines weiteren Iod-Atoms dann Diiodtyrosin. Da die TPO Häm als Bestandteil enthält, kann die Synthese von MIT und DIT (und infolgedessen auch die der Schilddrüsenhormone) durch einen Eisenmangel eingeschränkt sein.[2][3][4][5]
Hormonvorstufe (Mensch)
[Bearbeiten]Diiodtyrosin ist beim Menschen die Vorläufersubstanz des Schilddrüsenhormons L-Thyroxin (T4) und einer der Vorläufersubstanzen des Schilddrüsenhormons Triiodthyronin (T3).
DIT liegt zusammen mit MIT in der Schilddrüse an Thyreoglobuline (TG) gebunden vor. Durch Zusammenlagerung (Koppelung über eine Etherbrücke[6]) im TG-Molekül von einem MIT- und einem DIT-Molekül wird T3 (ca. 11 μg/Tag[5]), durch Zusammenlagerung von zwei DIT-Molekülen T4 (ca. 100 μg/Tag[5]) gebildet. In der Schilddrüse wird T3 sowohl in Form von 3,5,3'-Triiodthyronin (T3, ca. 10 μg/Tag) als auch als inaktives[7] 3,3',5'-Triiodthyronin (rT3, für: reverses Triiodtyronin, ca. 1 μg/Tag) gebildet.[5] Auch bei diesen Koppelungsvorgängen ist wieder die Thyreoperoxidase beteiligt. [2][3][5]
- DIT ist die Hauptvorstufe sowohl von (in den Zielzellen gebildetem) fT3 als auch von T4/fT4,
- MIT ist die unmittelbare Vorstufe des in geringen Mengen in der Schilddrüse produzierten T3, hauptsächlich aber mittelbare Vorstufe der aus DIT produzierten Schilddrüsenhormonanteile,
- fT4 die unmittelbare Hauptvorstufe von fT3.
Obwohl DIT Vorstufe von Schilddrüsenhormonen ist, kann es nicht durch vermehrte (künstliche) Zufuhr zur Steigerung der Schilddrüsenhormonproduktion verwendet werden, da es paradoxerweise als Thyreostatikum[8] wirkt.
Weblinks
[Bearbeiten]- 3,5-Diiodotyrosine bei DrugBank
- Thyroperoxidase (EC 1.11.1.8) (engl.) bei ExPASy
- Thyroxine 5'-deiodinase (EC 1.97.1.10) (engl.) bei ExPASy
- Thyroxine 5-deiodinase (EC 1.97.1.11) (engl.) bei ExPASy
- Diiodotyrosine transaminase (EC 2.6.1.24) (engl.) bei ExPASy
Thyreoperoxidase
[Bearbeiten]Speicherung von T3 und T4 in der Schilddrüse
[Bearbeiten]Thyreoglobin TG
[Bearbeiten]Follikel
[Bearbeiten]Kolloid
[Bearbeiten]Selen in der Schilddrüse
[Bearbeiten]Selen spielt eine wichtige Rolle bei der Produktion der Schilddrüsenhormone, genauer bei der „Aktivierung“ von Thyroxin (T4) zu Triiodthyronin (T3).
Selen ist Bestandteil eines Enzyms, der Thyroxin-5'-Deiodase, die für die Entfernung eines Iodatoms aus T4 verantwortlich ist. Durch diese Deiodierung entsteht T3. Ein Selenmangel führt zu einem Mangel an Thyroxin-5'-Deiodase, wodurch nur noch ein Teil des verfügbaren T4 deiodiert werden kann. Da T3 im Stoffwechsel wesentlich wirksamer ist, resultiert aus einem T3-Mangel eine Schilddrüsenunterfunktion. Eine zusätzliche Einnahme von Selenpräparaten (Natriumselenit) in hohen Dosen von 200–300 μg täglich ist nach ärztlicher Abklärung z. B. bei Hashimoto-Thyreoiditis wahrscheinlich sinnvoll, da damit die Höhe der Antikörpertiter reduziert werden kann. Ob die Ausbildung einer Hypothyreose verhindert werden kann, ist noch offen.[10]
Vergleiche dazu auch:
- D. Behne, A. Kyriakoupoulos, H. Meinhold, J. Köhrle: Identification of type I iodothyronine 5'-deiodinase as a selenoenzyme. In: Biochem. Biophys. Res. Comm. 173, 1143–1149, 1990 [2]
- J. R. Arthur, F. Nicol und G. J. Beckett: Selenium deficiency, thyroid hormone metabolism, and thyroid hormone deiodinases. In: Am. J. Clinical Nutrition, 57, 236–239, 1993 [3].
- C. Ekmekcioglu C: Spurenelemente auf dem Weg ins 21. Jahrhundert – zunehmende Bedeutung von Eisen, Kupfer, Selen und Zink. In: Journal für Ernährungsmedizin, 2 (2), 18–23, 2000,
Siehe *http://www.trace-elements.org/Service/Jod/Jod_und_Selen/jod_und_selen.html
Transport der SD Hormone im Blut
[Bearbeiten]L-Thyroxin (T4) liegt beim Menschen im Blut zu über 99,9 % an Transportproteine gebunden vor, nur etwa 0,03 % sind freies Hormon (fT4). Trijodthyronin (T3) ist ebenfalls zu über 99 % gebunden, etwa 0,3 % sind frei (fT3).
Das Thyroxin-bindendes Globulin (TBG) ist das wichtigste Transportprotein für Schilddrüsenhormone im Blut.
Weitere Proteine, die mit niedrigerer Affinität T4 und T3 binden können, sind Transthyretin (TTR) sowie unspezifisch auch Albumin oder Präalbumin. Dies macht einen kleineren Anteil aus. Auch SHBG (Sexualhormon-bindendes Globulin) vermag die Schilddrüsenhormone zu binden.
TBG besitzt zum eine außergewöhnlich hohe Bindungsaffinität zu Thyroxin (T4) und Trijodthyronin (T3). Außerdem weist es eine große Spezifität für T3 und T4 auf.
TBG
[Bearbeiten]
Die Primärstruktur von TBG besteht aus 395 Aminosäuren.[11] TBG besitzt einer Molekülmasse von etwa 54 kDalton. Es kann pro Molekül ein Molekül Schilddrüsenhormon binden. Seine Serum-Konzentration beträgt beim Menschen etwa 260 nmol/l (15 µg/ml). Da durch die Proteinbindung die schnelle Ausscheidung über die Niere verhindert wird, beträgt die biologische Halbwertszeit von T4 etwa 5 bis 8 Tage, für T3 nur etwa 19 Stunden, da es eine 10 bis 20fach geringere Affinität zu TBG hat und an Transthyretin überhaupt nicht bindet. Das biologisch inaktive rT3 hat eine noch geringere Bindung an die Serumproteine und daher nur eine Serum-Halbwertszeit von etwa vier Stunden.
Die Gesamt-Konzentration von T4 und T3 – nicht aber die Konzentration der biologisch wirksamen freien Hormone – hängt im Wesentlichen von der Konzentration und Zusammensetzung der Bindungsproteine ab.
Normalwerte
[Bearbeiten]TBG wird aus 1 ml Serum bestimmt.
Altersgruppe Normbereich -------------------------------------- Kinder bis 15 Jahre 2,0-3,0 mg/dl Erwachsene 1,6-3,0 mg/dl
TBG erhöht bei
[Bearbeiten]- Schwangerschaft
- Östrogenerhöhungen: z.B. Ovulationshemmer
- Androgene
- Hypothyreose
- konnatal: angeborener TBG-Exzeß: ~1:6000 bis 1:17.600 Geburten
- hereditärere TBG-Varianten mit veränderter Affinität zu T4 (sehr selten)
erniedrigt
[Bearbeiten]- kongenital: angeborener kompletter TBG-Mangel: Werte <5 mg/l ~1:15 000 Geburten
- partieller TBG-Mangel: ~1:5000 Geburten
- Eiweißverluste (enteral, renal)
Quellen
[Bearbeiten]- ↑ Europäischer FOREGS-Atlas, 2005 (Forum of the European Geological Surveys Directors, Text/PDF, Karte)
- ↑ 2,0 2,1 2,2 2,3 2,4 2,5 2,6 Abschnitt Physiologie in „Schilddrüse“ bei DPC-Bühlmann GmbH
- ↑ 3,0 3,1 3,2 3,3 3,4 3,5 Aritikel „Jod“ im Lexikon für Orthomolekulare Medizin – Vitalstoff-Lexikon
- ↑ 4,0 4,1 4,2 Abschnitt 1.5.3 in Jörg Sasse: Dissertation: „Plasmakonzentrationen von Prolaktin, Cortisol, Trijodthyronin und Thyroxin bei Schlafentzug-Respondern unter Tryptophan-Depletion im Rahmen einer endogenen Depression“. Medizinische Fakultät Charité der Humboldt Universität zu Berlin, 10. Oktober 2000.
- ↑ 5,00 5,01 5,02 5,03 5,04 5,05 5,06 5,07 5,08 5,09 5,10 5,11 5,12 5,13 Abschnitt 1.1.2 in Katarzyna Agata Fischmann: Inaugural-Dissertation: „Veränderungen der Schilddrüsenparameter TSH, fT3 und fT4 im Verlauf einer Entgiftungs-/Entwöhnungstherapie bei Alkoholkranken“. Medizinische Fakultät der Eberhard-Karls-Universität zu Tübingen, 2005.
- ↑ 6,0 6,1 6,2 Abschnitt 1.1.1 in Christoph Kraft: Inaugural-Dissertation: „Der Einfluß von Triiodtyronin auf die extrazelluläre Matrix von Rattenherzen und Rattennieren“. Fachbereich Humanmedizin der Justus-Liebig-Universität Giessen, 2001.
- ↑ 7,0 7,1 7,2 Thyroxine 5-deiodinase (EC 1.97.1.11) (engl.) bei ExPASy
- ↑ 8,0 8,1 ATC-H03BX01-Eintrag (engl.) bei ATC/DDD Index 2007
- ↑ 3,5-Diiodotyrosine (DB03374). in: DrugBank
- ↑ http://edoc.ub.uni-muenchen.de/archive/00000751/
- ↑ UniProt P05543
Transthyretin (TTR, Thyroxin bindendes Präalbumin, TBPA) ist ein Serumtransportprotein, das vorwiegend in der Leber gebildet wird. Es ist am Transport der Schilddrüsenhormone beteiligt.
Transthyretin (TTR) hat eine mäßig hohe Affinität und mäßig hohe Kapazität für T4, so dass es etwa 15 % des T4 bindet. Seine Bindungskapazität für T3 ist so niedrig, dass es kaum T3 bindet. Seine Konzentration im Serum liegt bei 250 mg/l. Es weist eine strukturelle Verwandtschaft mit verschiedenen gastrointestinalen Proteohormonen auf (Döcke, Friedemann 1994).
In der Serumelektrophorese wandert Transthyretin vor der Albuminfraktion (Präalbumin). Es ist beteiligt an der Bindung von Thyroxin und Retinol und hat eine molare Masse von ca. 55 kDa. Bei chronisch-aktiven Entzündungszuständen ist Transthyretin vermindert. Es wird daher als Anti- Akute-Phase-Protein bezeichnet.
Im Alter ist Transthyretin an der Entstehung der senilen Amyloidose beteiligt. Genetisch veränderte Varianten des Transthyretin können zu vererblichen Amyloidosen mit autosomal-dominantem Erbgang führen.
Transport durch Zellmembranen
[Bearbeiten]Schilddrüsenhormone sind lipophile (fettlösliche} Substanzen, so dass sie passiv durch Zellmembranen treten können. Dennoch gibt es beim Menschen mindestens 10 verschiedene aktive, energieabhängige und genetisch regulierbare Transporter (humane Iodothyronintransporter). Damit wird erreicht, dass der Spiegel von Schilddrüsenhormonen in der Zelle höher als im Blutplasma oder in Gewebeflüssigkeiten liegt[1].
Einzelnachweise
[Bearbeiten]- ↑ Dietrich, J. W., K. Brisseau und B. O. Boehm (2008). "Resorption, Transport und Bioverfügbarkeit von Schilddrüsenhormonen." Deutsche Medizinische Wochenschrift 133 (31/21): 1644-8. DOI 10.1055/s-0028-1082780 PMID 18651367
Umbau und Abbau der SD-Hormone
[Bearbeiten]Ein Enzym namens Dejodase spaltet aus dem T4 ein Jodatom ab und wandelt so die Hormonvorstufe T4 in das zehnfach aktivere T3 um.
Deiodase
[Bearbeiten]Die menschliche Typ I 5'-Deiodase sitzt vor allem in der Leber, Niere, Schilddrüse und Hypophyse. Sie ist ein Schlüsselenzym der Schilddrüsenhormonwirkung, da sie Thyroxin (T4) zum biologisch aktiven T3 umbaut.
Auch nach einer kompletten Entfernung der Schilddrüse reicht die Dejodase in den Organen außerhalb der Schilddrüse völlig aus, um genügend T3 aus dem T4 zu bilden.
Deiodase ist ein Selenoenzyme, d.h. Selen ist als Spurenelement in dem Emzym vorhanden.
Die Deiodase wird durch verschiedene Einflüsse in ihrer Aktivität verändert:
Bremsend auf die Dejodase wirken
[Bearbeiten]- verschiedene Tumoren,
- akute Entzündungsreaktionen
- "Niederes-T3-Syndrom"
- Amiodaron
Als Folge ist die T3-Bildung reduziert.
Grafik des Umbaus und Abbaus der Schilddrüsenhormone
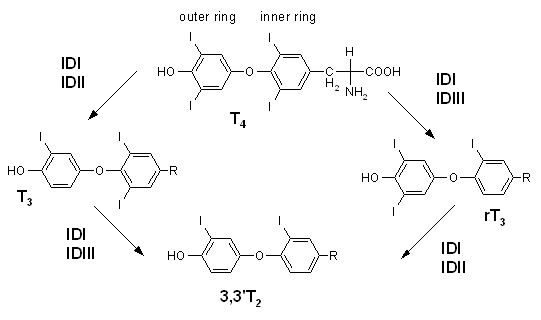
Wirkung von T3 und T4
[Bearbeiten]T3 = Trijodthyronin T4 = Thyroxin
Schilddrüsenhormone sind für den Menschen und wohl alle höheren Tiere lebenswichtig
Schilddrüsenhormone sensibilisieren die Körperperipherie gegenüber den Katecholaminen Adrenalin und Noradrenalin.
Wachstum:
- Schilddrüsenhormonmangel führt zu Verzögerungen beim Knochenwachstum und bei der Gehirnreifung.
Energiestoffwechsel:
- Schilddrüsenhormone steigern den Zellstoffwechsel, d. h. den Grundumsatz und erhöhen den Sauerstoffverbrauch.
Eiweiß- und Kohlenhydratstoffwechsel:
- Physiologische Schilddrüsenhormonkonzentrationen fördern, erhöhte Konzentrationen hemmen die Protein- und Glykoproteinsynthese.
Fettstoffwechsel:
- Schilddrüsenhormonmangel verzögert den Cholesterinabbau, ein Hormonüberschuss beschleunigt ihn.
Mineralhaushalt:
- Phosphat- und Kalziumbilanz sind bei Hyperthyreose negativ, bei Hypothyreose positiv.
Herz und Kreislauf: Eine Überfunktion der Schilddrüse
- erhöht die Herzfrequenz,
- das Schlagvolumen und
- die Blutdruckamplitude.
Psyche:
- Eine Unterfunktion der Schilddrüse führt zur Apathie,
- eine Überfunktion zur Übererregbarkeit und manchmal zur Psychose
Muskulatur:
- Bei Hyper- und Hypothyreose kann eine Myopathie auftreten,
- bei einer Hypothyreose sind die Sehneneigenreflexe verlangsamt.
Es bestehen Wechselbeziehungen zwischen der Schilddrüse und anderen endokrinen Organen, nämlich Keimdrüsen und Nebenniere. Dies erklärt die Amenorrhoe bzw. habituelle Aborte bei einer Schilddrüsenfunktionsstörung.
Rezeptoren für Schilddrüsenhormone
[Bearbeiten]TR = thyroid hormone receptor
TRalpha
- wichtig für die postnatale Entwicklung
- und die kardiale Funktion
- DNS auf Chromosom 17
TRbeta
- kontrolliert die Entwicklung des Innenohrs und der Retina
- kontrolliert den Leberstoffwechsel
- kontrolliert die Spiegel der Schilddrüsenhormone
- DNS auf Chromosom 3
- Ursächlich für die periphere SDHormon Resistenz
- (resistance to thyroid hormone (RTH))
Molekulargenetische Diagnostik von Thyreoidea- Hormon-Rezeptor-ß (THRB, THR1, ERBA2) Resistenz
[Bearbeiten]Bei gleichzeitig erhöhten Schildrüsenhormonwerten (fT3, fT4) mit normalen (85%) oder leicht erhöhten (15%) TSH ist an eine THR-Resistenz zu denken. Das klinische Bild der Erkrankung ist sehr variabel. Generell findet man eine Struma, die von Hyperaktivität, Lern-, Hörstörungen, klassischen Symptomen einer Hyperthyreose (z.B. Tachyarrhythmie), Thyreotoxikose usw. bis zur Entwicklungsstörungen von ZNS und Skelett (z.B. Epiphysendysgenesie) begleitet werden kann.
Es gibt mindestens 4 bekannte Rezeptoren der Zielorgane von Schilddrüsenhormonen, die in unterschiedlicher Zusammensetzung gewebsspezifisch vorkommen, unter anderem den alpha-Rezeptor, der vorwiegend im ZNS vorkommt unnd dessen Gen auf dem Chromosom 17 - Bande q11.2- liegt und den ß-Rezeptor, dessen Gen auf dem Chromosom 3 - Bande p24.3- liegt und der hauptsächlich in Zellkernen der Leber vorkommt. Beide Gene sind auch als Tumorgene ERBA-1 bzw. ERBA-2 bekannt.
Molekulargenetische Defekte bei generalisierter THR-Resistenz sind für das THR-ß-Gen beschrieben. Einige Fälle sind sporadisch, wenige auch rezessiv erblich. Die meisten folgen einem dominanten Erbgang (Verlust der Rezeptorfunktion bei Mutation in einer Bindungsdomäne).
Je nach Art der Mutation im THR-ß-Gen können verschiedene Phänotypen auftreten, die darüber hinaus von bisher unbekannten Fktoren zusätzlich variiert werden. Genaue Zahlen über die Häufigkeit der THR-Resistenz sind gegenwärtig nicht bekannt.
Untersuchungsmaterial:
[Bearbeiten]- 5 - 10 ml EDTA-Blut
- Die Proben sollten umgehend auf dem normalen Postwege zugesandt werden.
- Der Befund liegt nach etwa 4 - 6 Wochen vor.
Literatur
[Bearbeiten]- Yen PM, Ando S, Feng X, Liu Y, Maruvada P, Xia X.
- Thyroid hormone action at the cellular, genomic and target gene levels.
- Mol Cell Endocrinol. 2006 Feb 26;246(1-2):121-7. Epub 2006 Jan 25. Review.
- PMID: 16442701
- Thyroid hormone action at the cellular, genomic and target gene levels.
- O. E. Janssen Medizinische Klinik, Klinikum Innenstadt, Ludwig-Maximilians-Universität München, XX
- Resistenz gegen Schilddrüsenhormone
- Der Internist Verlag Springer Berlin / Heidelberg
- Heft Volume 39, Number 6 / Juni 1998 Seiten 613-618
- Resistenz gegen Schilddrüsenhormone
Regelkreis der Schilddrüsenhormonproduktion
[Bearbeiten]Die Freisetzung von Schilddrüsenhormonen wird durch einen mehrschleifigen Regelkreis gesteuert. Man spricht von einer Hierarchie der Hormonregulation.
Die oberste Stufe der Hierarchie befindet sich im Hypothalamus, einem Teil des Gehirnes, welcher auch für andere Hormonsysteme des Körpers die Schaltstelle zwischen Nervensystem und Hormonsystem darstellt. Im Hypothalamus werden sogenannte Releasing-Faktoren gebildet, die in nachgeordneten endokrinen Drüsen die Freisetzung von Hormonen anregen. Einer dieser Freisetzungsfaktoren ist TRH, Thyreotropin-Releasing Hormone. Es bewirkt eine Freisetzung von TSH (Thyreotropin) in der Hypophyse, der Hirnanhangsdrüse. Über diese Zwischenstufe wird dann letztendlich die Schilddrüse selbst angeregt, ihre Hormone T3 und T4 auszuschütten.
Steigt der Hormonspiegel im Blut an, dann erhält der Hypothalamus und die Hypophyse über eine Gegenkoppelung (hemmende Rückkoppelung) die Information: Es ist genügend Hormon im Blut vorhanden. Als Folge wird die Ausschüttung der Freisetzungshormone TRH und TSH wieder zurückgefahren.
Weitere Schleifen des Regelkreises umfassen z. B. einen Ultrashort-Feedback-Mechanismus von TSH auf seine eigene Ausschüttung (Brokken-Wiersinga-Prummel-Regelkreis) und ein Long-Feedback von T4 auf TRH.
Hierarchie der Schilddrüsenhormone
[Bearbeiten] Hypothalamus TRH - Nervenzellen <----
| |
TRH |
| |
| |
V |
Hypophysenvorderlappen <<<-----------|
| | * |
TSH ------- |
| Rückkopplung ( Bremsung der oberen Ebene)
| |
V |
Schilddrüse |
| |
T3,T4 -------->>-------------------
|
|
V
Körperzellen * Prummel-Wiersinga-Regelkreis
Siehe auch
Literatur
[Bearbeiten]- Der Hypophysen-Schilddrüsen-Regelkreis: Entwicklung und klinische Anwendung eines nichtlinearen Modells. Spektrum medizinischer Forschung, Bd. 2 (Taschenbuch)
- von Johannes W. Dietrich (Autor)
- Taschenbuch: 195 Seiten Logos Verlag Berlin (2002) ISBN 3897228505
- von Johannes W. Dietrich (Autor)
TRH
[Bearbeiten]TRH ist die Abkürzung für Thyrotropin releasing Hormon. TRH ist ein Freisetzungshormon, das im Hypothalamus, einem Teil des Gehirnes, gebildet wird. Über das hypothalamisch-hypophysäre Pfortadersystem wird TRH zur Hirnanhangsdrüse (Hypophyse) transportiert. In der Hypophyse stimuliert TRH die Bildung und die Ausschüttung von TSH, dem sogenannten Thyreoidea Stimulierenden Hormon und darüber indirekt auch die Ausschüttung von T3 und T4 in der Schilddrüse.
Neben seiner Hauptwirkung auf die Hypophyse stimuliert TRH auch die Freisetzung von Prolaktin, einem Hormon, welches die Milchproduktion der weiblichen Brust anregt.
Bei Patienten mit Akromegalie oder Riesenwuchs kommt es in etwas der Hälfte der Fälle nach TRH-Gabe zu einem Anstieg der Wachstumshormon-Sekretion. Bei gesunden Personen wird dies nicht beobachtet.
Die Struktur des TRHs wurde 1969 erstmals von den Forschergruppen Guillemin und Schally veröffentlicht.
Es handelt sich um ein L-pyroglutamyl-L-histidyl-L-prolinamid (L-pGlu-L-His-L-ProNH2).
Siehe auch : *[4]
Ein größerer Teil des TRHs hat eine direkte Wirkung im Gehirn, die nichts mit der Wirkung im Schilddrüsenregelkreis zu tun hat. So erklärt sich auch die geringe bremsende Wirkung eines erhöhten Blutspiegels von T3 und T4 auf den TRH Spiegel.
TRH ist als Neurotransmitter im Gehirn
- an der Thermoregulation,
- an der Schmerzunterdrückung
- an der Schlaf-Wachregulation
- an der Bremsung von Nahrungs- und Flüssigkeitsaufnahme
und an einer Vielzahl weiterer Steuerungsvorgänge beteiligt.
TRH hat auch indirekte vegetative Wirkungen:
- Es stimuliert über den Vagusnerv die Magensäureproduktion und die Magen-Darm-Peristaltik
- Es stimuliert über den Sympathikus die Insulinsekretion
- Es stimuliert daneben auch die Bauchspeicheldrüse in ihrer exokrinen Funktion.
- Es steigert Herzfrequenz und Blutdruck.
TSH
[Bearbeiten]
Thyreotropin, auch thyreotropes Hormon oder Thyroidea-stimulierendes Hormon (TSH), ist ein Hormon des Hypophysenvorderlappens mit stimulierender Wirkung auf die Schilddrüse für die Hormonproduktion.
Der am weitesten verbreitete Name für das Hormon ist die Abkürzung TSH.
TSH wird in den basophilen Zellen des Hypophysenvorderlappens gebildet. Es ist ein Proteohormon, d.h. es besteht aus einer längeren Kette von Aminosäuren, und hat ein Molekulargewicht von ca. 28.000 Dalton. TSH regt die Schilddrüse zu vermehrter Hormonproduktion an.
Physiologie
[Bearbeiten]Mit Hilfe des Releasing-Hormons Thyreoliberin (TRH), das durch ein besonderes Portalgefäßsystem in hoher Konzentration zum Hypophysenvorderlappen gelangt, stimuliert der Hypothalamus die Ausschüttung von TSH aus den thyreotropen Zellen. TSH regt dann in der Schilddrüse die Bildung der jodhaltigen Schilddrüsenhormone Thyroxin (T4) und Trijodthyronin (T3) an, zudem fördert es in der Peripherie die Umwandlung von T4 in das wirksamere T3. Umgekehrt hemmen Schilddrüsenhormone im Rahmen des thyreotropen Regelkreises die Ausschüttung von TSH aus dem Hypohysenvorderlappen, so daß schließlich konstante und bedarfsadaptierte Gleichgewichtsspiegel der beteiligten Hormone erreicht werden.
TSH-Mangel, TSH-Überproduktion
[Bearbeiten]Fehlt TSH oder kann es nicht ausreichend produziert werden, dann wird die Schilddrüse immer kleiner und verkümmert. Es resultiert eine hypophysäre Hypothyreose = sekundäre Schilddrüsenunterfunktion.
Produziert die Hypophyse beispielsweise wegen eines TSH produzierenden Adenoms zu viel TSH, dann resultiert eine Schilddrüsenüberfunktion, die man als hypophysäre Hyperthyreose oder auch sekundäre Hyperthyreose bezeichnet.
Diese sekundären Schilddrüsenfunktionsstörungen wegen eines TSH-Mangels oder einer TSH-Überproduktion sind selten.
Schließlich kann es durch Störungen der TRH-Sekretion von seiten des Hypothalamus oder der Signalübermittlung im hypothalamo-hypohysären Portalgefäßsystem (Pickardt-Syndrom) zu sekundären TSH-Mangelerscheinungen oder -überproduktionen und damit zu den sehr seltenen tertiären Hypo- oder Hyperthyreosen kommen.
TRAK hat TSH Wirkung
[Bearbeiten]Erstaunlicherweise hat ein Immunglobulin, welches v.a. bei der autoimmunen Erkrankung Morbus Basedow vermehrt produziert wird (jedoch auch bei an Hashimoto-Thyreoiditis erkrankten Personen vorkommen kann), eine ähnlich stimulierende Wirkung an der Schilddrüse wie das TSH. Dieser Antikörper wird als TRAK = Thyreoidea Rezeptor Antikörper bezeichnet.
Normwerte im Blutserum:
[Bearbeiten]bei vorhandener Schilddrüse:
TSH: 0,3 - 2,5 mU/l
(Der obere Referenzwert wurde 2003 überarbeitet, er war vorher - und ist es in vielen Laborbefunden auch noch 2006 - bis 4,0 mU/l. Grund war die Beobachtung, dass viele Probanden mit TSH-Werten zwischen 2,5 und 4 mU/l zwar zum Bestimmungszeitpunkt gesund waren, bei Langzeitnachuntersuchungen aber eine hohe Tendenz zeigten, später an Autoimmunthyreoiditis zu erkranken. Deshalb wird bei diesen Werten empfohlen, von Zeit zu Zeit auf Antikörper zu testen.)
bei operierter Schilddrüse mit Hormonersatztherapie:
TSH: 0,3 - 1,0 mU/l
TSH kann im Blut bestimmt werden. Bei der primären Schilddrüsenunterfunktion Hypothyreose ist es reaktiv erhöht. Bei der primären Schilddrüsenüberfunktion ist es erniedrigt.
TRH-Test
[Bearbeiten]Mittels des TRH-Tests kann die Stimulierbarkeit des TSH in der Hypophyse überprüft werden. Es werden zwei TSH-Bestimmungen im Abstand von etwa 30 Minuten vorgenommen. Unmittelbar nach der ersten Blutentnahme wird TRH zugeführt (heute zumeist via Nasenspray). Die TRH Gabe von außen regt die TSH-Bildung an, so dass die zweite TSH-Bestimmung in jedem Fall höhere Werte liefert. Hierbei wird eine Erhöhung (2. TSH-Wert minus 1. TSH-Wert) zwischen 2 und 16 mU/l als "normal" eingestuft. Erhöhungen oberhalb von 16 mU/l definieren eine Sonderform der subklinischen Hypothyreose (engl. "Grade 3 Hypothyroidism").
Nach derzeit vorherrschender Lehrmeinung wird der TRH-Test als "weitgehend überflüssig" eingestuft. Als Begründung wird dafür vor allem die heute mögliche hohe Genauigkeit der TSH-Bestimmungsverfahren (zwei Nachkommastellen und höher) angegeben.
Geschichte
[Bearbeiten]- TSH wurde 1929 durch Aron und Löb entdeckt.
- TSH wurde von??? sequenziert.
- 1965 wurde ein erster Radioimmuno-Assay für TSH durch Odell beschrieben.
(Radioimmunoassay of thyrotropin in human serum Odell,W.D., J.F.Wilber,E.E.Paul J.clin. endocr.; Vol: 25, 1965 (1179))
- Seit kurzem gibt es rekombinantes TSH, welches beispielsweise bei der Nachsorgediagnostik des Schilddrüsenkarzinomes eingesetzt wird.
Calcitonin
[Bearbeiten]Das Calcitonin (syn. Kalzitonin, Thyreocalcitonin) ist ein Hormon, das bei Säugetieren in den C-Zellen der Schilddrüse gebildet wird. Bei den übrigen Wirbeltieren erfolgt die Bildung im Ultimobranchialen Körper. Calcitonin reguliert zusammen mit dem Parathormon und dem Vitamin D den Calcium- und Phosphathaushalt des Körpers.
Mit dem Calcitonin verwandt ist das Calcitonin gene related peptide (CGRP). Beide gehen auf ein gemeinsames pimäres mRNA-Transkript zurück. Durch gewebespezifisches alternatives splicen wird in der Schilddrüse vorwiegend Calcitonin gebildet, während im Zentralnervensystem und im peripheren Nervensystem in sensorischen Neuronen hauptsächlich CGRP hergestellt wird.
Geschichte
[Bearbeiten]Calcitonin wurde 1961 von Copp und Cameron entdeckt.
Struktur
[Bearbeiten]Beim menschlichen (hCT) Calcitonin handelt sich um ein Polypeptid aus 32 Aminosäuren mit einem Molekulargewicht von circa 3420 Dalton.
Primärsequenz: H-Cys-Ser-Asn-Leu-Ser-Thr-Cys-Val-Leu-Gly-Lys-Leu-Ser-Gln-Glu-Leu-His-Lys-Leu-Gln-Thr-Tyr-Pro-Arg-Thr-Asp-Val-Gly-Ala-Gly-Thr-Pro-NH2
Eine Ringstruktur gebildet durch eine Disulfidbrücke zwischen Cys1 und Cys7 und ein amidierter C-Terminus (Prolinamid) sind wichtig für die biologische Aktivität. CT(8-32) ohne die Ringstruktur bindet zwar an den Calcitonin-Rezeptor, bewirkt aber keine Rezeptoraktivierung, sondern wirkt als kompetitiver Antagonist.
Siehe http://www.personal.psu.edu/users/s/m/smk249/calcitonin.gif
Regulation und Wirkung
[Bearbeiten]Die Calcitoninfreisetzung wird stimuliert durch:
- hohes Calcium
- gastrointestinale Hormone,
- Pentagastrin
Calcitonin senkt den Blutcalciumspiegel. Es hemmt die Calciumfreisetzung aus dem Knochen (Osteoklasten werden gebremst). Außerdem erhöht es die Calcium-Ausscheidung über die Niere.
Calcitonin hat in höherer Dosierung beim Menschen eine diuretische Wirkung. Diese vermehrte proximale Natriurese wird circa 80 Minuten nach der intravenösen Calcitoningabe durch eine vermehrte distale Natriumreabsorption wieder ausgeglichen.
Im Vergleich zu den anderen calciumregulierenden Hormonen Parathormon (PTH) und D-Hormon (Calcitriol) scheint Calcitonin allerdings eine stark untergeordnete Rolle zu spielen.
Therapie
[Bearbeiten]Calcitonin wird als Lachscalcitonin zur Senkung stark erhöhter Calciumspiegel eingesetzt. Außerdem wirkt es bei Knochenmetastasen schmerzlindernd. Als Nebenwirkung kann dabei ein Flush auftreten.
Blutspiegel
[Bearbeiten]Das Calcitonin wird als Tumormarker beim medullären Schilddrüsenkarzinom verwendet.
Der Normalwert bei Erwachsenen ist kleiner als 100 ng/l.
Einen zu niedrigen Calcitoninwert findet man bei einer Schilddrüsenunterfunktion.
Einen zu hohen Wert findet man bei:
- manchmal bei der Schilddrüsenüberfunktion
- beim medullären Schilddrüsenkarzinom
- Niereninsuffizienz
- Leberzirrhose
Literatur
[Bearbeiten]- Azria, M.: Calcitonins. Physiology and Pharmacology. Freiburg 1988.
- Keck, E.: Calcitonin und Calcitonintherapie. Stuttgart 1996.
Links
[Bearbeiten]- Gut verständliche Zusammenfassung
- Roche Lexikon
- http://www.igb.fhg.de/WWW/GF/MolBiotech/pharmaproteine/dt/Calcitonin.html
- synthetisches Calcitonin
- Ärzteblatt
- Muß man bei einer Struma nodosa Calcitonin mitbestimmen ??
Entwicklung und Fehlbildungen der Schilddrüse
[Bearbeiten]
Einleitung
[Bearbeiten]In der Entwicklungsgeschichte der Schilddrüsenhormone sind 3 Fragen besonders interessant:
1.Wann gab es in der Evolution der Tiere erstmals so etwas wie Schilddrüsenhormon-produzierende Zellen und später so etwas wie eine kompakte Schilddrüse ?
2.In welchem Abschnitt der Embryonalentwicklung entsteht die Schilddrüse und welche Fehlbildungen lassen sich aus der Ontogenese erklären ?
3.In welchem Maße wird die Entwicklung eines Tieres durch die Schilddrüsenhormone beeinflußt und welche Entwicklungsstörungen lassen sich durch einen Mangel oder einen Überschuß an Schilddrüsenhormon erklären ?
Interessant ist, daß die ersten groben Messungen des Schilddrüsenhormonspiegels mittels eines biologischen Testes an Kaulquappen durchgeführt wurden. Man hatte beobachtet, daß beim Vorhandensein von Schilddrüsenhormon in der Kaulquappennahrung eine zu schnelle Umwandlung der Kaulquappe in den Frosch erfolgt.
Die Metamorphose wird bei den Fröschen durch die Schilddrüsenhormone ausgelöst.
Entfernt man bei der Kaulquappe die Schilddrüse oder hemmt die Funktion chemisch, so unterbleibt die Metamorphose. Die Tiere wachsen zu Riesenlarven heran.
Die Verfütterung von Schilddrüsengewebe oder -hormonen an junge Larven führt hingegen zu einer verfrühten Metamorphose.
Die Umwandlung der Kaulquappe wird durch einen allmählich ansteigenden Spiegel an Schilddrüsenhormonen gesteuert, wobei manche Gewebe bereits auf niedrige Hormonkonzentrationen ansprechen: So beginnt die Entwicklung der Beine bei niedrigeren Konzentrationen und damit früher als die Resorption des Schwanzes.
Siehe auch:
- http://www.bossert-bcs.de/biologie/amphentw.htm
- Schulversuch zur Amphibienentwicklung
- http://www.trace-elements.org/Service/Jod/Evolution/evolution.html
- Evolution der biologischen Funktionen von Jod
- http://www.froschkeller.de/download/nitrat.pdf
- Einfluß der Nitratkonzentration auf die Froschentwicklung
Evolution der Schilddrüse
[Bearbeiten]In der Phylogenese lässt sich die Schilddrüse auf das bei den basalen Chordatieren vorhandene Endostyl zurückführen, bei anderen wirbellosen Tieren sind keine gleichwertigen Strukturen vorhanden. Das Endostyl bildet bei den Schädellosen, den Manteltieren sowie den Ammocoetes-Larven der Neunaugen eine vorne im Kiemendarm gelegene Flimmerrinne, die sogenannte Hypobranchialrinne, mit einem Drüsenepithel.

Die Zellen des Endostyls reichern Jod aus der Umgebung an und bauen dieses in Moleküle des Hormons Thyroxin ein. Das Drüsenepithel produziert ein Schleimnetz, welches sich über die Kiemenspalten legt und mit dem im Kiemendarm gefilterte Nahrungspartikel eingefangen werden.
Dieses wird in der Epibrachialrinne gesammelt und gibt die enthaltenen Nährstoffe an das darüberliegende Dorsalgefäß ab.
( Quelle Alfred Goldschmid: Chordata, Chordatiere. in: Westheide, Rieger (Hrsg.): Spezielle Zoologie. Teil 1: Einzeller und Wirbellose Tiere. Gustav Fischer, Stuttgart/Jena 1997, 2004; Seiten 835ff. ISBN 3-8274-1482-2 )
In der weiteren Entwicklung innerhalb der Wirbeltiere verliert der Kiemendarm seine Funktion bei der Nahrungsaufnahme und dient weitgehend zur Atmung, während die Nahrung über die nun kieferbewehrte Mundöffnung aufgenommen und im Darm verdaut wird. Das Schilddrüsengewebe befindet sich entsprechend bei den basalen Wirbeltieren (Knorpel- und Knochenfische) vorne im Bereich der Kiemen während sie bei den Landwirbeltieren vor der Luftröhre im Bereich des Kehlkopfes lokalisiert ist. Embryonal wird sie bei allen Wirbeltieren im ventralen Kiemendarmepithel gebildet und sie stellt bei allen Wirbeltieren eine Ansammlung von Drüsenzellen dar, die von Bindegewebe umgeben ist.
(Quelle: Westheide, Rieger (Hrsg.): Spezielle Zoologie. Teil 2: Wirbel- und Schädeltiere. Gustav Fischer, Stuttgart/Jena 1997, 2004; Seiten 130ff. ISBN 3-8274-1482-2)
Bei den Knorpelfischen liegt die Schilddrüse als scheibenförmige Drüse im Bereich des Unterkiefers. Bei vielen Knochenfischen ist die kompakte Drüse aufgelöst und bildet mehrere Zellhaufen im Bereich der Verzweigung der Ventralaorta, wobei häufig mehrere kleine akzessorische Schilddrüsen weit ab der Hauptschilddrüse liegen.
(Quelle Alfred F. Romer, Thomas S. Parsons: Vergleichende Anatomie der Wirbeltier. 5. Auflage, Paul Parey Verlag, Hamburg und Berlin 1991; Seiten 534 ff. ISBN 3-490-11218-0)
Bei ihnen treten auch die zwei paarigen Nebenschilddrüsen (Glandulae parathyreoideae) erstmals auf, die sich gemeinsam mit dem Thymus und dem Ultimobranchialkörper im Epithel des Kiemendarms im Bereich der vierten und fünften Kiementaschen entwickeln. Letztere werden bei den Säugetieren als Calcitonin-produzierende Zellen (C-Zellen) in die Schilddrüse eingelagert.
Bei allen Landwirbeltieren bildet die Schilddrüse wieder kompakte Organe. Sie sind bei den Amphibien als unpaare Schilddrüsen seitlich am Kehlkopf ausgebildet, wobei die Nebenschilddrüsen bei neotänen Amphibien, die während ihres gesamten Lebens Kiemen besitzen, fehlen. Bei den Amphibien sind die Schilddrüsenhormone an der ontogenetischen Entwicklung beteiligt und kontrollieren die Metamorphose von der Larve zum adulten Tier.
Bei Reptilien ist die Schilddrüse unpaar und liegt an der Aufspaltung der großen Halsgefäße. Bei Vögeln liegen beide Schilddrüsen als kleine Knötchen an der Luftröhre vor dem Brusteingang, etwa in Höhe des Schlüsselbeins und damit viel weiter unten als bei den anderen Wirbeltieren. Die Mauser der Vögel wird durch den Einfluß der Schilddrüsenhormone verstärkt.
Wie beim Menschen besteht die Schilddrüse der meisten Säugetiere aus zwei Seitenlappen, die über eine schmale Engstelle (Isthmus) miteinander verbunden sind. Dieser Isthmus kann aus Drüsengewebe (Isthmus glandularis, z. B. bei Raubtieren) oder nur aus Bindegewebe (Isthmus fibrosus, z. B. bei Pferden bestehen, bei einigen Arten auch ganz fehlen. Ein Rest des Ductus thyreoglossus tritt beim Menschen oft in Form eines Lobus pyramidalis auf. Die Schildform ist nur für den Menschen, Affen und Schweine typisch.
Entwicklung der Schilddrüse beim Menschen
[Bearbeiten]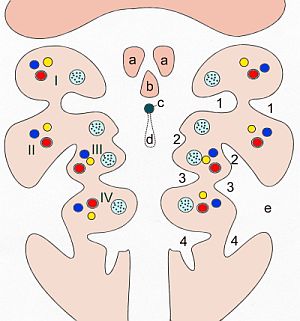
I-IV Kiemenbogen, 1-4 Schlundtaschen (innen) bzw. Kiemenfurchen (außen), a Tuberculum laterale, b Tuberculum impar, c Foramen cecum, d Ductus thyreoglossus, e Sinus cervicalis
Embryonal entsteht die Schilddrüse aus einer Aussprossung vom Boden des Kopfdarms im Bereich der Kiemenbogen. Dieser sogenannte Ductus thyroglossus (Schilddrüsenzungengang) verschließt sich aber normalerweise, so dass die definitive Schilddrüse keine Verbindung mehr zum Kopfdarm hat.
In die Schilddrüsenanlage wandern zudem bei den Säugetieren noch Zellen aus der 4. Schlundtasche ein, aus denen sich die C-Zellen entwickeln. Diese bilden bei Vögeln noch ein eigenes Organ .(Ultimobranchialer Körper).
Aus dem Wandbereich der 4. Schlundtasche entsteht auch das obere Epithelkörperchen.
Fehlbildungen
[Bearbeiten]- Aplasie
- ( Völliges Fehlen der Schilddrüse)
- Hypoplasie
- ( zu kleine Schilddrüse)
- Zungengrundstruma
- ( Reste der Schilddrüseanlage bleiben am Zungengrund liegen und bilden dort Schilddrüsengewebe )
- Persistierender Ductus thyroglossus
Tabelle genetischer Ursachen einer angeborenen Schilddrüsenunterfunktion
[Bearbeiten]Kretinismus
[Bearbeiten]Siehe SD Krankheiten Kretinismus
Literatur
[Bearbeiten]- Über die Wirkung der Schilddrüse auf Kaulquappen
- Adolf Jarisch Institut für experimentelle Pharmakologie der Universität Graz, Österreich
- Zeitschrift Pflügers Archiv European Journal of Physiology Verlag Springer Berlin / Heidelberg
- Heft Volume 179, Number 1 / Dezember 1920 Seiten 159-176
Unter dem Einflusse einer einmaligen entsprechend grossen Gabe von Schilddrüsensubstanz werden die Larvenorgane der Kaulquappen in kürzester Zeit zurückgebildet. Die Rückbildung betrifft auch die Kiemen, und deshalb ersticken die Tiere.
- Der Einfluß der Schilddrüse auf Entwicklung und Wachstum von Amphibienlarven unter verschiedenen Ernährungsbedingungen
- Zeitschrift Clinical and Experimental Medicine Verlag Springer Milan Heft Volume 103, Number 1 / April 1938 Seiten 163-169
- Heinz Doetsch Anthropologischen Institut der Universität Köln, Köln, Deutschland
Links
[Bearbeiten]- http://www.diss.fu-berlin.de/2007/376/ambrugger1.pdf
- DISSERTATION: Störungen der Schilddrüsenhormonsynthese und des Schilddrüsenhormontransportes
Symptome bei Schilddrüsenkrankheiten
[Bearbeiten]
Symptome bei Schilddrüsenkrankheiten
[Bearbeiten]Anamnese
[Bearbeiten]siehe Schilddrüse:_Untersuchung#Anamnese_Vorgeschichte_erfragen
Liste
[Bearbeiten]- Kloßgefühl im Hals
- Gewichtszunahme
- Gewichtsabnahme
- Schwitzen
- Kropf
- Haarausfall
- Zuckerkrankheit
- Herzrasen
- Herzrhythmusstörungen
- Abgeschlagenheit
- Leistungsabfall
- Sexualprobleme
- Unerfüllter Kinderwunsch
- Durchfall
- Verstopfung
- Muskelschwäche
- Probleme in der Schwangerschaft
- Augenprobleme
- Wasser in den Beinen
- Schmerzen im Hals
- Knotenbildung am Hals

Systematisch
[Bearbeiten]- Lokale Beschwerden im Halsbereich
- Störungen des Allgemeinbefindens
- Herz-Kreislaufstörungen
- Augenbeschwerden
- Gewichtsveränderungen
- Verdauungsprobleme
- Haut und Haare
- Sexualprobleme
- Unerfüllter Kinderwunsch
- Schilddrüsenprobleme in der Schwangerschaft
- Bösartige Schilddrüsenerkrankungen
Literatur
[Bearbeiten]Kann man aus Anamnese und Untersuchung eine Hyper- oder Hypothyreose vermuten ?
[Bearbeiten]- Can the initial clinical assessment of thyroid function be improved?
- White GH, Walmsley RN (1978).
- Lancet ii: 933-5
- White GH, Walmsley RN (1978).
Symptome bzw. Zeichen für mögliche Schilddrüsenfunktionsstörungen ( Hyperthyreose oder Hypothyreose)
500 konsekutive Patienten (stationär + ambulant),
- bei denen Labortests durchgeführt wurden
- und eine vorher bekannte SD-Erkrankung ausgeschlossen war
wurden auf Schilddrüsenspezifische Symptome befragt und untersucht
Folgende 27 Symptome bzw. Zeichen wurden abgefragt oder untersucht:
- schilddrüsenbezogen (metabolisch)
- Schilddrüsenvergrößerung,
- Schilddrüsenknoten,
- feiner Tremor,
- Gewichtsverlust,
- Appetitzunahme,
- enge Lidspalten,
- vermehrtes Schwitzen,
- Wärmeintoleranz,
- Familienanamnese für SD-Erkrankung
- Lethargie,
- Gewichtszunahme,
- Heiserkeit,
- trockene Haut,
- Haarausfall,
- Kälteempfindlichkeit,
- verzögerte Reflexe,
- Obstipation,
- Kleinwuchs
- kardiovaskulär
- Arrhythmien,
- beschleunigter Puls > 90/min
- Myokardinfarkt,
- chronische Herzinsuffizienz,
- koronare Herzkrankheit,
- Hypertonie
- andere
- Pneumonie,
- Asthma,
- Diabetes
Erst bei dem Vorhandensein von 5 oder mehr Symptomen konnte man mit mehr als 70 % von einer Schilddrüsenerkrankung ausgehen.
Anzahl der Anzahl der Anzahl mit % mit Symptome/Zeichen Patienten SD-fkt.stör. SD-fkt.stör. ------------------------------------------------------------ 5 oder > 5 23 18 78 % 3 oder 4 35 1 2,9 % 0,1 oder 2 442 2 0,45 % --------------------------------------------------------------------------------------- Gesamt 500 21 4,2 %
Untersuchung der Schilddrüse
[Bearbeiten]
Einleitung
[Bearbeiten]Die Schilddrüse läßt sich mittlerweile recht schön mit verschiedenen Methoden untersuchen. Die wichtigsten Methoden zu Untersuchung der Schilddrüse sind
- die Laborwerte aus dem Blut,
- der Ultraschall und
- das Szintigramm.
Seltener angewendet werden die Zytologie, die Biopsie, die Kernspinuntersuchung, das CT und andere Untersuchungsverfahren.
Übersicht
[Bearbeiten]- Beschwerden des Patienten erfragen (Anamnese)
- Inspektion und tastende Untersuchung des Halses
- Laborwerte
- Ultraschall der Schilddrüse
- Szintigrafie der Schilddrüse (nuklearmedizinische Untersuchung der SD, SD Scan)
- Feinnadelpunktion der Schilddrüse
- Biopsie der Schilddrüse (Histologie)
- Computertomografie der Schilddrüse
- Kernspintomografie der Schilddrüse
- Andere Untersuchungsverfahren
- Röntgen d. Luftröhre (Trachealstenose?)
- EKG, Echo (Puls zu schnell? zu langsam? Herz überaktiv oder träge)
- LangzeitEKG (mittl. Herzfrequenz zu schnell? zu langsam?)
- CT der Hypophyse (sekundäre Hyper- oder Hypothyreose?)
- Hypophysen- und Hypothalamusdiagnostik
Anamnese Vorgeschichte erfragen
[Bearbeiten]Anamnese
[Bearbeiten]Als Anamnese bezeichnet man die Ermittlung der persönlichen medizinischen Vorgeschichte eines Patienten.
Häufig beginnt sie mit einem Fragebogen zu den Beschwerden.
Für die Diagnose einer Schilddrüsenkrankheit muß der Arzt z.B. wissen,
- ob Schilddrüsenerkrankungen in der Familie vorkommen,
- wann und mit welchem Ergebnis die Schilddrüse schon einmal untersucht wurde,
- welche Behandlung eingeleitet wurden und mit welchen Tabletten und welcher Dosis.
Wichtig sind
- Operationen der Schilddrüse,
- strahlentherapeutische Maßnahmen,
- Belastungen mit jodhaltigem Röntgenkontrastmittel oder jodhaltigen Medikamenten.
Am besten schreibt man sich das Wichtigste schon zu Hause auf und bringt Vorbefunde. Eigene Fragen sollte man auch aufschreiben.
Das Problem der Erkennung von Schilddrüsenkrankheiten:
- Die häufigste Schilddrüsenkrankheit , der Jodmangelkropf, macht keinerlei Beschwerden.
- Die zweithäufigste Schilddrüsenkrankheit, die Überfunktion der Schilddrüse, macht Beschwerden , die man nicht der Schilddrüse zuordnet.
- Auch die Schilddrüsenunterfunktion macht Beschwerden, die man nicht der Schilddrüse zuordnet.
Gezieltes Abfragen von Beschwerden bei Verdacht auf eine Schilddrüsenerkrankung
[Bearbeiten]- Haben Sie Beschwerden mit Ihrer Schilddrüse?
- Welcher Art sind diese?
- Können Sie an Ihrer Schilddrüse etwas auffälliges tasten?
- Nehmen oder nahmen Sie Jodtabletten ein?
- Benutzen Sie Jodsalz?
- Nehmen Sie irgendwelche SD Tabletten ein? Wenn ja welche?
- Körpergewicht
- Zunahme oder Abnahme
- Vermehrte Schweißneigung
- Allgemeine Unruhe, Schlaflosigkeit
- Allgemeine Müdigkeit, Apathie
- Trockene Haut
- Temperaturempfindlichkeit
- wärmeempfindlich,
- kälteempfindlich
- Haarausfall
- Herzrasen (Puls in Ruhe > 80 , in Ruhe > 100?)
- Stuhlverhalten (Obstipation, Diarrhöe)
- Beschwerden im Halsbereich
- Kloßgefühl,
- Schmerzen,
- Schluckbeschwerden,
- Heiserkeit
- Luftnot
- Augensymptome
- geschwollene Lider,
- Doppelbilder,
- Augentränen,
- verschwommenes Sehen
- trockene Augen
Allgemeiner Fragebogen zur Schilddrüsendiagnostik
[Bearbeiten]- Haben Sie Beschwerden mit der Schilddrüse?
- Haben Sie Beschwerden im Halsbereich?
- Welche?
- Kloßgefühl,
- Schmerzen
- Luftnot,
- Schluckbeschwerden
- Heiserkeit
- Haben Sie selbst einen Knoten am Hals getastet?
- Ist der Knoten in der letzten Zeit größer geworden?
- Haben Sie eine vergrößerte oder knotige Schilddrüse?
- Ist bei einem Familienmitglied eine Erkrankung der Schilddrüse bekannt?
Vorbehandlung
- Wurde bei Ihnen schon einmal die Schilddrüse untersucht?
- Wann und wo?
- Was wurde festgestellt?
- Welche Medikamente nehmen Sie für die SD ein?
- Nehmen Sie Jodsalz oder Jodtabletten ein?
- Wurde Ihre SD schon einmal operiert? Warum und wo ?
- Wurde schon einmal eine Radiojodbehandlung durchgeführt?
- Wenn Sie an folgenden Beschwerden leiden, geben Sie bitte an, seit wann das der Fall ist (seit Wochen, Monaten, Jahren, schon immer)
- Verdacht auf Schilddrüsenüberfunktion = Hyperthyreose?
- Haben Sie an Körpergewicht abgenommen?
- Seit wann und um wie viele kg?
- Neigen Sie ständig zu Schwitzen?
- Sind Sie in den letzten Wochen, Monaten innerlich unruhiger geworden?
- Haben Sie gelegentlich auftretendes Herzjagen?
- Sind Sie eher wärmeempfindlich?
- Besteht in der letzten Zeit ein vermehrter Stuhlgang oder Durchfallneigung?
- Haben Sie Beschwerden an den Augen?
- Welche? (z. B. Augentränen, geschwollene Lider
- verschwommenes Sehen, Doppelbilder, hervorgetretene Augen
- Augenjucken, trockene Augen, sonstiges ?)
- Verdacht auf Schilddrüsenunterfunktion = Hypothyreose?
- Ist in den letzten Monaten Ihre Haut trockener geworden?
- Sind Sie in den letzten Monaten zunehmend träger geworden?
- Sind Sie müder, langsamer geworden?
- Frieren Sie leicht an Händen und Füßen?
- Leiden Sie zunehmend unter Verstopfung?
- Für Frauen:
- Nehmen Sie die "Pille" oder andere weibliche Hormone (Östrogene)
- Präparat?
- Datum der letzten Regelblutung
- Besteht eine Schwangerschaft?
- Verdacht auf Schilddrüsenüberfunktion = Hyperthyreose?
- Genauere Fragen zur Vorbehandlung:
- Bitte geben Sie alle Medikamente an, die Sie z. Z. einnehmen, insbesondere Schilddrüsenmedikamente:
- Nehmen Sie Schilddrüsenhormontabletten wie Euythyrox, L-Thyroxin oder Novothyral ein?
- Wenn ja wie lange und in welcher Dosis?
- Nehmen Sie Schilddrüsenbremstabletten = Thyreostatika wie Carbimazol, Thiamazol oder Thyreostat ein ?
- Wenn ja wie lange und in welcher Dosis ?
- Nehmen Sie Jodsalz ein, nehmen Sie Jodtabletten ein?
- Essen Sie gerne Meeresfisch?
- Wurde bei Ihnen vor kurzem jodhaltiges Kontrastmittel zum Beispiel im Rahmen einer Röntgenuntersuchung der Gefäße = Angiografie oder des Herzens = Herzkatheter, Koronarangiografie gespritzt ?
- Gibt es in Ihrer Familie vermehrt Schilddrüsenerkrankungen?
- Sind sie bereits an der Schilddrüse operiert worden?
- Wenn ja, wann und warum?
- Ist die Schilddrüse wieder nachgewachsen?
- Geben Sie weitere Beschwerden und Krankheiten an, an denen Sie leiden oder die Sie durchgemacht haben:
- Vorangegangene Röntgenuntersuchungen (wann, welche?):
- Frühere nuklearmedizinische Untersuchungen mit radioaktiven Substanzen
- Wurde früher eine Strahlentherapie durchgeführt?
- Frühere Behandlungen mit radioaktiven Substanzen ?
- Sind Sie bereits mit Radiojod behandelt worden?
- Wenn ja, wann und warum ?
- Wann wurde das letzte Mal die Schilddrüse mittels Ultraschall untersucht?
- Welches Ergebnis kam dabei heraus?
- Wann wurde das letzte Mal die Schilddrüse mittels Szintigramm untersucht?
- Welches Ergebnis kam dabei heraus?
- Wann wurden das letzte Mal die Schilddrüseblutwerte = Hormonspiegel bestimmt?
- Welches Ergebnis kam dabei heraus ?
Körperliche Untersuchung
[Bearbeiten]
Der Hals wird betrachtet. Es wird die Schilddrüsenregion getastet. (Palpation)
Dabei lassen sich
- Vergrößerungen der Schilddrüse,
- knotenförmige Veränderungen
- ihre Konsistenz (weich oder derb),
- Schwirren bei verstärkter Durchblutung (bei einer Überfunktion) ertasten,
- die Schluckverschiebung (bei einem Kropf) und
- selten eine Schmerzhaftigkeit feststellen.
Das Abtasten erlaubt eine grobe Stadieneinteilung eines Kropfes.
Die körperliche Untersuchung beschränkt sich nicht nur auf die Halsregion, sondern auch auf die Augen, das Herz und die Beine und evtl. andere Körperregionen. Denn ein Hormonüberschuß oder Mangel wirkt zugleich auf andere Körperregionen.
Außerdem sollte Puls und Blutdruck erfasst werden.
Schlucktest
[Bearbeiten]Man kann seine eigene Schildrüse auch selber abtasten.
Eine weitere einfache Untersuchungsmaßnahme ist der Schlucktest:
- Man braucht dazu einen Spiegel und ein Glas Wasser.
- Man betrachtet im Spiegel den eigenen Hals. Die Schilddrüse liegt links und rechts der Luftröhre etwas unterhalb des Adamsapfels.
- Man legt den Kopf etwas zurück , behält aber weiter die Schilddrüsenregion im Auge.
- Man nimmt einen Schluck Wasser.
- Man versucht zu erkennen, ob während des Schluckens die Schilddrüse zu sehr hervortritt.
Das ganze wiederholt man am besten mehrfach.
Laborwerte
[Bearbeiten]siehe Schilddrüse: Labor
Bildgebende Verfahren
[Bearbeiten]Ultraschall
[Bearbeiten]Siehe auch Sonographie: Schilddrüse
Der Ultraschall liefert eine sehr schnelle und oft auch schon wegweisende Aussage über die Schilddrüse. Er ist somit bei der Schilddrüsendiagnostik sehr wertvoll, zumal er auch jederzeit und fast ohne Einschränkungen eingesetzt werden kann.

Bilderklärung
- 1 = Halsschlagader rechts (schwarzes rundes Gebilde ca 5 mm)
- 2 = rechte Schilddrüse (dreiecksförmig, gleichmäßig hellgrau)
- 3 = Luftröhre (schwarze Schallauslöschung durch die Luft in der Luftröhre
- 4 = linke Schilddrüse (dreiecksförmig, gleichmäßig hellgrau)
- 5 = Halsschlagader ( Art.Carotis Communis) links (schwarzes rundes Gebilde ca 5 mm)
- 6 = Drosselvene links ( Vena jugularis interna) (schwarzes rundes Gebilde ca 5 mm)

Im Ultraschall gut erkennbar sind
- Größe
- Form
- viele Knoten
- Zysten
- Lymphknoten in der Nachbarschaft der Schilddrüse
Schwieriger erkennbar oder leicht zu übersehen sind:
- manche Knoten, die sich wenig von normalem Gewebe unterscheiden
- Schilddrüsenentzündungen
Nicht zu unterscheiden sind oft:
- gutartige von bösartigen Knoten
- (Verlaufskontrolle, evtl. Punktion notwendig)
Voraussetzungen einer guten Ultraschalluntersuchung der Schilddrüse sind:
- ein gutes Ultraschallgerät
- ein erfahrener Untersucher
- ausreichend Zeit und eine ruhige Untersuchungsatmosphäre
Größe der Schilddrüse
[Bearbeiten]Im Ultraschall mißt man Breite , Tiefe und Länge der Schilddrüse . Daraus berechnet man dann das Volumen.
Berechnungsformel:
Breite mm * Tiefe mm * Länge mm / 2 / 1000 = Volumen rechts ml Breite mm * Tiefe mm * Länge mm / 2 / 1000 = Volumen links ml Volumen rechts ml + Volumen links ml = Gesamtvolumen ml
Schilddrüsenvolumen
[Bearbeiten]Aus dem Ultraschall kann das Volumen der Schilddrüse berechnet werden.
Größennormwerte der WHO:
- normal: Männer < 25 ml,
- Frauen < 18 ml
- 6 - 10jährige < 8 ml Gesamtvolumen
- 11 - 14jährige < 10 ml Gesamtvolumen
- 15 - 18jährige < 15 ml Gesamtvolumen
Schwachpunkt dieser Normwerte sind die fehlenden Untergrenzen.
Wann ist eine Schilddrüse zu klein?
geschätzte untere Normalgrenze:
- beim Mann > 12 ml
- bei der Frau > 10 ml
Achtung, diese Grenzen sind reine Schätzwerte und nicht validiert, haben sich aber im Alltag bewährt.
Beispiel Kind männlich 10 Jahre normale SD
[Bearbeiten]- Rechte Schilddrüse: normal groß, homogene Struktur, B 10 mm T 11 mm L 36 mm Volumen: 2,0 ml
- Linke Schilddrüse: normal groß, homogene Struktur, B 11 mm T 11 mm L 36 mm Volumen: 2,2 ml
- errechnetes Gesamtvolumen: 4,2 ml
Beispiel Kind weiblich 6 Jahre normale SD
[Bearbeiten]- Rechte Schilddrüse: homogene Struktur, normal groß, B 8 mm T 12 mm L 26 mm , Volumen:1.2 ml
- Linke Schilddrüse: homogene Struktur, normal groß, B 11 mm T 9 mm L 27, Volumen:1.3 ml
- errechnetes Gesamtvolumen: 2.6 ml
Literatur
[Bearbeiten]- ANDERMANN P, SCHLOEGL S, MÄDER U, LUSTER M, LASSMANN M, REINERS C.
- Intra- and interobserver variability of thyroid volume measurements in healthy adults by 2D versus 3D ultrasound.
- Nucl Med 2007;46:1-7.
- Intra- and interobserver variability of thyroid volume measurements in healthy adults by 2D versus 3D ultrasound.
Sehr bewährt hat sich der Ultraschall auch zur Lokalisation von Knoten bei gezielten Punktionen.
Feinnadelpunktion der Schilddrüse
[Bearbeiten]Zelluntersuchung = Zytologie Diese dient zur genaueren Beurteilung der Schilddrüsenzellen.
Biopsie der Schilddrüse (Histologie)
[Bearbeiten]Gewebsuntersuchung = Histologie Siehe Sonographie:_Schilddrüse#Ultraschallgezielte_Biopsie_aus_der_Schilddr.C3.BCse Siehe auch http://www.madeasy.de/6/sdhisto.htm
Szintigrafie der Schilddrüse
[Bearbeiten]
nuklearmedizinische Untersuchung der SD, SD Scan [5]
- Beispiel eines kaltes Knotens am unteren Pol der linken schilddrüse.
Die Schilddrüsenszintigraphie ist eine nuklearmedizinische Methode, die zur Bildgebung und Beurteilung der Schilddrüsenfunktion angewendet wird. Sie eignet sich vor allem zur Unterscheidung von kalten und heißen Knoten sowie zur Beurteilung der Morphologie bzw. Gewebestruktur.
Die Schilddrüsenszintigraphie ist immer noch die häufigste nuklearmedizinische Untersuchung in Deutschland. Jährlich werden etwa 1 - 1,4 Mio. Schilddrüsen-Szintigramme mit Tc-99m durchgeführt, das sind knapp 50 % aller nuklearmedizinischen Untersuchungen mit offenen Radionukliden.
Die Schilddrüsenszintigraphie ist in der Schwangerschaft kontraindiziert.

Prinzip
[Bearbeiten]
Follikel mit Kolloid (1), Follikelepithelzellen (2), Endothelzellen der Kapillaren (3).
Die Follikelzellen der Schilddrüse benötigen Iod für die Synthese der iodhaltigen Schilddrüsenhormone. Dies macht man sich bei der Schilddrüsenszintigraphie zu Nutze. Man benutzt bestimmte Radionuklide, die in ihren chemischen Eigenschaften mit dem stabilen Iod identisch sind oder ihm ähneln.
Das Radionuklid wird dem Patienten in einer für ihn unschädlichen Menge in eine Vene gespritzt und reichert sich nach etwa 10 bis 20 Minuten in der Schilddrüse an.
Die von den inkorporierten Radionukliden ausgesandte γ-Strahlung wird von einer speziellen Kamera aufgezeichnet, so dass die Schilddrüse dargestellt und die Schilddrüsenfunktion beurteilt werden kann. Bei einer Schilddrüsenautonomie reichert sich in autonomen Schilddrüsenzellen beispielsweise mehr Radionuklid an, als in den „normalen“ Follikelzellen. Darüber hinaus lässt sich mit mehreren Aufnahmen in zeitlichen Abständen die biologische Halbwertszeit des Iodabbaus messen und daraus Schlussfolgerungen für eine gegebenenfalls abnorm verstärkte oder verminderte Aktivität der Schilddrüse ziehen.
Radiopharmaka
[Bearbeiten]
Die Aufnahme mit einem Pinhole-Kollimator ist nicht maßstabsgerecht.
Bei der Schilddrüsenszintigraphie werden Radionuklide, sogenannte Radiopharmaka verwendet. Als Radiopharmakon kommt routinemäßig vor allem Technetium-Pertechnetat (99mTc) zur Anwendung. Bei besonderen Fragestellungen wird auch 123Iod (123I) verwendet, im Rahmen eines Radioiodtestes auch 131Iod.
Bei 99mTc handelt es sich um einen reinen Gammastrahler mit relativ geringer effektiver Halbwertzeit. Im Vergleich dazu sind 123I und 131I auch Betastrahler, außerdem sind die Halbwertzeiten länger als bei 99mTc.
Aufgrund der geringeren Strahlenbelastung für den Patienten und geringeren Kosten kommt heute bei der Schilddrüsenszintigraphie bevorzugt 99mTc zur Anwendung. Die Anwendung von 123I bleibt speziellen Fragestellungen vorbehalten, zum Beispiel bei der Frage nach dystopem Schilddrüsengewebe.
Indikationen
[Bearbeiten]
A: normale Schilddrüse B: Basedow-Krankheit C: autonomes Adenom D: toxisches Adenom E: Thyroiditis
Einer Schilddrüsenszintigraphie geht in der Regel eine Tastuntersuchung (Palpation) der Schilddrüse, eine labormedizinische Untersuchung von Schilddrüsenparametern sowie eine Ultraschalluntersuchung (Sonographie) voraus. Besteht aufgrund dieser Untersuchungen der Verdacht auf funktionelle Veränderungen der Schilddrüse, insbesondere auf eine funktionelle Schilddrüsenautonomie oder ein Schilddrüsenkarzinom, kann eine Schilddrüsenszintigraphie zur weiteren Abklärung angezeigt sein.
Mit der 99mTc-Szintigraphie lassen sich Aussagen über die funktionelle Bedeutung morphologischer Veränderungen treffen sowie eine quantitative Bewertung der Funktionsveränderungen vornehmen. Außerdem sind, wie beim Ultraschall, Aussagen über Lage und Größe möglich. Man kann damit in erster Linie kalte, warme und heiße Knoten sowie eine diffuse Mehrspeicherung nachweisen.
Interpretation
[Bearbeiten]
Mit der ROI-Technik kann computergesteuert der sog. globale und regionale 99mTc-Uptake, d. h. die in die Follikelepithelzellen aufgenommene Menge des Radionuklids, ermittelt werden. Für eine adäquate Interpretation eines Schilddrüsenszintigramms ist die Kenntnis der aktuellen Schilddrüsenparameter erforderlich.
Quantitative Parameter der Schilddrüsenszintigraphie
[Bearbeiten]- Tc-99m-Thyreoidea-Uptake (TcTU)
- Radioiod-Thyreoidea-Uptake (RITU)
Beide zeigen eine gute Korrelation zur Iodid-Clearance.
Hohe Iodidclearance
[Bearbeiten]Eine hohe Iodid-Clearance bedeutet, dass die Schilddrüse pro Minute eine große Menge Plasma von Iodid befreit.
Ursachen dafür
- Iodmangel
- Hyperthyreose
Niedrige Iodid-Clearance
[Bearbeiten]Wenig Plasma wird vom Iod geklärt
Ursachen dafür:
- die Iodversorgung ist ausreichend
- der TSH-Stimulus fehlt
fehlende oder sehr niedrige Iod-Clearance
[Bearbeiten]Bei einem Iod-Exzess findet man eine scheinbar fehlende oder sehr niedrige Iod-Clearance.
Weblinks
[Bearbeiten]Informationen für Patienten
[Bearbeiten]Weiterführende Informationen
[Bearbeiten]- „Diagnostik der Schilddrüsenerkrankungen“, Springer-Verlag
- „Verfahrensanweisung für die Schilddrüsenszintigraphie“ der Deutschen Gesellschaft für Nuklearmedizin e. V.
Computertomografie der Schilddrüse
[Bearbeiten]Kernspintomografie der Schilddrüse
[Bearbeiten]Andere Untersuchungsverfahren
[Bearbeiten]Röntgen d. Luftröhre
[Bearbeiten]
Einengung der Luftröhre (Trachealstenose)? [6]
EKG, Echo
[Bearbeiten]Puls zu schnell? zu langsam? Herz überaktiv oder träge)
LangzeitEKG
[Bearbeiten]- mittl. Herzfrequenz zu schnell?
- mittl. Herzfrequenz zu langsam?
- Extrasystolie ?
CT der Hypophyse
[Bearbeiten](sekundäre Hyper- oder Hypothyreose?)
Hypophysen- und Hypothalamusdiagnostik
[Bearbeiten]Hormonwertbestimmung
PET der SD und des restlichen Körpers
[Bearbeiten]
Zurück zur Schilddrüse
Laborwerte bei Schilddrüsenkrankheiten
[Bearbeiten]
Vorbemerkung:
[Bearbeiten]Bei den Einheiten der Schilddrüsen Laborwerte herrscht leider eine unnötige Vielfalt. Deswegen ist es unbedingt wichtig, bei der Angabe eines Meßwertes immer die Einheit und den Normalbereich des Labors mit anzugeben. Die Deutsche Schilddrüsen-Liga sollte dem Wildwuchs ein Ende bereiten und eine Vereinheitlichung herbeiführen.
Häufige Untersuchungen + Normalbereiche
[Bearbeiten]Freies T4 10-23 pmol/l = 0,8 - 2,0 ng/dl Freies T3 3,5-9 pmol/l = 0,2 - 0,4 ng/dl TSH 0,3-2,5 milliUnits/Liter (mU/l)
Typische Laborkonstellationen
[Bearbeiten]
- Euthyreose:
- TSH, FT4 und FT3 im Normbereich
- Primäre Hyperthyreose
- TSH supprimiert, FT4 und FT3 erhöht
- Überfunktion mit der Ursache in der Schilddrüse
- TSH supprimiert, FT4 und FT3 erhöht
- Sekundäre Hyperthyreose
- TSH erhöht, FT4 und FT3 erhöht
- Überfunktion mit der Ursache hypophysär bedingt (selten)
- TSH erhöht, FT4 und FT3 erhöht
- Primäre Hypothyreose
- TSH erhöht, FT4 und FT 3 erniedrigt
- Unterfunktion mit der Ursache in der Schilddrüse
- TSH erhöht, FT4 und FT 3 erniedrigt
- Sekundäre Hypothyreose
- TSH erniedrigt, FT4 und FT3 erniedrigt
- Unterfunktion mit der Ursache hypophysär oder hypothalamisch
- TSH erniedrigt, FT4 und FT3 erniedrigt
- Latente Hyperthyreose oder T4 Therapie
- TSH supprimiert, T3 und T4 noch im Normbereich
- T3-Hyperthyreose
- TSH supprimiert, FT4 im Normbereich, FT3 erhöht
- Subklinische Hypothyreose
- TSH erhöht, FT4 und FT3 im Normbereich
- Sonderform (englisch "Grade 3 Hypothyreoidism") TSH, FT4 und FT3 im Normbereich, im TRH-Test ΔTSH > 16 mU/l
- TSH erhöht, FT4 und FT3 im Normbereich
- Periphere Resistenz gegen Schilddrüsenhormon
- T3, T4 hoch, klinisch Zeichen der Hypothyreose
Schilddrüsenantikörper
[Bearbeiten]Schilddrüsenantikörper sind bei Autoimmunerkranklungen der Schilddrüse wie dem Morbus Basedow oder der Hashimotothyreoiditis erhöht. Es gibt im wesentlichen 3 Sorten von Antikörper:
- TRAK = TSH-Rezeptor-Antikörper
- < 9 U/l negativ , d.h unauffällig und normal
- 9-14 fraglich positiv (Kontrolle empfohlen)
- > 14 U/l positiv , d.h. auffällig hohe Werte
oder nach der Meßmethode DYNOtest® TRAKhuman
negativ: < 1 IU/l (keine erhöhten Antikörper)
Grenzbereich: 1 - 2 IU/l
positiv: > 2 IU/l (erhöhte Antikörper)
- Peroxydase Antikörper (TPO)
- < 80 U/ml negativ
- 80-150 U/ml grenzwertig
- 150 U/ml positiv
oder < 35 IU/ml negativ
Es sollten die TPO-AK bevorzugt eingesetzt werden, da die MAK (mikrosomale Antikörper) sich gegen mehrere Proteine richten und damit weniger spezifisch sind.
- TAK = Thyreoglobulin Antikörper
- < 100 IU/l negativ
oder < 60 U/ml negativ
Tabelle
[Bearbeiten]Die folgende Tabelle zeigt die ungefähre Häufigkeit positiver Antikörperbefunde bei verschiedenen Erkrankungen.
|
Erkrankung |
TPO + |
TAK+ |
TRAK+ |
Hashimoto-Thyreoiditis |
60-90% |
30-40% |
10% |
Primäres Myxödem |
40-70% |
20-30% |
0 - 5% |
Morbus Basedow |
60-70% |
10-20% |
|
- aktiv (Hyperthyreose) |
80-100% |
||
- Remission |
10-30% |
||
Postpartum-Thyreoiditis |
50 - 70% |
30% |
50-70% |
Zytokininduzierte Thyreoiditis |
30 - 40 % | 10-20 % | |
Subakute Thyreoiditis (de Quervain) |
< 5 % |
0 - 20 % |
selten |
Unifocale Autonomie der SD |
0 - 5 % |
0 - 5 % |
0 - 5 % |
Normalpersonen |
5 - 15% |
4 - 8% |
0 - 5 % |
TRAK
[Bearbeiten]Bewertung
[Bearbeiten]Wert Beurteilung --------------------------------------------------- <9 % unauffällig 9-14 % fraglich positiv (Kontrolle empfehlenswert) >14 % erhöhter Wert
Tabelle erhöhte Werte
[Bearbeiten]Krankheit Häufigkeit ------------------------------------- Basedow 80-100 % postpartale Thyreoiditis 50-70 % Hashimoto-Thyreoiditis 10 % Primäres Myxödem 0-5 % Schilddrüsen-Autonomie ca. 5 % Normalpersonen negativ
Allgemeines
[Bearbeiten]TRAK (Thyreoidea-Rezeptor-Autoantikörper, üblicherweise TSH-Rezeptor-Autoantikörper genannt) sind vom Körper gegen den TSH-Rezeptor gebildete Antikörper, die am TSH-Rezeptor ähnliche Wirkungen entfalten wie das eigentlich dort bindende Hormon TSH . Der Begriff Autoantikörper leitet sich vom griechischen Auto- im Sinne von Eigen, Selbst ab und bedeutet daß der Körper unsinnigerweise Antikörper gegen sich selbst produziert. TRAK sind spezifische Immunglobuline die eine gewisse Strukturverwandtschaft mit TSH haben, jedenfalls stimulieren sie genauso wie TSH den TSH Rezeptor der Schilddrüse.
Wirkung auf die Schilddrüse
[Bearbeiten]TRAK unterscheiden sich von den meisten anderen Autoantikörpern, da sie unmittelbar für die klinischen Symptome der Erkrankung verantwortlich sind, und nicht nur als Nebenprodukt dieser Erkrankung auftreten. Außerdem sind sie im Gegensatz zu anderen Autoimmunerkrankungen nicht zerstörend, sondern im Gegenteil stimulierend. TRAK sind verantwortlich für die klinischen Symptome des Morbus Basedow, da sie am TSH-Rezeptor zu einer unkontrollierten Stimulation des Rezeptors und damit zur Überfunktion der Schilddrüse führen. Auch bei der Hashimotothyreoiditis sind sie in einem gewissen Prozentsatz nachweisbar.
LATS
[Bearbeiten]Früher hießen die TRAK auch LATS = Long acting Thyreoidea Stimulating Factor, da man noch nicht wußte, daß es sich hierbei um Immunglobuline handelt.
Bedeutung für die Diagnostik
[Bearbeiten]Dieser unmittelbare Zusammenhang zwischen TRAK und Morbus Basedow macht sie zu einem geeigneten Diagnostikum für die Erkrankung. Das Vorhandensein von TRAK im Blut eines Patienten ist praktisch beweisend für die Diagnose Morbus Basedow. Wenn bei einem Patienten mit Schilddrüsen Überfunktion keine TRAK nachweisbar sind, dann sind andere Gründe (nicht autoimmune Ursache) für diese Überfunktion verantwortlich (z. B. ein so genanntes Autonomes Adenom).
Weitere Unterscheidung der TRAK
[Bearbeiten]In der Schilddrüsenforschung werden die TRAK noch weiter unterteilt:
- in solche mit stimulierenden Eigenschaften (thyroid stimulating antibodies, TSAb)
- und solche mit blockierenden Eigenschaften (thyroid blocking antibodies , TBAb).
Bei den meisten Patienten mit Morbus Basedow treten zumindest in Europa die stimulierenden Antikörper auf. Umstritten ist noch die Bedeutung der blockierenden Antikörper.
In der Routinediagnostik werden ausschließlich die TRAK beim Laborarzt bestimmt. Eine Unterscheidung in TSAb und TBAb erfolgt nicht. Positive TRAK im Blut sichern die Diagnose Morbus Basedow, wobei diese Laboruntersuchung nur ein Bestandteil des diagnostischen Verfahrens neben körperlicher Untersuchung, Ultraschall der Schilddrüse und anderen Methoden darstellt.
Neuere Erkenntnisse
[Bearbeiten]Nach neuesten Studien ist die Konzentration der TRAK auch mit dem Verlauf der Erkrankung Morbus Basedow assoziiert. Patienten mit sehr hohen TRAK-Werten haben ein Risiko von über 90 %, nach medikamentöser Therapie erneut einen Rückfall zu bekommen. Leider gilt die umgekehrte Aussage nicht. Patienten mit niedrigen TRAK-Werten können durchaus ebenfalls ein Rezidiv der Erkrankung bekommen. Manche Autoren schlagen daher vor, bei hohen TRAK-Werten der Patienten möglichst rasch eine sogenannte definitive Therapie (Operation, Radiojodtherapie) anzustreben. Dies ist jedoch noch nicht durch prospektive Studien belegt und wird von anderen eher zurückhaltend gesehen.
TRAK und Endokrine Orbitopathie
[Bearbeiten]Nach neuesten Studien stehen TRAK und Endokrine Orbitopathie (EO) in einem ähnlichen Zusammenhang wie TRAK und Morbus Basedow. Die EO ist eine vermutlich autoimmune Erkrankung der Augenhöhle, die eng mit dem Morbus Basedow zusammenhängt, und in der Regel zusammen mit der Schilddrüsenerkrankung auftritt (nicht jedoch immer zeitgleich). Bei einer schweren EO sind im Blut auch hohe TRAK-Konzentrationen nachweisbar. Ob die TRAK auch bei der EO die Ursache der Erkrankung sind oder nur ein Beiprodukt des ablaufenden Autoimmunprozesses, ist derzeit noch Gegenstand von Untersuchungen. Diagnostische Bedeutung haben die TRAK aber auch bei der EO, insbesondere zur Vorhersage des Schweregrads der Erkrankung.
Autoantikörper gegen Schilddrüsen Peroxidase (TPO)
[Bearbeiten]Allgemeines
[Bearbeiten]Als Thyreoperoxidase-Antikörper (Thyreoperoxidase-Antikörper, TPO-AK, Mikrosomale Antikörper, MAK) werden gegen die Thyreoperoxidase gerichtete Antikörper bezeichnet, deren Serumspiegel bei verschiedenen Autoimmunthyreopathien erhöht sein kann.
Die Thyreoperoxidase spielt eine wichtige Rolle in der Synthese der Schilddrüsenhormone. Das Enzym ist in der apikalen Zellmembran der Schilddrüsenzelle gelegen, das heißt auf der Seite der Zelle, die dem Schilddrüsenfollikel zugewandt ist. Die bei Autoimmunthyreopathien nachweisbaren Antikörper sind gegen den extrazellulären Anteil der Thyreoperoxidase gerichtet. Es ist nicht geklärt, wie die Thyreoperoxidase die apikale Zellseite beziehungsweise den Inhalt des Schilddrüsenfollikels verlässt und somit für das Immunsystem erreichbar wird.
Nachweis
[Bearbeiten]Thyreoperoxidase-Antikörper lassen sich mit verschiedenen quantitativen Immunoassay-Verfahren nachweisen, zu denen beispielsweise Radioimmunoassays (RIA und IRMA) und Enzyme-linked Immunosorbent Assay zählen. Als Antigen dient in diesen Tests rekombinante Thyreoperoxidase. Das Messergebnis wird in internationalen Einheiten pro Liter (IU/l) angegeben. Trotz üblicher Referenzierung mit einem Standard sind die Messergebnisse verschiedener Labors nur bedingt miteinander vergleichbar.
Vorkommen
[Bearbeiten]Thyreoperoxidase-Antikörper sind bei über 90 Prozent der Patienten mit chronischer Autoimmunthyreoiditis (Hashimoto-Thyreoiditis) und über 70 % der Patienten mit einem aktiven Morbus Basedow nachweisbar. Allerdings sind bei etwa 30 Prozent der Erkrankten die Antikörper-Titer nur grenzwertig oder leicht erhöht. Da zudem bei etwa 20 Prozent der Patienten mit nicht-autoimmunen Schilddrüsen-Erkrankungen (zum Beispiel Struma nodosa oder Schilddrüsenautonomie) sowie bei euthyreoten Gesunden ebenfalls leicht erhöhte Werte auftreten können, ist die Spezifität eingeschränkt: bei Nachweis von Thyreoperoxidase-Antikörpern mit niedrigem Titer kann nicht zwangsläufig auf das Vorliegen einer Autoimmunthyreopathie geschlossen werden.
Mehrere Autoimmunerkrankungen beim selben Patienten treten gelegentlich auf. Drei Prozent aller Patienten mit einem Typ-1-Diabetes haben eine manifeste Hypothyreose, und 13 bis 34 Prozent positive Thyreoperoxidase-Antikörper und gleichzeitig ein erhöhtes TSH.
Klinische Wertigkeit
[Bearbeiten]Bei funktionell und sonografisch eindeutigem Befund einer Hashimoto-Thyreoiditis (deutliche Hypothyreose, kleine und echoarme Schilddrüse) wird man auf die zusätzliche Bestimmung der Thyreoperoxidase-Antikörper meist verzichten können. In weniger klaren Situationen können aber erhöhte Thyreoperoxidase-Antikörper zur Diagnosestellung beitragen. Bei Patienten mit Verdacht auf Morbus Basedow, die jedoch negativ für TRAK (TSH-Rezeptor-Antikörper) sind, können erhöhte Thyreoperoxidase-Antikörper ebenfalls ein wichtiger diagnostischer Hinweis auf die Ursache der Schilddrüsenüberfunktion sein.
Patienten mit erhöhtem Thyreoperoxidase-Antikörper-Titer, aber aktuell normaler Stoffwechsellage der Schilddrüse, wird empfohlen, jährlich den TSH-Wert bestimmen zu lassen, da sie eine Wahrscheinlichkeit von fünf Prozent pro Jahr haben, eine Unterfunktion zu entwickeln. Wegen der besonderen Bedeutung der mütterlichen Schilddrüsenhormone für das Kind sollen Schwangere mit positiven Thyreoperoxidase-Antikörper sogar alle 3 Monate das TSH bestimmen lassen. Patientinnen mit Autoantikörpern der Schilddrüse haben ebenfalls ein erhöhtes Risiko eine Postpartum-Thyreoiditis zu entwickeln.
Quellen
[Bearbeiten]- Lothar-Andreas Hotze, Petra-Maria Schumm-Draeger. Schilddrüsenkrankheiten. Diagnose und Therapie. Berlin 2003 ISBN 3-88040-002-4
- Mariotti et al.: Antithyroid peroxidase autoantibodies in thyroid diseases. J Clin Endocrinol Metab. 1990;71(3):661-9. PMID 2168432
Autoantikörper gegen Thyreoglobulin (TAK)
[Bearbeiten]Normalwerte
[Bearbeiten]Frauen < 100 IU/ml Männer < 60 IU/ml
Bei erhöhtem Thyreoglobulinspiegeln können falsch niedrige Werte der TAK-AK vorkommen.
Allgemeines
[Bearbeiten]Thyreoglobulin ist ein starkes Autoantigen. Auch im Blut von Gesunden lassen sich B-Lymphozyten mit membranständigen IgM-Antikörpern gegen Thyreoglobulin nachweisen. Falls sich im Blut hohe Titer von IgG-Antikörper gegen Thyreoglobulin (TAK) nachweisen lassen, dann spricht dies - bei gleichzeitig erhöhten TPO-Antikörpern - für eine chronische autoimmune Thyreoiditis Typ Hashimoto.
Indikation
[Bearbeiten]Insgesamt ist die diagnostische Wertigkeit von TAK gegenüber TPO und TRAK geringer.
- V.a. Hashimoto-Thyreoiditis
- Verlaufskontrolle der Hashimoto-Thyreoiditis.
- Nachsorge bei Patienten mit Schilddrüsenkarzinom
- zum Ausschluß einer Interferenz bei der Bestimmung von Thyreoglobulin als Tumormarker
Spezialuntersuchungen
[Bearbeiten]- Gesamt-T4: 77-142 nmol/l = 5-12 mikrog/dl
- T4 Uptake
- Gesamt T3:1-3 nmol/l = 80 - 260 ng /dl
- Gesamt Jod im Blut: 260 - 680 nmol/l
- Reverses T3 gesamt: 0,3 - 0,9 nmol/l
- Thyroxinbindendes Globulin (TBG): 13-30 mg/l (220 - 510 nmol/l)
- Thyreoglobulin bei völlig entfernter Schilddrüse: < 4 ng/ml
- Thyreoglobulin bei Gesunden: < 50 ng/ml
- Thyreoglobulin bei Jodmangel: < 70 ng/ml
- Calcitonin < 15 ng/l: (< 4,2 pmol/l)
- Parathormon: 10 - 65 pg/ml (eigentlich kein Schilddrüsenhormon}
- Jod Ausscheidung im Urin: 150 - 300 µg/g Kreatinin
- Jod Ausscheidung im Urin bei Jodmangel: < 150 µg/g Kreatinin
- Strukturparameter:
TBG = Thyroxin bindendes Globulin
[Bearbeiten]siehe TBG
Normalwerte
[Bearbeiten]TBG wird aus 1 ml Serum bestimmt.
Altersgruppe Normbereich -------------------------------------- Kinder bis 15 Jahre 2,0-3,0 mg/dl Erwachsene 1,6-3,0 mg/dl
TBG erhöht bei
[Bearbeiten]- Schwangerschaft
- Östrogenerhöhungen: z.B. Ovulationshemmer
- Androgene
- Hypothyreose
- konnatal: angeborener TBG-Exzeß: ~1:6000 bis 1:17.600 Geburten
- hereditärere TBG-Varianten mit veränderter Affinität zu T4 (sehr selten)
erniedrigt
[Bearbeiten]- kongenital: angeborener kompletter TBG-Mangel: Werte <5 mg/l ~1:15 000 Geburten
- partieller TBG-Mangel: ~1:5000 Geburten
- Eiweißverluste (enteral, renal)
TRH Test
[Bearbeiten]- normal TSH Anstieg um 2 - 25 mU/l
- bei Hyperthyreose mangelhafter Anstieg
- bei Hypothyreose überschießender Anstieg
Jod im Urin zur Feststellung eines Jodmangels
[Bearbeiten]Material: 10 ml Spontanurin
Normalbereich: 150-250 µg/g Kreatinin
Bewertung:
Ergebnis Bewertung ======================================================== >1000 µg Jod/g Kreatinin Jodkontamination -------------------------------------------------------- 150-250 µg/g Kreatinin Normal -------------------------------------------------------- 100-150 µg/g Kreatinin Graubereich 50-100 µg Jod/g Kreatinin mäßiger Jod-Mangel 10-50 µg Jod/g Kreatinin ausgeprägter Jod-Mangel <10 µg Jod/g Kreatinin schwerer Jod-Mangel --------------------------------------------------------
Tumormarker
[Bearbeiten]- Calcitonin
- Thyreoglobulin
- Thyreoglobulin bei völlig entfernter Schilddrüse < 4 ng/ml
- Thyreoglobulin bei Gesunden < 50 ng/ml
- Thyreoglobulin bei Jodmangel < 70 ng/ml
- Calcitonin < 15 ng/l ( < 4,2 pmol/l)
Zitat:
Die immunometrische Bestimmung von Serum Thyreoglobulin (S-Tg), ist nach Thyreoidektomie und Radiojodablation in der Nachsorge des differenzierten Schilddrüsenkarzinomen (DTC) ein verlässlicher und sensitiver Parameter eines Rezidivs in hypothyreoter Stoffwechsellage. Allerdings bilden ca. 20% der differenzierten Schilddrüsenkarzinome Thyreoglobulinantikörper aus, die neben der molekularen Heterogenität des Tg - Moleküls ursächlich für falsch negative Ergebnisse im Immunoassay sein können.
Links Laborwerte
[Bearbeiten]- http://www.bioscientia.de
- bioscientia.de/public/AnzGrPub.asp?Grafik=/B56/B564.gif
- http://www.endokrinologikum.com/index.php?cccpage=ae_diagnostik_anabasis_hormone_detail&set_z_anabasis_hormone=77
- http://www.schilddruesenpraxis.de
- http://www.med4you.at/laborbefunde/lbef_ft3.htm
- Labowerte sehr gut erklärt
- Laborwerte SD
Statistik der Schilddrüsenkrankheiten
[Bearbeiten]
Einleitung
[Bearbeiten]Eine gute Übersicht über die Schilddrüsenkrankheiten in Deutschland liefert die Statistik Gesundheitsberichterstattung des Bundes. Aus diesen Statistiken wurden einige übernommen und unten dargestellt. Die ambulanten Behandlungen wegen Schilddrüsenkrankheiten, die sicherlich die stationären Behandlungen weit übertreffen, sind leider nicht so gut erfasst, weil im ambulanten Bereich die Diagnoseverschlüsselung noch nicht so konsequent durchgeführt wird.
Bei der Statistik der Schilddrüsenkrankheiten fällt folgendes auf:
- die 3 - 4 fach höhere Krankheitshäufigkeit bei Frauen bei fast allen Schilddrüsenkrankheiten
- die recht hohe Sterblichkeit von circa 2 % bei Hypothyreose, verglichen mit der Hyperthyreose von nur 0,3 % bei den stationäre Schilddrüsenkrankheiten.
Interessant wäre ein Vergleich der Schilddrüsendaten in Deutschland mit einem Land wie der Schweiz, welches seit langem eine Jodprophylaxe durchführt.
SD- Diagnosedaten der Krankenhäuser ab 2006 (Fälle Pflegetage, Verweildauer Sterbefälle)
[Bearbeiten]Angezeigte Werte beziehen sich auf: Alle Altersgruppen, Beide Geschlechter, Deutschland, 2006, alle Fälle
ICD10 Fälle Pflegetage Verweildauer Sterbefälle Sterbefälle an allen Fällen in % E00-E90 Hormone,Stoffwechsel,Ernährung 471.375 4.357.268 9,2 Tage 9.341 2,0 E00-E07 Krankheiten der Schilddrüse 134.455 690.985 5,1 216 0,2 E00 Angeborenes Jodmangelsyndrom - - - - - E01 Jodmangelbedingte SD-Krankheiten 1.688 8.167 4,8 2 0,1 E02 Subklinische Jodmangel-Hypothyreose 6 ? 539? ?89,8?? - - E03 Sonstige Hypothyreose 1.650 16.388 9,9 34 2,1 E04 Sonstige nichttoxische Struma 75.331 363.141 4,8 25 0,03 E05 Hyperthyreose [Thyreotoxikose] 53.517 287.344 5,4 150 0,3 E06 Thyreoiditis 2.160 14.887 6,9 5 0,2 E07 Sonstige Krankheiten der SD 103 519 5,0 - - Alle Diagnosen/Behandlungsanlässe 17.142.476 144.803.781 8,4 389.339 2,3
SD-Diagnosedaten der Krankenhäuser Deutschland 2006 MÄNNER
[Bearbeiten]ICD10 Fälle Pflegetage Verweildauer Sterbefälle Sterbefälle an allen Fällen in % ----------------------------------------------------------------------------------------------------------------------- E00-E90 Hormone,Ernährung,Stoffwechsel 188.833 1.964.959 10,4 3.931 2,1 E00-E07 Krankheiten der Schilddrüse 34.343 179.075 5,2 60 0,2 E00 Angeborenes Jodmangelsyndrom - - - - - E01 Jodmangelbedingte SDkrankheiten 447 2.283 5,1 1 0,2 E02 Subklinische Jodmangel-Hypothyreose 1 ?523 523,0? - - E03 Sonstige Hypothyreose 392 3.609 9,2 11 2,8 E04 Sonstige nichttoxische Struma 19.168 92.596 4,8 8 0,0 E05 Hyperthyreose [Thyreotoxikose] 13.889 76.695 5,5 40 0,3 E06 Thyreoiditis 400 3.112 7,8 - - E07 Sonstige Krankheiten der SD 46 257 5,6 - - Alle Diagnosen/Behandlungsanlässe 7.995.913 66.980.828 8,4 194.709 2,4
SD-Diagnosedaten der Krankenhäuser Deutschland 2006 FRAUEN
[Bearbeiten]ICD10 Fälle Pflegetage Verweildauer Sterbefälle Sterbefälle an allen Fällen in % ----------------------------------------------------------------------------------------------------------------------- E00-E90 Hormone,Ernährung,Stoffwechsel 282.536 2.392.271 8,5 5.410 1,9 E00-E07 Krankheiten der Schilddrüse 100.111 511.907 5,1 156 0,2 E00 Angeborenes Jodmangelsyndrom - - - - - E01 Jodmangelbedingte SDkrankheiten 1.241 5.884 4,7 1 0,1 E02 Subklinische Jodmangel-Hypothyreose 5 16 3,2 - - E03 Sonstige Hypothyreose 1.258 12.779 10,2 23 1,8 E04 Sonstige nichttoxische Struma 56.163 270.545 4,8 17 0,0 E05 Hyperthyreose [Thyreotoxikose] 39.627 210.646 5,3 110 0,3 E06 Thyreoiditis 1.760 11.775 6,7 5 0,3 E07 Sonstige Krankheiten der SD 57 262 4,6 - - Alle Diagnosen/Behandlungsanlässe 9.146.276 77.820.871 8,5 194.627 2,1
Interpretation:
- Auffällig ist die 3 - 4 fach höhere Krankheitshäufigkeit bei Frauen bei fast allen Schilddrüsenkrankheiten
- Auffällig ist die recht hohe Sterblichkeit von circa 2 % bei Hypothyreose, verglichen mit der Hyperthyreose von nur 0,3 %
- Auffällig ist ein Außreißer in der Position E02 Subklinische Jodmangel-Hypothyreose
Interessant wäre ein Vergleich dieser Daten mit einem Land wie der Schweiz, welches seit langem eine Jodprophylaxe durchführt.
SD-Operationen in Deutschland 2006
[Bearbeiten]ICD10 Ops Anteil der OP-Patienten an allen Pat. in % Verweildauer ------------------------------------------------------------------------------------------------------------------ Alle Diagnosen/Behandlungsanlässe 5.389.936 31,4 8,5 E00-E90 Hormone,Ernährung,Stoffwechsel 121.536 25,8 10,1 ------------------------------------------------------------------------------------------------------------------ E00-E07 Krankheiten der Schilddrüse 75.210 55,9 4,9 E01 Jodmangelbedingte SDkrankheiten 1.453 86,1 4,7 E02 Subklinische Jodmangel-Hypothyreose 2 33,3 1,0 E03 Sonstige Hypothyreose 65 3,9 14,6 E04 Sonstige nichttoxische Struma 61.476 81,6 4,8 E05 Hyperthyreose [Thyreotoxikose] 11.339 21,2 5,4 E06 Thyreoiditis 843 39,0 5,4 E07 Sonstige Krankheiten der Schilddrüse 32 31,1 4,9 C73-C75 Krebs der SD + sonstiger Hormondrüsen 5.840 26,8 8,7
Es fehlt in dieser Tabelle die nicht unbedeutsame Zahl der OPs bei gutartige Neubildungen der Schilddrüse und Neubildungen unsicheren oder unbekannten Verhaltens.
Im Jahr 2012 wurden in Deutschland nach Angaben des Statistischen Bundesamtes 90000 Schilddrüsenoperationen durchgeführt. Die häufigste Indikation ist eine bilaterale Struma multinodosa.
Literatur
[Bearbeiten]- LORENZ R, REINERS C.
- Untersuchung zu Diagnose, Therapie, Altersverteilung und Versorgungsform von stationären Patienten mit Schilddrüsenerkrankung.
- Nucl Med 2007;46:A73.
- Untersuchung zu Diagnose, Therapie, Altersverteilung und Versorgungsform von stationären Patienten mit Schilddrüsenerkrankung.
ICD Nummern der Schilddrüsenkrankheiten (Diagnoseverschlüsselung)
[Bearbeiten]
Einleitung
[Bearbeiten]Mit dem ICD Code werden medizinische Diagnosen zu statistischen und abrechnungstechnischen Zwecken verschlüsselt. Die meisten Schilddrüsenkrankheiten finden sich im Kapitel E ( Hormonelle Erkrankungen ) unter E0. Einige wichtige Infektionskrankheiten wie die seltene Tuberkulose der Schilddrüse, aber auch die echten Tumoren der Schilddrüse sind davon ausgenommen und finden sich in anderen Kapiteln.
Auch für Patienten und medizinische Laien ist dieser Code interessant, da man mit den Ziffern über den Qualitätsbericht eines Krankenhauses herausfinden kann, wieviele Patienten mit dieser Krankheit dort behandelt werden.
ICD Übersicht
[Bearbeiten]A18 - Tuberkulose der Schilddrüse
C73 - Bösartige Neubildung der Schilddrüse Schilddrüsenkarzinom
C79.8 Schilddrüsenmetastase
D34 - Gutartige Neubildung der Schilddrüse
D44 - Unklare Neubildung der Schilddrüse
E00 - Angeborenes Jodmangelsyndrom
E01 - Schilddrüsenerkrankungen durch Jodmangel und verwandte Zustände Schilddrüsenunterfunktion
E02 - Subklinische Jodmangel-Hypothyreose
E03 - Andere Formen der Schilddrüsenunterfunktion (Hypothyreose)
E04 - Sonstige nichttoxische Struma
E05 - Schilddrüsenüberfunktion (Hyperthyreose)
E06 - Schilddrüsenentzündung (Thyreoiditis)
E07 - Andere Krankheiten der Schilddrüse
E35 - Störungen endokriner Drüsen
E89 - Endokrine und Stoffwechselstörungen nach medizinischen Maßnahmen, anderenorts nicht klassifiziert
F02 - Demenz als Folge anderer Krankheiten Schilddrüsenunterfunktion
I43.8 Thyreotoxische Herzkrankheit +
M82 - Knochenschwund als Folge anderer Erkrankungen Schilddrüsenüberfunktion
O90.5 Postpartale Thyreoiditis
P72.1 Hyperthyreose beim Neugeborenen
R64 - Abmagerung (Kachexie) Schilddrüsenüberfunktion
T38 - Vergiftung durch Hormone Schilddrüsenhormone
Details
[Bearbeiten]TBC
[Bearbeiten]A18 - Tuberkulose der Schilddrüse
gutartige und bösartige Tumoren der SD
[Bearbeiten]C73 Bösartige Neubildung der Schilddrüse C79.8;Schilddrüsenmetastase D34 Gutartige Neubildung der Schilddrüse
E00.- Angeborenes Jodmangelsyndrom
[Bearbeiten]Inkl.: Endemische Krankheitszustände durch direkten umweltbedingten Jodmangel oder infolge mütterlichen Jodmangels. Einige dieser Krankheitszustände gehen aktuell nicht mehr mit einer Hypothyreose einher, sind jedoch Folge unzureichender Schilddrüsenhormonsekretion des Feten in der Entwicklungsphase. Umweltbedingte strumigene Substanzen können beteiligt sein.
Soll eine damit verbundene geistige Retardierung angegeben werden, ist eine zusätzliche Schlüsselnummer (F70-F79) zu benutzen. Exkl.: Subklinische Jodmangel-Hypothyreose
(E02)
E00.0 Angeborenes Jodmangelsyndrom, neurologischer Typ
Endemischer Kretinismus, neurologischer Typ E00.1 Angeborenes Jodmangelsyndrom, myxödematöser Typ
Endemischer Kretinismus: - hypothyreot -myxödematöser Typ E00.2 Angeborenes Jodmangelsyndrom, gemischter Typ
Endemischer Kretinismus, gemischter Typ E00.9 Angeborenes Jodmangelsyndrom, nicht näher bezeichnet
Angeborene Jodmangel-Hypothyreose o. n. A. Endemischer Kretinismus o. n. A.
E01.- Jodmangelbedingte Schilddrüsenkrankheiten und verwandte Zustände
[Bearbeiten]E01.- Jodmangelbedingte Schilddrüsenkrankheiten und verwandte Zustände
Exkl.: Angeborenes Jodmangelsyndrom (E00.-)
Subklinische Jodmangel-Hypothyreose (E02)
E01.0 Jodmangelbedingte diffuse Struma (endemisch)
E01.1 Jodmangelbedingte mehrknotige Struma (endemisch)
Jodmangelbedingte knotige Struma E01.2 Jodmangelbedingte Struma (endemisch), nicht näher bezeichnet
Endemische Struma o. n. A. E01.8 Sonstige jodmangelbedingte Schilddrüsenkrankheiten und verwandte Zustände
Erworbene Jodmangel-Hypothyreose o. n. A.
E02.- Subklinische Jodmangel-Hypothyreose
[Bearbeiten]Erworbene Jodmangel-Hypothyreose o. n. A.
E03.- Sonstige Hypothyreose
[Bearbeiten]E03.- Sonstige Hypothyreose
Exkl.: Hypothyreose nach medizinischen Maßnahmen (E89.0)
Jodmangelbedingte Hypothyreose (E00- E02)
E03.0 Angeborene Hypothyreose mit diffuser Struma
Struma congenita (nicht toxisch): - parenchymatös - angeborene Hypothyreose bei Jodfehlverwertung - o. n. A. Exkl.: Transitorische Struma congenita mit normaler Funktion (P72.0)
E03.1 Angeborene Hypothyreose ohne Struma
Angeboren: - Atrophie der Schilddrüse - angeborene Hypothyreose bei Schilddrüsenaplasie - angeborene Hypothyreose bei Schilddrüsendysplasie - angeborene Hypothyreose bei ektoper Schilddrüsendysplasie - angeborene Hypothyreose bei TSH-Mangel - Hypothyreose o. n. A. Aplasie der Schilddrüse (mit Myxödem) E03.2 Hypothyreose durch Arzneimittel oder andere
exogene Substanzen Soll die äußere Ursache angegeben werden, ist eine zusätzliche Schlüsselnummer (Kapitel XX) zu benutzen. - Thyreostatikainduzierte Hypothyreose (Y42.2) - Hypothyreose bei Jodexzeß (Y54.9) E03.3 Postinfektiöse Hypothyreose
E03.4 Atrophie der Schilddrüse (erworben)
Exkl.: Angeborene Atrophie der Schilddrüse
(E03.1)
E03.5 Myxödemkoma
E03.8 Sonstige näher bezeichnete Hypothyreose
- Sekundäre Hypothyreose - Hypothyreose bei chronischer Autoimmunthyreoiditis - Hypothyreose bei nicht-immunogener Schilddrüsenentzündung E03.9 Hypothyreose, nicht näher bezeichnet
Myxödem o. n. A.
E04.- Sonstige nichttoxische Struma
[Bearbeiten]E04.- Sonstige nichttoxische Struma
Exkl.: Jodmangelbedingte Struma (E00-E02) Struma congenita: - diffus (E03.0) - parenchymatös (E03.0) - o. n. A. (E03.0) E04.0 Nichttoxische diffuse Struma
Struma, nichttoxisch: - diffusa (colloides) - simplex - diffuse Struma bei Akromegalie E04.1 Nichttoxischer solitärer Schilddrüsenknoten
Nichttoxische einknotige Struma Solitäre Schilddrüsenzyste Schilddrüsenknoten (zystische) Struma o. n. A. Struma nodosa E04.2 Nichttoxische mehrknotige Struma
Mehrknotige (zystische) Struma Struma mit multiplen Zysten Knotenstruma bei Immunthyreopathie Knotenstruma bei nichtimmunogener Schilddrüsenentzündung Knotenstruma bei Akromegalie Zystische Struma o. n. A. E04.8 Sonstige näher bezeichnete nichttoxische Struma
Diffuse Struma ausgelöst durch strumigene Substanzen Knotenstruma ausgelöst durch strumigene Substanzen E04.9 Nichttoxische Struma, nicht näher bezeichnet
Struma nodosa (nichttoxisch) o. n. A. Struma o. n. A.
E05.- Hyperthyreose [Thyreotoxikose]
[Bearbeiten]E05.- Hyperthyreose [Thyreotoxikose]
Exkl.: Chronische Thyreoiditis mit transitorischer Hyperthyreose (E06.2)
Hyperthyreose beim Neugeborenen (P72.1)
E05.0 Hyperthyreose mit diffuser Struma
Basedow-krankheit [Morbus Basedow]
- mit endokriner Orbitopathie
- ohne endokriner Orbitopathie
Hyperthyreose bei anderer Immunthyreopathie
Disseminierte Autonomie der Schilddrüse
Jodinduzierte Hyperthyreose bei M. Basedow
Toxische diffuse Struma
Toxische Struma o. n. A.
E05.1 Hyperthyreose mit toxischem solitärem Schilddrüsenknoten
- Hyperthyreose mit toxischer einknotiger Struma
- Unifokale Autonomie der Schilddrüse
E05.2 Hyperthyreose mit toxischer mehrknotiger Struma
- Multifokale Autonomie der Schilddrüse
- Jodinduzierte Hyperthyreose bei funktioneller Autonomie der Schilddrüse (Y54.9)
- Toxische Struma nodosa o. n. A.
E05.3 Hyperthyreose durch ektopisches Schilddrüsengewebe
E05.4 Hyperthyreosis factitia
E05.5 Thyreotoxische Krise
E05.8 Sonstige Hyperthyreose
Überproduktion von Thyreotropin
Soll die äußere Ursache angegeben werden, ist eine zusätzliche Schlüsselnummer (Kapitel XX) zu benutzen. Neugeborenenhyperthyreose
Jodinduzierte Hyperthyreose (Y54.9)
E05.9 Hyperthyreose, nicht näher bezeichnet
- Hyperthyreose o. n. A.
- Thyreotoxische Herzkrankheit + (I43.8*)
E06.- Thyreoiditis
[Bearbeiten]E06.- Thyreoiditis
Exkl.: Postpartale Thyreoiditis (O90.5)
E06.0 Akute Thyreoiditis
Abszeß der Schilddrüse Thyreoiditis:
- eitrig
- pyogen
Soll der Infektionserreger angegeben werden, ist eine zusätzliche Schlüsselnummer (B95-B97) zu benutzen.
E06.1 Subakute Thyreoiditis
Thyreoiditis:
- de-Quervain
- granulomatös
- nichteitrig
- Riesenzell-
Exkl.: Autoimmunthyreoiditis (E06.3)
E06.2 Chronische Thyreoiditis mit transitorischer Hyperthyreose
Exkl.: Autoimmunthyreoiditis (E06.3)
E06.3 Autoimmunthyreoiditis
Hashimoto-Thyreoiditis Hashitoxikose (transitorisch) Lymphozytäre Thyreoiditis Struma lymphomatosa [Hashimoto] Atrophische Autoimmunthyreoiditis
E06.4 Arzneimittelinduzierte Thyreoiditis Soll die Substanz angegeben werden, ist eine zusätzliche Schlüsselnummer (Kapitel XX) zu benutzen.
E06.5 Sonstige chronische Thyreoiditis Thyreoiditis: chronisch:
- fibrös
- o. n. A.
- eisenhart
- Riedel-Struma (invasiv-sklerosierende Thyreoiditis)
E06.9 Thyreoiditis, nicht näher bezeichnet
E07.- Sonstige Krankheiten der Schilddrüse
[Bearbeiten]E07.- Sonstige Krankheiten der Schilddrüse
E07.0 Hypersekretion von Kalzitonin
C-Zellenhyperplasie der Schilddrüse Hypersekretion von Thyreokalzitonin E07.1 Dyshormogene Struma
Familiäre dyshormogene Struma Pendred-Syndrom Exkl.: Transitorische Struma congenita mit normaler Funktion (P72.0)
E07.8 Sonstige näher bezeichnete Krankheiten der Schilddrüse
Abnormität des Thyreoglobulin Euthyroid-Sick-Syndrom Schilddrüse: - Blutung - Infarzierung Schilddrüsenhormonresistenz Struma bei Systemerkrankung Intrathorakale Struma Zungengrundstruma Dystop gelegene Struma E07.9 Krankheit der Schilddrüse, nicht näher bezeichnet
E89.0 Hypothyreose nach medizinischen Maßnahmen
[Bearbeiten]Inkl.:
- Hypothyreose nach Bestrahlung
- Postoperative Hypothyreose
Links
[Bearbeiten]- Tabelle der SD-Krankheiten in Wikipedia
- http://www.lumrix.de/icd.php
- ICD Suchmaschine von Lumrix
- Geben Sie einfach Schilddrüse als Suchwort ein oder die Ihnen bekannte Nummer
- ICD Suchmaschine von Lumrix
Krankheiten der Schilddrüse
[Bearbeiten]| ICD-10-GM 2007 |
|---|
| E00-E07 - Krankheiten der Schilddrüse |
Allgemeines
[Bearbeiten]Schilddrüsenkrankheiten treten mit ungefähr 3:1 häufiger bei Frauen als bei Männeren auf. Dies gilt nicht nur für die Jodmangelkrankheiten wie den Kropf und die Autonomen Knoten , sondern auch für die Autoimmunerkrankungen der Schilddrüse. In Ländern mit einer ausreichenden Jodversorgung sind Krankheiten der Schilddrüse weitaus seltener als in Jodmangelgebieten.
Häufige Krankheiten
[Bearbeiten]Die häufigsten Krankheiten der Schilddrüse sind:
- Jodmangelstruma = Kropf
- ohne Knoten, diffus
- mit Knoten
- Überfunktion der Schilddrüse
- Morbus Basedow
- Autonome Adenome
- Entzündungen der Schilddrüse
- Unterfunktion der Schilddrüse
- Schilddrüsenkrebs
- Kretinismus
Daneben gibt es einige seltene Schilddrüsenkrankheiten.
Iodmangel
[Bearbeiten]Allgemeines zum Thema Iodmangel
[Bearbeiten]Iodmangel entsteht, wenn der Körper über die Nahrung oder das Trinkwasser zu wenig des Spurenelements Iod aufnimmt. Iod wird nahezu ausschließlich zum Aufbau der Schilddrüsenhormone benötigt; ein Erwachsener benötigt täglich mindestens ca. 150 µg. Die Schilddrüse kann bei guter Versorgung 10 mg Iod bevorraten, das entspricht dem Iodbedarf für drei Monate. Die Deutsche Gesellschaft für Ernährung empfiehlt zur Sicherheit höhere Tagesdosen (Stand: 2005):
| Personengruppe | Empfohlene tägliche Aufnahme |
|---|---|
| Säuglinge | 50 - 80 µg |
| Kinder bis zum 9. Lebensjahr | 100 - 140 µg |
| Jugendliche und Erwachsene | 180 - 200 µg |
| Schwangere Frauen | 230 µg |
| Stillende Mütter | 260 µg |
Die Schilddrüse kann etwa 40 % des verzehrten Iods aus dem Blut aufnehmen und anreichern. Der Rest wird über den Darm und die Nieren ausgeschieden. Die Iodmenge, die täglich über den Urin ausgeschieden wird, ist ein gutes Maß für die Iodversorgung des Organismus. Der Messwert der täglichen Iodausscheidung wird auf Kreatinin bezogen, ein Stoffwechsel-Abfallprodukt, welches ebenfalls über den Urin ausgeschieden wird; so kann man einen altersunabhängigen Parameter erhalten. Der Sollwert beträgt nach Empfehlung der DGE 150 µg/g Kreatinin.
Die Weltgesundheitsorganisation (WHO) teilt den Iodmangel folgendermaßen ein:
| WHO-Grad des Iodmangels | Iodausscheidung |
|---|---|
| Kein Iodmangel | > 150 µg Iod / g Kreatinin im Urin |
| 0 | 100 - 150 µg/g |
| I | 50 - 100 µg/g |
| II | 180 - 200 µg |
| III | 25 - 50 µg/g |
| IV | < 25 µg/g |
Ursachen
[Bearbeiten]In Mitteleuropa enthalten die landwirtschaftlich genützten Böden vergleichsweise wenig Iodid (Salzverbindungen des Iods). Dies gilt nicht nur für die Alpenregion, auch die Böden der Küstenebenen (Dänemark, Niederlande) sind relativ iodarm.
Europäischer FOREGS-Atlas, 2005 (Forum of the European Geological Surveys Directors, Text/PDF, Karte).
Die Böden der humiden Klimazonen sind deswegen so arm an Iod, weil dieses im Laufe der Erdgeschichte ausgewaschen wurde. Der Iodgehalt in der sekundären Umwelt (Wasser, Ackerböden) ist vielen Einflussfaktoren unterworfen. Meeresferne, gebirgige Regionen sind eher von Iodmangel betroffen als das Flachland
Symptome
[Bearbeiten]Geringer Iodmangel verursacht zunächst keine Symptome. In der Embryonalentwicklung und in den ersten drei Lebensjahren kann es aber zu einer Beeinträchtigung der Hirnentwicklung mit resultierenden Entwicklungsverzögerungen (Motorik, Sprache, Verhalten, Aufmerksamkeit und Intelligenz) kommen. Der über Jahrzehnte beständige Wachstumsreiz auf das Schilddrüsengewebe kann einen Kropf verursachen, Schilddrüsenknoten oder krankhaft erhöhte Hormonproduktion.
Ausgeprägter Iodmangel kann eine Unterproduktion von Schilddrüsenhormon verursachen, allerdings kommt dies in Mitteleuropa aufgrund der gestiegenen Iodaufnahme praktisch nicht mehr vor. Hauptursache für Unterfunktionen ist heute die Hashimoto-Thyreoiditis, die nicht auf Iodmangel beruht, sondern von einer Überversorgung mit Iod tendenziell begünstigt wird. Früher drohten bei mangelversorgten Müttern auch Fehlgeburten und Fehlbildungen des Kindes. Kleinkinder konnten unbehandelt an schweren Entwicklungsstörungen leiden ( Kretinismus).
Vorbeugung
[Bearbeiten]Bereits im alten China empfahlen Ärzte den Verzehr von Meeresalgen und Schwämmen. In Meersalz ist entgegen der geläufigen Vorstellung kaum Iod enthalten. Seit dem 19. Jahrhundert ist reines Iodid verfügbar. In Fleischwaren, Milchprodukten, Brot, Fertiggerichten, Kantinenessen und handelsüblichem Kochsalz wird es zur Steigerung der Iodversorgung auf freiwilliger Basis zugesetzt. Iodsalz enthält in Deutschland 20 µg Iod pro g Salz in Form von Kaliumiodat; in der Schweiz liegt die Konzentration nicht höher als in Deutschland - jedoch der Anteil des Iodsalzes bei den gewerblichen Lebensmitteln (Schweiz: um 70%, Deutschland: um 30%). Die haushaltsübliche Iodsalzmenge erhöht die Iodversorgung der Konsumenten um ca. 20 µg täglich, hinzu kommt das Iod in Fertignahrungsmitteln. Außerdem wird in mehreren Ländern, unter anderem in Deutschland, das Tierfutter iodiert. Grenzwerte legt die EU fest.
In Gebieten, in denen eine Salziodierung nicht möglich ist, kann im Ein- oder Zweijahresrythmus mit einer mit Iod angereicherten Ölkapsel supplementiert werden. Dies ist meist in Entwicklungsländern der Fall, wenn die Salzversorgung dezentralisiert ist, oder die Salzgewinnung privat erfolgt.
Eine gesetzlich vorgeschriebene Iodprophylaxe gibt es
- in der Schweiz,
- in Österreich,
- den USA
sowie bis zur Wiedervereinigung in der DDR. Im vereinigten Deutschland setzt der Gesetzgeber auf Freiwilligkeit.
Situation in Deutschland
[Bearbeiten]Zahlreiche epidemiologische Arbeiten der letzten Jahrzehnte belegen den natürlichen Iodmangel in Deutschland. Die größte Studie (ca. 6000 Personen) wurde von Hampel et al. 1993-1994 erhoben und 1995 vorgelegt. Die durchschnittliche Urin-Iodausscheidung betrug 72 µg Iod pro g Kreatinin.
- Nur 9 % der Probanden war ausreichend (> 150 µg/g) mit Iod versorgt.
- 17 % hatten einen Iodmangel Grad 0 (WHO),
- 25 % Grad I,
- 17 % Grad II und
- 2 % Grad III.
Bewohner der Küstenregionen hatten keine höhere Iodausscheidung als die Einwohner der Mittelgebirge und des Voralpenlandes.
Die Iodmangelsituation führte noch Ende der 90er Jahre in Deutschland zu ca. 100.000 Schilddrüsen-Operationen jährlich. Iodsalz war zwar schon seit 1959 verfügbar, jedoch bis 1981 zunächst nur für Krankenbehandlungen zugelassen. Erst 1989 wurde es in die Zusatzstoffzulassungsverordnung aufgenommen und in den folgenden Jahren auch die Deklarationspflichten für die Produzenten reduziert.
Durch die Öffentlichkeitsarbeit der Bundeszentrale für gesundheitliche Aufklärung und des industriefinanzierten Arbeitskreises Jodmangel und die zunehmende Verwendung von Iod-angereichertem Speisesalz in Haushalten (83 %), in Großküchen und in der Nahrungsmittelindustrie (29 %) hat sich seither die Iodausscheidung nach neueren Studien deutlich erhöht, vor allem bei Kindern. Flächendeckende Daten liegen noch nicht vor, doch ist wegen der Freiwilligkeit dieser Maßnahmen mit hohen regionalen und individuellen Schwankungen zu rechnen. Auch die neuesten Studien zeigen immer noch einen hohen Anteil von unterversorgten Personen. Die Messungen von Hampel et al. 2001 an 3000 Schulkindern aus 128 Städten in Deutschland ergaben z.B. eine mittlere Iodausscheidung von 148 µg/g, jedoch hatten 27 % noch immer einen Iodmangel Grad I oder schlechter. Ein Bericht der WHO gruppiert Deutschland im Jahr 2003 als "optimal versorgt" (bis auf Schwangere und Stillende). Nach Vorgabe der WHO sollten alle 5 Jahre flächendeckende Daten zur Iodversorgung erhoben werden. Dies ist in Deutschland 1996 und 2006 erfolgt.
Zur aktuellen epidemiologischen Situation der Iodversorgung von Kindern und Jugendlichen liegen Ergebnisse aus dem Kinder- und Jugendgesundheitssurvey des Robert Koch-Instituts vor: mediane Iodurie von 117 µg/l. http://www.kiggs.de/experten/downloads/Basispublikation/Thamm_Jod.pdf. Die Situation der Anwendung von Schilddrüsenpräparaten von Erwachsenen und zu Serumspiegeln der Schilddrüsenhormone wird in einer GBE-Publikation aus den bevölkerungsrepräsentativen Daten der RKI-Gesundheitssurveys dargestellt.
Folgen des Iodmangels
[Bearbeiten]Ein chronischer Iodmangel führt an der Schilddrüse zunächst zu einer Größenzunahme ( Hyperplasie später Hypertrophie ) Dies macht sich als "Kropf" (Struma) bemerkbar. Die Iodmangelstruma war in früheren Jahrhunderten geradezu das Kennzeichen ganzer Bevölkerungen, z.B. in Bayern, der Schweiz oder Österreich. Besteht der Iodmangel längere Zeit, kann sich eine sogenannte Knotenstruma mit autonomen Adenomen entwickeln. Wird die Iodmangelsituation dann plötzlich behoben (z.B. durch vermehrte Iodzufuhr mit der Ernährung oder durch Gabe von stark iodhaltigen Röntgenkontrastmitteln), kann sich durch überschießende Hormonproduktion durch die autonomen Areale eine Schilddrüsenüberfunktion entwickeln.
Die Hormone T3 und T4sind von entscheidender Bedeutung für die frühkindliche Entwicklung des Gehirns. Ein bei Geburt bestehender ausgeprägter Mangel an diesen Hormonen führt zur mehr oder minder schweren geistigen Schäden (bis zum Kretinismus). Deswegen wird routinemäßig jedes Neugeborene auf das Vorliegen einer Hypothyreose (Schilddrüsenunterfunktion) untersucht um diese möglichst bald zu behandeln. Wird die Behandlung nur um wenige Wochen verzögert, kann dies eine geistige Behinderung zur Folge haben, die eine spätere höhere Schulbildung nicht mehr möglich macht. Die häufigste Ursache für die Hypothyreose beim Neugeborenen ist die unzureichende Iodzufuhr während der Schwangerschaft. Daher ist die ausreichende Iodzufuhr gerade in der Schwangerschaft von besonderer Bedeutung. Eine zusammenfassende Analyse aus 10 verschiedenen Studien zeigte, das ein chronischer Iodmangel zu einer mittleren Intelligenzquotient-Minderung um 13,5 Punkte führte.
Bleichrodt N, Born MP. A meta-analysis of research on iodine and its relationship to cognitive development. In: Stanbury JB (ed.): The damaged brain of iodine deficiency. New York, Cognizant Communication, 1994:195–200. Dass chronischer Iodmangel bei Kindern zu Intelligenzminderung führt wurde durch Studien aus allen Teilen der Welt belegt.
- Pineda-Lucatero A, Avila-Jiménez L, Ramos-Hernández RI, Magos C, Martínez H. Iodine deficiency and its association with intelligence quotient in schoolchildren from Colima, Mexico. Public Health Nutr. 2008 Jan 21:1-9 PMID 18205986
- Qian M, Wang D, Watkins WE, Gebski V, Yan YQ, Li M, Chen ZP. The effects of iodine on intelligence in children: a meta-analysis of studies conducted in China. Asia Pac J Clin Nutr. 2005;14(1):32-42. PMID 15734706
- Santiago-Fernandez P, Torres-Barahona R, Muela-Martínez JA, Rojo-Martínez G, García-Fuentes E, Garriga MJ, León AG, Soriguer F. Intelligence quotient and iodine intake: a cross-sectional study in children. J Clin Endocrinol Metab. 2004;89(8):3851-7. PMID 15292317.
Iodmangel gilt als the world's greatest single cause of preventable brain damage and mental retardation (die weltgrößte vermeidbare Ursache von geistiger Behinderung).
Delange F. Iodine deficiency as a cause of brain damage. Postgrad Med J. 2001;77(906):217-20. PMID 11264481
Probleme
[Bearbeiten]Daten aus den Ländern mit gesetzlich verpflichtender Salziodierung wie Österreich zeigten, dass es während der ersten Jahre nach der Einführung bei höherer Iodierung zu einer Verstärkung von Autoimmunerkrankungen der Schilddrüse (Morbus Basedow) kommen kann (http://steiermark.orf.at/stories/147669/), anschließend zu einer Verminderung (Baltisberger BL, et al.: Decrease of incidence of toxic nodular goitre in a region of Switzerland after full correction of mild iodine deficiency. Eur J Endocrinol 132 (1995):546-549 Abstract). Eine optimale Prophylaxe sollte deshalb bedarfsgerecht, d.h. unter Vermeidung eines Überangebots, erfolgen und sorgfältig epidemiologisch überwacht werden. Patienten mit solchen Erkrankungen sollten frühzeitig identifiziert und behandelt werden.
Kritiker der Iodierung wie der Journalist Udo Pollmer weisen darauf hin, dass die Hersteller für mögliche Schäden bei Konsumenten nach dem Produkthaftungsrecht haften (http://das-eule.de/1296.html). Sie kritisieren dabei nicht den hohen Iodgehalt von Meeresfisch, sondern die Tierfutteriodierung, die den Iodgehalt von Milchprodukten von Milch und Eiern in einigen Ländern stärker erhöht hat, ohne dass die Verbraucher darüber aufgeklärt wurden. Um gesundheitlichen Schäden vorzubeugen, hat die Europäische Behörde für Lebensmittelsicherheit empfohlen, die erlaubte Iodierung des Tierfutters, also letztlich auch die der Menschen, einzuschränken (http://www.efsa.europa.eu/de/science/feedap/feedap_opinions/808.html). Daraufhin wurden per EU-Verordnung Nr.1459/2005 die Obergrenzen für die Jodierung des Tierfutters für Hühner und Kühe halbiert. Die EU hat hierbei versucht, die gesamte Iodaufnahme des Menschen, der am Ende der Nahrungskette steht, zu berücksichtigen. Allerdings sind bei voller Ausreizung des aktuellen Grenzwerts (5mg/kg) und ausschließlicher Kraftfutterfütterung immer noch Dosen von 400 - 1200 µg/l in Kuhmilch möglich (http://idw-online.de/pages/de/news150087 ), was einem Vielfachen der empfohlenen Tagesdosis entspricht. In Deutschland beträgt der Iodgehalt des Kraftfutters nur 1 mg/kg bei durchschnittlich 50 % Kraftfutter-Anteil (mit resultierendem durchschnittlichem Milch-Iodgehalt von 100 µg/l) (Flachowsky G, et al.: Zur Jodanreicherung in Lebensmitteln tierischer Herkunft. Ernährungs-Umschau 53 (200):17ff).
Die Stiftung Warentest bestimmte in einem großen Milchtest (Heft 11/2007) auch den Milch-Iodgehalt: Er lag zwischen 30 und 180 µg/l; Bio-Milchen lagen dabei im unteren Drittel dieser Spanne.
Quellen
[Bearbeiten]Weblinks
[Bearbeiten]- Arbeitskreis Jodmangel
- Iodine Status Worldwide. WHO 2004 (englisch, PDF)
- Zur Jodanreicherung in Lebensmitteln tierischer Herkunft, Ernährungsumschau 2006
- Karte zur Tierfutterjodierung in Europa
- Standpunkt des Bundesinstituts für Risikobewertung zur Iodprophylaxe, 2004 (PDF)
- Standpunkt der Dtsch. Ges. für Ernährung, 2003
- Bericht des Robert-Koch-Instituts über Schilddrüsenerkrankungen in Deutschland
Kropf (Struma)
[Bearbeiten]
Eine Vergrößerung der Schilddrüse wird als Kropf oder Struma bezeichnet.
Man kann den Kropf dann noch näher eingrenzen:
- Euthyreote Struma ( Kropf mit normaler Schilddrüsenhormonfunktion)
- Knotenkropf
- Hyperthyreote Struma ( Kropf mit Überfunktion der Schilddrüse)
Die Mehrzahl der Strumen sind euthyreot.
In der medizinischen Fachsprache sind folgende Begriffe üblich:
- Struma diffusa - Vergrößerung der Schilddrüse ohne Knoten
- Struma nodosa - Vergrößerung der Schilddrüse mit Knoten

Ein etwas grober Medizinermerksatz lautet: Ist der Hals dicker als der Kopf, dann handelt es sich um einen Kropf.
Allgemeines
[Bearbeiten]Die Struma (lateinisch struma „Drüsenschwellung“; Mehrzahl Strumae oder eingedeutscht Strumen) oder der Kropf bezeichnet eine sichtbare Vergrößerung der Schilddrüse. Der untere Halsbereich verdickt sich dabei. Die Schilddrüse hat bei der Frau im Mittel ein normales Volumen von bis zu 18 ml, beim Mann bis zu 25 ml. Bei hohem Jodangebot in der Nahrung ist sie kleiner, da hier nicht soviel jodverarbeitende Zellen notwendig sind. Sie kann sich bei einem Iodmangel um ein Mehrfaches vergrößern.
Ursachen
[Bearbeiten]Die Schilddrüse nimmt das aus der Nahrung angebotene Iod auf, speichert es und verbraucht es bei der Produktion der Schilddrüsenhormone Thyroxin und Triiodthyronin.

Bei Iodmangel wächst die Schilddrüse, um ihre Leistung erhöhen zu können. Sie kann dann bis zu 98 % des vom Körper aufgenommenen Jods aus dem Blut verwerten. Dies ist zunächst eine biologisch sinnvolle Anpassung an eine iodärmere Umgebung, bekommt aber Krankheitswert, wenn Funktionsbeeinträchtigungen und Beschwerden im Halsbereich hinzukommen.
Als Folge des Jodmangels entstehen in der vergrößerten Schilddrüse auch Zysten, sowie kalte und heiße Knoten. Ob der Jodmangel auch die Krebshäufigkeit erhöht ist statistisch unsicher. Sicherlich ist der Effekt nur gering, da der Schilddrüsenkrebs auch in Jodmangelgebieten nur selten ist.
Ein Kropf kann außerdem entstehen durch Schilddrüsenüberfunktion (Hyperthyreose) und Unterfunktion (Hypothyreose) verschiedener Ursache. Die genaue Klärung der Ursache muss einer Therapie immer vorausgehen, da bei Autoimmunerkrankungen eine zusätzliche Gabe von Iod nicht sinnvoll ist.
Eine Struma kann auch während der Schwangerschaft auftreten. Die Schilddrüse produziert während der Schwangerschaft vermehrt Thyroxin. Diese Mehrleistung kann manchmal als Kropf bei Schwangeren sichtbar werden. Meist verschwindet er einige Zeit nach der Entbindung wieder.
Haben sich in einem Kropf bereits Zysten oder Knoten gebildet, bilden sich diese in der Regel nicht mehr zurück.
Vorbeugung des Kropfes
[Bearbeiten]Zur Vorbeugung des Kropfes werden seit langem das Speisesalz und seit ein paar Jahren auch andere Lebensmittel in den Industrieländern mit Iod versetzt. Dadurch ist die Häufigkeit der Strumen stark zurückgegangen.
Allerdings ist ein Iodüberschuss bei Vorliegen autoimmuner Schilddrüsenerkrankungen (z. B. Morbus Basedow, Hashimoto-Thyreoiditis) zu vermeiden, was die Versorgung mit Lebensmitteln bei diesem Personenkreis schwierig macht, zumal auch über das Tierfutter Milch, Eier, Fleisch in unbekannter Menge Iod enthalten. Eine Pflicht zur Deklaration mit genauen Mengenangaben würde dieses Problem mindern.
Behandlung
[Bearbeiten]Zur Vorbeugung eines Kropfes wird bei Iodmangel Iodsalz oder Iodtabletten gegeben. Eine zusätzliche Verkleinerung der Schilddrüse kann man mit der Gabe des Schilddrüsenhormons Thyroxin erreichen. Man muß dabei allerdings darauf achten, daß man keine Überfunktion erzeugt.
Ist die Schilddrüse bereits knotig umgebaut, erreicht man meist weder durch die Jod noch durch die Hormongabe eine Verkleinerung des Organes.
Bei autonomen Knoten und beim Morbus Basedow ist die Jodgabe kontraindiziert.
Eine operativ Entfernung des Kropfes ist nur beim Verdacht auf Bösartigkeit und bei mechanischen Problemen beispielsweise der Einengung der Luftröhre notwendig.
Literatur
[Bearbeiten]- A five-year follow-up study of goiter and thyroid nodules in three regions withdifferent iodine intakes in China.
- Autor/-en: Yu, X; Fan, C; Shan, Z; Teng, X; Guan, H; Li, Y; Teng, D; Jin, Y; Chong, W; Yang, F; Dai, H; Yu, Y; Li, J; Chen, Y; Zhao, D; Shi, X; Hu, F; Mao, J; Gu, X; Yang, R; Tong, Y; Wang, W; Gao, T; Li, C; Teng, W
- Quelle: J Endocrinol Invest. 2008 Mar;31(3):243-50.
- Autor/-en: Yu, X; Fan, C; Shan, Z; Teng, X; Guan, H; Li, Y; Teng, D; Jin, Y; Chong, W; Yang, F; Dai, H; Yu, Y; Li, J; Chen, Y; Zhao, D; Shi, X; Hu, F; Mao, J; Gu, X; Yang, R; Tong, Y; Wang, W; Gao, T; Li, C; Teng, W
Gute Arbeit über die Auswirkungen des Jodmangels an der Schilddrüse
- Medizinische Klinik
- Volume 100, Number 9, 542-546, DOI: 10.1007/s00063-005-1074-5
- Die LISA-Studie—eine randomisierte, doppelblinde, vierarmige, plazebokontrollierte, multizentrische Studie an 1 000 Patienten über die medikamentöse Therapie der Struma in Deutschland
- Martin Grussendorf, Renate Vaupel, Christoph Reiners, Karl Wegscheider and
- http://clinicaltrials.gov/ct2/show/NCT00277589
- Leider ohne Veröffentlichung der Ergebnisse
- Die LISA-Studie—eine randomisierte, doppelblinde, vierarmige, plazebokontrollierte, multizentrische Studie an 1 000 Patienten über die medikamentöse Therapie der Struma in Deutschland
- Volume 100, Number 9, 542-546, DOI: 10.1007/s00063-005-1074-5
- Endoscopic Minimally Invasive Thyroidectomy (eMIT): A Prospective Proof-of-Concept Study in Humans.
- Wilhelm T, Metzig A.
- World J Surg. 2010 Nov 19. [Epub ahead of print]
- Wilhelm T, Metzig A.
- Tumour Biol. 2010 Nov 16. [Epub ahead of print]
- Papillary thyroid carcinoma shows elevated levels of 2-hydroxyglutarate.
- Rakheja D, Boriack RL, Mitui M, Khokhar S, Holt SA, Kapur P.
- Papillary thyroid carcinoma shows elevated levels of 2-hydroxyglutarate.
- Korean J Radiol. 2010 Nov;11(6):594-602. Epub 2010 Oct 29.
- Role of Duplex Power Doppler Ultrasound in Differentiation between Malignant and Benign Thyroid Nodules.
- Algin O, Algin E, Gokalp G, Ocakoğlu G, Erdoğan C, Saraydaroglu O, Tuncel E.
- Role of Duplex Power Doppler Ultrasound in Differentiation between Malignant and Benign Thyroid Nodules.
- Med Clin North Am. 2010 Sep;94(5):1003-15.
- The patient with a thyroid nodule.
- Miller MC.
- The patient with a thyroid nodule.
- Benign predominantly solid thyroid nodules: prospective study of efficacy of sonographically guided radiofrequency ablation versus control condition.
- Baek JH, Kim YS, Lee D, Huh JY, Lee JH.
- AJR Am J Roentgenol. 2010 Apr;194(4):1137-42.
- Baek JH, Kim YS, Lee D, Huh JY, Lee JH.
- Utility of contrast-enhanced ultrasound for evaluation of thyroid nodules.
- Zhang B, Jiang YX, Liu JB, Yang M, Dai Q, Zhu QL, Gao P.
- Thyroid. 2010 Jan;20(1):51-7.
- Zhang B, Jiang YX, Liu JB, Yang M, Dai Q, Zhu QL, Gao P.
- Radiofrequency ablation (RFA) of benign thyroid nodules in patients with incompletely resolved clinical problems after ethanol ablation (EA).
- Lee JH, Kim YS, Lee D, Choi H, Yoo H, Baek JH.
- World J Surg. 2010 Jul;34(7):1488-93.
- Lee JH, Kim YS, Lee D, Choi H, Yoo H, Baek JH.
Weblinks
[Bearbeiten]- Informationen und Forum zu Schilddrüsenerkrankungen und NMUs
- http://edoc.hu-berlin.de/dissertationen/bittermann-heike-1999-10-22/HTML/bittermann.html
- Jodversorgung deutscher Wehrpflichtiger im Alter von 17,5 bis 21 Jahren
Knoten
[Bearbeiten]Was sind überhaupt Schilddrüsenknoten?
Der Begriff Knoten ist eine unscharfe Definition. Seine ursprüngliche Bedeutung ist eine tastbare Verhärtung der Schilddrüse. Dieser Begriff wurde dann durch andere Untersuchungsverfahren abgeändert,
- jede Lücke im Szintigramm wird als kalter Knoten bezeichnet
- jede vermehrte umschriebene Anreicherung im Szintigramm wird als heißer Knoten bezeichnet
- jeder umschriebene inhomogene Gewebsbezirk im Ultraschall wir als Knoten bezeichnet
Statt Knoten wäre oft die Bezeichnung "Bezirk" oder "Bereich" im Ultraschall und Szintigramm besser.
Schilddrüsenknoten sind in Jodmangelgebieten häufig und zum größten Teil gutartig.
Kriterien für gutartige Knoten
[Bearbeiten]- Familiäre Vorgeschichte einer Hashimoto Thyreoiditis
- Familiäre Vorgeschichte von gutartigen Knoten oder Kropf
- Zeichen der Schilddrüsenunter- oder überfunktion
- schmerzhafte Knoten
- ein weicher, glatter und verschieblicher Knoten
- mehrere ähnlich große Knoten in derselben Schilddrüse
- warme Knoten im Szintigramm
- Zysten im Ultraschall
- Im MIBI Szintigramm nicht speichernd
Kriterien für krebsverdächtige Knoten
[Bearbeiten]Die Liste enthält einige wichtige Kriterien, die einen Krebsverdacht begründen, die aber natürlich nicht immer zutreffen !!
- schnell wachsend I
- derb tastbar
- unregelmäßige Oberfläche
- nicht verschieblich
- szintigrafisch kalt
- im MIBI Szintigramm speichernd
- sonografisch echoarm
- solitär
- tastbare Lymphknoten
- Schilddrüsenkrebs in der Familie
- Alter < 20
- Alter > 70
- Männliches Geschlecht
- Neu aufgetretene Schluckbeschwerden
- Neu aufgetretene Heiserkeit
- Vorgeschichte mit Bestrahlungen im Kopf-Nackenbereich während der Kindheit
- In der Vorgeschichte bereits Schilddrüsenkrebs
- Menschen, die im Fallout Gebiet von Tschernobyl leben oder lebten.
- Tc-99m-MIBI-Tumorszintigraphie der Schilddrüse
- Sie kann bei negativem szintigraphischem Befund mit sehr hoher Wahrscheinlichkeit ein Malignom ausschließen.
Kalte Knoten
[Bearbeiten]
Der Begriff kalter Knoten kommt aus der Befundung von Schilddrüsen Szintigrammen. Jeder Bereich der im Szintigramm nicht anreichert wird zunächst als kalter Knoten bezeichnet. Dahinter kann sich dann auch eine einfache Zyste verbergen.
Beispiel
[Bearbeiten]- Beispiel eines kaltes Knotens am unteren Pol der linken schilddrüse.
Krebs oder nicht ?
[Bearbeiten]Die wichtigste Frage bei einem kalten Knoten ist die Frage: Kann der Knoten ein Krebsknoten sein oder nicht. Dies kann man vor allem an Hand der Kriterien für bösartige Knoten beantworten ( siehe oben). Wichtig sind sonografische Größenmessungen im Verlauf. Eine Zytologie ( Zelluntersuchung ) oder Histologie ( Gewebsuntersuchung) aus dem Knoten kann bei dieser Fragestellung weiter helfen. Auch wenn die Wahrscheinlichkeit eines Krebsknotens bei einem kalten Knoten höher ist als bei einem heißen Knoten, so sind immer noch 90 % aller kalten Knoten gutartig ( abhängig von der untersuchten Patientengruppe) .
Heiße Knoten
[Bearbeiten]
Der Begriff heißer Knoten kommt aus der Befundung von Schilddrüsenszintigrammen. Jeder Bereich der im Szintigramm vermehrt anreichert wird zunächst als heißer Bezirk bezeichnet. Meist verbirgt sich dahinter ein gutartiges, vermehrt Schilddrüsenhormon produzierendes autonomes Adenom.
- Siehe

Dieser Knoten wurde mit Alkohol verödet und war nach der Behandlung szintigrafisch verschwunden. Im Ultraschall war er noch als kleiner Narbenknoten nachweisbar. Die restliche Schilddrüse wurde wieder aktiv.
Die lokale Verödung von heißen Schilddrüsenknoten ist eine elegante Methode zur Behandlung solitärer autonomer Adenome. Im Gegensatz zur Radiojodtherapie wird die restliche Schilddrüse geschont. Leider gibt es kein Adressverzeichnis der Doktoren, die die Methode beherrschen. Auch wird sie nur schlecht vergütet. Deswegen kommt sie nur selten zur Anwendung.
Die Ampullen des 95 % Alkohols gibt es von der Firma Braun zu 10 Stück mit 20 ml Inhalt . 10 Ampullen kosten circa 35 Euro.
Wachstumsdynamik heißer Knoten
[Bearbeiten]Gibt es heiße Knoten, die unkontrolliert aktiv sind und an Hand des TSH Spiegel noch nicht erkennbar sind ?
Die Frage ist für einen einzelnen heißen Knoten leicht zu beantworten: Es hängt einfach von der Größe und Aktivität des heißen Knotens ab.
Ist der Knoten noch sehr klein ( unter 1 cm ), dann sind die Blutwerte noch normal.
Wird der Knoten langsam größer, dann bremst er die restliche SD und der TSH Spiegel sinkt ab. Die T3 und T4 Werte sind zu diesem Zeitpunkt noch normal. Woher die Hypophyse weiß, daß der Knoten vorhanden ist und die TSH Produktion reduziert, das ist bis heute nicht klar. Wahrscheinlich sind die T3, T4 Spiegel über den ganzen Tag betrachtet, eben doch schon etwas zu hoch.
Wird der Knoten noch größer ( so etwa ab 2 - 3 cm ) , dann kann die Hypophyse Ihre Produktion nicht mehr weiter drosseln , die restliche SD ist fast stillgelegt und der heiße Knoten produziert jetzt auch eindeutig meßbar zuviel T3 und T4 . Dann muß man den Knoten auch dringend behandeln.
Der zeitliche Verlauf des Wachstums ist dabei sehr langsam und zieht sich meist über mehrere Jahre hin.
Literatur
[Bearbeiten]- Abklärung des euthyreoten Schilddrüsenknotens: Wann punktieren? Stellenwert der Sonographie.
- DMW Deutsche Medizinische Wochenschrift 2009; 134 (49): S. 2498-2503
- Chirurgisches Forum 2008
- Deutsche Gesellschaft für Chirurgie, 2008, Volume 37, IX., 139-141, DOI: 10.1007/978-3-540-78833-1_51
- Thermoablationsverfahren an der Schilddrüse — Vergleich der Laserinduzierten Thermotherapie (LITT) und der Radiofrequenzinduzierten Thermotherapie (RFITT) als neue Therapiesysteme zur lokalen Behandlung von nodulären Schilddrüsenveränderungen
- Thomas Schumann, K. S. Lehmann, U. Zurbuchen, H. J. Buhr and J. P. Ritz
- Thermoablationsverfahren an der Schilddrüse — Vergleich der Laserinduzierten Thermotherapie (LITT) und der Radiofrequenzinduzierten Thermotherapie (RFITT) als neue Therapiesysteme zur lokalen Behandlung von nodulären Schilddrüsenveränderungen
- Deutsche Gesellschaft für Chirurgie, 2008, Volume 37, IX., 139-141, DOI: 10.1007/978-3-540-78833-1_51
- Wale A, Miles KA, Young B, et al.
- Combined 99mTc-methoxyisobutylisonitrile scintigraphy and fine-needle aspiration cytology offers
- an accurate and potentially cost-effective investigative strategy
- for the assessment of solitary or dominant thyroid nodules.
- Eur J Nucl Med Mol Imaging 2014; 41: 105–15
- Wienhold R, Scholz M, Adler JB, Günster C, Paschke R:
- The management of thyroid nodules—a retrospective analysis of health insurance data.
- Dtsch Arztebl Int 2013; 110(49): 827–34.
- The management of thyroid nodules—a retrospective analysis of health insurance data.
- Gharib H, Papini E, Paschke R, et al.:
- American Association of Clinical Endicrinologists, AME and European Thyroid Association
- medical guidelines for clinical practice for the diagnosis and management of thyroid nodules.
- J Endocrinol Invest 2010 33: 287–91
Links
[Bearbeiten]- http://www.sonoweb.de/kasu0401.htm
- Schönes Beispiel eine kalten Knotens mit Krebsverdacht
- http://www.laekh.de/upload/Hess._Aerzteblatt/2003/2003_06/2003_06_06.pdf
- gute Zusammenfassung des Themas
- http://www.meb.uni-bonn.de/nuclearmedizin/sdambulanz/mibi/mibi.html
- Kurze Erklärung der MIBI Szintigrafie
Zysten
[Bearbeiten]Die meisten Zysten der Schilddrüse sind harmlos und lassen sich leicht im Ultraschall erkennen und kontrollieren. Man kann Zysten leicht punktieren. Sie laufen aber nicht selten wieder voll.
Entzündungen (Thyreoiditis)
[Bearbeiten]Siehe http://www.schilddruesenpraxis.de/lex_entzuendung.html
Chronische Autoimmunthyreoiditis Hashimoto
[Bearbeiten]siehe weiter unten
Chronisch atrophische Thyreoiditis (Ord-Thyreoiditis)
[Bearbeiten]Morbus Basedow
[Bearbeiten]siehe weiter unten
Infektiöse Thyreoiditis
[Bearbeiten]Viral - bakteriell
Die bakterielle Thyreoiditis ist sehr selten. Die virale Thyreoiditis ist möglicherweise häufiger, es wird aber nur sehr selten der Beweis einer viralen Entzündung gebracht werden. So verläuft manche virale Entzündung unter dem Aspekt einer unspezifischen ungeklärten Schilddrüsenentzündung.
Subakute granulomatöse Thyreoiditis de Quervain
[Bearbeiten]Die subakute Thyreoiditis wurde erstmals 1904 von Fritz de Quervain beschrieben.
Ihre Ursache ist bis heute noch ungeklärt, vermutet wird eine vorausgehende Virusinfektion. Bei dieser Erkrankung bilden sich im Gewebe "Riesenzellen", was ihr deshalb auch den Namen Riesenzellenthyreoditis einbrachte. Symptom ist vor allem der bis ins Ohr, Ober- und Unterkiefer ausstrahlende Schmerz. Die Schmerzen im Halsbereich wechseln häufig von einer Seite auf die andere. Zusätzlich leiden die Patienten an allgemeinem Krankheitsgefühl, Fieber, Abgeschlagenheit und Leistungsschwäche, wie bei einem schweren viralen Infekt. Dabei geht der subakuten Thyreoiditis meist mit einem zeitlichen Abstand von einigen Wochen ein Atemwegsinfekt voraus. Durch die Entzündungsreaktion kommt es zu einer Schädigung der Thyreozyten. Als Folge werden die Schilddrüsenhormonspeicher ins Blut entleert. Im Blut steigt die Schilddrüsenhormonkonzentration deutlich an. Beschwerden im Sinne einer Hyperthyreose sind die Folge. Nach dieser vorübergehenden Phase folgt eine Hypothyreose, da das beschädigte Schilddrüsengewebe nicht mehr in der Lage ist, neue Schilddrüsenhormone zu produzieren. Die Erkrankung dauert meist 1 bis 4 Monate, selten auch mal bis zu 6 Monate. Durch eine entsprechende Therapie können die Symptome schnell abgemildert werden. Während eine ursachenspezifische Therapie nicht bekannt ist, sind die Symptome durch Gabe von Salicylsäure oder Diclofenac bei einer leichten bzw. von Glukokortikoiden bei einer schweren Thyreoiditis angehbar. Eine Behandlung der hormonellen Überfunktion ist wirkungslos. Nach Ausheilung behält die Schilddrüse in der Regel ihre normale Funktion. Manchmal entwickelt sich eine Unterfunktion, die durch die Gabe von Schilddrüsenhormon (L-Thyroxin) behandelt werden kann.
Postpartale Thyreoiditis
[Bearbeiten]Medikamentös induzierte Thyreoiditiden
[Bearbeiten]invasiv-fibrosierende Thyreoiditis Riedel
[Bearbeiten]Sehr selten , schwer zu behandeln. Siehe [8]
Paraneoplastische Thyreoiditis
[Bearbeiten]Iatrogene Thyreoiditis
[Bearbeiten]Stichwort Interferon
Hashimotothyreoiditis
[Bearbeiten]Allgemeines
[Bearbeiten]| ICD-10-Codes Hashimoto-Thyreoiditis | ||
|---|---|---|
|
Bei der Hashimoto-Thyreoiditis (auch lymphozytäre oder autoimmune Thyreoiditis) handelt es sich um eine Autoimmunerkrankung, die zu einer chronischen Entzündung der Schilddrüse führt. Bei dieser Erkrankung kommt es infolge eines fehlgeleiteten Immunprozesses zur Zerstörung des Schilddrüsengewebes durch T-Lymphozyten. Darüber hinaus ist eine Antikörperbildung gegen schilddrüsenspezifische Antigene nachweisbar. Diese Krankheit wurde nach dem japanischen Arzt Hakaru Hashimoto (1881-1934) benannt, der sie 1912 als erster beschrieb.
Literatur:
- Hashimoto, H. (1912)
- Zur Kenntnis der lymphomatösen Veränderung der Schilddrüse (Struma lymphomatosa).
- Archiv für klinische Chirurgie, Berlin 97: 219-248.
- Zur Kenntnis der lymphomatösen Veränderung der Schilddrüse (Struma lymphomatosa).
Es sind können 2 verschiedene Verlaufsformen unterscheiden werden:
- die Hashimoto-Thyreoiditis i.e.S. (Autoimmunthyreopathie Typ 1A und 2A), mit einer Vergrößerung der Schilddrüse.
- die Ord-Thyreoiditis (Autoimmunthyreopathie Typ 1B und 2B), mit einer Verkleinerung (Atrophie) der Schilddrüse. Sie wurde nach William Miller Ord benannt, der sie erstmals im Jahre 1878 beschrieb.
Literatur:
- Ord, W.M. (1878)
- On myxedema, a term proposed to be applied to an essential condition in the "cretinoid" affection occasionally observed in middle-aged women.
- Medico-Chir Trans 61: Seite 57.
- On myxedema, a term proposed to be applied to an essential condition in the "cretinoid" affection occasionally observed in middle-aged women.
Da sich die Symptome, Diagnostik, Therapie und Prognose der beiden Formen nicht wesentlich unterscheiden und beide Formen jeweils ineinander übergehen können, werden sie heute in der Regel unter dem Begriff der Hashimoto-Thyreoiditis zusammengefasst. Bei beiden Verlaufsformen, sowohl atrophe und hypertrophe Form, kommt es auf Dauer zu einer Schilddrüsenunterfunktion, wobei sich am Beginn der Erkrankung – bedingt durch die Zerstörung des Schilddrüsen-Gewebes – auch Phasen der Überfunktion zeigen können (sog. "Leck-Hyperthyreose", im Extremfall Hashitoxikose). Die Krankheit gilt als nicht heilbar.
Häufigkeit
[Bearbeiten]Die Hashimoto-Thyreoiditis ist eine der häufigsten Autoimmunerkrankungen des Menschen und die häufigste Ursache der primären Schilddrüsenunterfunktion. Eine US-Erhebung (http://www.ncbi.nlm.nih.gov/entrez/query.fcgi?itool=abstractplus&db=pubmed&cmd=Retrieve&dopt=abstractplus&list_uids=11836274) ergab bei 10 % der Probanden einer Bevölkerungsstichprobe erhöhte Antikörper und 5 % Hypothyreosen (0.3 % klinisch manifest). Eine neuere Studie (http://www.ncbi.nlm.nih.gov/entrez/query.fcgi?itool=abstractplus&db=pubmed&cmd=Retrieve&dopt=abstractplus&list_uids=15731735) ergab 10 % klinische und subklinische Hypothyreosen. Für Westeuropa liegen ähnliche Daten vor (http://www.ncbi.nlm.nih.gov/entrez/query.fcgi?db=pubmed&cmd=Retrieve&dopt=AbstractPlus&list_uids=2004476&query_hl=11&itool=pubmed_docsum, http://www.ncbi.nlm.nih.gov/entrez/query.fcgi?db=pubmed&cmd=Retrieve&dopt=AbstractPlus&list_uids=15731735&query_hl=14&itool=pubmed_docsum). Lehrbüchern zufolge liegt die Erkankungshäufigkeit der mit einer Hashimoto-Thyreoiditis häufig einhergehenden Schilddrüsen-Unterfunktion in Westeuropa bei 1-2 %; subklinische Verläufe sind jedoch häufiger und liegen im Bereich von 6-8% (Classen, Diehl, Kochsiek. Innere Medizin, 5. Auflage. Verlag Urban & Fischer). Frauen erkranken deutlich öfter als Männer (Verhältnis ca. 8 : 1 bis 10 : 1). Die Veranlagung für Hashimoto wird vererbt (d.h. es finden sich familiäre Häufungen), es kommt jedoch nicht zwangsläufig in jedem Fall zum Ausbruch der Krankheit. Bisherige Beobachtungen zeigen, dass die Hashimoto-Thyreoiditis häufig im Zusammenhang mit hormonellen Umstellungen (Pubertät, Entbindung, Wechseljahre), aber auch infolge von Belastungssituationen ausbrechen kann.
Ursachen
[Bearbeiten]Die genauen Wirkfaktoren, die zum Ausbruch einer Hashimoto-Thyreoiditis führen können, sind noch nicht hinreichend geklärt. Zur Debatte stehen neben einer familiären (genetischen) Vorbelastung (z.B. X-Chromosome Inactivation) auch Stress, schwer verlaufende Viruserkrankungen (wie Pfeiffer-Drüsenfieber), Dysfunktionen der Nebennierenrinde und Umweltauswirkungen nicht abschließend. Heftig debattiert wird z.Z. über die Bedeutung einer übermäßigen Iodzufuhr für den Ausbruch der Krankheit. Während als relativ sicher gelten kann, dass sie, genau wie Morbus Basedow, durch hohe Ioddosen (Iodexzess) ausgelöst werden kann (z.B. durch iodhaltige Kontrastmittel), werden die möglichen Gefahren, die von einer Iodierung der Nahrungsmittel (als Folge der Futtermitteliodierung bei Nutztieren und der Kochsalziodierung) ausgehen, kontrovers diskutiert.
Symptome und Krankheitsverlauf
[Bearbeiten]Aufgrund der möglichen anfänglichen Schilddrüsenüberfunktionen können für eine gewisse Zeit folgende Symptome im Vordergrund stehen:
- Nervosität
- Reizbarkeit
- Rastlosigkeit
- Zittern der Hände
- Schlafstörungen
- Schwitzen
- feuchtwarme Haut
- Heißhunger und Durst
- Gewichtsverlust trotz guten Appetits
- Störungen im Menstruationszyklus (unregelmäßige oder verstärkte Blutungen, Ausbleiben der Regelblutung)
Langfristig werden diese dann von Symptomen der Schilddrüsenunterfunktion abgelöst:
- Niedrige Körpertemperatur
- Erhöhte Kälteempfindlichkeit
- Ödeme (Schwellungen durch Wassereinlagerungen, besonders an Lidern, Gesicht, Extremitäten --> prätibiales Ödem)
- Kloß im Hals, Druckgefühl am oder im Hals, Strangulationsgefühl (auch nur phasenweise),
- Häufiges Räuspern und Hüsteln, heisere oder belegte Stimme (Stimmbandödem)
- Depressive Verstimmung, Motivationslosigkeit, Antriebslosigkeit
- Muskelschwäche
- Muskelverhärtungen
- trockene, rissige Haut und damit verbundener Juckreiz
- trockene Schleimhäute
- brüchige Haare und Fingernägel, Haarausfall
- schnelle und starke (fast unkontrollierbare) Gewichtszunahme
- Verdauungsstörungen
- verringerte Libido
- veränderter Zyklus (bei Frauen)
- Gelenkschmerzen
- Konzentrations- u. Gedächtnisstörungen
- Müdigkeit
Der Krankheitsverlauf ist bei einem Großteil der Erkrankten leicht, doch sind auch mittlere und schwere Verläufe bekannt. Die Symptome sind vielfältig und – gerade am Beginn der Erkrankung - schwer zu fassen. Dazu kommt, dass die Vielzahl und Variabilität der Symptome und der schleichende Verlauf es sowohl für den Patienten wie auch den behandelnden Arzt schwierig machen, sie zuzuordnen.
Neben körperlichen können auch eine Reihe psychischer Symptome in Erscheinung treten. Nicht selten werden Patienten wegen der unklaren Symptomlage als Hypochonder abgestempelt oder ihre Beschwerden als psychosomatisch eingestuft, ohne dass eine ausreichende Abklärung einer möglichen Schilddrüsen-Funktionsstörung erfolgt.
Unterfunktions-Symptome können bereits bei subklinischen (noch als euthyreot geltenden) Wertekonstellationen auftreten, weil der individuelle Wertespielraum in der Regel sehr viel kleiner ist als das auf statistischen Auswertungen beruhende, interindividuelle Referenzwertspektrum. Selbst subklinische Wertekonstellationen können daher bereits eine Minderung der Lebensqualität nach sich ziehen.
In extrem selten Fällen geht mit der Krankheit die Hashimoto-Enzephalopathie einher mit Symptomen wie epileptischen Anfällen, psychiatrischen Symptomen oder Halluzinationen.
Erkennung
[Bearbeiten]Diagnostisch relevant sind:
- TPO-AK (Antikörper gegen Thyreoperoxidase)
- TG-AK (Antikörper gegen Thyreoglobulin)
Im weit überwiegenden Teil der Fälle sind die Anti-TPO erhöht (mit oder ohne Erhöhung der Anti-TG). In einem weitaus geringeren Teil der Fälle sind nur die Anti-TG erhöht. Es existieren darüber hinaus - wenn auch selten - Fälle, in denen eine Hashimoto-Thyreoiditis vorliegt, ohne dass die genannten Antikörper erhöht sind.
Für die Stoffwechsellage der Schilddrüse sind folgende Werte relevant:
- TSH (Thyroidaea-Stimulierendes Hormon) ,
- T3 (Triiodthyronin --> Hormon der Schilddrüse, wird aus T4 gebildet), bzw. freies T3 = fT3 (Anmerkung: Freie Werte sind – v.a. bei Frauen - wesentlich aussagekräftiger als der gesamt-T-Wert, da die Gesamt-T-Werte im Gegensatz zu den "freien" Werten starken Wechselwirkungen mit den weiblichen Hormonen unterliegen und durch diese verfälscht werden können)
- T4 (Levothyroxin = L-Thyroxin = Tetraiodthyronin = Tetrajodthyronin --> Hormon der Schilddrüse), bzw. freies T4 = fT4 (Anmerkung: Freie Werte sind – v.a. bei Frauen - wesentlich aussagekräftiger als der gesamt-T-Wert, da die Gesamt-T-Werte im Gegensatz zu den "freien" Werten starken Wechselwirkungen mit den weiblichen Hormonen unterliegen und durch diese verfälscht werden können)
Eine Schilddrüsendiagnostik, die sich ausschließlich auf den TSH stützt, ist zur Erkennung einer Hashimoto-Thyreoidis meist nicht aussagekräftig genug. Denn auch normwertiges TSH und normwertige freie T-Werte sind keine Ausschlusskriterien für das Vorhandensein einer Hashimoto-Thyreoiditis.
Sehr wichtig zur Diagnosestellung ist zudem das Bild der Schilddrüse im Ultraschall, das typischerweise inhomogen und echoarm ist und damit auf den laufenden Zerstörungssprozess hinweist. Zudem kann die im Doppler-Sonogramm erkennbare verstärkte Durchblutung des Schilddrüsengewebes ein Hinweis auf das Vorhandensein eines Entzündungsherdes sein. Auch die Größe der Schilddrüse kann im Sonogramm beurteilt werden. Da die hypertrophe Form der HT mit einer Struma einhergehen kann, sind Größen über ca. 20 ml (Frauen) bzw. ca. 28 ml (Männer) Gesamtvolumen (Hashimoto-Thyreoiditis i.e.S.) als auffällig anzusehen. Kleine Schilddrüsen mit einer Größe unter 8 ml (Frauen) bzw. 12 ml (Männer) sind hingegen typisch für die atrophische Verlaufsform (Ord-Thyreoiditis), wobei einschränkend angemerkt werden muss, dass diese Größenangaben - je nach Autor - stark schwanken und Gegenstand der Diskussion sind. Hierzulande ist diese sogenannte atrophische Verlaufsform mit schrumpfender Schilddrüse häufiger als die hypertrophe Form mit Kropfbildung (Struma).
Insbesondere in der Anfangsphase der Erkrankung kann die Unterscheidung zwischen einer Hashimoto-Thyreoiditis und Morbus Basedow (eine Autoimmunerkrankung, die zur Überproduktion von Schilddrüsenhormonen führt) schwierig sein, da auch bei Hashimoto anfängliche Überfunktionsschübe auftreten können. Meist kann dann eine Szintigraphie Klarheit bringen.
Endgültige Sicherheit bringt die histologische (feingeweblich, mikroskopische) Untersuchung des Schilddrüsengewebes, man erkennt bei der Hashimoto-Thyreoiditis im Gegensatz zur gesunden Schilddrüse neben anderen Kriterien vor allem ein dichtes Infiltrat von Lymphozyten und auch Lymphfollikel (siehe Abbildung), die ein Ausdruck der entzündlichen Vorgänge sind.
Behandlung
[Bearbeiten]Die Hashimoto-Thyreoiditis selbst ist zum gegenwärtigen Zeitpunkt nicht heilbar; die Unterfunktion der Schilddrüse kann (muss) jedoch therapiert werden. Die Therapie erfolgt durch (einschleichende) Substitution von Hormonen, die der Körper aufgrund der chronischen Entzündung der Schilddrüse nicht mehr selber in ausreichendem Maße oder gar nicht mehr herstellen kann.
Die Substitution erfolgt durch die Gabe von Schilddrüsen-Hormonen. Dafür stehen unterschiedliche Präparate zur Verfügung:
- Thyroxin (=T4, Levothyroxin)
- Kombination von T4 und T3, wobei diese entweder als Kombinationspräparat mit festem T4/T3-Verhältnis oder als frei dosierbare Einzelpräparate verwendet werden.
Iod hingegen sollte bei einer Hashimoto-Thyreoiditis nicht zusätzlich eingenommen werden, da Iodüberschuss die Entzündung der Schilddrüse fördern kann.
Die Blutwerte TSH, fT3 und fT4 sollten regelmäßig überprüft werden, da sich im Laufe der Erkrankung Veränderungen einstellen, die eine Dosisanpassung erfordern. Zusätzlich sollte die Schilddrüse in regelmäßigen Abständen (alle 6-12 Monate) durch eine Sonographie auf ihrer Struktur hin geprüft werden.
Die erfolgreiche Einstellung dauert meist mehrere Monate. Bei der Behandlung ist sehr viel Geduld erforderlich. Je länger eine Unterfunktion andauert und je schwerer sie ist, umso langwieriger ist es in der Regel, einen befriedigenden Hormonstatus und Wohlbefinden zu erreichen. Auch Schwankungen oder Schübe können zum Krankheitsbild gehören und stellen erhöhte Anforderungen an Patient, Arzt und Umfeld.
Die zusätzliche Gabe von Selen ist noch nicht als wirksam anerkannt. Einzelne Studien scheinen eine positive Wirkung des Spurenelements auf Immunthyroiditiden zu belegen [9] [10].
Die genannten Behandlungsalternativen greifen jedoch nicht in allen Fällen. Die davon betroffenen Patienten sind aufgrund anhaltender Symptome dauerhaft in ihrer Lebensqualität beeinträchtigt.
Sonstiges
[Bearbeiten]Vorsorglich ist Erkrankten daher zu empfehlen, Iod in hohen Dosen zu meiden, da es die Aktivität der Schilddrüse erhöht, was die Angriffe des Autoimmunsystems verstärken kann. Iod- und Iodkombinationspräparate (u.a. als Nahrungsergänzungsmittel erhältlich) müssen also gemieden werden. Auch auf iodiertes Speisesalz, Meeresalgenprodukte, Seefisch und größere Mengen sonstiger iodreicher Lebensmittel sollte vorsichtshalber weitgehend verzichtet werden. Übliche Iodkonzentrationen in Lebensmitteln verursachen aber in der Regel keine unmittelbaren Probleme, wobei individuell höhere Empfindlichkeiten gegenüber Iod möglich sind.
Da eine Schilddrüsenunterfunktion manchmal mit einem Mangel an Spurenelementen, Selen, Eisen, Magnesium und Vitaminen (z.B. B6, B12) einhergehen kann, kann sich eine diesbezügliche Abklärung lohnen. Ebenso ist vor Beginn der Hormon-Substitution eine Abklärung erforderlich, ob eine Erkrankung der Nebennierenrinde vorliegt.
Mögliche Begleiterkrankungen
[Bearbeiten]Hashimoto-Patienten haben - gegenüber nicht-autoimmun Erkrankten - eine erhöhte Wahrscheinlichkeit, an weiteren Leiden mit möglichem oder gesichertem autoimmunologischem Hintergrund zu erkranken. Hierzu zählen unter anderem: Morbus Addison (sog. Schmidt-Syndrom), perniziöse Anämie, Diabetes vom Typ I, Sarkoidose, Morbus Crohn, Colitis ulcerosa, Vitiligo, Lichen sclerosus, Rosacea, Lupus erythematodes.
Bleibt die Hashimoto Thyreoiditis lange unerkannt, können unter anderem die Nebennieren geschwächt werden. Vor der Behandlung mit Schilddrüsenhormonen sollten deshalb immer die entsprechenden Werte im Blut kontrolliert und nötigenfalls Cortison verabreicht werden.
Zudem scheint ein Zusammenhang zu bestehen zwischen Hashimoto und unerfülltem Kinderwunsch:
- Bei erhöhtem TSH-Wert kann es durch die Ähnlichkeit des PRH (Prolaktin Releasing Hormone) mit dem Thyrotropin (TSH) zu einer Überproduktion des Prolaktins kommen, was wiederum den Eisprung verhindert.
- Da die Schilddrüse wesentlichen Anteil an der Steuerung der Sexualhormone hat, kann eine Schädigung der Schilddrüse durch Hashimoto zu einer Störung des Hormonhaushaltes führen. Eine optimal angepasste Einnahme von Schilddrüsenhormonen ist deshalb sehr wichtig. Einige Patientinnen machen sehr gute Erfahrungen mit natürlichen Schilddrüsenhormonen (aus Schweineschilddrüsen gewonnen, z.B. Armour Thyroid, etc.).
- Auch ist bei etwa 50% der Hashimoto-Frauen die Anzahl der natürlichen Abwehrzellen des Immunsystems erhöht, und es bestehen weitere Anzeichen für ein überreaktives Immunsystem. Es wird vermutet, dass die Eizellen deshalb Schwierigkeiten bei der Einnistung haben sowie ein erhöhtes Fehlgeburtsrisiko besteht.
Literatur
[Bearbeiten]- Mary Shomon: Die gesunde Schilddrüse, Was Sie unbedingt wissen sollten über Gewichtsprobleme, Depressionen, Haarausfall und andere Beschwerden im Zusammenhang mit Hashimoto Thyreoiditis. (Originaltitel: Living well with Hypothyroidism), Goldmann Verlag, 2002, ISBN 3442163889
- Leveke Brakebusch, Armin Heufelder: Leben mit Hashimoto Thyreoiditis. Ein Ratgeber. 2. Auflage (August 2005), Zuckschwerdt Verlag, ISBN 3886038831
- P.-M. Schumm-Draeger: Schilddrüsendiagnostik und -Therapie. Bayer. Ärzteblatt 4/2005
- Terry F. Davies (2003): Ord-Hashimoto's Disease: Renaming a Common Disorder - Again. Thyroid 13 (4) 317
Weblinks
[Bearbeiten]- Selbsthilfe-Netzwerk für Deutschland, Österreich und Schweiz
- Selbsthilfegruppe für autoimmune Schilddrüsen-Erkrankungen Österreich
- Die Schmetterlinge e. V.
- Schilddrüsenliga Deutschland e. V.
- www.schilddruesenspezialisten.de Authentische Erfahrungsberichte von Betroffenen, eine Arztliste, FAQ u. v. m
- Gute Zusammenfassung der Infos zum Thema Hashimoto
en:Hashimoto's thyroiditis
Überfunktion der Schilddrüsen
[Bearbeiten]Eine Hyperthyreose ist eine Schilddrüsenüberfunktion. Die Schilddrüse produziert zu viel der Hormone Thyroxin und Trijodthyronin. Das Gegenteil, ein Mangel an Schilddrüsenhormonen wird dagegen als Hypothyreose bezeichnet. Hyper heißt dabei zuviel und hypo heißt dabei zuwenig. Diese beiden Vorsilben kann man leicht verwechseln. Eine Sonderform der Hyperthyreose ist die Thyreotoxikose, wörtlich übersetzt ist das eine Vergiftung des Körpers mit Schilddrüsenhormon, d.h. also eine schwere Schilddrüsenüberfunktion.
Schweregrade
[Bearbeiten]Eine subklinische Hyperthyreose sind veränderte Laborwerte, die noch nicht mit Symptomen einhergehen.
Im Gegensatz dazu kann die latente Hyperthyreose mit Symptomen einhergehen oder asymptomatisch sein. Sie ist dadurch gekennzeichnet, daß die TSH-Aktivität im Blutserum erniedigt ist, die peripheren Schilddrüsenhormone Thyroxin (T4) und Trijodthyronin (T3) aber noch normal sind. Bei der manifesten Hyperthyreose sind dagegen sowohl die TSH-Aktivität als auch die Plasmaspiegel der peripheren Schilddrüsenhormone pathologisch.
Eine Hyperthyreose mit klinischen Beschwerden ist immer behandlungsbedürftig. Die schwerste und lebensbedrohliche Form ist die thyreotoxische Krise.
Ursachen der Schilddrüsenüberfunktion
[Bearbeiten]Englisches Wort für Hyperthyreose : hyperthyroidism
häufig:
[Bearbeiten]- Morbus Basedow: ein Autoimmunprozess - immunogene Form der Hyperthyreose, durch stimulierende TSH-Rezeptor-Autoantikörper verursacht,
- Autonome Knoten: Knoten, die von der Steuerung durch TSH unabhängig Jod aufnehmen und Hormon bilden, aber nicht bedarfsgerecht abgeben
- Hashimoto-Thyreoiditis: ein anfangs vermehrter Hormonaustritt infolge Zellzerstörung bei Entzündungen ("Freisetzungshyperthyreose").
selten:
[Bearbeiten]- eine periphere Überempfindlichkeit gegenüber Schilddrüsenhormon,
- eine Hyperthyreosis factitia bei Überdosierung von T4 oder T3;
- übermäßige Einnahme von Schilddrüsenhormonen ( iatrogene Hyperhyreose )
- eine postpartale Hyperthyreose bei postpartaler Thyreoiditis
sehr selten:
[Bearbeiten]- ein TSH produzierender Hypophysentumor (leicht erkennbar an einer erhöhten TSH-Konzentration bei hohem FT3-Spiegel),
- extrathyreoidale SD Hormonproduktion ( zb Zungengrundstruma mit heißem Knoten )
- eine paraneoplastisch vermehrte Produktion stimulierender Substanzen,
- erhöhte Hormonproduktion durch große Tumormasse eines differenzierten Schilddrüsenkarzinoms.
- Jodexzeß
- Thyreoidea- Hormon-Rezeptor-ß (THRB, THR1, ERBA2) - Resistenz
Latente Hyperthyreose
[Bearbeiten]TSH-Suppression, FT3 und FT4 normal
Nichtthyreoidale Ursachen für eine Laborkonstellation der latenten Hyperthyreose
[Bearbeiten]- Schwere andere Erkrankungen (Nonthyroidal illness, NTI):
- Organinsuffizienzen,
- Tumoren,
- Hunger,
- Anorexie,
- Alkoholismus,
- Cushing-Syndrom,
- Hypophysenvorderlappeninsuffizienz,
- Nebennierenrindeninsuffizienz,
- "Critical illness"
- Medikamente:
- Schilddrüsenhormone,
- Jodid,
- Glukokortikoide,
- Dopamin und -agonisten,
- Somatostatin und -analoga,
- Neuroleptika,
- Phenytoin,
- Kalziumantagonisten,
- Salizylate,
- Heparin
- Fortgeschrittenes Alter
- Depression
- Labortechnische Störeinflüsse
Thyreoidale Ursachen für eine Laborkonstellation der latenten Hyperthyreose
[Bearbeiten]- Behandelte Hyperthyreosen jeder Genese (während und öfter persistierend auch nach Therapie)
- Latente Hyperthyreose jeder Genese (Alle mit Hyperthyreosen einhergehenden Thyreopathien sind möglich)
- Asymptomatische latente Hyperthyreose (inzidentelle biochemische Aktivität)
- symptomatische latente Hyperthyreose
Literatur:
[Bearbeiten]- Latente Hyperthyreosen
- U. Tuschy, M. Derwahl, U. Deuß, R. Hampel, W. Meng, A. Meyer, J.Rendl, B. Saller
- UNI-MED Verlag AG, D-28323 Bremen
- U. Tuschy, M. Derwahl, U. Deuß, R. Hampel, W. Meng, A. Meyer, J.Rendl, B. Saller
Symptome der Überfunktion
[Bearbeiten]- Herzrasen : Ruhe-Puls über 90/min
- evtl. Hochdruck, Herzrhythmusstörungen
- evtl. erhöhte Blutdruckamplitude
- (Hoher systolischer Blutdruck, niedriger diastolischer Blutdruck)
- Unruhe, Hyperaktivität
- Gewichtsabnahme trotz übermäßigem Appetit
- vermehrtes Schwitzen, Überempfindlichkeit gegen Wärme
- Ist die Haut warm und feucht? Liegt eine vermehrte Zittrigkeit vor?
- evtl. Durchfall, Haarausfall etc.
- evtl. Schlaflosigkeit
- depressive Verstimmung bis zur Depression
- Reizbarkeit
- Augenerkrankungen (typisch für Morbus Basedow):
- Hervortretende Augen (Exophtalmus), trockene, brennende Augen, einseitig oder beidseitig (endokrine Orbitopathie)
Anamnesefragen
[Bearbeiten]- Ist Ihnen häufig warm, schwitzen Sie leicht?
- Sind Sie nervös und unruhig, leicht reizbar?
- Leiden Sie unter Konzentrationsstörungen?
- Haben sie einen schnellen Pulsschlag oder manchmal Herzrasen?
- Haben Sie aus unerklärlichen Gründen an Gewicht verloren?
- Haben Sie Schlafstörungen?
- Haben Sie häufig Stuhlgang, teilweise durchfallartig?
- Können Sie schlecht schlucken, haben Sie ein Engegefühl im Hals?
Diagnose
[Bearbeiten]- Bestimmung der Schilddrüsenhormonwerte T3, T4 und TSH und TRAK im Blut
- Ultraschall der Schilddrüse
- Szintigrafie der Schilddrüse
Beispiel einer typischen Hyperthyreose bei Morbus Basedow
[Bearbeiten]- FT4 5,5 ng/dl (normal 0,71 - 1,85)
- FT3 22,5 pg/ml (normal 1,64 - 3,45)
- TSH < 0,03 mU/l (normal 0,3 - 4,00)
- TRAK 20 mU/l (normal < 1)
In 90 % der Fälle sind die Auto-Antikörper TRAK bei Basedow positiv (diagnostischer Beweis). Bei autonomen Adenomen (heiße Knoten) sind die TRAK meist negativ und die Schilddrüse ist auch im Ultraschall oder der Szintigraphie sichtbar anders verändert, als bei Basedow.
Behandlung
[Bearbeiten]- Schilddrüsenbremsende Medikamente z. B. Thiamazol
- Betablocker
- Radiojodbehandlung
- Operative Entfernung der Schilddrüse
- Einzelne heiße Knoten können durch eine gezielte Alkoholverödung behandelt werden.
Weblinks
[Bearbeiten]Thyreotoxische Krise
[Bearbeiten]| ICD-10-Code | ||
|---|---|---|
|
Eine thyreotoxische Krise ist eine lebensbedrohliche Verschlimmerung einer Schilddrüsenüberfunktion. Meist entwickelt sich die Krise ziemlich akut.
Einteilung
[Bearbeiten]Grad 1
- Herz
- Tachykardie, oft absolute Arrhythmie
- Extreme Sinustachykardie (>150/min) oder Tachyarrhythmie bei bestehendem Vorhofflimmern
- Herzinsuffizienz durch Tachykardie
- Tachykardie, oft absolute Arrhythmie
- Hyperthermie
- hohes Fieber (38-41°C) mit Schwitzen
- Gastrointestinale Symptome
- Nausea
- Erbrechen
- profuse Durchfälle
- Exsikkose, Dehydratation
- Neurologische Symptome:
- Tremor,
- Unruhe, Agitiertheit
- Muskelschwäche vor allem der proximalen Muskulatur und des Schultergürtels und/oder Bulbärparalyse
Grad 2
- Zusätzlich zu Grad 1
- Bewußtseinsstörungen (Somnolenz,Stupor),
- Desorientiertheit und psychotische Symptome
Grad 3
- Zusätzlich zu Grad 1
- Koma
- Grad 3a:
- jünger als 50 Jahre
- Grad 3b:
- älter als 50 Jahre
- Grad 3a:
- Koma
Diagnose
[Bearbeiten]- TSH niedrig
- T3 und T4 erhöht
Diagnostisches Punktesystem bei thyreotoxischer Krise
[Bearbeiten]Körpertemperatur (°C) Punkte ---------------------------- 37,2–37,7 5 37,8–38,2 10 38,3–38,8 15 38,9–39,4 20 39,5–39,9 25 > 40 30 ---------------------------- Herzfrequenz Punkte ---------------------------- 99–109 5 110–119 10 120–129 15 130–139 20 >140 25 ---------------------------- ZNS Symptome Punkte ---------------------------- mild (Agitiert) 10 mässig 20 (Delirium, Psychose, Lethargie) schwer 30 (Krampfanfall, Koma) ---------------------------- Herzinsuffizienz Punkte ---------------------------- mild 5 (Knöchelödeme) mässig 10 (bilaterale Rasselgeräusche) schwer 15 (Lungenödem) Vorhofflimmern 10 ---------------------------- GI/Leber Symptome Punkte ---------------------------- mässig 10 (Diarrhoe, Übelkeit, Erbrechen,Abdominalschmerzen) schwer (Ikterus) 20 ---------------------------- Auslösende Faktoren Punkte ---------------------------- keine bekannt 0 bekannt 10
Der Gesamtpunktwert wird durch Addition der Punktwerte der einzelnen Rubriken ermittelt.
- Werte >45 sprechen für eine hohe Diagnosewahrscheinlichkeit
- Werte 25 - 44 sprechen für eine mittelere Diagnosewahrscheinlichkeit
- Werte < 25 sprechen für eine niedrige Diagnosewahrscheinlichkeit
(modifiziert nach Burch / Wartofsky )
Differentialdiagnose
[Bearbeiten]- hochfieberhafter Infekt + Hyperthyreose
- Entzugsdelir + Hyperthyreose
- Sepsis + Hyperthyreose
Therapie
[Bearbeiten]- Ein Patient mit einer thyreotoxischen Krise gehört auf eine Intensivstation
- intravenöse thyreostatische Therapie (Thiamazol ((Favistan)) 80 mg 3x/die)
- diese hohe Thiamazolgabe nur bei gesicherter thyreotoxischer Krise !!
- Kaliumperchlorat (1.200 - 2.000 mg/Tag)
- nur bei gesicherter Diagnose
- unselektiver β-Blocker (Propranolol,3 x 80 mg p.o./die)
- alternativ Metoprolol iv nach Herzfrequenz und Blutdruck
- alternativ Esmolol iv
- Esmolol 0,5 - 1 mg Bolus iv, dann 5 - 15 mikrog/kg/min
- Digitalis: bei Tachyarrhythmia absoluta
- Prednisolon intravenös (50 mg 3x/die)
- über einen zentralen Venenkatheter Flüssigkeits- und Kalorienzufuhr (3 l/die, 2500 Kcal/die)
- engmaschige Elektrolytkontrolle und Bilanzierung
- Paracetamol: Fiebersenkung
- Sedativa (z.B. Diazepam): Ruhigstellung
Reduktion und Umsetzung der Therapie auf Tabletten nach klinischem Bild und Laborkontrollen.
Literatur
[Bearbeiten]- Thyreotoxische Krise - : ein Update KARGER S. ; FÜHRER D. ; Deutsche medizinische Wochenschrift 2008, vol. 133,no10, pp. 479-484
- Cooper DS. Hyperthyroidism. Lancet 2003;362:459–68.
- Davies TF. New thinking on the immunology of Grave’s disease. Thyroid Today 1992;15:1–11.
- Klein I, Ojamaa K. Thyroid hormone and the cardiovascular system: from theory to practice. J Clin Endocrinol Metab 1994;78:1026–7.
- Ross DS. Hyperthyroidism, thyroid hormone therapy, and bone. Thyroid 1994;4:319–26.
- O’Brien T, Katz K, Hodge D, Nguyen TT, Kottke BA, Hay ID. The effect of the treatment of hypothyroidism and hyperthyroidism on plasma lipids and apolipoproteins AI, AII and E. Clin Endocrinol 1997;46:17–20.
- Burch HB, Wartofsky L. Life-threatening thyrotoxicosis. Thyroid storm. Endocrinol Metab Clin North Am 1993;22: 263–77.
- Cooper DS. Antithyroid drugs. N Engl J Med 1984;311: 1353–62.
- Roti E, Robuschi G, Gardini E, Montermini M, Salvi M, Manfredi A, et al. Comparison of methimazole, methimazole and sodium ipodate, and methimazole and saturated solution of potassium iodide in the early treatment of hyperthyroid Graves’ disease. Clin Endocrinol (Oxf) 1988;28:305–14.
- Geffner DL, Hershman JM. Beta-adrenergic blockade for the treatment of hyperthyroidism. Am J Med 1992;93:61–8.
- Torring O, Tallstedt L, Wallin G, Lundell G, Ljunggren JG, Taube A, et al. Graves’ hyperthyroidism. Treatment with antithyroid drugs, surgery, or radioiodine. A prospective,randomised study. Thyroid Study Group. J Clin Endocrinol Metab 1996;81:2986–93.
- Franklyn, The management of hyperthyroidism, New Engl J Med, 1994 330: 1731-1738
- Feely et al., Propranolol dosage in thyrotoxicosis, J Clin Endocrinol Metab, 1980 51:658-661
- Newman et al., Amiodarone and the thyroid : a practical guide to the management of thyroid dysfunction induced by amiodarone therapy, Heart 1998 79:121-127
- Daniels, Amiodarone-induced thyrotoxicosis, J Clin Endocrinol Metab, 2001 86(1) 3-8
- McKenna, Graves` disease, The Lancet, 2001 357: 1793-1796
- Martino et al., The effects of amiodarone on the thyroid, Endocrine Rev., 2001 22:240-254
- Bogazzi et al., Color flow doppler sonography rapidly differentiates type I and type II amiodaroneinduced thyrotoxicosis, Thyroid 1997 7: 541-545
- Chopra and Baber, Use of oral cholecystographic agents in the treatment of amiodarone-induced hyperthyroidism, J Clin Endocrinol Metab, 2001 86(10): 4707-4710
- Ligtenberg et al., Plasmapheresis in thyrotoxicosis, Ann Int Med 1999, 131: 71-72
- Aghini-Lombardi, Treatment of amiodarone iodine-induced thyrotoxicosis with plasmapheresis and methimazole, J Endocrinol Invest, 1993 16(10): 823-826
- Binimelis et al., Massive thyroxine intoxication : evaluation of plasma extraction, Int Care Med, 1987 13(1) :33-38
- Amaras and Marel, Failure of plasmapheresis, corticosteroids and thionamides to ameliorate a case of
protracted amiodarone-induced thyroiditis, Clin Endocrinol, 1996 45(3): 365-368
- Gough and Meyer-Witting, Surgery and anaesthesia for amiodarone-associated thyrotoxicosis, Aust N Z J Surg, 2000 70:155-156
- Claxton et al., Refractory amiodarone-associated thyrotoxicosis : an indication for thyroidectomy, Aust N Z J Surg, 2000 70:174-178
- Burger A.G., Philippe J. :Thyroid emergencies. Bailliere Clinical Endocrinology and Metabolism, 6,77-93,1992.
- Hehrmann R.: Thyrotoxic crisis. Pitfalls in diagnosis- intensive therapy. Fortschr Med.,114, 114- 117,1996.
- Die thyreotoxische Krise und das Myxödemkoma Zeitschrift Intensivmedizin und Notfallmedizin Heft Volume 41, Number 8 / November 2004 Seiten 573-582 S. Zierhut und C. Girlich
- Herrmann, J.: Neuere Aspekte in der Therapie der thyreotoxischen Krise (Übersicht). Dtsch. Med.Wochenschr. 103, 166 (1978)
- Pickardt, C. R., Gröschel, G., Horn, K., Rinke, H., Schramm, W., Unterholzner, H.: Plasmapherese an Hohlfasermembranen in der Behandlung der thyreotoxischen Krise. Verh. Dtsch. Ges. Inn. Med. 86 (1980)
- Das kann eine thyreotoxische Krise sein! BARWITZ Harald J. K. ; MMW. Fortschritte der Medizin ISSN 1438-3276 2002, vol. 144, no6, pp. 38-40
- B. Mödl, A. Wirtzfeld, R. Terfloth, H.J. Hetzer, M.M. Linder, A. Witzfeld: Thyreotoxische Krise mit Multiorganversagen, Intensivmed (1999), 36: 454-461
Links
[Bearbeiten]- http://www.medicalforum.ch/pdf/pdf_d/2005/2005-37/2005-37-075.PDF
- Fallbericht aus der Schweiz
- http://www.praxis.ch/pdf/2001/PX_19/Px_2001_90_853.pdf
- Fallbericht 2 aus der Schweiz
Basedowsche Krankheit (Graves Disease)
[Bearbeiten]| ICD-10-Codes Morbus Basedow | ||
|---|---|---|
|
Morbus Basedow oder Basedowsche Erkrankung (lateinisch „Morbus“ = die Krankheit) ist im deutschen Sprachraum benannt nach dem deutschen Erstbeschreiber (1840) Carl von Basedow. Im englischsprachigen Raum wird sie nach dem Erstbeschreiber Dr. Graves (1835) Graves Disease genannt, weitere Bezeichnungen sind Autoimmunthyreopathie Typ 3, Immunthyreopathie oder Immunhyperthyreose.

Allgemeines
[Bearbeiten]Es handelt sich um eine Autoimmunerkrankung, die im Allgemeinen eine mäßige Vergrößerung (Struma Kropf) und Überfunktion der Schilddrüse zur Folge hat. Die vom Körper gegen das Schilddrüsengewebe gebildeten Antikörper binden an den Rezeptor für Thyreotropin (TSH), ein Hormon welches von der Hypophyse (Hirnanhangdrüse) zur Stimulierung und somit zur Regelung der Schilddrüsenfunktion gebildet wird.
Diese Antikörper heißen TSH-Rezeptor-Antikörper (TRAK) und stimulieren nun ständig die hormonbildenden Zellen (Hyperthyreose). Positive TRAK beweisen einen Morbus Basedow. Gleichzeitig sinkt im Allgemeinen der Anteil des von der Hypophyse produzierten TSHs stark ab, weil die Hypophyse im Rahmen des Regelkreises von Hypophyse und Schilddrüse die Information bekommt, weniger TSH zu produzieren, weil bereits ausreichend Hormone gebildet werden (nur leider in einem pathologischen Zusammenhang, doch dies wird nicht differenziert).
Die Diagnose gelingt in vielen Fällen allein durch eine Blutuntersuchung. Erniedrigte (oft nicht messbare) TSH Werte und erhöhte Hormonwerte (idealerweise sollen die freien Hormone untersucht werden, also fT3 oder fT4) sowie das Vorhandensein von TRAK sind beweisend für einen Morbus Basedow. Als ergänzende Untersuchung wird oft eine Sonographie der Schilddrüse und gelegentlich auch eine Szintigraphie durchgeführt.
Frauen erkranken sieben Mal häufiger als Männer. Dabei liegt der Krankheitsbeginn bei ihnen häufig in Zeiten des hormonellen Umbruches (Pubertät, Schwangerschaft, Klimakterium). Insgesamt sind ca. 6 % der Bevölkerung betroffen. Es existiert eine genetische Anlage für die Krankheit. Weitere Ursachen der Erkrankung sind nach wie vor nicht geklärt.
Ursachen
[Bearbeiten]Wie bei vielen Autoimmunerkrankungen sind auch bei Morbus Basedow die genauen Ursachen der Krankheit nicht bekannt. Es wird davon ausgegangen, dass – neben der genetischen Veranlagung – ein oder mehrere Faktoren zum Ausbruch der Krankheit führen:
- Psychische Belastung (Stress). Stress als akuter Auslöser ist durch zahlreiche anekdotische Berichte belegt (unter anderem durch Erfahrungsberichte von Ferdinand Sauerbruch im 1. Weltkrieg und während seiner Zeit an der Charité in Berlin). Auch aktuelle Berichte liegen vor. Nach einer Studie im Fachblatt "Thyroid" stieg nach dem Krieg auf dem Balkan in den 1990ern die Zahl der Morbus Basedow Neuerkrankungen in Serbien deutlich an.
- Infektion durch Bakterien (Yersinien) oder Viren. Dieser Auslöser wird allerdings zunehmend kontrovers diskutiert.
- zu hohe Iodaufnahme zum Beispiel im Rahmen der Iodmangelprophylaxe, Kontrastmittelinjektionen oder Einnahme von stark iodhaltigen Medikamenten, wie z. B. Amiodaron. Allerdings führt eine hohe Jodaufnahme bei gesunden Menschen nur selten zu einem Morbus Basedow.
Symptome
[Bearbeiten]Die Symptome der Basedowschen Erkrankung bestehen aus den Symptomen der Schilddrüsenüberfunktion und denen der Immunerkrankung. Typisch für die Basedow-Erkrankung gilt die sog. Merseburger Trias (benannt nach dem Geburtsort Basedows, Merseburg):
- Struma (Kropf), eine Vergrößerung der Schilddrüse
- Tachykardie (Pulsbeschleunigung)
- Exophthalmus (Hervortreten des Augapfels)
Diese Trias sieht man heute nur noch selten, da die meisten Fälle von Basedow schon frühzeitig erkannt werden, so daß die Augensymptome nur noch selten zu finden sind.
Symptome der Schilddrüsenüberfunktion
[Bearbeiten]- Erhöhter Puls, Herzrasen, Herzrhythmusstörungen (vor allem Vorhofflimmern)
- hoher Blutdruck
- Nervosität, Reizbarkeit, Ruhelosigkeit
- Schlafstörungen
- Zittern der Hände, plötzliche Grobmotorik
- Wärmeintoleranz
- Schwitzen
- Gewichtsverlust trotz hoher Nahrungsaufnahme
- Durchfall
- Hunger
- Durst
- Zyklusstörungen
- Angst-/ Panikattacken
- häufiger nächtlicher Harndrang
Mögliche Symptome der Immunerkrankung
[Bearbeiten]- Augenerkrankung (Endokrine Orbitopathie)
- Gelenkschmerzen
- Rückenschmerzen
- Muskelschmerzen
- Haarausfall
- Ödeme an den Unterschenkeln (prätibiales Myxödem), welches sich durch eine gelbliche, bzw. blaurote und grobporige Schwellung an der Tibia (Schienbein) kennzeichnet.
Symptome der endokrinen Orbitopathie
[Bearbeiten]
Die bei Morbus Basedow sehr häufig vorkommende Augenerkrankung äußert sich in folgenden Symptomen
- Hervortreten der Augen
- Ungenügender Lidschluss
- Trockenheit
- erhöhte Lichtempfindlichkeit
- Druck- und Fremdkörpergefühl
- Rötung
- Vermehrtes Auftreten von Bindehautentzündungen
- Brennen und Tränen der Augen
- das Sehen von Doppelbildern
Beim letztgenanntem Symptom ist ein Augenarztbesuch nicht mehr aufzuschieben, denn die im Rahmen des Immunprozesses ablaufenden Veränderungen in der Augenhöhle führen nicht nur zu Fehlstellungen (Schielen), sondern können auch auf den Sehnerv drücken und zu bleibenden Schäden führen (eingeschränkte Sehfunktion!)
Therapie
[Bearbeiten]Bei der Therapie des Morbus Basedow handelt es sich immer nur um die Behandlung der Symptome. Eine Behandlung der Ursachen ist bislang nicht möglich.
Folgende Therapieformen werden zur Zeit eingesetzt:
Medikamentös
[Bearbeiten]Durch die Gabe von Thyreostatika (Thiamazol, Carbimazol, Propylthiouracil)wird der Iodeinbau in die Schilddrüse und damit die Hormonproduktion gehemmt. Die Therapiedauer beträgt 6 bis 12 Monate. Hierbei wird die Dosierung die Thyreostatika langsam so weit reduziert, bis normale Schilddrüsenhormonwerte im Blut nachzuweisen sind (Euthyreose). Danach wird das Medikament abgesetzt (Auslassversuch). Zum Teil kommt es hiernach zu einer spontanen (Selbst-)„Heilung“. Die Rezidivrate ist jedoch sehr hoch (insbesondere bei Patienten mit hohen TRAK Werten) und wird in der Literatur mit 40 - 60 % angegeben. Aufgrund der möglichen Nebenwirkungen der Thyreostatika (u. a. Verminderung der weißen Blutkörperchen, Erhöhung der Leberwerte) sollten diese nicht in zu hoher Dossis eingesetzt werden. Bei Vorliegen eines Rezidives ist eine weitere medikamentöse Therapie nicht mehr erfolgversprechend, so dass eine definitve Therapie (Radioiodtherapie oder Operation) empfohlen wird.
Radioiodtherapie
[Bearbeiten]Durch Gabe von radioaktivem Iod-131 werden die Zellen der Schilddrüse bei der Radioiodtherapie so geschädigt, dass sie innerhalb von 2-6 Monaten nach der Therapie die Produktion von Schilddrüsenhormonen einstellen. Je nach verabreichter Dosis ist eine nachfolgende Unterfunktion wahrscheinlich und Ziel der Therapie. Die lebenslange Einnahme von Schilddrüsenhormonen (als Tabletten oder Tropfen) ist dann notwendig. Im Gegensatz zu den Thyreostatika können diese relativ problemlos über lange Zeit eingenommen werden.
Operativ
[Bearbeiten]
Das Schilddrüsengewebe wird bei einer Schilddrüsenresektion bis auf einen minimalen Rest operativ entfernt. Die Nebenschilddrüsen, die für den Kalziumhaushalt des Körpers überlebenswichtig sind, müssen erhalten bleiben. Womit auch schon ein mögliches Operationsrisiko erwähnt wurde, nämlich die Beschädigung respektive versehentliche Mitentfernung der Nebenschilddrüsen (relativ seltenes Risiko, da diese im Falle einer Entfernung gegebenenfalls auch wieder eingepflanzt werden können) Patienten, denen die Nebenschilddrüsen fehlen oder deren Funktion dauerhaft gestört ist, müssen das fehlende Kalzium und Vitamin D als Tabletten, ggf. sogar per Infusion zu sich nehmen.
Ebenfalls besteht das Risiko einer Beschädigung des Stimmbandnerven, es kann zu einer vorübergehenden Sprachunfähigkeit (Rekurrensparese) kommen. Auch diese Komplikation ist heute seltener, da moderne Einsatzgeräte (Neuromonitor) in vielen Kliniken zum Einsatz kommen. Angestrebt wird auch hier eine Unterfunktion, die ebenfalls mit Tabletten oder Tropfen ausgeglichen wird, denn die nun fehlenden Schilddrüsenhormone müssen ersetzt werden, da der Körper auf sie angewiesen ist (gegeben wird in der Regel ein T4 Präparat, Thyroxin, es darf kein Iodpräparat verschrieben werden). Jedoch können auch Kombipräparate, eine Mischung aus T4 und T3, eingesetzt werden. Die Patienten sollten nach individueller Wohlfühldosis eingestellt werden, wobei ein TSH-Wert um 1 herum angestrebt wird.
Literatur
[Bearbeiten]- Graves RJ. New observed affection of the thyroid gland in females.(Clinical lectures.) London Medical and Surgical Journal (Renshaw), 1835; 7: 516-517. Nachdruck in Medical Classics, 1940;5:33-36.
- Von Basedow KA. Exophthalmus durch Hypertrophie des Zellgewebes in der Augenhöhle. [Casper's] Wochenschrift für die gesammte Heilkunde, Berlin, 1840, 6: 197-204; 220-228. Englische Übersetzung in: Ralph Hermon Major (1884-1970): Classic Descriptions of Disease. Springfield, C. C. Thomas, 1932. 2nd edition, 1939; 3rd edition, 1945.
- Von Basedow KA. Die Glotzaugen. [Casper's] Wochenschrift für die gesammte Heilkunde, Berlin, 1848: 769-777.
- Brakebusch / Heufelder / Zuckschwerdt: „Leben mit Morbus Basedow“ Ein Ratgeber für Betroffene. Ausführliche Erläuterungen zu Symptomen, Therapie, Hormonen und Ursachen, 2002, ISBN 3-88603-799-1
Weblinks
[Bearbeiten]- Gut verständliche, ausführliche Beschreibung der Krankheit
- www.morbusbasedow.de - Umfangreiche Informationen bezüglich der Krankheit, geschrieben von zwei Medizinern
- www.schilddruesenspezialisten.de Authentische Erfahrungsberichte von Betroffenen, eine Arztliste, FAQ u. v. m
Endokrine Orbitopathie (EO)
[Bearbeiten]Die endokrine Orbitopathie (EO) ist eine entzündliche Erkrankung der Augenhöhle, die meist im Zusammenhang mit einer autoimmunen Schilddrüsenerkrankung vom Typ Morbus Basedow auftritt. Ausmaß der Schilddrüsen Überfunktion, ein großes Schilddrüsen-Volumen und hohe TSH-Rezeptor-Antikörper (TRAK) Spiegel stehen in Zusammenhang mit einem schweren Krankheitsverlauf.
Rauchen und Stress zählen zu den Umwelteinflüssen, die die EO beeinflussen. Weiterhin besteht eine starke genetische Veranlagung. Die Festlegung des Klinischen Aktivitäts- Scores und des Schweregrades der EO ist Ausgangspunkt für die Stadien abhängige Therapie.
Bei aktiver Erkrankung stehen die orale und die intravenöse (Megadosis) Steroidtherapie und/oder Orbitaspitzenbestrahlung noch immer an erster Stelle. Der Effekt neuer antientzündlicher Medikamente (Somatostatinanaloga, Antioxidantien) muss noch in kontrollierten Studien geprüft werden.
Im inaktiven Stadium stehen neue und klassische Operationstechniken zur Verfügung. Dabei sollte ein Orbitaeingriff zuerst, anschließend Augenmuskelchirurgie und zuletzt die Lidchirurgie erfolgen.
Epidemiologie
[Bearbeiten]Vorkommen und Häufigkeit
[Bearbeiten]Die Endokrine Orbitopathie tritt am häufigsten (90-95 %) im Rahmen einer Autoimmunthyreopathie vom Typ Morbus Basedow (MB), das heißt mit Schilddrüsen Überfunktion und positiven TRAK, seltener (3-5 %) im Rahmen einer Autoimmunthyreopathie vom Typ Hashimoto, das heißt mit Schilddrüsen Unterfunktion, Thyroxinperoxidase- und Thyreoglobulin-Antikörpern und ganz selten (0.5-5 %) ohne begleitende Schilddrüsen-Erkrankung auf.
Die Häufigkeit des Morbus Basedow beträgt 22 von 1000 Personen.
Zeitlicher Zusammenhang zur Manifestation der Schilddrüsen-Überfunktion
[Bearbeiten]Bei 46-60 % der Patienten tritt die Endokrine Orbitopathie innerhalb von 6 Monaten zusammen mit der Schilddrüsen-Überfunktion auf. Bei ca. 30 % manifestiert sich die Schilddrüsen-Überfunktion Jahre bis Jahrzehnte vor der Augenerkrankung. Die Augenerkrankung tritt dann häufig mit einem Rezidiv der Schilddrüsen-Überfunktion auf. In einem kleinen Prozentsatz (ca. 10 %) gehen die Symptome der Augenerkrankung der Schilddrüsen Erkrankung wenige Jahre voraus.
Manifestationsalter und Geschlechtsverteilung
[Bearbeiten]Am häufigsten manifestiert sich die Endokrine Orbitopathie zwischen dem 40. und 50. Lebensjahr. Manche Autoren geben auch eine zweigipflige Häufigkeitskurve mit einem weiteren Gipfel zwischen dem 25. und 35. Lebensjahr an. Bei der Schilddrüsen-Überfunktion zeigt sich eine deutliche Bevorzugung des weiblichen Geschlechts (5-10 Frauen : 1 Mann) etwas geringer für die Endokrine Orbitopathie (2-5 Frauen : 1 Mann).
Genetische Veranlagung
[Bearbeiten]Wie bei allen Autoimmunerkrankungen wird eine genetische Veranlagung diskutiert, was im wesentlichen aus Studien an Zwillingen resultiert. Für die Endokrine Orbitopathie und den Morbus Basedow besteht eine Konkordanzrate von 35 % für monozygote und von 3 % für dizygote Zwillinge. Daraus ergibt sich eine genetische Prädisposition für beide Erkrankungen von 79 %. Bei einem bereits vorhandenen Patienten in der Familie haben weibliche Verwandte ersten Grades ein 5-8 %iges Risiko ebenfalls zu erkranken. Das Risiko für männliche Verwandte ist wesentlich geringer.
Klinisches Bild
[Bearbeiten]Der typische Symptomenkomplex besteht (in absteigender Häufigkeit) aus
- Lidretraktion (Zurückbleiben des Oberlides)
- Weichteilschwellungen (z.B. Ödeme)
- Exophthalmus (Hervortreten der Augen, "Glubschaugen")
- Bewegungsstörung der Augen
- Sehstörung
Die entzündlichen Veränderungen des Bindegewebes der Augenhöhle erzeugen bei fast allen Patienten ein sehr charakteristisches Krankheitsbild. Allerdings kann das Ausmaß der Manifestation sehr stark variieren, sowohl zwischen unterschiedlichen Patienten als auch bei einem Patienten zwischen beiden Augen. Circa 50 % aller Basedow-Patienten entwickeln klinisch sichtbare Augensymptome. Im Kernspin sind jedoch Muskelverdickungen auch bei 2/3 der Patienten sichtbar, die klinisch keine Zeichen einer EO aufweisen. Bei den meisten Patienten verläuft die EO mild bis mittelschwer, nur in 3 – 5 % entwickeln die Patienten eine schwerste EO mit Kompression des Sehnervs (Optikuskompression).
- Lidretraktion: Die häufigste (ca. 90 %) und zugleich typischste Manifestation ist die Lidretraktion am Oberlid (sogenanntes Dalrymple-Zeichen). Diese ist entweder funktionell bedingt durch eine verstärkte Innervation des M. tarsalis Müller (folge eines erhöhten Sympathikotonus durch Schilddrüsen Überfunktion), oder bedingt durch eine fibrotische Verkürzung der Lidretraktoren bzw. eine erweiterte Lidspalte auf Grund eines starken Exophthalmus. Das Stellwag-Zeichen bezeichnet einen seltenen Lidschlag bei endokriner Orbitopathie.
- Weichteilschwellungen: Am zweithäufigsten treten bei ca. 80 % der Patienten in der aktiven Phase der Erkrankung entzündliche Weichteilsymptome auf (Lidödeme, Lidrötung, Karunkelschwellung, Bindehautinjektion, Bindehautchemosis, Limbuskeratitis).
- Exophthalmus: Zwischen 50-60 % der Patienten entwickeln aufgrund der Volumenzunahme in der Augenhöhle (Orbita), vor allem durch Zunahme des dortigen Fettgewebes, an einem oder beiden Augen einen Exophthalmus und einen Fettprolaps durch das Septum orbitale hindurch. Wenn diese beiden Mechanismen den Entlastungsdruck des zunehmenden Augenhöhlengewebes nicht auffangen, führt dies - besonders bei Patienten mit einer kleinen knöchernen Orbita - zu einem Anstieg des orbitalen Gewebedrucks, der sich direkt auf das Auge überträgt. Dies führt zu einem erhöhten Augendruck, der meist auch ein Anzeichen für eine beginnende Kompression des Sehnervs (nervus opticus) darstellt.
- Bewegungsstörungen:: Um 40 % der Patienten, die eine Muskelbeteiligung aufweisen, entwickeln eine Einschränkung der Augenbeweglichkeit mit Doppelbildern. Am häufigsten kommt es zu einer Einschränkung der Dehnbarkeit der Mm. recti inferiores und damit zu einem ein- /oder beidseitigen Hebungsdefizit. Am zweithäufigsten sind die Mm. recti mediales betroffen. Bei stärkerer Verkürzung dieser Muskeln entwickelt der Patient ein Innenschielen. Das Moebius-Zeichen bezeichnet eine Konvergenzschwäche bei endokriner Orbitopathie.
- Sehstörungen: Bei ausgeprägter Schwellung der Augenmuskeln im sogenannten Muskelkonus besteht die Gefahr einer Sehnervkompression. Begleitend sieht man eine deutliche Abflusstauung des Blutes mit Erweiterung der Venen rund um die Hornhaut (rote Augen!), und es kommt zu einem starken Anstieg des Augeninnendruckes. Eine Sehnervkompression bemerkt der Patient durch Farbsehstörungen (besonders der Farbentsättigung), Minderung der Sehschärfe (Visusminderung) und Verschwommensehen.
Die am häufigsten vom Patienten beklagten Symptome im Falle einer aktiven EO entstehen durch die Entzündung: Schmerzen bzw. Druckgefühl hinter den Augäpfeln und Schmerzen bei Augenbewegung, sowie wechselnde Doppelbildwahrnehmung. Über die Hälfte der Patienten beklagt Symptome der Benetzungsstörung: Fremdkörpergefühl, Augenbrennen, Trockenheitsgefühl, erhöhte Lichtempfindlichkeit. Weiterhin fühlen sich die Patienten durch Ihr verändertes Aussehen erheblich beeinträchtigt.
Krankheitsverlauf
[Bearbeiten]Die Erkrankung folgt in der Regel einem dreiphasigen Verlauf. Nach einer Phase der kontinuierlichen Verschlechterung erreicht die EO ein Plateau, um danach in vielen Fällen kontinuierlich wieder besser zu werden. Allerdings wird mit dem inaktiven Endstadium nur selten der Ausgangszustand wieder erreicht. Wichtig ist es, die Verschlechterung in der Phase der aktiven Erkrankung zu stoppen bzw. den Rückgang der Entzündung zu beschleunigen. Ferner sollte man das Erreichen des inaktiven Stadiums erkennen, um dann die operativen Korrekturen verbliebener Veränderungen zu beginnen. Zur Beurteilung der Prognose ist es wichtig zu wissen, dass sich bei 65 % der Patienten mit leichter und moderater EO die Erkrankung nach Erreichen einer normalen Schilddrüsenfunktion ganz ohne Therapie bessert. Bei 22 % bleibt die EO gleich und nur bei 13 % tritt eine Verschlechterung ein.
Behandlung der Erkrankung
[Bearbeiten]Kurzübersicht
[Bearbeiten]Aktive Form
[Bearbeiten]Milde EO und geringe subjektive Beschwerden
- Symptomatische Therapie- Licht/Windschutz, künstliche Tränen, Hochlagern des Kopfes beim Schlafen
Milde EO und geringe entzündliche Zeichen
- Abwarten des Spontanverlaufs
Schwere EO und hohe entzündliche Aktivität
- Glukokortikoide ( zb wöchentlich 1 * 0,5 g Prednison iv )
- evt Retrobulbärbestrahlung
Optikusneuropathie
- 0,5 - 1 g Prednisolon intravenös - wenn erfolglos
- Operative Dekompression
Alternative Verfahren:
- Ciclosporin, Octreotid, Immunglobuline in Kombination mit Glukokortikoiden
Inaktive Form
[Bearbeiten]Korrektur bleibender Defekte bei inaktiver EO Exophtalmus
- Ossäre Dekompression
Fettansammlung
- Fettgewebsresektion
Diplopie
- Operative Augenmuskelkorrektur
Lidretraktion
- Operative Korrektur
Medikamente
[Bearbeiten]Nach Erreichen einer euthyreoten Stoffwechsellage ist bei einer aktiven bzw. fortschreitenden EO ohne Spontan-Besserungstendenz eine antientzündliche bzw. immunsuppressive Therapie angezeigt, insbesondere bei entsprechendem Leidensdruck des Patienten.
Bei der Indikationsstellung muss man beachten, dass 65 % der Patienten mit leichter und moderater EO sich nach Erreichen einer euthyreoten Stoffwechsellage ganz ohne Therapie bessern. Ein Patient mit allen Risikofaktoren für einen schlechten Verlauf (hohe bzw. ansteigende TRAK, hohe Aktivität der Erkrankung, hoher Schweregrad, Raucher) sollte im Zweifelsfall behandelt werden.
Standard ist eine Steroidstoßtherapie, was in zwei randomisierten prospektiven Studien bewiesen wurde. Studien belegten auch, dass die Steroide intravenös besser toleriert wurden als wenn sie als Tabletten verabreicht wurden. Die intravenöse Gabe führte zu weniger Knochendemineralisierung und einem stärkeren Rückgang der TRAK.
Bei therapieresistenter EO gibt es folgende Alternativen:
Cyclosporin A: In einer randomisierten Studie (Steroide in absteigender Dosierung gegen Cyclosporin A über 12 Wochen) erwiesen sich die Steroide als besser wirksam. Allerdings sind Steroide in Kombination mit Cyclosporin A wirksamer als Steroide allein.
Somatostatin-Rezeptor-Agonisten: In einer Studie erwies sich Octreotide über 3 Monate s.c. weniger effektiv als Prednison über 3 Monate. Lanreotide erwies sich in einer kleinen kontrollierten Studie vergleichbar wirksam wie Octreotide. Die Besserung der EO war signifikant stärker als in der Kontrollgruppe.
Antioxidantien: Vielversprechend sind die Ergebnisse der „Münchner EO prevention study“. Untersucht wurde die Häufigkeit der Entwicklung einer EO bei Patienten, die bei Manifestation der SD-Überfunktion noch keine Zeichen einer EO aufwiesen. Nur 6 von 28 in der Antioxidantiengruppe (Selen, N-Acetyl-Cystein, Nicotinamid, Alpha-Liponsäure und Vitamine C und E), aber 13 Patienten der Placebogruppe entwickelten nach 18 Monaten eine EO.
Orbitaspitzenbestrahlung: Eine Orbitaspitzenbestrahlung ist bei Patienten mit mittelschwerer EO und Bewegungsstörungen angezeigt. Die Ergebnisse in jüngster Zeit veröffentlichter Studien haben den Wert der Orbitaspitzenbestrahlung etwas in Frage gestellt. Relativ konsistent ist jedoch der Nachweis der Besserung der Augenbeweglichkeit. Nach dem Stand der Literatur würde man eine Orbitaspitzenbestrahlung bei Patienten mit mittelschwerer EO und Motilitätsstörungen im Anschluss an oder parallel zu eine(r) Steroidtherapie empfehlen.
Für den Wirkungsnachweis von Methotrexat, Cyclophosphamid und Pentoxifilline gibt es nur unkontrollierte Studien. Im Durchschnitt wird eine Ansprechrate zwischen 50-60 % beschrieben.
Operation
[Bearbeiten]Voraussetzung für alle operativen Maßnahmen (außer der knöchernen Dekompression bei Optikuskompression, einer akuten Notsituation!) ist eine inaktive EO und unveränderte Befunde über 6 Monate. Weiterhin sollte möglichst der Auslassversuch der medikamentösen Schilddrüsentherapie erfolgt sein und mindestens 6 Monate zurückliegen, da in den ersten 6 Monaten nach Absetzen dieser Medikamente 80-90 % der Rezidive der Schilddrüsen Überfunktion auftreten (Insgesamt Rezidivrate der Schilddrüse 50 %). Bei einem Rezidiv der Schilddrüsen Überfunktion kann die EO wieder aktiviert werden. Im Falle eines Rezidivs der Schilddrüsen Überfunktion bzw. bei medikamentös nicht einstellbarer Schilddrüsen Funktion sollte die ablative Therapie der Schilddrüse (Radiojodtherapie, Operation der Schilddrüsen) vor den chirurgischen Korrekturen der EO erfolgen. Vor allem nach einer Radiojodtherapie muss man darauf achten, dass der Patient eine normale Schilddrüsen Funktion hat und regelmäßig kontrolliert wird.
Ist die optimale Ausgangssituation für die chirurgischen Maßnahmen erreicht, sollte man eine bestimmte Reihenfolge einhalten.
1. Orbitachirurgische Maßnahmen
Neben der Notfallsituation einer Optikuskompression sind ein entstellender Exophthalmus (knöcherne Dekompression) oder ein starker Prolaps des orbitalen Fettgewebes (Orbitafettresektion) Indikationen zu einem Orbitachirurgischen Eingriff. Eine Orbitadekompression reduziert den Exophthalmus, verbessert den venösen Abfluss reduziert aber die Augenbeweglichkeit.
2. Augenmuskeloperationen
Ziel der Augenmuskeloperation sind Verbesserung der Augenbeweglichkeit, Reduktion von Doppelbildwahrnehmung und Kopfzwanghaltung.
3. Lidoperationen
Ziel der Operation der Ober-und Unterlidretraktion sind die Reduktion einer eventuell vorhandenen Benetzungsstörung und die Wiederherstellung eines normalen Aussehens.
Einflussfaktoren auf den Krankheitsverlauf
[Bearbeiten]Rauchen
[Bearbeiten]Das Rauchen hat sich als starker Einflussfaktor für die EO erwiesen. Das Vorkommen einer EO unter Rauchern mit Morbus Basedow ist signifikant höher als bei Nichtrauchern. Weiterhin zeigte sich eine von der Zigarettenzahl abhängige Zunahme des Schweregrades der EO. In zwei prospektiven Studien konnte gezeigt werden, dass Rauchen das Risiko Fortschreitens der EO nach Radiojodtherapie erhöht und den Effekt der Steroidtherapie und der Orbitaspitzenbestrahlung reduziert.
Einfluss der Schilddrüsen Funktion
[Bearbeiten]Allein der zeitliche Zusammenhang zwischen Auftreten einer Schilddrüsen Überfunktion und einer EO lässt einen engen Zusammenhang zwischen beiden Erkrankungen vermuten. Die TRAK sind durch ihre TSH-Rezeptor Stimulation verantwortlich für die Schilddüsen Überfunktion. Ihre Bedeutung bei der EO wurde lange Zeit kontrovers diskutiert. In den jüngeren Arbeiten unter Nutzung neuer sensitiverer Assays zur TRAK Bestimmung wurde jedoch ein klarer Zusammenhang zwischen TRAK und der Aktivität sowie des Schweregrads der EO gefunden. Darüber hinaus haben Patienten mit Therapie resistenter EO signifikant häufiger höhere TRAK als Patienten, bei denen die klinische Aktivität durch die Therapie zurückgeht. In einer Verlaufsbeobachtung (TRAK-Bestimmung alle 3 Monate über 2 Jahre) wiesen Patienten mit einer milden EO signifikant niedrigere TRAK-Spiegel im Vergleich zu Patienten mit moderater bis schwerer EO auf. Diese Daten zeigen, dass man bei mehr als der Hälfte der Patienten den Verlauf der EO anhand der TRAK-Spiegel schon bei der ersten Kontrolle voraussagen kann.
Weiterhin erwartet man eine schlechte Prognose bei initial großer Schilddrüse und starker Überfunktion. Eine schlecht eingestellte Schildrüsen Funktion beeinflusst Manifestation und Verlauf einer EO negativ. Deshalb sind das Erreichen und die Aufrechterhaltung einer gleichmäßig normalen Schilddrüsen Funktion ein primäres Ziel der erfolgreichen EO Therapie.
Auch die Art der Schilddrüsen Therapie beeinflusst den Verlauf der EO. Obwohl in der Literatur nicht dokumentiert, lehrt die Erfahrung, dass sich die EO schon allein durch die thyreostatische Therapie bessert. Das ist sicher einerseits durch das Erreichen der Euthyreose bedingt andererseits aber auch durch die leichte immunsuppressive Wirkung der Antithyreostatika. Methimazol hemmt die Bildung freier Radikale der Monozyten. Zwei prospektive Studien zeigten, dass eine Radiojodtherapie bei 24-33 % der Patienten die Verschlechterung einer vorbestehenden EO bewirken kann. Das Risiko des Neuauftretens einer EO ist jedoch gering. Im Vergleich dazu liegt das Risiko der Verschlechterung einer EO unter thyreostatischer Therapie nur bei 4-10 % und nach Schilddrüsen Operation bei subtotaler Resektion bei 7-16 % und bei totaler Resektion bei 6%. Ursächlich werden für die höhere Verschlechterungsrate der EO nach einer Radiojodtherapie die Freisetzung von Schilddrüsen Antigenen durch die radiogene Zerstörung der Schilddrüse, die danach ansteigenden Schilddrüsen-Autoantikörperspiegel und die häufig erst mit Latenz nach der Radiojodtherapie diagnostizierte Schilddrüsen Unterfunktion (Hypothyreose) diskutiert.
Stress
[Bearbeiten]Auch sogenannte „stressful life events“ haben Einfluss auf die Entwicklung einer Autoimmunthyreopathie mit EO. Bei chronischem psychischen Stress ist der Erfolg der thyreostatischen Therapie ebenfalls geringer.
Spezialisten für EO
[Bearbeiten]- Herr Prof. Dr. George J. Kahaly, Mainz
Links
[Bearbeiten]- http://www.tellmed.ch/include_php/previewdoc.php?file_id=3627
- Schöne Zusammenfassung über die Behandlung der EO
Unterfunktion der Schilddrüse
[Bearbeiten]siehe Schilddrüse: Unterfunktion
Gutartige Schilddrüsentumoren
[Bearbeiten]Schilddrüsenkrebs
[Bearbeiten]Als Schilddrüsenkrebs (Schilddrüsenkarzinom, lat. Struma maligna) wird eine bösartige (maligne) Neubildung der Schilddrüse bezeichnet.
Vorkommen und Ursachen
[Bearbeiten]Frauen sind etwa dreimal so häufig betroffen wie Männer, der Altersgipfel liegt zwischen dem 25. und 50. Lebensjahr. Die Ursachen sind im Einzelnen nicht vollständig geklärt. Es besteht ein kausaler Zusammenhang mit dem Iodmangel (etwa 2,3fach erhöhtes Risiko). Auch radioaktive Strahlung spielt - wie bei vielen Krebserkrankungen - eine wesentliche Rolle: nach den Atombombenabwürfen auf Hiroshima und Nagasaki stieg das Risiko in den betroffenen Gebieten, ein Schilddrüsenkarzinom zu entwickeln, um ein Vielfaches an.
Symptome
[Bearbeiten]Als Symptome gelten derbe Knotenbildung im Bereich der Schilddrüse mit Wachstumstendenz, Heiserkeit und vergrößerte Halslymphknoten (Spätsymptome).
Diagnostik
[Bearbeiten]- Palpation ( Abtasten der Schilddrüse)
- Man tastet einen odere mehrere derbe , nicht verschiebliche Knoten
- Sonographie
- Szintigraphie,
- kalter Knoten
- Feinnadelpunktion oder Gewebsprobe des kalten Knotens mittels Punktion
(Beurteilung der entnommenen Zellen unter dem Mikroskop
- Bestimmung des Calcitoninspiegels im Serum (Erhöhung pathologisch, jedoch Abgrenzung zu einer Schilddrüsenüberfunktion notwendig)
- Kehlkopfspiegelung (Laryngoskopie)
- Bei einem krebsverdächtigen Knoten wird meist direkt eine Thyreoidektomie (Entfernung der Schilddrüse) mit anschließender Beurteilung des Zellgewebes (Histologie) durchgeführt.
Differentialdiagnose
[Bearbeiten]- Zyste
- Struma nodosa ( Knotenkropf (kalter Knoten / heißer Knoten)
- Adenom
- Metastasen (bspw. von einem Brustkrebs)
- Riedelstruma
Tumorarten und Therapie
[Bearbeiten]Im Wesentlichen liegen epitheliale Neubildungen (Karzinome) vor. Lymphome, Metastasen anderer Tumore oder andere Tumorformen können vorkommen, sind aber selten.
Follikuläres und papilläres Karzinom
[Bearbeiten]Sie machen 80 % aller bösartigen Schilddrüsentumore aus. Die Therapie besteht aus Kombination von radikaler Thyreoidektomie und Resektion aller verdächtigen Lymphknoten, einer (bzw. falls notwendig, mehrerer) Radiojodtherapie(n) sowie einer dauerhaften Einstellung auf eine leichte Schilddrüsenüberfunktion (Suppressionstherapie), um auffällige im Körper verbliebene kleinste Schilddrüsenreste (die möglicherweise bösartig sein könnten) vom Wachstum abzuhalten. Regelmäßige Kontrollen (Tumormarker Thyreoglobulin und Ultraschall) müssen lebenslang durchgeführt werden. Der Haupmetastasierungsweg des papillären Karzinoms ist lymphogen, wobei besonders regionäre Halslymphknoten betroffen sind. Das follikuläre Karzinom metastasiert in der Regel zuerst hämatogen.
Anaplastisches Karzinom
[Bearbeiten]Das anaplastische Karzinom macht 1-2 % aller bösartigen Schilddrüsentumore aus. Es ist hochmaligne. Die Behandlung erfolgt als totale Thyreoidektomie inkl. Neck-Dissection. Eine Chirurgische Intervention ist anzustreben, das anaplastische Karzinom ist jedoch oftmals inoperabel. Die Metastasierung erfolgt lymphogen und hämatogen.
Medulläres Karzinom (C-Zellkarzinom)
[Bearbeiten]Es macht circa 5 % bis 10 % der bösartigen Schilddrüsentumore aus. Die Mehrzahl der medullären Karzinome tritt sporadisch auf, bei 20 % läßt sich eine Mutation am ret-Proto-Onkogen nachweisen. Das medulläre Karzinom kann familiär gehäuft auftreten oder im Rahmen der Multiplen endokrinen Neoplasie Men2A oder 2B vermehrt vorkommen.
Der Tumormarker des medullären Karzinomes ist das Calcitonin.
Bei gefährdeten Personen sind enge Kontrollen des Schilddrüsenultraschalles und des Tumormarkers notwendig.
Als Behandlung sollte die Thyreoidektomie und Neck-Dissection bds. erfolgen. Adjuvante Therapieformen sind bis jetzt noch wenig effektiv, allerdings gibt es einige Ansätze in der Erprobung.
Nachsorge
[Bearbeiten]Zitat:
Die immunometrische Bestimmung von Serum Thyreoglobulin (S-Tg), ist nach Thyreoidektomie und Radiojodablation in der Nachsorge des differenzierten Schilddrüsenkarzinomen (DTC) ein verlässlicher und sensitiver Parameter eines Rezidivs in hypothyreoter Stoffwechsellage. Allerdings bilden ca. 20% der differenzierten Schilddrüsenkarzinome Thyreoglobulinantikörper aus, die neben der molekularen Heterogenität des Tg - Moleküls ursächlich für falsch negative Ergebnisse im Immunoassay sein können.
Prognose
[Bearbeiten]Folgende 5-Jahres-Überlebensraten werden im Allgemeinen angegeben (bei Behandlung):
- papilläres Karzinom 80-90 %
- follikuläres Karzinom 80 %
- medulläres Karzinom 60-70 %
- anaplastisches Karzinom unter 10 %
Literatur
[Bearbeiten]- Current management of medullary thyroid cancer.
- Sippel, Rebecca S; Kunnimalaiyaan, Muthusamy; Chen, Herbert
- Oncologist. 2008 May;13(5):539-47.
- Gute Übersichtsarbeit über das medulläre SD-CA
- Sippel, Rebecca S; Kunnimalaiyaan, Muthusamy; Chen, Herbert
Weblinks
[Bearbeiten]- http://www.krebshilfe.de/fileadmin/Inhalte/Downloads/PDFs/Blaue_Ratgeber/009_schilddruese.pdf
- Guter Patientenratgeber zum Thema Schilddrüsenkrebs
- www.dmoz.org - Schilddrüsenkrebs im Open Directory Project
- http://www.schilddruesenkrebs.de
- http://www.c-zell-karzinom-online.info
- http://www.selbsthilfegruppe.at/
- Selbsthilfegruppe für Schilddrüsencarcinom-PatientInnen Österreich
- http://www.forpath.org/0201/
- Ausführlicher Text über die histopathologische Differentialdiagnose von Schilddrüsentumoren
- In Englisch
- Ausführlicher Text über die histopathologische Differentialdiagnose von Schilddrüsentumoren
Fall
[Bearbeiten]36-Jähriger männlicher Patient aserbaidschanischer Herkunft stellt sich mit folgendem Befunden vor: ein szintigraphisch kalter Knoten links sowie eine sonografisch gesehene eher zystische Struktur mit 0,6cm Durchmesser zentral bis rechts im Lobus pyramidalis bei Struma nodosa. Palpatorisch und inspektorisch ist die Schilddrüse unauffällig. Der Calcitonin-Wert ist um das zehnfache erhöht (148,44pg/ml vs 15 als Normwert). Intraoperative Schnellschnitte (primär war eine Hemithyreoidektomie geplant) ergeben für den zentralen Prozess ein papilläres CA und für den linken kalten Knoten überraschenderweise ein medulläres CA, sowie in der entnommenen rechten Schilddrüsenhälfe noch ein bisher nicht gesehenes papilläres CA. Die OP wird ausgedehnt auf eine totale Strumektomie, sowie, wegen dem medullären CA, auf eine komplette modfizierte Neckdisektion beidseits mit Entfernung aller Lymphknoten entlang der Vagina Carotica und des m. Sternocleidomastoideus.
Seltene SD-Krankheiten
[Bearbeiten]Resistenz gegen Schilddrüsenhormone (resistance to thyroid hormone, RTH)
[Bearbeiten]Diese seltene Krankheit wird nach dem Entdecker auch Refetoff-Syndrom bezeichnet. Die Schilddrüsenhormonspiegel sind hoch, gleichzeitig wirken die Hormone vermindert. Die typische Laborkonstellation der Erkrankung lautet:
- erhöhter Thyroxin (T4)-und Trijodthyronin (T3)-Serumspiegel
- normaler oder erhöhter Thyreoidea stimulierendem Hormon (TSH) spiegel.
Ursächlich liegt eine Mutation der Beta1-Form des Schilddrüsenhormonrezeptors (thyroid hormone receptor, TR) vor.
Bisher wurden circa 600 Fälle in der Literatur beschrieben.
Riedel-Struma
[Bearbeiten]Die Riedel-Struma (Riedel-Thyreoiditis, „eisenharte Struma“) ist eine sehr seltene invasiv sklerosierende Schilddrüsenentzündung (Thyreoiditis), die meist bei Frauen mittleren Alters auftritt.
- Invasiv heißt hier: in die Umgebung einwachsend.
- Sklerosierend heißt: vernarbend.
Die Ursache der Erkrankung ist unbekannt. Es kommt es zu einer kompletten Zerstörung des Schilddrüsengewebes durch eine fibrosierende Proliferation (bindegewebigen Umbau) . Häufig ist eine Überschreitung der Schilddrüsenkapsel mit Infiltration des umgebenden Halsgewebes zu beobachten.
ICD 10
[Bearbeiten]E06.5 Riedel-Struma
Diagnostik
[Bearbeiten]Bei der klinischen Untersuchung zeigt sich eine tastbare und „eisenharte“ Schilddrüsenvergrößerung (Struma). Diese kann zu lokalen Problemen mit Einengung der Luftröhre und der Halsgefäße, aber auch zu einer Verdrängung großer Halsnerven bis zu einer Rekurrensparese führen. Die Schilddrüse ist beim Schluckakt nicht mehr verschieblich als Zeichen der Verwachsung mit dem umliegenden Halsgewebe, zeigt jedoch nur selten eine Schmerzempfindlichkeit.
Bei der Ultraschalluntersuchung der Schilddrüse lassen sich das Volumen bestimmen und knotige Veränderungen sowie Infiltration in das Halsgewebe nachweisen. Typischer Weise zeigt das Szintigramm bei der Riedel-Struma eine insgesamt erniedrigte Aufnahme des Technetiums. Bei Nachweis von kalten Knoten ergibt sich immer der Verdacht eines Krebses, was eine operative Entfernung zur Folge hat.
Man kann auch gezielt eine Gewebsprobe aus der betroffenen Schilddrüse entnehmen, um die Diagnose zu stellen.
Differentialdiagnosen
[Bearbeiten]Abzugrenzen sind vor allem Schilddrüsenkrebs und die fibröse Variante der Hashimoto-Thyreoiditis.
Therapie
[Bearbeiten]Da die Riedel-Struma ausschließlich lokale Probleme am Hals verursacht, sollte sie möglichst frühzeitig operativ entfernt werden. Bei der anschließenden feingeweblichen Beurteilung des entnommenen Gewebes kann dann auch eine Krebserkrankung ausgeschlossen (oder nachgewiesen) werden.
Es existieren keine gesicherten Erfahrungen mit konservativen Therapieansätzen. Nach der operativen Entfernung der Schilddrüse müssen lebenslang künstliche Schilddrüsenhormone eingenommen werden.
Literatur
[Bearbeiten]- Wien Klin Wochenschr. 1988 Apr 1;100(7):210-5.
- Chronic invasive fibrous thyroiditis (Riedel struma). Case report with special reference to preoperative diagnosis
- Beham A, Langsteger W, Schmid C, Lind P, Kronberger D. Institut fur Pathologische Anatomie, Universitat Graz.
- Artikel in deutscher Sprache
- Chronic invasive fibrous thyroiditis (Riedel struma). Case report with special reference to preoperative diagnosis
Weblinks
[Bearbeiten]- http://www.madeasy.de/6/riedel.htm
- http://www.emedicine.com/med/topic2036.htm
- Ausführlicher Übersichtsartikel mit Histologiebildern in Englisch
Behandlung von Schilddrüsenkrankheiten (Therapie)
[Bearbeiten]Therapie (Behandlung) von Schilddrüsenkrankheiten
Therapie Übersicht
[Bearbeiten]- oft ist keine Therapie notwendig, sondern nur Kontrolluntersuchungen
- beispielsweise bei harmlosen Schilddrüsenknoten
- Jodsalz,
- Jodtabletten
- bei Jodmangel und zur Kropfvorbeugung
- Thyroxin (T4)
- zur Behandlung der Unterfunktion und teilweise auch zur Kropfrückbildung
- Levothyroxin kann auch abends eingenommen werden
- Triiodthyronin (T3)
- zur Behandlung spezieller Unterfunktionserkrankungen
- Medikamente die die Schilddrüsenfunktion reduzieren
- Thiamazol
- Carbimazol
- Propylthiouracil
- Perchlorat = Irenat)
- bei Überfunktion
- Betablocker (Propanolol, Bisoprolol, Metoprolol, ....)
- bei Überfunktion
- Alkoholbehandlung von heißen Schilddrüsenknoten
- Radiojodbehandlung
- bei Überfunktion und Schilddrüsenkrebs
- Operation der Schilddrüse
- Begrenzte Schilddrüsen Operation
- Subtotale Schilddrüsen Operation
- Radikale Schilddrüsen Entfernung
- Schilddrüsen Operation + Lymphknotenausräumung am Hals
- Sonstige Therapie der Schilddrüse
- Pharmafirmen mit Schilddrüsenpräparaten
- Henning Berlin
- Merck Darmstadt
- ....
Medikamentenliste der wichtigen Schilddrüsenwirkstoffe
[Bearbeiten]Verschiedene Namen für den gleichen Wirkstoff
Jodpräparate
[Bearbeiten]- Jodetten Henning
- Jodid Beta
- Jodid Dura
- Jodid Hexal
- Jodid ratiopharm
- Jodid Verla
- Kalium Jodatum
- Kaliumiodid
- Mono-Jod
- Strumedical
- Strumex
- ....
T4-Thyroxin-Monopräparate
[Bearbeiten]- Berlthyrox (50, 100, 150 Berlin-Chemie)
- Eferox (25, 50, 75, 100, 125, 150 Lindopharm)
- Euthyrox (25, 50, 75, 100, 125, 150, 175, 200 Merck KGaA)
- Lixin liquid (Henning Berlin)
- L-Thyrox (25, 50, 75, 100, 125, 150, 175, 200 Hexal)
- L-Thyroxin beta (25, 50, 75, 100, 125, 150, 175, 200 betapharm)
- L-Thyroxin Henning (25, 50, 75, 100, 125, 150, 175, 200 Henning-Berlin)
- Thevier (50, 100 Glaxo Smith Kline)
- ....
Thyreostatika Überfunktionsbremser
[Bearbeiten]Wirkstoff Thiamazol:
[Bearbeiten]- Favistan
- Methizol
- Thyrozol
Wirkstoff Carbimazol:
[Bearbeiten]- Carbimazol
- Carbistad
- Neo-Thyreostat
Wirkstoff Propylthiouracil:
[Bearbeiten]- Propycil
- Prothiucil
- Thyreostat
Wirkstoff Natriumperchlorat:
[Bearbeiten]Betablocker
[Bearbeiten]Propranolol
[Bearbeiten]Bisoprolol
[Bearbeiten]......
[Bearbeiten]Schilddrüsenmedikamente im Einzelnen
[Bearbeiten]Iodbedarf in Mikrogramm pro Tag
[Bearbeiten]Säuglinge 50 – 80 Kleinkinder 100 – 120 Schulkinder 140 – 200 Jugendliche 200 Erwachsene bis 35 Jahre 200 Erwachsene über 35 Jahre 180 Schwangere und Stillende 230 – 260
Links
[Bearbeiten]- http://www.iod-fuer-zwei.de/
- Iodbehandlung in der Schwangerschaft
Jod Salz
[Bearbeiten]Jod Tabletten
[Bearbeiten]Anwendung:
[Bearbeiten]- Vorbeugung eines Jodmangels, zur Vorbeugung eines Kropfes in Jodmangelgebieten und nach Entfernung eines Jodmangelkropfes,
- Behandlung eines Kropfes bei Neugeborenen, Kindern, Jugendlichen, Erwachsenen und Schwangeren.
Gegenanzeigen
[Bearbeiten]- Autoimmunerkrankungen der Schilddrüse (Morbus Basedow, Hashimoto Thyreoiditis)
- Manifeste Schilddrüsenüberfunktion.
- Latente Schilddrüsenüberfunktion
- Diffuse und fokale Autonomien (autonome Adenome).
Präparate:
[Bearbeiten]- Jodetten ® 100 Henning enthält 130,8µg Kaliumjodid, entspricht 100µg Jod
- Jodetten ® 200 Henning enthält 261,6µg Kaliumjodid, entspricht 200µg Jod
- Jodetten ® depot Henning enthält 2mg Kaliumjodid, entspricht 1,53mg Jod
- Strumedical 400 Henning®
- Strumex®
- Jodid®
- Jodid ratiopharm®
- Jodid Verla®
- Kaliumiodid BC 200®
- Kalium Jodatum 0,1g®
- Mono-Jod®
siehe auch http://www.madeasy.de/6/jodid.htm
Thyroxin (Schilddrüsenhormon)
[Bearbeiten]siehe http://www.madeasy.de/6/euthyrox.htm
Anwendung
[Bearbeiten]- Schilddrüsenunterfunktion (SD-Hormonmangel)
- Ausgleich eines angeborenen oder erworbenen Schilddrüsenhormonmangels
- nach einer operativen Entfernung der Schilddrüse
- nach einer Radiojodtherapie mit folgendem Schilddrüsenhormonmangel
- nach einer Erkrankung der Schilddrüse und Untergang von Schilddrüsengewebe.
- chronische Autoimmunthyreoiditis Hashimoto (im Anfangsstadium umstritten, in jedem Fall in der Endphase)
Wirkstoff Thyroxin (T4) ist enthalten in
[Bearbeiten]( Wirkstärken meist in mikrogramm )
- Euthyrox® 25/-50/-75/-88/-100/-112/-125/-137/-150/-175/-200 Mikrogramm Tabletten
- L-Thyroxin® Henning 25 /50 /75 /100 /150 /175 /200 /300
- L-Thyrox® HEXAL® 25/-50/-75/-88/-100/-112/-125/-150/-175/-200 mikrog
- Berlthyrox® 50 /100 /150
- Eferox® 25 /50 /75 /100 /125 /150 /175
- L-Thyroxin® Henning depot 1mg
- Thevier® 50/ Thevier 100
- L-Thyroxin HF® 50 /75 /100 /125
Kombinationspräparate Jod + T4
- Jodthyrox®
- Thyreocomb N®
- Thyronajod®
Kombinationspräparate T4 + T3
- Novothyral® 75µg + 15µg / 100µg + 20µg
T4 und T3 intravenös
[Bearbeiten]Schilddrüsenhormone müssen manchmal auch intravenös verabreicht werden. Dafür gibt es 2 Präparate in Deutschland:
- L-Thyroxin Henning® inject.
- L-Thyroxin Henning® inject. Durchstechflasche mit Trockensubstanz und Lösungsmittel
- Thyrotardin®-inject.
- Thyrotardin®-inject. Durchstechflasche mit Trockensubstanz und Lösungsmittel (Mono)
Das erste Präparat hat eine relativ hohe Dosis von 500 mikrog T4 und hat nur die Zulassung zur Therapie des hypothreoten Comas. Das zweite Präparat hat eine Dosis von 100 mikrog T3 und wird deswegen auch bei Patienten verwendet, die einen Hormonersatz brauchen, aber nicht schlucken können.
L-Thyroxin Henning® inject. 500
[Bearbeiten]- Zusammensetzung
- 1 Durchstechflasche enthält Levothyroxin-Natrium 514,1 μg (entspr. 0,5 mg Levothyroxin).
- Weitere Bestandteile:
- Natriummonohydrogenphosphat
- 2H2O,
- Mannitol,
- Natriumchlorid,
- Wasser f. Inj.-zwecke,
- zur pH-Einstellung:
- Phosphorsäure,
- Natriumhydroxid.
- Kosten
- 1 Durchstechfl. (N1) Trockensubstanz u. Lsgm. (AP) Circa 50 Euro
Anwendung
- Notfalltherapie bei hypothyreotem Koma.
- Dosierung
- i.v. Infusion von 0,3-0,5 mg gemäß Gebrauchsanweisung.
Gegenanzeigen
- Unbehandelte Hyperthyreose.
- Frischer Myokardinfarkt,
- Myokarditis,
- Pankarditis,
- unbehandelte hypophysäre oder Nebennierenrinden-Insuffizienz.
In Notfallsituationen individuell abwägen.
- Anwendungsbeschränkung:
- Patienten bei welchen sich unter einer lang andauernden Hypothyreose bereits eine Coronar- oder Herzinsuffizienz ausgebildet hat oder eine Hypophysenvorderlppen-Insuffizienz besteht (Infusion unter EKG-Kontr. zusätzliche Glucocorticoid-Gabe).
- Hypertonie,
- Angina Pectoris,
- tachykarde Herzrhythmusstörungen
- Nebenwirkungen
- Hyperthyreose
- Bei Überdosierung (insbesondere bei zu schneller Steigerung der Dossis zu Beginn der Behandlung):
Hyperthyreotische Erscheinungen (z. B. Fingertremor, Tachykardie, Hyperhidrosis, Diarrhö, Gewichtsabnahme, innere Unruhe) Bei zu hoher Anfangsdosis kann bei besonders empfindlichen Patienten Vorhof- bzw. Kammerflimmern ausgelöst werden.
- Toxizität
- Hyperthyreose
- Tachykardie,
- Heißhunger,
- Herzpalpitation,
- vermehrtes Schwitzen
- Hitzegefühl, Wärmeintoleranz,
- Unruhe,
- Fingertremor,
- lebhaft gesteigerte Reflexe,
- Diarrhöen,
- Fieber,
- Blutdruckabfall,
- pektanginöse Beschwerden.
- Hyperthyreose
Eine thyreotoxische Krise ist bei Überdosierung von Schilddrüsenhormonpräparaten bisher nicht beschrieben worden, und es ist zweifelhaft, ob sie überhaupt auftreten kann.
Therapie der Überdosierung:
- Sedierende Mittel,
- v. a. Reserpin,
- Schlafmittel,
- Betarezeptorenblocker,
- Corticoide, ggf. Digitalis.
- Bei thyreotoxischer Krise: u. U.
- künstliche Hibernation,
- Peritonealdialyse,
- Hämoperfusion über Kohle od. Austauscherharze.
Thyrotardin®-inject 100 mikrog T3
[Bearbeiten]Zusammensetzung
- 1 Durchstechflasche enthält Liothyronin = T3 0,1 mg.
Weitere Bestandteile: Natriummonohydrogenphosphat 2H2O, Mannitol, Natriumchlorid, Wasser f. Inj.-zwecke, zur pH-Einstellung: Phosphorsäure, Natriumhydroxid.
Kosten
- 1 Durchstechflasche (N1) Trockensubstanz und Lösungsmittel circa 50 €
Anwendung
- Notfalltherapie bei hypothyreotem Koma,
- zur Substitution, wenn eine orale Applikation nicht möglich ist.
Dosierung: i.v. Infusion von 0,1 mg gemäß Gebrauchsanweisung.
Gegenanzeigen
- Unbehandelte Hyperthyreose.
- Frischer Myokardinfarkt,
- Myokarditis,
- Pankarditis,
- unbehandelte hypophysäre oder Nebennierenrinden-Insuffizienz.
In Notfallsituationen individuell abwägen.
- Anwendungsbeschränkung:
- Patienten bei welchen sich unter einer lang andauernden Hypothyreose bereits eine Coronar- oder Herzinsuffizienz ausgebildet hat oder eine Hypophysenvorderlppen-Insuffizienz besteht (Infusion unter EKG-Kontr. zusätzliche Glucocorticoid-Gabe).
- Hypertonie,
- Angina Pectoris,
- tachykarde Herzrhythmusstörungen
- Nebenwirkungen
- Hyperthyreose
- Bei Überdosierung (insbesondere bei zu schneller Steigerung der Dossis zu Beginn der Behandlung):
Bei zu hoher Anfangsdosis kann bei besonders empfindlichen Patienten Vorhof- bzw. Kammerflimmern ausgelöst werden.
Hyperthyreotische Erscheinungen (z. B. Fingertremor, Tachykardie, Hyperhidrosis, Diarrhö, Gewichtsabnahme, innere Unruhe)
- Toxizität
- Hyperthyreose
- Tachykardie,
- Heißhunger,
- Herzpalpitation,
- vermehrtes Schwitzen
- Hitzegefühl, Wärmeintoleranz,
- Unruhe,
- Fingertremor,
- lebhaft gesteigerte Reflexe,
- Diarrhöen,
- Fieber,
- Blutdruckabfall,
- pektanginöse Beschwerden.
- Hyperthyreose
Eine thyreotoxische Krise ist bei Überdosierung von Schilddrüsenhormonpräparaten bisher nicht beschrieben worden, und es ist zweifelhaft, ob sie überhaupt auftreten kann.
Therapie der Überdosierung:
- Sedierende Mittel,
- v. a. Reserpin,
- Schlafmittel,
- Betarezeptorenblocker,
- Corticoide, ggf. Digitalis.
- Bei thyreotoxischer Krise: u. U.
- künstliche Hibernation,
- Peritonealdialyse,
- Hämoperfusion über Kohle od. Austauscherharze.
Schilddrüsenbremser
[Bearbeiten]Anwendung
- manifeste oder latente Schilddrüsenüberfunktionen
- bei gutartigen, hormonbildenden Knoten oder unkontrolliert hormonbildenden Bezirken
- Morbus Basedow
Thiamazol
[Bearbeiten]Wirkstoff Thiamazol
- Methizol® = 1 Tbl. enthält 5mg Thiamazol
- Favistan® = 1 Tbl. enthält 20mg Thiamazol
- Thyrozol® 5/10/20 = 1 Tbl. enthält 5/10/20mg Thiamazol
Thiamazol iv,im,sc (Favistan)
[Bearbeiten]Anwendung:
- Thyreotoxische Krise,
- Basedow-Koma.
Zusammensetzung:
- 1 ml enthält Thiamazol 40 mg.
Weitere Bestandteile:
- Wasser für Injektionszwecke,
- Stickstoff als Schutzgas
Kosten
10 Amp. (N1) 1 ml 16,40 Euro
Gegenanzeigen:
- Schwere vorausgegangene Überempfindlichkeitsreaktionen (z. B. Agranulozytose)
- Leberschäden durch das anzuwendende Thyreostatikum in der Vorgeschichte
Wechselwirkungen:
- Jodmangel verstärkt das Ansprechen auf Thiamazol.
Hinweise:
- Es wurde wiederholt über Kinder von mit Thiamazol behandelten Müttern berichtet, die mit einer Aplasia cutis im Kopfbereich geboren wurden, die nach einigen Wochen spontan abheilte.
Dosierung: Injektions-Lösung:
- 3-4 mal täglich 1 ml i.v.,
- in schweren Fällen bis zu 3mal täglich 2 ml.
- Bei eingeschränkter Leberfunktion individuelle Dosisanpassung.
Es ist zu unterscheiden zwischen der Behandlung im akuten Stadium und der Dauerbehandlung nach Erreichen der euthyreoten Stoffwechsellage.
Carbimazol
[Bearbeiten]- Wirkstoff Carbimazol
- Carbimazol® 5mg/ 10mg
- Neo-Thyreostat® = 1 Tbl. enthält Carbimazol 10mg
Propylthiouracil
[Bearbeiten]
- Propycil 50® = 1 Tbl. enthält 50mg PTU
- Thyreostat II/ 50mg® = 1 Tbl. enthält 25mg /50mg PTU
Perchlorat (Irenat)
[Bearbeiten]Natriumperchlorat ist das Natriumsalz der Perchlorsäure. Es besitzt die Summenformel NaClO4. Natriumperchlorat (Handelsname Irenat®) hemmt kompetitiv die Aufnahme von Iod und Technetium in die Schilddrüse. Es wurde daher früher häufig zur Behandlung der Hyperthyreose eingesetzt. Heute wird es fast nur noch zur Blockade der Schilddrüse bei Verabreichung iodhaltiger Kontrastmittel oder schilddrüsengängiger Radiopharmaka (123I, 131I, 99mTc) verwendet. Letzeres geschieht, um die Strahlenbelastung der Schilddrüse gering zu halten, es sei denn, es soll die Schilddrüse selbst dargestellt werden.
Zusammensetzung
[Bearbeiten]1 ml Irenat entsprechend ca. 15 Tropfen enthält 344,2 mg Natriumperchlorat 1H2O Weitere Bestandteile sind Ammoniumchlorid, Magnesiumchlorid, Calciumchlorid, Wasser.
Dosierung
[Bearbeiten]Perchlorat wird als Tropfen verabreicht.
Substanz Handelsname Verabreichung Anfangsdosis Erhaltungsdosis --------------------------------------------------------------------------------- Perchlorat Irenat Tropfen (15 Tropfen = 300 mg) 1200 mg/die 400 mg/die
Einnahme auf 4 mal pro Tag verteilen !
Irenat Tropfen werden mit Wasser verdünnt eingenommen. Irenat Tropfen werden auf 4-6 Einzeldosen verteilt. Anfangsdosis 40-50 Tropfen täglich, in Ausnahmefällen 75 Tropfen täglich.
Erhaltungsdosis 20 Tropfen täglich Hirnszintigraphie 10-20 Tr., in Einzelf. 50 Tr. Perchlorat Discharge-Test einmalig 30-50 Tr.
Kosten
[Bearbeiten]40 ml (N2) 17,16 Euro
Anwendung
[Bearbeiten]- Hyperthyreose
- Blockade der Schilddrüse bei szintigraphischen Untersuchungen anderer Organe mit radioaktiv markiertem Iod
- Hirnszintigraphie)
- Immunszintigraphien
- Tumorsuche mit Radioiod-markierten Anitikörpern
- Perchlorattest
Gegenanzeigen
[Bearbeiten]- Retrosternale Struma.
- Plummerung zur Operationsvorbereitung.
- Bereits früher unter Perchlorat-Gabe aufgetretene Blutbildveränderungen.
- Schwangerschaft
- Stillzeit
Nebenwirkungen
[Bearbeiten]- Gelegentlich.:
- flüchtiges Exanthem,
- Übelkeit oder Brechreiz,
- Mundtrockenheit,
- Reizungen im Rachenbereich,
- Lymphadenopathie,
- Leukopenie,
- Purpura,
- fieberhafte Gelenkschmerzen,
- Arzneimittelfieber.
- Selten:
- anfängl. Durchfall,
- leichte Muskelkrämpfe,
- Brennen in den Füßen,
- Schwere im Kopf,
- Eosinophilie,
- Juckreiz,
- Ikterus.
- Agranulozytose.
- In Einzelfällen:
- Thrombozytopenie,
- aplastische Anämie,
- Agranulozytose mit tödlichem Ausgang
- Albuminurie,
- nephrotisches Syndrom,
- Haarausfall,
- Akne,
- Dermatitis,
- Urtikaria,
- Leberschädigung mit akutem Leberversagen,
- Erythema nodosum mit Fieberschüben,
- antinukleären und antierythrozytären Antikörpern und Eosinophilie.
- Durchbruch eines Zwölffingerdarmgeschwüres.
Wechselwirkungen
[Bearbeiten]Die Radiojod- bzw. 99m Tc-Pertechnetat-Aufnahme wird dosisabhängig durch Perchlorat gehemmt. Die TSH-Stimulierbarkeit der Radiojodaufnahme wird durch Perchlorat nicht beeinflußt. Wirkungsverstärkung durch Propylthiouracil, Thiamazol, Carbimazol. Eine gleichzeitige Thiamazolgabe verursacht einen positiven Perchlorat Discharge-Test. Eine gleichzeitige Jodgabe vermindert die Irenat Tropfen-Wirkung.
Hinweise
[Bearbeiten]Bei Langzeitanwendung von Irenat Tropfen sind regelmäßige Blutbildkontrollen und Kontrollen der Schilddrüsenfunktion erforderlich.
Literatur
[Bearbeiten]- Wolff J: Perchlorate and the thyroid gland. Pharmacol Rev 1998; 50: 33–8.
Betablocker (Propranolol, Bisoprolol, Metoprolol)
[Bearbeiten]Betablocker schützen das Herz und andere Organe bei einer Schilddrüsenüberfunktion vor der Wirkung der erhöhten und dann auch gefährlichen Schilddrüsenhormone. Betablocker sind im allgemeinen gut verträglich. Bei Asthma, Diabetes und Durchblutungsstörungen der Beine muß man mit der Gabe von Betablockern zurückhaltend sein. Ob es echte Vorteile in der herzschützenden Wirkung der verschiedenen Betablocker gibt, ist umstritten. Bei Schilddrüsenüberfunktion wird meistens mit Propranolol behandelt. Bisoprolol ist wahrscheinlich genauso gut wirksam und hat den Vorteil, daß man es nur einmal am Tag nehmen muß. Die Dosis des Bisoprolol liegt zwischen 2,5 und 10 mg. Sie wird als Einmalgabe morgens eingenommen( 1-0-0) .
siehe Schilddrüse: Bisoprolol
Selen
[Bearbeiten]Bei Hashimotothyreoditis läßt sich die Höhe der Antikörper Titer durch die Gabe von Selen reduzieren, auch fühlen sich die Patienten wohler. ( täglich Gabe von 200 mikrog Natrium selenit zb Cefasel, selen-loges) Ob die Einnahme von Selen auch die Ausbildung einer Hypothyreose verhindert ist noch unklar. Der Einsatz beim Basedow und der Endokrionen Orbitopathie ist auch noch nicht sauber geklärt.
Literatur
[Bearbeiten]Ultraschalltherapie von Schilddrüsenknoten
[Bearbeiten]Man kann Schilddrüsenknoten auch mit einem fokusierten starken Ultraschallstrahl behandeln. Die Behandlung ähnelt der Steinzertrümmerung von Nierensteinen mit Ultraschall ( Lithotrypsie ). Sie kann nur bei gutartigen Knoten angewendet werden und wird teilweise noch nicht von den Krankenkassen bezahlt.
Adressen in Deutschland für die Ultraschallknotenbehandlung
- Nuklearmedizin Reumontstraße 35, 33102 Paderborn – Deutschland
- 0 52 51 41 77 9 – 10
- kontakt(at)nm-pb.de
- Webseite : www.nuklearmedizin-pb.de
- 0 52 51 41 77 9 – 10
- Borad
- Neustraße 17a – 46236 Bottrop – Deutschland
- 02041.1840-150
- info(at)borad.de
- www.borad.de/standorte/bottrop/
Schilddrüsenoperation
[Bearbeiten]Vorbemerkungen
[Bearbeiten]Durch eine regelmäßige Untersuchung lassen sich viele Operationen der Schilddrüse vermeiden. In Deutschland werden im Vergleich zur Schweiz etwa 5 mal mehr Schilddrüsenoperationen / 1 Million Einwohner durchgeführt. In einem Jahr sind das etwa 120 000 Eingriffen. Der entscheidende Grund dafür ist der nach wie vor bestehende Jodmangel in Deutschland.
Vor allem die diffuse Vergrößerung der Schilddrüse, die Knotenbildung in der Schilddrüse und ein Teil der Fälle mit Überfunktion ließe sich mit einer ausreichenden Jodversorgung stark reduzieren. Betroffen vom Jodmangel sind dabei vor allem Frauen. Ihr Anteil bei den Schilddrüsenoperationen liegt etwa bei 75 %.
Statistik der Schilddrüsenoperationen
[Bearbeiten]Mit der Studie Papillon 2007 liegt eine retrospektive Untersuchung von 56.300 Patienten vor, die in Deutschland an der Schilddrüse operiert wurden.
Grund zur Operation -------------------------------------- Knotenkropf 65 % Struma diffusa 15 % andere Schilddrüsenerkrankungen 20 % Komplikationen der Operation -------------------------------------- Rekurrenzparese 2 % Hypoparathyreoidismus 3,6 % Rezidivkropf 20 %
40 Prozent der Patienten, die an der Schilddrüsen operiert wurden, hatten vor ihrer Operation keine Schilddrüsentabletten bekommen.
Wann ist eine Operation unvermeidlich ?
[Bearbeiten]Der Hauptgrund für eine Schilddrüsenoperation ist der Verdacht auf eine bösartige Schilddrüsenkrankheit. Weitere OP-Indikationen sind:
- Mechanische oder mechanisch-kosmetische Veränderungen
- Hormonüberproduktion
Notwendige Voruntersuchungen
[Bearbeiten]- Allgemeine Voruntersuchungen mit der Frage der Opfähigkeit
je nach Alter und Vorerkrankungen können folgende Untersuchungen notwendig sein:
- Röntgen Thoraxaufnahme
- EKG und Echokardiografie
- Laboruntersuchungen insbesondere Blutbild, Gerinnung
- Lungenfunktion
- eventuell Belastungs-EKG
- Spezielle Voruntersuchungen der Schilddrüse
- Schilddrüsenultraschall und eventuell ein Szintigramm, CT oder NMR der Schilddrüse
- aktueller Hormonbefund
- Prüfen der Stimmbandfunktion
- Vorbesprechung des operativen Eingriffes ambulant beim verantwortlichen Chirurgen
- Schriftliche Einverständnis zur Operation
Wann ist eine Operation nicht möglich oder nicht sinnvoll?
[Bearbeiten]- wenn der Patient aus internistischer Sicht nicht opfähig ist
- Schwere Herzerkrankung
- Schwere Lungenerkrankung
- Schwere Lebererkrankung
- Schwere Nierenerkrankung
- Schwere Bluterkrankung
- notwendig ist ein Hb > 10
- Schlechte Gerinnungswerte
- (notwendig ist ein Quick > 50 %, Thrombos > 50000 PTT < 50 sek)
- Schwere Infektionskrankheit
- Schwere Tumorkrankheit
- Andere schwere Krankheit die den Operationserfolg beinträchtigt
- wenn der Patient nicht mit der Operation einverstanden ist
- wenn ein deutlicher positiver Effekt durch die Operation nicht zu erwarten ist
Risiken einer Schilddrüsen Operation
[Bearbeiten]Das Operationsrisiko hängt entscheidend von den Begleiterkrankungen des betroffenen Patienten ab. Außerdem ist die Erfahrungs des Operationsteams sehr wichtig. Eine Mindestzahl von 40 - 50 Schilddrüsenoperation / Jahr ist zu fordern. Es gibt allerdings Zentren die pro Jahr mehr als 500 Schilddrüsen OPs durchführen und damit vor allem für Problemfälle empfehlenswert sind.
Circa 24 Stunden lang ist nach der Operation eine intensivmedizinische Überwachung empfehlenswert, um eine bedrohliche Nachblutung mit Luftröhrenkompression oder sonstige Komplikationen sofort erkennen zu können.
- allgemeine Operationsrisiken
- Typische Risiken einer Schilddrüsenoperation
- Nachblutung in den Hals mit Kompression der Luftröhre
- Wundinfektion am Hals
- Verletzung des Stimmbandnerves
- Entfernung der Nebenschilddrüse mit nachfolgender Unterfunktion der Nebenschilddrüse
(Hypoparathyreodismus mit tetanischen Krämpfen)
Ablauf einer Schilddrüsenoperation
[Bearbeiten]( Vorsicht! Der folgende Abschnitts ist m.E.überarbeitungsbedürftig Benutzer:Rho)
Die Schilddrüsenchirurgie ist eine nahezu jahrhundertealte, bewährte Methode zur Behandlung von Schilddrüsenerkrankungen. In erster Linie werden drei Erkrankungsformen der Schilddrüse operativ erfaßt:
bösartige (Struma maligna), entzündliche (Thyreoiditis) Erkrankungen und die stoffwechsel störenden(funktionelle,hormonelle)Veränderungen.
Allen Operationsmethoden gemein ist die Verkleinerung oder die Entfernung des ganzen Organs mit dem Ziel das veränderte Gewebe aus dem Körper zu eliminieren oder die schädigenden Stoffwechsel produkte (Hormone) zu reduzieren.
Ein gänzliches Fehlen von Schilddrüsenhormonen ist mit dem Leben nicht vereinbar.Zu keinem Lebensalter. Ein Grundsatz, der niemals außer acht gelassen werden darf.
Genauso bedeutet ein Überangebot an Schilddrüsenhormon eine ernste Gefahr für dessen Träger:alle Organfunktioen arbeiten auf einem erhöhten Energielevel, d.h. die Reserven werden leichter erschöpft,was zu anhaltenden Organstörungen führen kann (!! Herzversagen !!).
Bis in die 70er Jahre wurde die Schilddrüsenchirurgie in Lokaler Betäubung vorgenommen,was für den Operateur gewisse Vorteile bot (geringeres Risiko einer Nervenverletzung) andererseits aber für den Patienten gelegentlich eine unerträgliche Qual darstellte, wenn z.B. die Masse der Schilddrüse zu voluminös war und operationstechnische Schwierigkeiten auftraten. Die Vollnarkose durch einen Narkosearzt ist daher obligat und vereinfacht das Verfahren erheblich.
Kurz umrissen sollen die Ziele der Operation bei den drei großen Schilddrüsenerkrankungen genannt sein:
- Schilddrüsenkrebs:
- möglichst totale Entfernung des erkrankten Organs. Bei Befall von ortsständigen Lymphknoten deren radikale Entfernung und bei Einbruch in Nachbarorgane deren Beseitigung (neck dissection)
- Schilddrüsenentzündung:
- totale Entfernung des gesamten Organs. Da dieses meist im Zuge einer sog.Autoimmunerkrankung miterkrankt (Hashimoto-,Riedel -Thyreoiditis) und das Organ ohnehin durch den Entzündungsprozess ausbrennt. Bakterielle Schilddrüsenentzündungen sind heutzutage nahezu ausgestorben.
- Hormonelle Schilddrüsenerkrankungen:
- hier werden über- oder unteraktiver Knoten ("heiß" oder "kalt) aus dem Gewebe entfernt. Die Schilddrüse ganz oder zum Teil entfernt.
Stets muss nach allen Operationen Schilddrüsenhormon in angemessener Dosis (nach dem Körpergewicht und Alter) eingenommen werden.
Mit dem Kocherschen Zugang werden am Hals und nach hinten abgeknickten Kopf ca 4-6 cm vom oberen Brustbeinende Haut- und Muskelplatte (Platysma) durchtrennt.
In allen Operationsschritten ist von nun an auf subtilste Blutstillung zu achten ,da die Schilddrüse extrem gut durchblutet ist. Möglichst stumpf d.h. ohne Einsatz von Skalpell und Schere werden die kurzen Halsmuskeln von der Schilddrüse abgeschoben und die spiegelnde Kapsel zur Darstellung gebracht.
Mit dem Zeigefinger kann man, nach Freilegung, das Organ umfahren und damit vorsichtig aus seiner Umgebung lösen. Doch: bietet sich dem Finger irgendeinen Widerstand: sofort denselben in seinem Tatendrang bremsen. Denn es finden sich massenhaft feiner Venen, die ekelig bluten und die man selten wiederfindet.
Mit großen runden Nadeln durchsticht man ein oder mehrmals die beiden Seiten-Lappen. Und legt damit sog. Haltefäden an, mit denen man einfach die Schilddrüsenlappen aus ihrer Loge mobilisieren kann.
Im nächsten Schritt werden die sog. oberen Polgefäße unterbunden (Aa.thyr.supp) und abgetrennt. Anschließend der Steg zwischen den beiden Seitenlappen (Isthmus). Nun folgt eine Sissyphus - Arbeit: das Aufsuchen und Unterbinden der unterschiedlich vorhandenen dicken oder dünnen, vielen oder wenigen, dick- oder dünnwandigen Seitenvenen. Dann werden die unteren Polgefäße dargestellt, unterbunden und durchtrennt. Ein nicht ganz leichter Akt,den im Gegensatz zu den oberen Polgefäßen teilen sich die unten oft schon vor der Schilddrüse oder sind nicht dort anzutreffn, wo man sie erwartet,weil sie aus einem tieferliegenden Blutgefäß entspringen als die oberen. Hier droht auch die erste Nervenverletzung (N.recurrens. Früher verzichtete man oft auf diesen nicht ungefährlichen Operationsschritt und versorgte die Blutung bei der späteren Kapselnaht. Ist die Versorgung der unteren Polgefäße geglückt, folgt die Schilddrüsen Resektion, d.h. die Verkleinerung oder Entfernung des Drüsenkörpers.
Hierbei muss immer der Nervus recurrens dargestellt werden. Seine Lähmung hat immer eine Katastrophe für den Operierten zur Folge:
Stimmbandlähmung! Er kann nicht mehr beschwerdefrei atmen, nicht mehr laut sprechen,nie wieder einen Ton singen ! Trotz sorgfältigster Unterbindung der zu und abführenden Blutgefässe ist stets mit einer mehr oder minder ausgeprägten Blutung bei der eigentlichen Resektion zu rechnen,was daran liegt, dass dieses höchststoffwechselaktive Organ auch noch aus vielen kleinen Gefässen mit versorgt wird. Es folgt die Kapselnaht,d.h. das Restgewebe wird mit einer fortlaufenden Naht zusammengezogen,um die Blutung zu beenden. Der N. wird fortgesetzt streng beachtet und nicht verletzt!
Es werden heiße Mullstreifen in die entstandnen Logen der Schilddrüsenlappen eingebracht und mit Haken festgehalten und einige Minuten abgewartet. Abschließend werden diese wieder hinausgelöst und die Bluttrochkenheit kontrolliert. Zwei Saugdrainagen werden eingebracht und die Halsmuskulatur kulissenartig vor die Schilddrüsenlogen gebracht bzw., nach Durchtrennung, wieder vernäht. Im letzten Schritt wird der Kopf des Operierten wieder nach vorne gebeugt und nur die Haut geklammert (Kölner Sparklammern) oder intracutan genäht. Beendet wird der Eingriff mit einem sterilen Wundverband.Die Muskelplatte (Platysma) darf nicht genäht werden :Narbenbildung.
Präparat zur Histologie
Im Aufwachraum läßt der Operateur den Patienten nacht Entfernen des Tubus "Amerika" sagen. Das geht nur, wenn der Nerv heil geblieben ist.
OP-Verfahren
[Bearbeiten]
- Solitäres autonomes Adenom:
- Knotenresektion
- Nur der heiße Knoten wird entfernt , die restliche gesunde Schilddrüse wird belassen
- Knotenresektion
- Euthyreote Struma
- subtotale Resektion. bds
- Entfernung der Schilddrüse beidseits bis auf einen kleinen Rest
- subtotale Resektion. bds
- Multifokale Adenome:
- funktionsorientierte Resektion bis zur subtotalen Resektion bds.
- Entfernung der knotigen Schilddrüseanteile beidseits
- funktionsorientierte Resektion bis zur subtotalen Resektion bds.
- Neckdissection
- Entfernung aller Lymphknoten am Hals bei Schilddrüsenkrebs mit Lymphknotenbefall oder Kehlkropfkrebs
- Die radikale Neckdissektion wird nur selten durchgeführt. Man macht häufiger die modifizierte Neckdiessektion. Dabei bleibt der M. sternocleidomasteoideus, die V. Jugularis interna, der N. vagus und der N. accessorius erhalten.
- Entfernung aller Lymphknoten am Hals bei Schilddrüsenkrebs mit Lymphknotenbefall oder Kehlkropfkrebs

OP-Technik
[Bearbeiten]Subtotale Resektion:
- Lagerung:
- halbsitzende Position mit Reklination des Kopfes
- Unterpolsterung der Fersen und Knie mit einem Polster.
- Halbrolle unter die Oberschenkel
Ablauf:
- Kocherscher Kragenschnitt: Haut, Subkutis und Platysma
- Durchtrennung der Faszie und Präparation der Faszienvenen die ligiert und durchtrennt werden
- Längsspaltung der geraden Halsmuskulatur, bei großen Strumen wird die Muskulatur quer durchtrennt
- Stumpfes Freilegen des Strumalappens
- Durchtrennen des Isthmuses und Freilegen der Trachea
- Hervorluxieren des SD-Lappens
- Eventuell Darstellung des N. laryngeus recurrens
- Ligatur der unteren SD-Arterie
- Ligatur und Durchtrennung der Gefäße am oberen Pol
- Entwicklung des unteren Poles
- Resektion der SD-Seite, über Kocherklemmen oder unter schneller Blutstillung
- Durchgreifende Kapselnaht mit Maxon
- Gleiches Vorgehen auf der anderen Seite
- Je eine Redondrainage 12 Charrier in die Wundhöhle
- Schichtweiser Wundverschluß
- Verband
Postoperative Nachsorge
[Bearbeiten]Statistik
[Bearbeiten]Alle medizinischen Operationen und aufwendigeren diagnostischen Methoden werden mittels eines Ziffernkataloges OPS-301 verschlüsselt. Die die OPS Nummern für Schilddrüsenoperationen sind im folgenden augelistet.
- Kapitel: 5
- OPERATIONEN
- (5-01...5-99)
- Operationen an endokrinen Drüsen
- (5-06...5-07)
- OPERATIONEN
Hinw.: Die Anwendung mikrochirurgischer Technik ist, sofern nicht als eigener Kode angegeben, zusätzlich zu kodieren ( 5-984 )
Die Anwendung von Lasertechnik ist, sofern nicht als eigener Kode angegeben, zusätzlich zu kodieren ( 5-985 )
Die Durchführung der Operation im Rahmen der Versorgung einer Mehrfachverletzung ist zusätzlich zu kodieren ( 5-981 )
Die Durchführung der Operation im Rahmen der Versorgung eines Polytraumas ist zusätzlich zu kodieren ( 5-982 )
Die Durchführung einer Reoperation ist, sofern nicht als eigener Kode angegeben, zusätzlich zu kodieren ( 5-983 )
Der vorzeitige Abbruch einer Operation ist zusätzlich zu kodieren ( 5-995 )
5-06 Operationen an Schilddrüse und Nebenschilddrüse
[Bearbeiten]Hinw.: Bei fehlender Seitenangabe ist die Operation als einseitiger Eingriff zu kodieren
Eine durchgeführte Neck dissection ist gesondert zu kodieren ( 5-403 )
- 5-060 Inzision im Gebiet der Schilddrüse
- 5-060.0 Ohne weitere Maßnahmen
- 5-060.1 Drainage
- 5-060.2 Exploration
- Inkl.: Biopsie der Schilddrüse
- 5-060.3 Revision der Operationswunde
- 5-060.x Sonstige
- 5-060.y N.n.bez.
- 5-061 Hemithyreoidektomie
- Hinw.: Eine durchgeführte Neck dissection ist gesondert zu kodieren ( 5-403 )
- 5-061.0 Ohne Parathyreoidektomie, ohne Monitoring des N. recurrens
- 5-061.1 Ohne Parathyreoidektomie, mit Monitoring des N. recurrens
- 5-061.2 Mit Parathyreoidektomie, ohne Monitoring des N. recurrens
- 5-061.3 Mit Parathyreoidektomie, mit Monitoring des N. recurrens
- 5-061.x Sonstige
- 5-061.y N.n.bez.
- 5-062 Andere partielle Schilddrüsenresektion
- 5-062.0 Exzision von erkranktem Gewebe
- 5-062.1 Exzision eines Knotens
- 5-062.2 Subtotale Resektion, einseitig
- 5-062.3 Subtotale Resektion, beidseitig
- 5-062.4 Subtotale Resektion, einseitig mit Exzision eines Knotens der Gegenseite
- 5-062.5 Subtotale Resektion, einseitig mit Hemithyreoidektomie der Gegenseite
- 5-062.6 Reexploration mit partieller Resektion
- 5-062.7 Resektion des Isthmus
- 5-062.x Sonstige
- 5-062.y N.n.bez.
- 5-063 Thyreoidektomie
- Hinw.: Eine durchgeführte Neck dissection ist gesondert zu kodieren ( 5-403 )
- 5-063.0 Ohne Parathyreoidektomie, ohne Monitoring des N. recurrens
- 5-063.1 Ohne Parathyreoidektomie, mit Monitoring des N. recurrens
- 5-063.2 Mit Parathyreoidektomie, ohne Monitoring des N. recurrens
- 5-063.3 Mit Parathyreoidektomie, mit Monitoring des N. recurrens
- 5-063.4 Reexploration mit Thyreoidektomie, ohne Monitoring des N. recurrens
- 5-063.5 Reexploration mit Thyreoidektomie, mit Monitoring des N. recurrens
- 5-063.x Sonstige
- 5-063.y N.n.bez.
- 5-064 Operationen an der Schilddrüse durch Sternotomie
- Hinw.: Eine durchgeführte Neck dissection ist gesondert zu kodieren ( 5-403 )
- 5-064.0 Exzision von erkranktem Gewebe
- 5-064.1 Subtotale Resektion
- 5-064.2 Hemithyreoidektomie
- 5-064.3 Thyreoidektomie
- 5-064.x Sonstige
- 5-064.y N.n.bez.
- 5-065 Exzision des Ductus thyreoglossus
- 5-065.0 Exzision einer medianen Halszyste, ohne Resektion des medialen Zungenbeines
- 5-065.1 Exzision einer medianen Halszyste, mit Resektion des medialen Zungenbeines
- 5-065.2 Exzision einer medianen Halsfistel, ohne Resektion des medialen Zungenbeines
- 5-065.3 Exzision einer medianen Halsfistel, mit Resektion des medialen Zungenbeines
- 5-065.4 Sekundärer Eingriff, ohne Resektion des medialen Zungenbeines
- 5-065.5 Sekundärer Eingriff, mit Resektion des medialen Zungenbeines
- 5-065.x Sonstige
- 5-065.y N.n.bez.
- 5-066 Partielle Nebenschilddrüsenresektion
- 5-066.0 Exzision von erkranktem Gewebe
- 5-066.1 Reexploration mit partieller Resektion
- 5-066.x Sonstige
- 5-066.y N.n.bez.
- 5-067 Parathyreoidektomie
- 5-067.0 Ohne Replantation
- 5-067.1 Mit Replantation (Autotransplantation)
- 5-067.x Sonstige
- 5-067.y N.n.bez.
- 5-068 Operationen an der Nebenschilddrüse durch Sternotomie
- 5-068.0 Exzision von erkranktem Gewebe
- 5-068.1 Parathyreoidektomie ohne Replantation
- 5-068.2 Parathyreoidektomie mit Replantation (Autotransplantation)
- 5-068.x Sonstige
- 5-068.y N.n.bez.
- 5-069 Andere Operationen an Schilddrüse und Nebenschilddrüsen
- 5-069.0 Naht (nach Verletzung)
- .00 Schilddrüse
- .01 Nebenschilddrüse
- 5-069.1 Plastische Rekonstruktion
- .10 Schilddrüse
- .11 Nebenschilddrüse
- 5-069.2 Exzision einer Zungengrundschilddrüse
- .20 Transoral
- .21 Transzervikal, ohne Resektion des medialen Zungenbeines
- .22 Transzervikal, mit Resektion des medialen Zungenbeines
- .2x Sonstige
- .2y N.n.bez.
- 5-069.x Sonstige
- 5-069.y N.n.bez.
- 5-069.0 Naht (nach Verletzung)
Adressen
[Bearbeiten]Literatur
[Bearbeiten]- Eva Nicole Seidel-Schneider
- DISSERTATION Die Risikofaktoren und Komplikationen in der chirurgischen Strumatherapie
- vorgelegt der Medizinischen Fakultät der Humboldt-Universität zu Berlin
- DISSERTATION Die Risikofaktoren und Komplikationen in der chirurgischen Strumatherapie
- Chirurgische Therapie bei beidseitiger benigner Struma nodosa: Abwägung zwischen Radikalität und Komplikationen
- Dtsch Arztebl Int 2014; 111(10): 171-8; DOI: 10.3238/arztebl.2014.0171
- Rayes, Nada; Seehofer, Daniel; Neuhaus, Peter
- Dtsch Arztebl Int 2014; 111(10): 171-8; DOI: 10.3238/arztebl.2014.0171
Links
[Bearbeiten]- http://www.schilddruesenguide.de/jaehne_beuleke.html
- Gut verständliche Angaben zur Schilddrüsen Operation
- http://www.aok.de/bund/tools/medicity/therapie.php?icd=57
- Allgemein verständliche Angaben zur Schilddrüsen Operation
- http://www.kueterscheck.de/folge_2.htm
- http://edoc.hu-berlin.de/dissertationen/seidel-schneider-eva-nicole-2004-04-30/PDF/Seidel-Schneider.pdf
Radiojodtherapie
[Bearbeiten]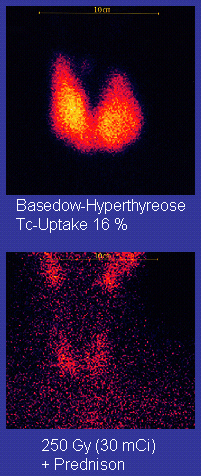
Allgemeines
[Bearbeiten]Die Radioiodtherapie (RIT, auch Radiojodtherapie, RJT) ist ein bewährtes, gut wirksames nuklearmedizinisches Therapieverfahren zur Behandlung der Schilddrüsenautonomie, der Basedow-Krankheit, der Schilddrüsenvergrößerung und bestimmter Formen des Schilddrüsenkrebses. Eingesetzt wird das radioaktive Iod-Isotop 131Iod, das ein überwiegender Beta-Strahler mit einer Halbwertszeit von acht Tagen ist und im menschlichen Körper nur in Schilddrüsenzellen gespeichert wird.
Die RIT unterliegt in vielen Ländern bestimmten gesetzlichen Voraussetzungen und kann in Deutschland nur stationär durchgeführt werden. Die Therapieform wird seit den 1940er Jahren angewendet und ist nebenwirkungsarm und auch in der langjährigen Verlaufsbeobachtung weitgehend sicher. In Deutschland existieren etwa 150 Therapieeinrichtungen, in denen etwa 60.000 bis 70.000 Behandlungen jährlich durchgeführt werden.
Grünwald">F. Grünwald, C. Menzel. Radioiodtherapie. In: T. Kuwert, F. Grünwald, U. Haberkorn, T. Krause. Nuklearmedizin. Stuttgart, New York 2008 ISBN 978-3-13-118504-4
Anwendungsgebiete
[Bearbeiten]Die Radioiodtherapie ist ein nuklearmedizinisches Therapieverfahren, das bei verschiedenen Erkrankungen der Schilddrüse durchgeführt wird. Die häufigsten Grüne für die Behandlung sind
- die autonomen Funktionsstörungen der Schilddrüse (Autonomes Adenom, multifokale Autonomie),
- die Basedow-Krankheit (Morbus Basedow) und
- diejenigen Formen des Schilddrüsenkrebses (Schilddrüsen-Karzinom), die Iod speichern:
- das papilläre und das follikuläre Schilddrüsenkarzinom.
Auch eine Schilddrüsenvergrößerung (Struma) ohne Funktionsstörung kann mittels Radioiodtherapie behandelt werden.
Eine Schwangerschaft gilt als absolute Kontraindikation für die Radioiodtherapie bei gutartigen Schilddrüsenerkrankungen. Aus allgemeinen strahlenbiologischen Erwägungen wird empfohlen, bis zu 6 Monate nach der RIT eine Schwangerschaft zu vermeiden. Tritt in dieser Zeit doch eine Schwangerschaft ein, so ist dies aber kein ausreichender Grund für einen Schwangerschaftsabbruch. Es wird jedoch empfohlen, eine genetische Beratung in Anspruch zu nehmen. Für die Radioiodtherapie beim Schilddrüsenkrebs in der Schwangerschaft gilt, dass zwar die theoretische Wahrscheinlichkeit für das Auftreten einer genetischen Schädigung berechenbar ist, solche Schäden in der Realität aber bisher nicht aufgetreten sind.
Alternative Behandlungsverfahren sind für die Funktionsstörungen die verschiedenen Formen der Schilddrüsenoperation. Der Morbus Basedow kann in einem Teil der Fälle unter der medikamentösen Behandlung mit Thyreostatika vorübergehend oder dauerhaft in seiner Aktivität nachlassen, als endgültige („definitive“) Therapie kommt neben der RIT auch die Operation in Frage. Bei den Schilddrüsen-Karzinomen kann nur beim papillären Karzinom im Frühstadium pT1a nach der Operation auf die Radioiodtherapie verzichtet werden. Zur Behandlung der gutartigen Schilddrüsenvergrößerung werden die medikamentöse Therapie, Operation und RIT eingesetzt.
Wenn die Wahl zwischen Operation und Radioiodtherapie besteht, sprechen folgende Argumente für die RIT:
- Wenn die Schilddrüse bereits operiert worden war oder bereits eine (einseitige) Lähmung des Stimmbandnervens (Rekurrensparese) vorliegt,
- bei Patienten in höherem Lebensalter oder mit schweren Begleiterkrankungen,
- wenn die Schilddrüse relativ klein ist oder
- der Patient unter Operationsangst leidet.
Jugendliches Alter gilt nicht mehr als Kontraindikation.
Folgende Argumente sprechen dagegen für die Operation:
- Verdacht auf Bösartigkeit,
- durch Iod verursachte Schilddrüsenüberfunktion (Hyperthyreose),
- Schwangerschaft und Stillzeit,
- floride Augenbeteiligung bei Morbus Basedow (endokrine Orbitopathie),
- Zeichen einer Einengung (Kompression) der Nachbarstrukturen
- Luftröhre: Stridor,
- Speiseröhre: ausgeprägte Schluckstörung,
- Halsgefäße: obere Einflussstauung
- Strahlenangst oder
- größere kalte Gebiete der Schilddrüse.
Gesetzliche Voraussetzungen
[Bearbeiten]In den meisten Ländern unterliegt die Durchführung der Radioiodtherapie bestimmten gesetzlichen und quasi-gesetzlichen Regelungen. In vielen Ländern kann die Radioiodtherapie ambulant durchgeführt werden. Deutschland hat dabei ziemlich strenge Regeln, in andern Ländern sind die Bestimmungen weitaus großzügiger, so daß oft ambulante Behandlungen durchgeführt werden.
In Deutschland regeln die Strahlenschutzverordnung und die vom Länderausschuss für Atomkernenergie herausgegebene Richtlinie „Strahlenschutz in der Medizin“ die Durchführung der Radioiodtherapie. Sie legen fest, dass die Therapie nur auf einer nuklearmedizinischen Therapiestation durchgeführt werden darf. Der durchführende Arzt muss eine entsprechende Umgangsgenehmigung haben, deren Erteilung unter anderem an die Fach- und Sachkunde auf dem Gebiet der Anwendung radioaktiver Stoffe in der Diagnostik und Therapie geknüpft ist. Die Anwesenheit eines Medizinphysikexperten ist notwendig. Den Erfordernissen des Strahlenschutzes ist in Bezug auf bauliche und personelle Aspekte Rechnung zu tragen. Insbesondere muss eine geeignete Abklinganlage für radioaktiv kontaminierte Abwässer vorhanden sein. Das betreuende Personal muss regelmäßig im Strahlenschutz unterwiesen werden.
Ambulante Therapien sind in Österreich möglich. Die Grenzaktivitäten sind auch hier gesetzlich festgelegt. Auch in Österreich ist die Anwesenheit eines Medizinphysikexperten vorgeschrieben.
In der Schweiz dürfen Radioiodtherapien mit einer applizierten Aktivität bis 200 MBq ambulant durchgeführt werden.
In den USA dürfen Radioiodtherapien bis zu einer Aktivität von 1110 MBq ambulant durchgeführt werden. Die Mehrzahl der Therapien bei gutartigen Schilddrüsenerkrankungen kann damit ambulant vorgenommen werden.
Therapieprinzip und physikalische Grundlagen
[Bearbeiten]
Das verwendete radioaktive Iod-Isotop 131Iod steht in Kapselform und flüssig zur Verfügung. Es wird in der Regel oral verabreicht, kann in Ausnahmefällen (zum Beispiel bei ausgeprägten Schluckstörungen) auch intravenös appliziert werden. Bei peroraler Aufnahme wird das Iod rasch über die Magenschleimhaut aufgenommen und an das Blut abgegeben. Über den Natrium-Iodid-Symporte gelangt das Iod in die Schilddrüsenzelle und wird letztlich im Schilddrüsenfollikel gespeichert. Unter der Wirkung von TSH oder TRAK (TSH-Rezeptor-Autoantikörpern) ist die Aufnahme von Iod in die Schilddrüsenzellen erhöht. Autonome Anteile der Schilddrüse nehmen Iod unabhängig vom TSH auf.
Die besondere Eleganz der Radioiodtherapie liegt darin begründet, dass nur Schilddrüsenzellen Iod – und damit auch Radioiod – aufnehmen, andere Organe speichern kein Iod. Das nicht in der Schilddrüse gespeicherte Iod wird innerhalb kurzer Zeit über die Nieren und die Harnblase aus dem Körper ausgeschieden. Geringe Mengen werden von den Schweißdrüsen und über den Darm ausgeschieden. In geringem Maße wird Iod zwar von den Speicheldrüsen und der Magenschleimhaut ausgeschieden, über den Magen-Darm-Trakt aber wieder aufgenommen. Wegen dieser besonderen Eigenschaften des Iod-Stoffwechsels ist es möglich, sehr große Strahlendosen im Zielgewebe zur erreichen, während die übrigen Gewebe nur eine geringe Strahlenexposition haben.
131Iod ist ein in Kernreakto]en hergestelltes Nuklid und hat eine Halbwertszeit von 8,02 Tagen. Bei seinem Zerfall zu stabilem Xenon wird ein Beta-Strahl mit der maximalen Energie von 0,61 MeV und einer mittleren Reichweite von 0,5 mm frei. Diese Strahlung ist für die therapeutische Wirkung verantwortlich. Darüber hinaus wird auch Gammastrahlung mit dem Hauptpeak bei 364 keV frei, die die Schilddrüse verlassen kann und daher einerseits für die unerwünschte Strahlenexposition des Patienten und der Umgebung verantwortlich ist, andererseits aber auch für die Bildgebung und den Radioiodtest verwendet werden kann.
Die Betastrahlen bewirken in der Umgebung der Schilddrüsenzellen Schäden in der Desoxyribonukleinsäure(DNA), insbesondere Doppelstrangbrüche, die letztlich zur Einleitung des programmierten Zelltods führen.
Die Radioiodtherapie bei gutartigen Schilddrüsenerkrankungen
[Bearbeiten]Vorbereitung
[Bearbeiten]Iodkarenz
[Bearbeiten]
Um eine optimale Aufnahme des Iods in die Schilddrüse zu erreichen, sollen vor dem Radioiodtest und der Therapie mit radioaktivem Iod zusätzliche Iodquellen gemieden werden (Iodkarenz). Solche Iodquellen sind insbesondere iodhaltige Kontrastmittel, das Antiarrhythmikum Amiodaron und bestimmte iodhaltige Desinfektionsmittel. Bei wasserlöslichen Kontrastmittel reicht eine Karenzzeit von 6 Wochen. Nach der Anwendung fettlöslicher Kontrastmitteln oder des ebenfalls fettlöslichen Amiodaron kann die Schilddrüse für viele Monate blockiert sein.
Iod in nennenswerten Mengen ist in vielen Multivitaminpräparaten und Nahrungsergänzungsmitteln enthalten, sowie in Seefisch, Meeresfrüchten und bestimmten Produkten aus Algen. Diese Iodquellen sollen für etwa eine Woche vor Iodtest und Therapie vermieden werden. Die Einnahme von Iod aus iodiertem Speisesalz und mit diesem zubereiteten, industriell gefertigten Lebensmitteln ist praktisch nicht vollständig zu vermeiden.
Stoffwechseleinstellung
[Bearbeiten]
Die Radioiodtherapie soll möglichst nicht bei manifest hyperthyreoter Stoffwechsellage durchgeführt werden, da die Überfunktion durch Freisetzung der Schilddrüsenhormone Thyroxin (T4) und Trijodthyronin (T3) verstärkt werden kann. Daher sollen mit der niedrigsten möglichen Dosis von Thyreostatika in den Wochen vor der RIT normale Werte für T4 und T3 eingestellt werden. Allerdings vermindern Thyreostatika die Iodaufnahme in die Schilddrüse, so dass empfohlen wird, diese wenigstens ein bis zwei Tage vor der Radioiodherapie abzusetzen.
Bei der Schilddrüsenautonomie soll der TSH-Wert supprimiert sein, um über den thyreotropen Regelkreis die Iodaufnahme in nicht-autonome Anteile der Schilddrüse zu minimieren. Gegebenenfalls müssen hierfür zur Vorbereitung Schilddrüsenhormone gegeben werden. Bei der euthyreoten Struma wird die Therapie in der Regel ohne begleitende Schilddrüsen-gerichtete Medikamente durchgeführt.
Ermittlung der geeigneten Therapie-Aktivität
[Bearbeiten]Die deutsche Richtlinie „Strahlenschutz in der Medizin“ schreibt vor: Bei der Planung einer nuklearmedizinischen Behandlung ist die Dosis für die zu behandelnden Organe oder Gewebe [...] im voraus zu ermitteln und die danach zu verabreichende Aktivität zu bemessen. Soweit patientenspezifische Parameter benötigt werden, sind hierfür individuelle Messungen und Daten heranzuziehen.
Referenz: Richtlinie "Strahlenschutz in der Medizin" (zur StrlSchV)[1]
Bei der Ermittlung der zur Therapie notwendigen Aktivität ist in Deutschland und in Österreich neben dem Nuklearmediziner auch ein Medizinphysikexperte hinzuzuziehen. In die Berechnung gehen die Zieldosis, das Zielvolumen und das Integral der Aktivität in der Schilddrüse über die Zeit ein.
Das Zielvolumen der Radioiodtherapie und die im Zielvolumen angestrebte Energiedosis richten sich nach der zu behandelnden Erkrankung. Beim Morbus Basedow, bei der Schilddrüsenvergrößerung ohne Autonomie und bei der disseminierten Autonomie wird das sonografisch bestimmte Gesamtvolumen der Schilddrüse als Zielvolumen angenommen, bei der unifokalen und multifokalen Autonomie nur das Volumen der Adenome. Die angestrebten Zieldosen laut Leitlinie der Deutschen Gesellschaft für Nuklearmedizin zur Radioiodtherapie bei benignen Schilddrüsenerkrankungen sind in folgender Tabelle angegeben.
| Unifokale Autonomie | etwa 300 bis 400 Gy | 4,8 Tage | 4,2 Tage |
| Multifokale Autonomie | etwa 150 Gy | 5,5 Tage | 4,8 Tage |
| Disseminierte Autonomie | etwa 150 Gy | 5,5 Tage | 4,8 Tage |
| Morbus Basedow | 4,2 Tage | ||
| Ablatives Konzept | etwa 200 bis 300 Gy | ||
| Funktionsoptimiertes Konzept | etwa 150 Gy | ||
| Struma zur Verkleinerung | etwa 120 bis 150 Gy | 5,5 Tage | |
Das Aktivitäts-Zeit-Integral kann mit dem Radioiodtest ermittelt werden. Hierzu wird eine geringe Menge Radioiod verabreicht (meist peroral): etwa 1 bis 5 MBq 131Iod oder – seltener – 5 bis 10 MBq 123Iod. Zu bestimmten Zeitpunkten wird die Aktivität über der Schilddrüse gemessen und ins Verhältnis zur Ausgangsaktivität und ihrem natürlichen Zerfall gesetzt. Zu bestimmen sind die maximale Aufnahme (uptake) in Prozent und die effektive Halbwertszeit in Tagen. Je mehr Messpunkte vorliegen, desto genauer kann die Fläche unter der Kurve bestimmt werden. Aus Gründen der praktischen (ambulanten) Durchführbarkeit wird meist nur nach 24 und 48 Stunden gemessen, unter Umständen auch nur nach 24 Stunden. Beim Morbus Basedow wird wegen des beschleunigten Iodumsatzes eine erste Messung bereits nach vier bis acht Stunden gefordert. Zur genauen Bestimmung der effektiven Halbwertszeit wird eine weitere Messung nach vier bis acht Tagen notwendig. Wegen nur geringer Unterschiede der effektiven Halbwertszeit zwischen den einzelnen Patienten mit gleicher Erkrankung und gleicher Stoffwechsellage, kann die effektive Halbwertszeit auch als empirisch ermittelter Wert angenommen werden (siehe Tabelle).
Die anzuwendende Therapie-Aktivität kann dann nach der Marinelli-Formel berechnet werden.
Marinelli LD, Quinby EH, Hine GJ. Dosage determination with radioactive isotopes. Practical considerations in therapy and protection. Am J Röntgenol 1948; 59:260 - 81
Hierbei ist A die zu errechnende Aktivität, HD die angestrebte Herddosis, V das bestimmte Zielvolumen, K eine empirisch ermittelte Konstante von 24,67, Umax der maximale uptake und t0,5 eff die effektive Halbwertszeit.
Cortison-Vorbehandlung bei endokriner Orbitopathie
[Bearbeiten]Eine endokrine Orbitopathie (eO) bei Morbus Basedow kann sich unter der Radioiodtherapie verschlechtern oder erstmals auftreten. Bei vorbestehender eO wird daher ab dem Tag der RIT oder dem Tag zuvor eine Behandlung mit Glucocorticoiden (Cortison) empfohlen, die Dosierung richtet sich nach dem Schweregrad der Augenerkrankung. Beim Morbus Basedow ohne endokrine Orbitopathie ist die prophylaktische Gabe von Glucocorticoiden umstritten. Die möglichen Nebenwirkungen und Kontraindikationen der Cortison-Therapie (Diabetes mellitus, Magengeschwüre und Elektrolytstörungen) sind zu beachten.
Aufklärung
[Bearbeiten]Vor Beginn von Radioiodtest und Radioiodtherapie erfolgt eine Aufklärung. In dieser wird der Patient auf den Ablauf von Test und Therapie hingewiesen. Neben den Risiken und Nebenwirkungen der RIT ist in den Ländern, in denen die RIT nur stationär durchgeführt werden kann, insbesondere die Tatsache, dass nach Gabe der Therapieaktivität der Patient die Therapiestation nicht verlassen darf, Gegenstand des Aufklärungsgespräches. Der Patient wird außerdem darauf hingewiesen, dass regelmäßige Nachuntersuchungen medizinisch geboten und gesetzlich vorgeschrieben sind (siehe → Abschnitt Nachsorge).
Durchführung
[Bearbeiten]Nach der meist peroralen – in Ausnahmefällen intravenösen – Gabe des 131Iod muss in Deutschland der Patient mindestens 48 Stunden auf der Therapiestation verbleiben. Es wird empfohlen, etwa eine Stunde nach peroraler Einnahme nüchtern zu bleiben, bis das Radioiod weitgehend resorbiert ist.[2]
Üblicherweise erfolgen dann regelmäßige Messungen der Strahlung, diese lassen Rückschlüsse auf die im gesamten Körper des Patienten beziehungsweise in der Schilddrüse verbliebene Aktivität. Erstere ist wichtig für den Zeitpunkt der Entlassung nach der Therapie, letztere im Maximalwert und im zeitlichen Verlauf zur Kontrolle des Therapieerfolges. Es lassen sich nämlich der tatsächlich erreichte maximale Uptake (Umax) und die tatsächlich erzielte effektive Halbwertszeit (t0,5 eff) ermitteln und durch Umstellung der Marinelli-Formel (siehe oben) die tatsächlich erzielte Herddosis (HD) bestimmen. Das Zielvolumen V und die empirisch ermittelte Konstante K sind unverändert.
Sollte die Herddosis vom geplanten Wert wesentlich nach oben abweichen, so ist mit höherer Wahrscheinlichkeit mit der Entwicklung einer Schilddrüsen-Unterfunktion nach der Therapie zu rechnen und die Nachsorge entsprechend zu planen.
Sollte die Herddosis dagegen wesentlich nach unten abweichen, kann noch während des stationären Therapie-Aufenthaltes eine zusätzliche Gabe von Radioiod erfolgen, um die erwünschte Zieldosis noch zu erreichen und den Therapieerfolg zu sichern. Dabei ist zu beachten, dass aufgrund der Frühwirkung der Radioiodtherapie („stunning“) der Uptake der zweiten Dosis regelmäßig niedriger liegt, als der der ersten.
Durch die Gabe geringer Mengen nicht-radioaktiven Iods oder von Lithium nach der Gabe des Radioiods lässt sich das Verbleiben des Radioiods in der Schilddrüse und damit die effektive Halbwertszeit t0,5 eff verlängern und eine um bis zu 30 % höhere Herddosis erzielen. Hierbei sind insbesondere beim Lithium Risiken und Nebenwirkungen sowie die geringe therapeutische Breite zu beachten.[2]
Risiken und Nebenwirkungen
[Bearbeiten]Strahlenexposition
[Bearbeiten]Aufgrund der biologischen Eigenschaften von Iod und der physikalischen Eigenschaften von 131Iod verursacht die Radioiodtherapie nur eine geringe Strahlenexposition der Organe, die kein Radioiod aufnehmen. Die Strahlenexposition ist in den der Schilddrüse benachbarten Strukturen wie dem Kehlkopf oder den Nebenschilddrüsen gering – bedingt durch die geringe Reichweite der Betastrahlung aus der Schilddrüse. Einige Gewebe, die den Natrium-Iodid-Symporter exprimieren, darunter die Speicheldrüsen, Magen und die Weibliche Brust, reichern vorübergehend Iod an. Nieren, Harnblase und Darm sind an der Ausscheidung des Anteils Radioiod, der nicht in der Schilddrüse gespeichert wird, beteiligt. In allen diesen Geweben liegt ein geringes Aktivitäts-Zeit-Integral vor, die Strahlenexposition ist entsprechend gering. Sie wird bei einem Uptake des Radioiods in die Schilddrüse von 25 % für die Magenwand mit 0,46 mGy/MBq angegeben, für die Ovarien mit 0,04 mGy/MBq, das rote Knochenmark 0,07 mGy/MBq, die Leber 0,035 mGy/MBq und die Hoden mit 0,028 mGy/MBq.[3] Im Zielgewebe Schilddrüse liegt dagegen die (erwünschte) Strahlendosis um vier bis fünf Zehnerpotenzen höher: bei einem Uptake von 25 % bei 350 mGy/MBq.[3]
Die Kohortenstudien von Hall 1992 mit über 45.000 Patineten[4] und Ron 1998 mit über 35.000 Patienten[5] haben keine erhöhte Krebsmortalität der mit radioaktivem Iod behandelten Patienten festgestellt. Die American Thyroid Association (amerikanische Schilddrüsengesellschaft) weist auf eine mögliche, minimal erhöhte Inzidenz von Schilddrüsen-Karzinomen nach einer Behandlung hin.[6]
Akute Nebenwirkungen
[Bearbeiten]Nur in wenigen Fällen kommt es zu akuten Nebenwirkungen, diese sind meist harmlos. Am häufigsten ist die Radiothyreoiditis, eine schmerzhafte Entzündungsreaktion der Schilddrüse bedingt durch die akute Strahlenwirkung, die etwa drei bis fünf Tage nach Einnahme des Radioiods auftreten kann. Durch Kühlung und entzündungshemmende Medikamente wie nichtsteroidale Antirheumatika oder Glucocorticoide lassen sich die Beschwerden, die innerhalb weniger Tage abklingen, meistens gut bessern. Die die Entzündung der Schilddrüse begleitende Schwellung kann lediglich bei vorbestehender Verengung der Luftröhre (Trachealstenose) zu ernsthaften Problemen wie Luftnot führen, so dass in diesen Fällen eine vorbeugende entzündungshemmende Behandlung empfoheln wird.
Entzündliche Schwellungen der Speicheldrüsen kommen meist nur bei höheren Therapie-Aktivitäten vor.
Bei vorbestehender Schilddrüsenüberfunktion kann sich diese etwa sieben bis zehn Tage nach Beginn der Behandlung verschlechtern, bedingt durch den beginnenden Zellzerfall und die damit verbundenene Freisetzung von Hormonen, die in der Schilddrüse gespeichert waren. Diese Komplikation kann durch eine gute Einstellung einer normalen Stoffwechsellage vor der Behandlung vermieden werden.
Eine seltene Nebenwirkung nach Radioiodtherapie wegen einer Schilddrüsenautonomie (zum Beispiel Autonomes Adenom) ist das zusätzliche Auftreten einer immunogenen Hyperthyreose wenige Wochen später. Dieses Phänomen wird Marine-Lenhart-Syndrom genannt und limitiert sich meistens selbst. Die Häufigkeit wird mit 0,5 bis 1 % angegeben. In einem Teil der Fälle muss aber wegen der neu aufgetreten Überfunktion eine zweite Radioiodtherapie durchgeführt werden.
Entlassung nach der Therapie
[Bearbeiten]In Deutschland beträgt die Mindest-Aufenthaltsdauer auf der Therapiestation 48 Stunden. Die Entlassung hängt von der im Körper verbliebenen Restaktivität ab. 1999 wurde der Grenzwert für die Restaktivität erhöht: die Dosisleistung darf in 2 Meter Abstand vom Patienten 3,5 µSv/h nicht überschreiten, wodurch innerhalb eines Jahres bei einem Abstand von 2 Metern eine Strahlenexposition von 1,0 mSv nicht überschritten wird. Dies entspricht einer Restaktivität von etwa 250 MBq. Ähnliche Regelungen gelten für Österreich. In der Schweiz sind 5 mSv in 1 Meter Abstand zulässig, wodurch eine höhere Restaktivität bei Entlassung möglich ist.
In Deutschland beträgt die mittlere Verweildauer noch etwa drei bis fünf Tage und hängt im Wesentlichen vom Zielvolumen ab. Bei sehr großen Strumen kann die Aufenthaltsdauer auch zehn Tage erreichen.[2]
Bei Entlassung wird der Patient auf eventuell nach Entlassung noch zu beachtende Strahlenschutzmaßnahmen hingewiesen. Diese betreffen insbesondere den Umgang mit kleinen Kindern und Schwangeren. Auf mögliche Probleme mit Radioaktivitätsmessungen – an Flughäfen, Kernkraftwerken, Abfallbeseitigung – ist der Patient hinzuweisen, gegebenenfalls wird dem Patienten eine entsprechende Bescheinigung mitgegeben.
In besonderen Fällen – zum Beispiel eine akute Erkrankung des Patienten, die eine Untersuchung und Behandlung des Patienten außerhalb der Therapiestation notwendig machen – ist in Deutschland eine vorzeitige Entlassung möglich. Diese muss bis zu einer Dosisleistung von 17,5 µSv/h der Aufsichtsbehörde angezeigt werden, ab 17,5 µSv/h muss eine Genehmigung eingeholt werden. Bei Verlegung des Patienten auf eine andere Station muss der zuständige Strahlenschutzbeauftragte dafür sorgen, dass dort geeignete Maßnahmen zum Strahlenschutz ergriffen werden, zum Beispiel vorübergehend ein Kontrollbereich eingerichtet wird.
Nachsorge und Erfolge
[Bearbeiten]In Deutschland ist der Arzt, der die Radioiodtherapie durchgeführt hat, auch für die Nachbetreuung verantwortlich. Es hat der für die Durchführung der Behandlung verantwortliche, fachkundige Arzt die Wirkung und die Nebenwirkungen der nuklearmedizinischen Behandlung durch geeignete, in angemessenen Zeitabständen erfolgende, Nachuntersuchungen zu erfassen und zu dokumentieren; ggf. hat er eine Behandlung einzuleiten. Der Nuklearmediziner kann Teile der Nachsorge an einen fachlich geeigneten Arzt übergeben, der diesem die Ergebnisse der Nachsorge mitzuteilen hat. Das enthebt den Nuklearmediziner aber nicht von seiner Verantwortung für die Nachsorge.[1]
Je nach behandelter Erkrankung der Schilddrüse und Stoffwechsellage beziehungsweise medikamentöser Vorbehandlung werden die ersten Kontrollen der Schilddrüsen-Laborwerte nach vier bis sechs Wochen durchgeführt, beim Morbus Basedow gegebenenfalls auch eher, um die Entwicklung einer Schilddrüsenunterfunktion rechtzeitig zu erkennen. Insbesondere bei vorbestehender endokriner Orbitopathie kann eine Unterfunktion ungünstige Auswirkungen haben und muss daher frühzeitig behandelt werden.
In den meisten Fällen tritt die vollständige Wirkung der Radioiodtherapie in den ersten drei bis sechs Monaten ein, so dass nach diesem Zeitraum eine abschließende Untersuchung zur Beurteilung des Therapieeffektes und -erfolges ansteht. Diese Umfasst üblicherweise neben der Bestimmung der Schilddrüsenhormone auch ein Schilddrüsen-Sonogramm und ein -Szintigramm. Da in einem Teil der Fälle auch nach sechs Monaten noch eine gewisse Spätwirkung der Radioiodtherapie zu erwarten ist, soll die Indikation zu einer Wiederholung der Behandlung nicht zu früh gestellt werden.
Für die verschiedenen Indikationen zur Radioiodtherapie gelten unterschiedliche Therapieziele und Erfolgsquoten. Für die Autonomie der Schilddrüse ist das Ziel die Ausschaltung der autonomen Anteile der Schilddrüse. Es wird bei einer angestrebten Herddosis von 300 bis 400 Gy eine Erfolgsquote von über 90 % angegeben. Etwa 10 % der Patienten müssen wegen einer Schilddrüsenunterfunktion nach der Therapie dauerhaft mit Schilddrüsenhormonen behandelt werden („Substitution“). Bei der fokalen Autonomie kann mit einer Abnahme des Volumens der autonomen Gebiete um etwa 80 % gerechnet werden, Die Abnahme des Volumens der Gesamtschildrüse liegt bei 20 bis 50 %.
Beim Morbus Basedow ist das Ziel die dauerhafte Beseitigung der Überfunktion. Beim ablativen Therapiekonzept mit angestrebter Herddosis von 200 bis 300 Gray liegt die Erfolgsquote bei über 90 %. Allerdings sind anschließend 80 bis 90 % der Patienten dauerhaft von einer Substitution mit Schilddrüsenhormonen abhängig. Beim sogenannten funktionsoptimierten Konzept mit einer angestrebten Herddosis von etwa 150 Gray liegt die Rate an behandlungsbedürftigen Unterfunktionen zwar nur bei 40 %, allerdings die Erfolgsquote auch nur bei etwa 70 %. Insbesondere bei schwierigen Verläufen mit medikamentös nur schwer einstellbarer Überfunktion, Augenbeteiligung (endokrine Orbitopathie) oder wiederholten Rückfällen ist diese niedrige Erfolgsquote nicht akzeptabel, so dass inzwischen überwiegend das ablative Therapiekonzept angewendetet wird. Für das alternative Therapieverfahren zur RIT, die Strumaresektion, ist ebenfalls regelhaft mit einer behandlungsbedürftigen Unterfunktion zu rechnen.
Das Therapieziel bei der Struma ohne Überfunktion ist vor allem eine Verminderung der Schilddrüsengröße und die Beseitigung eventuell durch die Größe verursachter Beschwerden. Bei einem Ausgangsvolumen von 50 bis 100 ml ist mit einer Größenreduktion um etwa die Hälfte zu rechnen, bei sehr großer Struma mit einem Volumen von über 250 ml nur mit einer Reduktion um etwa 30 bis 40 %. In insgesamt über 80 % der Fälle wird eine Besserung der Beschwerden erreicht.
Die Radioiodtherapie bei bösartigen Schilddrüsenerkrankungen
[Bearbeiten]
Grundlagen
[Bearbeiten]Die Karzinome der Schilddrüse, nämlich die häufigsten Untertypen papilläres Karzinom (etwa 70 %) und follikuläres Karzinom (etwa 20 %), und ihre Absiedlungen (Metastasen) haben noch ausgeprägte Ähnlichkeiten mit ihrem Ursprungsgewebe. Zum Einen exprimieren sie den Natrium-Iodid-Symporter und haben daher die Fähigkeit zur Iodspeicherung, zum Anderen produzieren sie Thyreoglobulin, das daher als Tumormarker dienen kann. Schilddrüsenkarzinome werden nicht selten als kalte Knoten auffällig, das heißt die Neigung zur Iodspeicherung ist geringer ausgeprägt als bei gesundem Schilddrüsengewebe. Unter der Stimulation mit hohen Spiegeln von TSH besteht aber auch bei bösartigen Schilddrüsenzellen eine Aufnahme von Iod.
Anwendung
[Bearbeiten]Zu unterscheiden sind die Radioiodtherapie zur Entfernung eventuell vorhandener Reste gesunden Schilddrüsengewebes im Sinne einer unterstützenden und die Nachsorge vereinfachenden (adjuvanten) Therapie von der Behandlung eventuell vorhandener Tumorreste oder -absiedlungen (Metastasen) unter einem Anspruch auf Heilung (kurative Therapie) oder zumindest auf Lebensverlängerung und Linderung der Beschwerden (palliative Therapie).
Eine Indikation zur ablativen Radioiodtherapie besteht bei fast allen Fällen der epithelialen Schilddrüsenkarzinome. Lediglich beim papillären Mikrokarzinom (Größe kleiner als 1 cm, mit der TNM-Klassifikation pT1 N0 M0, kann unter Umständen auf eine ablative RIT verzichtet werden.[7]
Keine Indikation zur Radioiodtherapie besteht meist beim medullären und beim anaplastischen Schilddrüsenkarzinom, da diese Tumoren in der Regel kein Iod speichern. Schwangerschaft und Stillzeit gelten als absolute Kontraindikation.[7]
Vorbereitung
[Bearbeiten]Operation
[Bearbeiten]Vor der Radioiodtherapie beim epithelialen Schilddrüsenkarzinom steht grundsätzlich die Schilddrüsenoperation.Sie wird meist als komplette Schilddrüsenentfernung durchgeführt. Ein kleiner Rest von gutartigem Schilddrüsengewebe verbleibt dabei trotzdem fast immer. Bei operationstechnisch schwierigen Verhältnissen – zum Beispiel bei sehr großer Struma oder voroperierten Patienten – kann dieser Rest auch größer ausfallen, was für die weitere Behandlung der Patienten und ihre Überlebensaussichten aber keinen Nachteil bedeutet. Daher wird nicht empfohlen eine absolut vollständige Entfernung der Schilddrüse anzustreben, um eine Schädigung des hinter der Schilddrüse verlaufenden Nervus laryngeus recurrensmzu vermeiden.
Wenn Tumorreste verblieben sind, bereits Absiedlungen bestehen oder ein lokaler Rückfall ( ein Rezidiv) vorliegt, soll zunächst operativ versucht werden, die Menge an bösartigem Gewebe so weit wie möglich zu reduzieren.
Iodkarenz
[Bearbeiten]Mehr noch als bei der Radioiodtherapie gutartiger Schilddrüsenerkrankungen muss in der Phase vor der RIT des Schilddrüsenkarzinoms darauf geachtet werden, dem Patienten kein zusätzliches Iod zukommen zu lassen.
Stimulation des Schilddrüsengewebes und Iodtest
[Bearbeiten]Um für die ablative Therapie die Aufnahme (uptake) des Radioiods in den Schilddrüsenrest zu erhöhen, beziehungsweise für die kurative oder palliative Therapie überhaupt eine nennenswerte Aufnahme zu erreichen, müssen die verbliebenen Schilddrüsenzellen mit einem hohen Spiegel an TSH stimuliert werden. Der TSH-Wert soll über 30 µU/l liegen[7], normal sind (je nach Labor) etwa 0,4 bis 4 µU/l. Dieser hohe Wert wird üblicherweise dadurch erreicht, dass der Patient zunächst nach der Operation nicht mit Schilddrüsenhormonen behandelt, wie es sonst nach einer vollständigen (Thyreoidektomie) oder weitgehenden Schilddrüsenentfernung (subtotale Strumaresektion) bei gutartigen Schilddrüsenerkrankungen üblich ist. Etwa drei bis vier Wochen nach der Operation befindet sich der Patient dann in einer Schilddrüsenunterfunktion (Hypothyreose). Häufig besteht durch die Unterfunktion eine Arbeitsunfähigkeit und die Patienten sind darauf hinzuweisen, in dieser Phase wegen der verminderten Reaktionsfähigkeit kein Kraftfahrzeug zu führen und keine gefährlichen Maschinen zu steuern.
Vor der ablativen Radioiodtherapie soll ein (verkürzter) Radioiodtest von 24 Stunden durchgeführt werden. Bei einem hohen uptake wird die Therapie mit verminderter Aktivität durchgeführt, bei sehr hohem uptake ist eine Zweitoperation zur Verminderung des Schilddrüsengewebes zu erwägen.
Als Alternative zur Unterfunktion steht seit einigen Jahren gentechnisch hergestelltes, rekombinantes, humanes TSH (rhTSH) zur Verfügung, das intramuskulär gegeben werden kann und mit dem sich durch Injektionen an zwei aufeinander folgenden Tagen TSH-Spiegel am dritten und vierten Tag von meist deutlich über 30 µU/l erreichen lassen.
Als mögliche Vorteile der Anwendung von rhTSH gegenüber der Hypothyreose können gelten: besseres Allgemeinbefinden; erhaltene Arbeitsfähigkeit; Fehlen eines anhaltenden Wachstumsreizes auf eventuell noch vorhandene Krebszellen durch mehrwöchig erhöhtes TSH; niedrigere Konzentration des 131Iod im Serum und damit geringere Strahlenexposition. Die Erfolgsraten der ablativen Radioiodtherapie sind in Unterfunktion und mit rhTSH gleich hoch.[7]
Als mögliche Nachteile sind zu erwähnen: deutlich verkürzte effektive Halbwertszeit, erhöhte Mengen an nicht-radioaktivem Iod im Körper des Patienten durch die fortgesetzte Gabe der (iodhaltigen) Schilddrüsenhormone; fehlender Nachweis einer Gleichwertigkeit bei der Behandlung von Metastasen; fehlende Möglichkeit, an eine Diagnostik mit Radioiod eine Therapie anzuschließen, da der TSH-Spiegel innerhalb von wenigen Tagen wieder abfällt; hohe Kosten.
Durchführung
[Bearbeiten]Die Standardaktivität für die ablative Radioiodtherapie beträgt 3,7 GBq. Wenn nach der Operation und vor der ersten (ablativen) Radioiodtherapie nennenswerte Reste von Schilddrüsengewebe verblieben sind, wird üblicherweise eine geringere Aktivität von 1,1 bis 1,85 GBq (entsprechend 30 bis 50 mCi) eingesetzt, um eine strahlenbedingte Entzündung benachbarter Gewebe zu vermeiden.
Wenn – auch nach Ausschöpfen der operativen Möglichkeiten – noch anzunehmen ist dass bösartiges Gewebe im Körper des Patienten verblieben ist, also ein Resttumor, ein Lokalrezidiv oder Metastasen vorliegen, werden höhere Aktivitäten angewendet. Diese liegen meist im Bereich von 3,7 bis 11,1 GBq, in Einzelfällen auch deutlich darüber.
Nach der Therapie wird ein Ganzkörperszintigramm angefertigt. Die Therapie wird in etwa dreimonatigen Abständen wiederholt, bis weder das Szintigramm, das Ultraschallbild der Halsregion, noch der Tumormarker Thyreoglobulin einen Hinweis auf verbliebenes Schilddrüsengewebe (gutartig oder bösartig) geben. Eine Gesamt-Aktivität über alle durchgeführten Radioiodbehandlungen von bis zu 74 GBq wird bei sonst gesunden Patienten meist problemlos vertragen. Darüber ist mit einem erhöten Risiko für eine dauerhafte Schädigung des Knochenmarks als blutbildendes Organ zu rechnen.
Bezüglich der Entlassung nach der Therapie gelten die gleichen Fristen und Grenzwerte, wie bei der Therapie gutartiger Schilddrüsenerkrankungen.
Risiken und Nebenwirkungen
[Bearbeiten]Bei den unerwünschten Effekten der Radioiodtherapie sind die kurzfristig und akut auftretenden von den langfristig und chronisch auftretenden Nebenwirkungen zu unterscheiden und ihre jeweiligen Häufigkeiten und Tragweiten zu beachten.
Im Vergleich zur Therapie gutartiger Schilddrüsenerkrankungen werden beim Schilddrüsen-Karzinom zum Teil wesentlich höhere Aktivitäten eingesetzt. Mit der erwünschten höheren Strahlendosis im Zielgewebe sind damit auch höhere Strahlendosen in anderen Geweben verbunden.
Relativ häufig treten während der Therapie Appetitverlust, Veränderung der Geschmacksempfindung, Übelkeit und Speicheldrüsenreizung auf; selten finden sich Nackenschmerz oder - schwellung, Kopfschmerz oder vorübergehende Veränderungen des Blutbildes.[8]
Schwerwiegende Langzeitauswirkungen sind selten und betreffen meist Speichel- und Tränendrüsen (vor allem verminderte Tränen- bzw Speichelproduktion), Knochenmar] (sehr selten bei Patienten >45 Jahren Knochenmarksdepression oder myeloische Leukämie), Lungen (sehr selten strahleninduzierte Lungenentzündung, besonders Verschlechterung bei vorbestehender Pneumonie, bzw. Neuauftreten bei diffusen Lungenmetastasen) und Ovarien (vorübergehend fehlender Eisprung, gering erhöhte Mißbildungsrate bei Schwangerschaft innerhalb des ersten Jahres nach Therapie) bzw. Hoden (Azoospermie] - selten dauerhaft).[9] Der Nutzen der Radioiodtherapie übersteigt die Nebenwirkungsrate um das 4 - 40 fache. Die zu erwartende Inzidenz von Zweitkarzinomen oder Leukämie ist dosisabhängig. Eine minimale Zunahme von Zweitkarzinomen fand sich in den Organen (Speicheldrüsen, Dickdarm und Blase), in denen sich während der Therapie vorübergehend auch Iod123 in nennenswerter Menge ansammelt.[8] In einer englischen Studie an 7417 Patienten zeigte sich eine statistisch signifikante Abnahme des Auftretens von Krebs der Luftwege (Bronchien und Luftröhre).[8]
Nachsorge: Radioioddiagnostik
[Bearbeiten]Erst nach vollständiger Entfernung des nach der Operation verbliebenen Restes (Ablation) ist Thyreoglobulin als Tumormarker zu verwenden.
Geschichte
[Bearbeiten]Im Vorfeld des Einsatzes der Radioiodtherapie wurde beim Schilddrüsenkarzinom postoperativ eine Nachbestrahlung (mit Röntgenstrahlen) allgemein eingesetzt und als effektiv angesehen.
Smith A.M.: Virginia M. Monthly, 69:318-324. 1942; zuletzt eingesehen am 10. März 2008
Leddy, E. T. [Mayo Clinic, Rochester, Minn. M. Clin. North Amerika, 25:973-1009. 1941; zuletzt eingesehen am 10. März 2008]
Die Diagnose des Schilddrüsenkarzinoms bereitete jedoch noch Mitte des letzten Jahrhunderts große Probleme,
[http://cancerres.aacrjournals.org/cgi/reprint/3/5/344.pdf Bonne, C.: Over Maligne Schildkliergezwellen, (Malignant tumors of the thyroid), South African M, J., 15:1477-152, 1941; zuletzt eingesehen am 10. März 2008
sodass Begriffsüberschneidungen in der Literatur dieser Zeit wahrscheinlich sind.
1939 und 1940 veröffentlichte Joseph G. Hamilton Arbeiten über den Iodmetabolismus der Schilddrüse, wobei er radioaktives Iod bei gesunden Probanden und solchen mit Strumen unterschiedlicher Ursache einsetzte.
- Joseph G. Hamilton and Mayo H. Soley: Studies in iodine metabolism of the thyroid gland in situ by the use of radio-iodine in normal subjects and in patients with various types of goiter, Am J Physiol -- Legacy Content, Oct 1940; 131: 135 - 143.
- Joseph G. Hamilton and Mayo H. Soley: Studies in iodine metabolism by the use of a new radioactive isotope of iodine, Am J Physiol -- Legacy Content, Sep 1939; 127: 557 - 572.
Bereits in den Vorjahren hatte er zur Wirkung von Radioaktivität auf den menschlichen Körper geforscht.
- Joseph G. Hamilton and Gordon A. Alles: The physiological action of natural and artificial radioactivity, Am J Physiol -- Legacy Content, Jan 1939; 125: 410 - 413.
- Joseph G. Hamilton: The rates of absorption of the radioactive isotopes of sodium, potassium, chlorine, bromine, and iodine in normal human subjects, Am J Physiol -- Legacy Content, Nov 1938; 124: 667 - 678.
1942 wendeten S. Hertz und A. Roberts erstmals die Radioiodtherapie beim Morbus Basedow an.
- Hertz, S., Roberts, A.: Application of radioactive iodine in therapy of Grave´s disease, J div 21 (624) (1942) zuletzt eingesehen am 10. März 2008
Im selben Jahr beschrieben A.S. Keston e.a. in einer Kasuistik die aus therapeutischen und diagnostischen Zwecken durchgeführte Anwendung radioaktiven Iodes bei einer im Oberschenkelknochen sitzenden Metastase eines Schilddrüsenkarzinoms, das auf die damals übliche Therapie mit Röntgenstrahlen nicht angesprochen hatte.
Eine andere Kasuistik aus dem Jahr 1942 zeigt, dass es sich dabei noch keineswegs um ein Routinevorgehen beim Schilddrüsenkarzinom handelte.
Noch 1949 veröffentlichte Henry A. Sloviter ein Tierexperiment, in dem er die lebensverlängernde Wirkung von Iod131 beim Schilddrüsenkarzinom darstellte.
Als Erfinder der Radioiodtherapie gilt Joseph Hamilton, Neurologe aus Berkeley. Während des Manhattan-Projekts untersuchte Hamilton die Wirkung der Falloutprodukte auf den Menschen. Die erste Anwendung von 131I beim Menschen führte er 1942 durch.
Literatur und Quellen
[Bearbeiten]- F. Grünwald, C. Menzel. Radioiodtherapie. In: T. Kuwert, F. Grünwald, U. Haberkorn, T. Krause. Nuklearmedizin. Stuttgart, New York 2008 ISBN 978-3-13-118504-4
- Leitlinie der Deutschen Gesellschaft für Nuklearmedizin (DGN): Radioiodtherapie (RIT) bei benignen Schilddrüsenerkrankungen online
- Leitlinie der DGN: Verfahrensanweisung zur Radioiodtherapie (RIT) beim differenzierten Schilddrüsenkarzinom online
- Bell, Eberhard; Grünwald, Frank:
- Radiojodtherapie.Bei benignen und malignen Schilddrüsenerkrankungen. 1999. X, 142 S. m. 51 z.
- Tl. farb. Abb. 24 cm. Gebunden. 412gr. ISBN 3-540-65913-7, -SPRINGER, BERLIN-49.95 EUR
- Radiojodtherapie.Bei benignen und malignen Schilddrüsenerkrankungen. 1999. X, 142 S. m. 51 z.
Einzelnachweise
[Bearbeiten]Einzelnachweise [Bearbeiten]↑ a b c d e f g h i j k l F. Grünwald, C. Menzel. Radioiodtherapie. In: T. Kuwert, F. Grünwald, U. Haberkorn, T. Krause. Nuklearmedizin. Stuttgart, New York 2008 ISBN 978-3-13-118504-4 ↑ a b Richtlinie "Strahlenschutz in der Medizin" (zur StrlSchV) PDF (1,74 MB) ↑ Leitlinie der Deutschen Gesellschaft für Nuklearmedizin (DGN): Radioiodtherapie (RIT) bei benignen Schilddrüsenerkrankungen ↑ Marinelli LD, Quinby EH, Hine GJ. Dosage determination with radioactive isotopes. Practical considerations in therapy and protection. Am J Röntgenol 1948; 59:260 - 81 ↑ a b Robertson IS. Dosimetry of radionuclides. In: Falk S (Hrsg.). Thyroid disease. New York: Raven 1997. Zitiert nach: F. Grünwald, C. Menzel. Radioiodtherapie. In: T. Kuwert, F. Grünwald, U. Haberkorn, T. Krause. Nuklearmedizin. Stuttgart, New York 2008 ISBN 978-3-13-118504-4 ↑ Hall P, Boice JD Jr, Berg G, Bjelkengren G, Ericsson UB, Hallquist A, Lidberg M, Lundell G, Mattsson A, Tennvall J, et al. Leukaemia incidence after iodine-131 exposure. Lancet. 1992 Jul 4;340(8810):1-4. PMID 1351599 ↑ Ron E, Doody MM, Becker DV, Brill AB, Curtis RE, Goldman MB, Harris BS 3rd, Hoffman DA, McConahey WM, Maxon HR, Preston-Martin S, Warshauer ME, Wong FL, Boice JD Jr. Cancer mortality following treatment for adult hyperthyroidism. Cooperative Thyrotoxicosis Therapy Follow-up Study Group. JAMA. 1998 Jul 22-29;280(4):347-55. PMID 9686552 ↑ Homepage der American Thyroid Association; zuletzt eingesehen am 13. März 2008 ↑ a b c d Verfahrensanweisung zur Radioiodtherapie (RIT) beim differenzierten Schilddrüsenkarzinom ↑ a b c Chow S.M.: Side effects of high-dose radioactive iodine for ablation or treatment of differenciated thyroidcarcinoma, Hong Kong College Radiologist, 2005, (:127 - 135; zuletzt eingesehen am 13. März 2008 ↑ Handelman D.J., e.a.: Azoospermia after iodine-131 treatment for thyroid carcinoma, British Medical Journal, 1980, 281:1527; zuletzt eingesehen am 13. März 2008 ↑ Smith A.M.: Virginia M. Monthly, 69:318-324. 1942; zuletzt eingesehen am 10. März 2008 ↑ Leddy, E. T. [Mayo Clinic, Rochester, Minn. M. Clin. North Amerika, 25:973-1009. 1941; zuletzt eingesehen am 10. März 2008] ↑ Bonne, C.: Over Maligne Schildkliergezwellen, (Malignant tumors of the thyroid), South African M, J., 15:1477-152, 1941; zuletzt eingesehen am 10. März 2008 ↑ Joseph G. Hamilton and Mayo H. Soley: Studies in iodine metabolism of the thyroid gland in situ by the use of radio-iodine in normal subjects and in patients with various types of goiter, Am J Physiol -- Legacy Content, Oct 1940; 131: 135 - 143. ↑ Joseph G. Hamilton and Mayo H. Soley: Studies in iodine metabolism by the use of a new radioactive isotope of iodine, Am J Physiol -- Legacy Content, Sep 1939; 127: 557 - 572. ↑ Joseph G. Hamilton and Gordon A. Alles: The physiological action of natural and artificial radioactivity, Am J Physiol -- Legacy Content, Jan 1939; 125: 410 - 413. ↑ Joseph G. Hamilton: The rates of absorption of the radioactive isotopes of sodium, potassium, chlorine, bromine, and iodine in normal human subjects, Am J Physiol -- Legacy Content, Nov 1938; 124: 667 - 678. ↑ Hertz, S., Roberts, A.: Application of radioactive iodine in therapy of Grave´s disease, J div 21 (624) (1942) zuletzt eingesehen am 10. März 2008 ↑ Paschke, R. e.a.: Therapie der uni- oder multifokalen Schilddrüsenautonomie, Dtsch Arztebl 2000; zuletzt eingesehen am 10. März 2008 ↑ Keston, A. S., Ball, R. P., Frantz, V. X., and Palmer, W. W.: Storage of radioactive iodine in a metastasis from thyroid carcinoma. Science, 95:362-363. 1942; zuletzt eingesehen am 10. März 2008 ↑ Wikle, H. T., and Ritzmann, A. J.: The course of carcinoma of the thyroid gland. Report of an unusual case. Am.JL SurE., 5 6 : 507-512, 1942; zuletzt eingesehen am 10. März 2008 ↑ Sloviter H.A.: The distribution and action of a radioactive oxaxine dye in tumor-bearing mice, Cancer Research, 9:677-80, 1949; zuletzt eingesehen am 10. März 2008
Weblinks
[Bearbeiten]- Suchmaske der DGN für Radioiodtherapiezentren in Deutschland
- Informationsseite der Uni-Klinik Hamburg
- Informationsseite des Therapiezentrums für Schilddrüsenerkrankungen
- Informationsseite der Uniklinik Würzburg
- Informationsseite der TU München
- Informationsseite der Uniklinik Düsseldorf
- http://www1.us.elsevierhealth.com/THB/chapter_M016.php
Liste der selten gebrauchten Schilddrüsenwirkstoffe
[Bearbeiten]T3-Monopräparate
[Bearbeiten]- Thybon
- Trijodthyronin
Auch nach einer kompletten Entfernung der Schilddrüse reicht die Dejodase in den Organen außerhalb der Schilddrüse völlig aus, um genügend T3 aus dem T4 zu bilden. Somit ist eine alleinige T4 Therapie völlig ausreichend und für eine T3 Therapie ergibt sich nur in den seltensten Fällen eine echte Indikation.
T3-/T4-Kombinationspräparate
[Bearbeiten]- Novothyral (Verhältnis 1 : 5)
- Prothyrid (Verhältnis 1 : 10)
- Thyreotom (Verhältnis 1 : 4)
- Thyroxin-T3 Henning (Verhältnis 1 : 5)
Jod-/T4-Kombinationspräparate
[Bearbeiten]- Eferox Jod (100 µg Jod / 100 µg T4)
- Jodthyrox (100µg Jod / 100 µg T4)
- L-Thyrox Jod (150 µg Jod / T4 variabel)
- Thyreocomb (115 µg Jod / 70 µg T4)
- Thyronajod (150 µg Jod / T4 variabel)
Natürliche SD-Hormonpräparate (Schweinethyroxin)
[Bearbeiten](Von Schulmediziner nicht empfohlen !)
- Armour Thyroid (Forest Pharmaceuticals)
- Nature Thyroid (Western Research Labs)
- Westthyroid (Western Research Labs)
- ....
Liste der unwirksamen Schilddrüsenwirkstoffe
[Bearbeiten]Pflanzliche Thyreostatika
[Bearbeiten]Achtung, Von Schulmediziner nicht empfohlen !
- Lycoaktin (Steigerwald)
- Mutellon (Klein)
- Prothyrysat (Bürger, Ysatfabrik)
- Thyreogutt (Schwabe, Willmar)
- Thyreo-loges (Dr. Loges)
Homöopathische Mittel
[Bearbeiten]Achtung, Von Schulmediziner nicht empfohlen, da unwirksam !
- Hewethyreon (Hevert)
- Presselin Thyro plus (Combustin)
- Strumeel (Heel)
- Thyreoidinum (DHU)
- Thyreoidea comp (Wala)
- Thyreo Pasc N (Pascoe)
- Thyreo EM (Kairos Remedia)
- Thyreo Gastreu (Reckeweg)
- Thyreo Cyl (Liebermann)
Referenzen
[Bearbeiten]Pathologie der Schilddrüse
[Bearbeiten]{{:Pathologie:_Schilddr%C3%BCse}}
Fallbeschreibungen von Schilddrüsenkrankheiten
[Bearbeiten]
Siehe auch
[Bearbeiten]Prominente
[Bearbeiten]Barbara Bush March 30, 1989
[Bearbeiten]Barbara Bush, die Frau des 41. US-Präsidenten, George H. W. Bush und Mutter des 43. US-Präsidenten, George W. Bush, wurde durch einen Gewichtsverlust und Augensymptome auf ihre Schilddrüsenüberfunktion aufmerksam. Ursache der Überfunktion war eine Autoimmunthyreoiditis vom Typ Basedow ( engl . Graves' Disease )
Sie wurde mit Methimazol ( = Thiamazol) behandelt.
George H. W. Bush May 4, 1991
[Bearbeiten]Wie seine Eehfrau entwickelte er einen Basedow und eine Überfunktion. Symptomatisch wurde er durch ein rezidivierendes Vorhofflimmern. Weitere Symptome waren :
- Müdigkeit
- Gewichtsveerlust
- Verschlechterung seiner Handschrift wegen eines feinschlägigen Tremors.
Im Gegensatz zu seiner Ehefrau wurde er mit Radioiod behandelt. Zusätzlich erhielt er 10 Tage lang Kaliumiodid um eine thyreotoxische Krise zu verhindern.
Innerhalb einiger Monate war die Überfunktion beseitigt. Es stellte sich ein Unterfunktion ein, die durch eine lebenslange Gabe von T4 Tabletten behandelt wurde.
Angeblich soll auch der Hund der Bushs einen Basedow gehabt haben. Deswegen wurden das Trinkwasser der Präsidentenfamilie vom FBI auf Iod und Lithium untersucht.
Siehe http://www.doctorzebra.com/prez/g41.htm
Suche
[Bearbeiten]- Pubmedsuche: http://www.ncbi.nlm.nih.gov/sites/entrez
- Stichwort: case report thyroid gland
Links
[Bearbeiten]- http://www.schilddruese.net/medien/muenchen_2004.pdf
- http://www.thieme-connect.com/ejournals/abstract/dmw/doi/10.1055/s-2001-17885;jsessionid=9805EB0F96A3A224AF6DFA1DACD4A711.jvm3
- Hyperthyreose, bei normaler Schilddrüse
- http://www.schilddruesenerkrankungen.at/site/de/Informationen/Schilddruesenbibliographie/Fallberichte/content.shtml
- Sammlung von Fallberichten
- http://www.sd-krebs.de/index.htm?http://www.sd-krebs.de/phpBB2/ftopic8822.html
- Fallberichte SD-Krebs
- http://www.tagesspiegel.de/zeitung/Sonderthemen;art893,2571490
- Fallbericht einer Schilddrüsenoperation
- http://www.tagesspiegel.de/zeitung/Sonderthemen;art893,2571475
- Fallbericht Radiojodtherapie
- http://www.tagesspiegel.de/zeitung/Sonderthemen;art893,2571415
- http://www.tagesspiegel.de/zeitung/Sonderthemen;art893,2571468
- Schilddrüsenoperation ohen Schnitt am Hals , Fallbericht , Minimal Invasiv
- http://thyroid.blogspot.com/
- Eindrucksvolle und lehrreiche Fallberichte in Englisch
Die Schilddrüse und das Herz
[Bearbeiten]
Die Schilddrüse und das Herz
Einleitung
[Bearbeiten]Das Schilddrüsenhormon T3 wirkt an einer Reihe von Zielstrukturen im Herzen und den Gefäßen. Es greift direkt im Zellkern der verschiedenen Zellarten an und aktiviert oder bremst eine Reihe von Proteinen. Ob eine indirekte Wirkung durch Potenzierung der Katecholamine Adrenalin und Noradrenalin auch noch vorhanden ist, ist in der Diskussion.
Molekulare Wirkung von T3 am Herzen
[Bearbeiten]Direkte Wirkung an der Herzmuskelzelle
[Bearbeiten]Trijodthyronin (T3) bindet an Rezeptoren des Zellkerns. Ein spezifisches Gen wird exprimiert. Der T3 Rezeptor ist im Zellkern an ein spezifisches T3 Response Element gebunden. Das Response Element besteht aus einer einzelnen Peptidkette.
schnelle nicht-nukleäre Wirkung
[Bearbeiten]T3 wirkt innerhalb von Minuten auf Ionenkanäle und Ionenpumpaktivität der Herzmuskelzelle. Ob dies eine echte physiologische Bedeutung hat ist bislang unklar.
Indirekte Wirkung über das adrenerge Nervensystem und über eine Adrenalin Sensibilisierung
[Bearbeiten]Herzkreislaufeffekte der Schilddrüsenhormone
[Bearbeiten]- Zunahme
- der Herzfrequenz
- des systolischen Blutdrucks
- des Herzminutenvolumens
- der Herzmuskelkraft
- des Sauerstoffverbrauches des Herzens
- Abnahme
- des diastolischen Blutdrucks
- des Gefäßwiderstandes des großen Kreislaufs
- der Dauer der Erregungsleitung im Herzen
Mögliche Folgen bei Schilddrüsenüberfunktion
[Bearbeiten]Es kann bei einer Schilddrüsenüberfunktion zu
- einer Tachykardie
- zu Vorhofflimmern
- zur Extrasystolie
- zu vermehrtem Herzklopfen
- zu Luftnot bei Belastung
- zu einem erhöhten systolischen Blutdruck
kommen
Mögliche Folgen bei Unterfunktion
[Bearbeiten]Ausgeprägte Herz- und Kreislaufeinflüsse der Hypothyreose waren früher viel häufiger zu finden, da die Diagnose und Therapie schwierig war als heute und es zu weit schwereren Verläufen der Krankheit kam. Die Auswirkungen der Unterfunktion sind meist auch weniger dramatisch als bei der Überfunktion.
Es kann bei einer Schilddrüsenunterfunktion am Herzen zu
- einer Bradykardie
- einer linksventrikuläre systolische und diastolische Dysfunktion ( Muskelschwäche des Herzens)
- einem Perikarderguß
- einer Veränderung des Blutvolumens
- einer Erhöhung des Blutdrucks und des systemischen Gefäßwiderstands
- zu einer Erhöhung des Cholesterins und Beschleunigung der KHK
kommen.
EKG
[Bearbeiten]Hypothyreose
[Bearbeiten]Bei einer Hypothyreose findet sich eine Verbreiterung des QRS-Komplexes und eine Verlängerung der QT Zeit. Dies gefährdet das Herz für lebensbedrohliche Rhythmusstörungen wie Kammertachykardie, Kammerflattern und Torsade de pointes. Endstreckenveränderungen mit spitz negativen T Wellen können eine Myokardischämie vortäuschen.
Hyperthyreose
[Bearbeiten]Literatur
[Bearbeiten]- Klein I, Ojamaa K.
- Thyroid hormone and the cardiovascular system.
- N Engl J Med. 2001 Feb 15;344(7):501-9. Review.
- PMID: 11172193
- Thyroid hormone and the cardiovascular system.
- Iervasi G et al.:
- Association between increased mortality and mild thyroid dysfunction in cardiac patients.
- Arch Intern Med 2007; 167: 1526-1532.
- Association between increased mortality and mild thyroid dysfunction in cardiac patients.
- Ojamaa K, Klemperer DJ, Klein I.
- Acute effects of thyroid hormone on vascular smooth muscle.
- Thyroid 1996; 6: 505–12.
- Acute effects of thyroid hormone on vascular smooth muscle.
- Ojamaa K, Kenessey A, Klein I.
- Thyroid hormone regulation of phospholamban phosphorylation in the rat heart.
- Endocrinology 2000; 141: 2139–44.
- Thyroid hormone regulation of phospholamban phosphorylation in the rat heart.
- Morkin E.
- Regulation of myosin heavy genes in the heart.
- Circulation 1993; 87: 68–73.
- Regulation of myosin heavy genes in the heart.
- Kahaly GJ, Nieswandt J, Wagner S, Schlegel J, Mohr-Kahaly S,Hommel G.
- Ineffective cardiorespiratory function in hyperthyroidism.
- J Clin Endocrinol Metab 1998; 98: 4075–8.
- Ineffective cardiorespiratory function in hyperthyroidism.
- Sawin CT, Geller A, Wolf PA, Belanger AJ, Baker E, Bacharach P, Wilson PWF, Benjamin EJ, D’Agostino RB.
- Low serum thyrotropin concentrations as a risk factor for atrial fibrillation in older persons.
- N Engl J Med 1993; 331: 1249–52.
- Low serum thyrotropin concentrations as a risk factor for atrial fibrillation in older persons.
- Krahn AD, Klein GJ, Kerr CR.
- How useful is thyroid function testing in patients with recent-onset atrial fibrillation.
- Arch Intern Med 1996; 156: 2221–4.
- How useful is thyroid function testing in patients with recent-onset atrial fibrillation.
- Ladenson PW.
- Thyrotoxicosis and the heart: something old and something new.
- J Clin Endocrinol Metab 1993; 77: 332–3.
- Thyrotoxicosis and the heart: something old and something new.
- Fatourechi V, Edwards WD.
- Graves’ disease and low output cardiac dysfunction: implications for autoimmune disease in endomyocardial biopsy tissue from eleven patients.
- Thyroid 2000; 10: 601–5.
- Graves’ disease and low output cardiac dysfunction: implications for autoimmune disease in endomyocardial biopsy tissue from eleven patients.
- Peters A, Ehlers M, Blank B, Exler D, Falk C, Kohlmann T, Fruehwald- Schultes B, Wellhoener P, Kerner W, Fehm HL.
- Excess triiodothyronine as a risk factor of coronary events.
- Arch Intern Med 2000; 160: 1993–9.
- Excess triiodothyronine as a risk factor of coronary events.
- Gallowitsch, H.J.:
- Thyroid and cardiovascular system.
- Wien Med Wochenschr. 2005; 155: 436–443.
- Thyroid and cardiovascular system.
- Dorr, M.; Volzke, H.:
- Cardiovascular morbidity and mortality in thyroid dysfunction.
- Minerva Endocrinol. 2005; 30: 199–216
- Cardiovascular morbidity and mortality in thyroid dysfunction.
- Iqbal, A.; Figenschau, Y.; Jorde, R.:
- Blood pressure in relation to serum thyrotropin: The Tromso study.
- J Hum Hypertens. 2006; 20: 932–966.
- Blood pressure in relation to serum thyrotropin: The Tromso study.
- Razvi, S.; Ingoe, L.; Keeka, G.; Oates, C.; McMillan, C.; Weaver, J.U.:
- The beneficial effect of L-thyroxine on cardiovascular risk factors, endothelial function and quality of life in subclinical hypothyroidism: randomised, crossover trial .
- J Clin Endocrinol Metab. 2007; 13 Epub ahead of print
- The beneficial effect of L-thyroxine on cardiovascular risk factors, endothelial function and quality of life in subclinical hypothyroidism: randomised, crossover trial .
- Woeber KA. Thyrotoxicosis and the heart. N Engl J Med 1992; 327: 94
Historisch
[Bearbeiten]- Parry CH.
- Enlargement of the thyroid gland in connection with palpitation of the heart.
- Collections from the unpublished papers of the late Caleb Hilliel Parry. Dis Heart 1825; 2: 111.
- Enlargement of the thyroid gland in connection with palpitation of the heart.
- Ginsberg AM.
- The historical development of the present conception of cardiac conditions in exophthalmic goiter.
- Ann Intern Med 1931; 5: 505–17.
- The historical development of the present conception of cardiac conditions in exophthalmic goiter.
- Rowe GG, Huson JH, Weinstein AB, Tuchman H, Brown JF, Crumpton CW.
- The hemodynamics of thyrotoxicosis in man with special reference to coronary blood flow and myocardial oxygen metabolism.
- J Clin Invest 1956; 35: 272–6.
- The hemodynamics of thyrotoxicosis in man with special reference to coronary blood flow and myocardial oxygen metabolism.
Links
[Bearbeiten]- http://www.kup.at/kup/pdf/1030.pdf
- http://www.forum-schilddruese.de/bauteile/texte/fs_fachinfo_herz_im_alter.rtf
- http://www.hormon.org/schilddruese-funktion/Hypothyreose-Herz.pdf
Schildrüse, Schwangerschaft, Frauen
[Bearbeiten]
Schwangerschaft und Schilddrüse
[Bearbeiten]Frauen und Schilddrüse
[Bearbeiten]Auffällig ist die 3 - 4 fach höhere Krankheitshäufigkeit bei Frauen gegenüber den Männern bei fast allen Schilddrüsenkrankheiten, nicht nur bei den Jodmangelerkrankungen.
Literatur
[Bearbeiten]- http://www.diss.fu-berlin.de/diss/receive/FUDISS_thesis_000000002217
- Monitoring der Urinjodausscheidung Neugeborener als Kriterium für die Wirksamkeit der Jodmangelprophylaxe
- von Eike, Esther
- Monitoring der Urinjodausscheidung Neugeborener als Kriterium für die Wirksamkeit der Jodmangelprophylaxe
Zitat
Die Medianwerte der Urinjodausscheidungen Berliner Neugeborener haben sich vervierfacht: 1991 30,0 µg/l und 2004 123,6 µg/l, im Stadtbezirk Berlin-Lichtenberg zum Vergleich 1991 35,9 µg/l und 2004 130,8 µg/l. Die Hälfte der Neugeborenen zeigten 2004 eine optimale Jodausscheidung (Berlin: 45,5%, Berlin-Lichtenberg 56,2%). In der Auswertung auffallend ist der Anteil der Jodausscheidungs-konzentrationen über 200 µg/l, im Jahr 2001 mit 23% und im Jahr 2004 mit 22%.
Die SD und jodhaltige Kontrastmittel
[Bearbeiten]
Wenn eine Gabe von jodhaltigem Kontrastmittel bei Schilddrüsenpatienten notwendig ist, sollte der aktuelle TSH Spiegel bestimmt werden. Probleme bietet der Jodanteil des Kontrastmittel vor allem bei Überfunktion der Schilddrüse.
Eine medikamentöse Vorbeugung kann das Risiko einer Iodinduzierten Hyperthyreose (IIH) nur vermindern, nicht beseitigen. Es sind daher klinische und laborchemische Kontrolluntersuchungen im weiteren Verlauf zb nach 1- 3 Monaten empfehlenswert.
Die Empfehlungen gelten nur für die Anwendung wasserlöslicher Röntgenkontrastmittel. Gallegängige Röntgenkontrastmittel sollten bei Risikopatienten grundsätzlich nicht eingesetzt werden.
Diese Aussage gilt nicht für die KM-Applikation bei der ERCP.
Vorgehen bei latenter Hyperthyreose
[Bearbeiten]- 3 x 20 Tropfen (= 900 mg) Perchlorat/Tag
- zusätzlich fakultativ (bei hohem Risiko) 20 mg Thiamazol/Tag
- Beginn der Therapie: spätestens 2–4 h vor Kontrastmittelapplikation
- Dauer der Therapie: 14 Tage
Vorgehen bei unklarem Schildrüsenfunktionszustand
[Bearbeiten]- Ultraschall der Schilddrüse
- Abnahme von TSH, T3,T4
- je nach Ergebnis Therapie mit Irenat und/oder Thiamazol
Vorgehen bei manifester Hyperthyreose
[Bearbeiten]- 3 x 20 Tropfen Perchlorat/Tag
- zusätzlich 20 mg Thiamazol/Tag
- maximal 80 mg Thiamazol/ Tag
- Beginn der Therapie: spätestens 2–4 h vor Kontrastmittelapplikation
- Dauer der Therapie:
- Perchlorat mindestens 14 Tage,
- Thiamazol in angepasster Dosis weiterführen
Literatur
[Bearbeiten]- Die jodinduzierte Hyperthyreose nach Röntgenkontrastmitteln. Tierexperimentelle und klinische Untersuchung.
- 200 Seiten ISBN-10: 3137154014 ISBN-13: 978-3137154013
Links
[Bearbeiten]- http://www.schilddruesenerkrankungen.at/site/de/Informationen/Jodgehalt_in_Medikamenten/Roentgenkontrastmittel/content.shtml
- http://aerzteblatt.lnsdata.de/pdf/98/7/a402.pdf
- Gute und ausführliche Zusammenfassung zum Thema
Die SD und Amiodaron
[Bearbeiten]
Die Schilddrüse und Amiodaron
Einleitung
[Bearbeiten]Amiodaron ist ein Medikament zur Behandlung von Herzrhythmusstörungen. Es besitzt eine dem Thyroxin (T4) verwandte chemische Struktur. Es enthält mit 37 % Gewichtsanteilen sehr viel Jod. Bei einer üblichen täglichen Erhaltungsdosis von 200 mg Amiodaron werden durch Dejodierung täglich etwa 7 mg Jodid freigesetzt. Der Tagesbedarf an Jodid ist demgegenüber mit 150 – 200 mikrog viel niedriger, d.h durch den Stoff entsteht ein ausgeprägter Jodüberschuß. Gleichzeitig ist die Abbaurate des Amiodarons mit einer Halbwertszeit von 40 – 60 Tage sehr lang.
Amiodaron enthält nicht nur viel Jod, es ist auch mit den Schilddrüsenhormonen strukturverwandt.
Unter Amiodaron kommt es häufig ( circa 40 % der Fälle) zu Veränderungen der Schilddrüsenhormonparameter kommen, die oft vom betroffenen Patienten gar nicht bemerkt werden.
Diese Veränderungen an der Schilddrüse werden
- durch den hohen Jodgehalt oder
- durch immunbedingte zytotoxische Effekte ( zytotoxisch = Zellzerstörend)
verursacht.
In der Peripherie führt Amiodaron zu einer
- Hemmung der Deiodase, d.h T4 wird weniger in T3 umgewandelt
- Hemmung der Schilddrüsenhormonrezeptoren.
Eine Radiojodtherapie kann man unter Amiodaron bis zu einem Jahr nach Absetzen des Medikamentes nicht durchführen, da das Radiojod nicht in die Schilddrüse aufgenommen wird.
Voruntersuchung
[Bearbeiten]- Vor Einleitung einer Amiodarontherapie sollten folgende Untersuchungen durchgeführt werden
- TSH basal
- FT3 und FT4
- TPO-AK
- TRAK
- Sonographie der Schilddrüse
- Bei Knoten > 1 cm SD-Szintigramm
Verlaufskontrolle
[Bearbeiten]- TSH basal alle 6 Monate
- FT3 und FT4 alle 6 Monate
Es kann unter der Amiodaronbehandlung zu folgenden typischen Krankheitsbildern an der Schilddrüse kommen:
Laborveränderungen unter Amiodaron
[Bearbeiten]Anfangs
[Bearbeiten]hemmende Wirkung von Jod auf die SD ( Wolff-Chaikoff-Effekt)
- vorübergehender Abfall des fT4-Spiegel
- vorübergehende TSH-Erhöhung
Weiterer Verlauf
[Bearbeiten]Amiodaron hemmt die Deiodase und den SD-Hormonrezeptor
- erhöhtes fT4
- erniedrigtes fT3,
- erhöhtes reverses T3
- TSH
- vorübergehender TSH-Anstieg (bis zu 20 mU/L)
- später TSH-Spiegel wieder normal oder leicht erniedrigt.
Typische Laborkonstellation der Amiodarondauertherapie beim euthyreoten Patienten
[Bearbeiten]- fT4-Anstieg um 20 bis 30 %,
- fT3-Abfall in den unteren Normbereich,
- TSH im unteren Normbereich beziehungsweise erniedrigt
Amiodaron-induzierte Unterfunktion der Schilddrüse (AIH)
[Bearbeiten]Durch das Amiodaron kann eine bereits vorhanden Autoimmunthyreoiditis verstärkt oder erst manifest werden, die dann zu einer Schilddrüsenunterfunktion führt. Bei Patienten mit positiven TPO-Antikörpern besteht dafür ein ca. 7-fache erhöhtes Risiko. Wie üblich wird die resultierende Unterfunktion einfach durch die Tabletteneinnahme von T4 behandelt. Wegen der Hemmung der Umwandlung von T4 nach T3 durch das Amiodaron ist die erforderliche Thyroxindosis meist etwas höher als üblich. Therapieziel ist ein TSHwert zwischen 1 und 2 , also im mittleren Normbereich. Amiodaron kann , wenn eine wichtige Indikation vorliegt, trotzdem weiter gegeben werden.
Amiodaron-induzierte Überfunktion Typ 1 (AIT I)
[Bearbeiten]Durch die exszessive Jodzufuhr kann es unter der längeren Therapie mit Amiodaron zur Ausbildung bzw zur schnelleren Manifestation heißer Knoten oder fokaler autonomer Bezirke kommen. Wie üblich findet man im Ultraschall vermehrt durchblutete und szintigrafisch warme oder heiße Knoten. Die Therapie wird wie üblich mit Thyreostatika durchgeführt. Wobei man meist Thiamazol ( bis 40 mg) und Perchlorat ( beispielsweise 3 x 15 gtt) kombiniert. Bei den relativ hohen Thiamazoldosen ist die Gefahr der Agranulozytose und der dosisabhängigen Leukopenie höher als bei den sonst üblichen niedrigeren Thiamzoldosen unter 20 mg / Tag. Deswegen sind regelmäßige Kontrollen des Blutbildes notwendig. Alternativ kann oder muß eine definitive Sanierung der Schilddrüse durch eine Operation erfolgen.
Amiodaron-induzierte Überfunktion Typ 2 (AIT II)
[Bearbeiten]Auch die Amiodaron-induzierte Überfunktion Typ 2 tritt häufig erst nach monatelanger Dauertherapie mit Amiodaron ein. Typischerweise findet sich sonografisch ein homogenes Gewebe ohne vermehrte Durchblutung. Der Uptake im Szintigramm ist erniedrigt. Charakteristisch sind die oft stark erhöhten Interleukin-6-Serumspiegel. Die AIT 2 ist meist milder als die AIT 1 und spricht nicht auf Thyreostatika an. Sie endet nicht selten in einer Unterfunktion, welche dann wieder mit einem Hormonersatz behandelt wird.
Patienten, bei denen sich bereits vor der Amiodaronbehandlung SD-Antikörpern oder eine subklinische Hypothyreose nachweisen lassen, sind stärker gefährdet, eine Amiodaron-induzierte Hypothyreose zu bekommen.
Da Thyreostatika bei der AIT 2 wirkungslos sind, muß mit Steroiden behandelt werden. (z. B. Prednison 40 mg / Tag über 2 – 3 Monate)
Bei Mischtypen oder unsicherer Einordnung von AIT 1 und AIT 2 ist eine Kombinationstherapie von Thyreostatika mit Steroiden angezeigt und Amiodaron sollte abgesetzt werden. Wenn Amiodaron nicht abgesetzt werden kann oder wenn die Tablettentherapie nicht wirksam ist, ist eine operative Entfernung der Schilddrüse notwendig.
Literatur
[Bearbeiten]- Amiodarone Trials Meta-Analysis Investigators: Effect of prophylactic amiodarone on mortality after acute myocardial infarction and in congestive heart failure: meta-analysis of individual data from 6 500 patients in randomized trials. Lancet 1997; 350: 1417–24.
Trip MD, Wiersinga WM, Plomp TA: Incidence, predictability, and pathogenesis of amiodarone-induced thyrotoxicosis and hypothyroidism. Am J Med 1991; 91: 507–11.
Martino E, Bartalena L, Bogazzi F, Braverman LE: The effect of amiodarone on the thyroid. Endocrine Rev 2001; 22: 240–54.
Basaria S, Cooper DS: Amiodarone and the thyroid. Am J Med 2005; 118: 706–14.
Harjai KJ, Licata AA: Effects of amiodarone on thyroid function. Ann Intern Med 1997; 126: 63–73.
Kahaly GJ, Dillmann WH: Thyroid hormone action in the heart. Endocrine Reviews 2005; 26: 704–28.
Brabant G, Kahaly GJ, Schicha H, Reiners C: Milde Formen der Schilddrüsenfehlfunktion. Dtsch Arztebl 2006; 103(31–32): A 2110–5.
Dietlein M, Schicha H: Amiodarone-induced thyrotoxicosis due to destructive thyroiditis. Therapeutic recommendations. Exp Clin Endocrinol Diab 2005; 113: 145–51.
Hermida JS, Jarry G, Tcheng E et al.: Radioiodine ablation of the thyroid to allow the reintroduction of amiodarone treatment in patients with a prior history of amiodarone-induced thyrotoxicosis. Am J Med 2004; 116: 345–8.
Goldschlager N, Epstein AE, Naccarelli G, Olshansky B, Singh B: Practical guidelines for clinicians who treat patients with amiodarone. Arch Intern Med 2000; 160: 1741–8.
Bartalena L, Wiersinga WM, Tanda ML, Bogazzi F, Piantanida E, Lai A, Martino E: Diagnosis and management of amiodarone-induced thyrotoxicosis in Europe: results of an international survey among members of the European Thyroid Association. Clin Endocrinol 2004; 61: 494–502.
Bartalena L, Grasso L, Brogioni S, Aghini-Lombardi F, Braverman LE, Martino E: Serum Interleukin-6 in amiodarone-induced thyrotoxicosis. J Clin Endocrinol Metab 1994; 78: 423–7.
Bartalena L, Bogazzi F, Braverman LE, Martino E: Effects of amiodarone administration during pregnancy on neonatal thyroid function and subsequent neurodevelopment. J Endocrinol Invest 2001; 24: 116–30.
Bartalena L, Brogioni S, Grasso L, Bogazzi F, Burelli A, Martino E: Treatment of amiodarone-induced thyrotoxicosis, a difficult challenge: results of a prospective study. J Clin Endocrinol Metab 1996; 81: 2930–3.
Brennan MD, Erickson DZ, Carney JA: Nongoitrous (type I) amiodarone-associated thyrotoxicosis: evidence of follicular disruption in vitro and in vivo. Thyroid 1995; 5: 177–83.
Bogazzi F, Bartalena L, Brogioni S et al.: Color flow doppler sonography rapidly differentiates type I and type II amiodarone-induced thyrotoxicosis. Thyroid 1997; 7: 541–5.
Bogazzi, F.; Dell’Unto, E.; Tanda, M.L.; Tomisti, L.; Cosci, C.; Aghini-Lombardi, F.; Sardella, C.; Pinchera, A.; Bartalena, L.; Martino, E.: Long-term outcome of thyroid function after amiodarone-induced thyrotoxicosis, as compared to subacute thyroiditis. J Endocrinol Invest. 2006 Sep;29(8):694–9.
Bogazzi F, Bartalena L, Cosci C et al.: Treatment of type II amiodarone-induced thyrotoxicosis by either iopanoic acid or glucocorticoids: a prospective, randomized study. J Clin Endocrinol Metab 2003; 88: 1999–2002.
Eaton SEM, Euinton HA, Newman CM, Weetman AP, Bennet WM: Clinical experience of amiodarone-induced thyrotoxicosis over a 3-year period: role of colour-flow Doppler sonography. Clin Endocrinol 2002; 56: 33–8.
O'Sullivan AJ, Lewis M, Diamond T: Amiodarone-induced thyrotoxicosis: left ventricular dysfunction is associated with increased mortality. Eur J Endocrinol 2006; 154: 533–6.
Woolf SH, Sox HC: The expert panel on preventive services: continuing the work of the USPSTF. Am J Prev Med 1991; 7: 326–30.
Wolff J: Perchlorate and the thyroid gland. Pharmacol Rev 1998; 50: 33–8.
Dickstein G, Shechner C, Adawi F, Kaplan J, Baron E, Ish-Shalom S: Lithium treatment in amiodarone-induced thyrotoxicosis. Am J Med 1997; 102: 454–8.
Hamoir E, Meurisse M, Defechereux T, Joris J, Vivario J, Hennen G: Surgical management of amiodarone-associated thyrotoxicosis: too risky or too effective? World J Surg 1998; 22: 537–42.
Ryan LE, Braverman LE, Cooper DS, Ladenson PW, Kloos RT: Can amiodarone be restarted after amiodarone-induced thyrotoxicosis? Thyroid 2004; 14: 149–53.
Kathofer S, Thomas D, Karle CA: The novel antiarrhythmic drug dronedarone: comparison with amiodarone. Cardiovasc Drugs Rev 2005; 217–30.
Links
[Bearbeiten]- http://www.aerzteblatt.de/v4/archiv/artikel.asp?src=suche&id=58371
- Übersichtsartikel im Deutschen Ärzteblatt
- Kahaly, George J.; Dietlein, Markus; Gärtner, Roland; Mann, Klaus; Dralle, Henning
- Amiodaron und Schilddrüsendysfunktion
- Amiodarone-Induced Thyroid Dysfunction
- Dtsch Arztebl 2007; 104(51-52): A-3550
- Übersichtsartikel im Deutschen Ärzteblatt
Die SD und Lithium
[Bearbeiten]Die SD und Lithium
[Bearbeiten]Schilddrüsenbremsende Wirkung des Lithiums
[Bearbeiten]In den meisten Fällen gilt: Lithium führt zu einer Bremsung der SD-Funktion , so daß sich bei einer sonst normalen SD ein Trend zur SD Unterfunktion einstellen kann.
Durch die abfallenden T3 und T4 Werte kommt es wie üblich als Gegenregulation der Hypophyse zu einem TSH Anstieg .
Der erhöhte TSH Spiegel regt an der SD wiederum eine gewiße Vergrößerung des Organes im Sinne einer leichten Kropfbildung an.
So reagieren die meisten Patienten auf Lithium und man kann den SD bremsenden Effekt bei einer SD Überfunktion ganz gut nutzen.
Bildet sich unter der Therapie mit Lithium eine SD Unterfunktion aus , so muß man diese durch die Gabe von SD Hormon T4 = Thyroxin in angepasster Dosis behandeln.
Autoimmunstimulierende Wirkung des Lithiums
[Bearbeiten]In einigen wenigen Fällen liegen die Dinge anders: Lithium hat auch einen immunstimulierenden Effekt: Leider führt dies nicht zu einer besseren Abwehrlage sondern zu einem vermehrten Auftreten von Autoimmunerkrankungen.
Es gibt wenige Fallberichte die zeigen , daß Lithium an der SD sowohl einen Basedow als auch eine Autoimmunthyreoiditis auslösen kann.
Kontrolle und Testung
[Bearbeiten]Will man herauszufinden , wie denn nun das Lithium im Einzelfall an der SD reagiert , so muß man dies austesten.
Auf den Fall einer Hyperthyreose bezogen:
Läßt man das Lithium weg und es kommt zu einem Anstieg des T3 und T4 Spiegels , trotz gleichbleibender Carbimazol und T4 Therapie, reagiert das Lithium wie in der Mehrzahl der Fälle bremsend auf die SD und wirkt sich günstig auf die Hyperthyreose aus.
Läßt man das Lithium weg und es kommt nicht zu einem Anstieg des T3 und T4 Spiegels , sondern eher zu einer Normalisierung der SD Funktion , so daß man Carbimazol weglassen kann, dann muß man davon ausgehen , daß das Lithium über seinen autoimmunen Effekt , die Hyperthyreose erst erzeugt hat und sich ungünstig auf die SD auswirkt.
==> Man muß sich gut überlegen , ob man so eine Testprozedur machen soll, die über mehrere Wochen und mit mehreren Messung durchgeführt werden muß.
Man riskiert ein Rezidiv der Depression .
Wenn man also meint , daß man auf das Lithium nicht verzichten kann, dann muß man bei einer Hyperthyreose :
Regelmäßig die SD Funktion testen und danach angepasst die Carbimazol und T4 Therapie einstellen. Außerdem sollte man die SD Größe sonografisch kontrollieren und die körperlichen Zeichen der SD Überfunktion immer wieder abfragen .
Insbesondere die Herzfrequenz in Ruhe und der Blutdruck sind da ganz brauchbare Kontrollwerte
Literatur:
[Bearbeiten]- Nervenarzt 1998 Mar;69(3):189-95
- Thyroid gland function in lithium treatment.
- Bschor T, Bauer M
- Psychiatrische Klinik und Poliklinik, Freien Universitat Berlin.
- PMID: 9565972,
- Thyroid gland function in lithium treatment.
Lithium als Therapeutikum bei Thyreotoxikose
[Bearbeiten]Literatur
[Bearbeiten]- Gerdes, H., Littmann, K.P., Joseph, K., Mahlstedt, J.:
- Die Behandlung der Thyreotoxikose mit Lithium.
- Dtsch. Med. Wochenschr.98, 1551–1554 (1973)
- Die Behandlung der Thyreotoxikose mit Lithium.
- Temple, R., Berman, M., Robbins, J., Wolff, J.:
- The use of lithium in the treatment of thyrotoxicosis.
- J. Clin. Invest.51, 2746–2756 (1972)
- The use of lithium in the treatment of thyrotoxicosis.
Die Schilddrüse und Interferon
[Bearbeiten]
Literatur
[Bearbeiten]- http://scidok.sulb.uni-saarland.de/volltexte/2007/1123/pdf/Doktorarbeit.pdf
- Untersuchung zu Reaktionen der Schilddrüse auf eine tägliche Interferontherapie bei chronischer Hepatitis C
- Gehring, S.; Kullmer, U.; Koeppelmann, S.; Gerner, P.; Wintermeyer, P.; Wirth, S.:
- Prevalence of autoantibodies and the risk of autoimmune thyroid disease in children with chronic hepatitis C virus infection treated with interferon-alpha.
- World J Gastroenterol. 2006 Sep 28;12(36):5787–92
- Prevalence of autoantibodies and the risk of autoimmune thyroid disease in children with chronic hepatitis C virus infection treated with interferon-alpha.
Umwelteinflüsse auf die Schilddrüse
[Bearbeiten]Umwelttoxine
[Bearbeiten]Folgende Umweltgifte können einen Einfluß auf die Schilddrüse haben:
- radioaktives Jod
- Überdosis von Jod
- polychlorierte Biphenyle (PCB),
- Weichmacher,
- Dioxin,
- Blei
- Kann eine SD Unterfunktion auslösen
- aromatische Kohlenwasserstoffe
- MTBE Methyltertiärbutyl, ein mit Sauerstoff angereicherter Stoff, der dem Benzin zugesetzt
Zitat:
Wachstumsstörungen treten bei Kindern mit Blutbleiwerten von 150 - 250 μg/l auf. Sie beruhen einerseits auf einer Störung des Vitamin-D-Stoffwechsels, gefolgt von einer Beeinträchtigung des Kalzium-Stoffwechsels und andererseits möglicherweise auf der Störung des Hypophysen-Schilddrüsen-Systems.
Strumigene Subtanzen
[Bearbeiten]Als strumigene Substanzen bezeichnet man Stoffe die einen Kropf hervorrufen können, ohne das ein Jodmangel vorliegt.
Strumigen sind auch Stoffe, die thyreostatisch wirken, da sie den TSH Spiegel erhöhen und durch den erhöhten TSH Spiegel, das Kropfwachstum angeregt wird.
- Thiocyanat
Strumigene Substanzen in der Nahrung können sein: Blumenkohl
Strumigene im Trinkwasser können sein: Fluor und Chlor Zu den strumigenen Substanzen im Wasser zählen der Nitrat- und Nitritgehalt, der meist als Folge einer Überdüngung landwirtschaftlich genutzter Böden entsteht.
Arzneimittel die strumigen wirken sind beispielsweise das
- Lithium
- Irenat
Lebensmittelzusatzstoffe mit vermehrtem Jodgehalt
[Bearbeiten]- E 127 Erythrosin Roter Lebensmittelfarbstoff
- E 400 - 405 Alginate
- E 406 Agar Agar
- E 407 Carrageen
Literatur
[Bearbeiten]- http://archiv.ub.uni-heidelberg.de/volltextserver/volltexte/2008/8184/pdf/bo_Feb15_132211.pdf
- Umweltbezogene Einflußfaktoren auf die Strumaentwicklung
- Promotionsarbeit Uni Heidelberg
- Umweltbezogene Einflußfaktoren auf die Strumaentwicklung
Schilddrüsenexperten
[Bearbeiten]
Schilddrüsenexperten
Einleitung
[Bearbeiten]Für die Beurteilung der Schilddrüsenfunktion oder der Schilddrüsengröße reichen die Laborwerte und der Ultraschall völlig aus. Auch die Kontrolle der Größe eines Schilddrüsenknotens im zeitlichen Verlauf bietet keine allzu großen Schwierigkeiten. Dazu braucht man keinen Schilddrüsenspezialisten, sondern der eigene Hausarzt oder Internist können einen dabei gut und kompetent beraten. Bei schwierigeren Fällen kann die Untersuchung und Behandlung von einem Experten ratsam sein.
Die Schilddrüse wird von den verschiedensten Ärzten untersucht und behandelt: Diagnostiker und Therapeuten:
- Ultraschallexperten mit Spezialisierung Schilddrüse
- Nuklearmediziner mit Spezialisierung Schilddrüse
- Endokrinologen mit Spezialisierung Schilddrüse
- Pathologen mit Spezialisierung Schilddrüse
- Chirurgen mit der Spezialisierung Schilddrüse, Endokrine Chirurgie
Die Radiojodbehandlung der Schilddrüse wird von Nuklearmedizinern durchgeführt.
Operationen der Schilddrüse werden von Viszeralchirurgen oder HNO-Ärzten durchgeführt.
Neben der klinischen Medizin gibt es auch
- Pharmazeuten, die neue Medikamente für die SD entwickeln.
- Anatomen, Physiologen, Biochemiker, Biologen die sich mit der SD beschäftigen.
- Veterinärmediziner, die sich mit der SD der Tiere beschäftigen.
Wie findet man einen guten Schilddrüsenoperateur ?
[Bearbeiten]Über eine im Internet nutzbare Datenbank
[Bearbeiten]Diese Frage ist mittlerweile relativ leicht zu beantworten. Jedes Krankenhaus muß seine Leistungen in einem Qualitätsbericht veröffentlichen. Recht gut und vergleichend dargestellt werden die Leistungsziffern von der Weißen Liste.
Leider müssen niedergelassene Fachärzte ihre Leistungszahlen nicht veröffentlichen. Sonst könnte man, ähnliche wie bei den Krankenhäusern, abfragen, welcher Facharzt welche SchilddrüsendSchilddrüsendiagnostik und -therapie wie oft im Jahr durchführt.
Eigene Recherche in den Qualitätsberichten
[Bearbeiten]Man sucht sich die entsprechende OPS-Ziffer (Behandlungsziffer) aus dem OPS Katalog. Dann durchsucht man den Qualitätsbericht der in Frage kommenden Krankenhäuser nach dieser OPS Nummer und kann so nachsehen wieviel Schilddrüsen OPs in den Krankenhäusern gemacht wurden. Die Zahl der Operation läßt zumindest indirekt auf die Qualität schließen.
OPS Ziffern der Schilddrüse und Nebenschilddrüse
[Bearbeiten]- 5-06 Operationen an Schilddrüse und Nebenschilddrüse
- Info.: Eine durchgeführte Neck dissection ist gesondert zu kodieren(5-403)
- 5-060 Inzision im Gebiet der Schilddrüse
- 5-061 Hemithyreoidektomie
- 5-062 Andere partielle Schilddrüsenresektion
- 5-063 Thyreoidektomie
- 5-064 Operationen an der Schilddrüse durch Sternotomie
- 5-065 Exzision des Ductus thyreoglossus
- 5-066 Partielle Nebenschilddrüsenresektion
- 5-067 Parathyreoidektomie
- 5-068 Operationen an der Nebenschilddrüse durch Sternotomie
- 5-069 Andere Operationen an Schilddrüse und Nebenschilddrüsen
Beispiel einer Suche im Raum München
[Bearbeiten]- Eingabe der Suchangabe 5-061 Hemithyreoidektomie und München in Google oder einer anderen Suchmaschine.
- Dort findet man unter anderem das Mariatheresia Krankenhaus.
Man sucht in diesem Angebot den Qualitätsbericht beispielsweise aus dem Jahr 2007.
Der Qualitätsbericht wird meistens im PDF-Format abgespeichert, man braucht also den Acrobat Reader oder ein ähnliches Programm zum Lesen der PDF Datei.
Lassen Sie sich durch die Länge des Berichtes nicht abschrecken. Gehen Sie einfach auf die Suchfunktion des Acrobat Readers und geben die OPS Ziffer 5-061 ein: Meist haben Sie dann sehr schnell die richtige Tabelle gefunden.
Sie finden eine Tabelle der SD Operationen auf Seite 17
Schilddrüse OPERATIONSSTATISTIK
---------------------------------------------
STRUMA NODOSA OPS 2006 2007
---------------------------------------------
Hemithyreoidektomie 5-061.0 102 140
Subtotale Resektion
- einseitig 5-062.1/.8 5 6
- beidseitig 5-062.4/.8 31 21
- einseitig + Hemith.5-062.5 170 150
Thyreoidektomie 5-063.0 505 584
Minimal-inv. Hemith. 5-061.0 8 5
--------------------------------------------
REZIDIV-STRUMA
Restthyreoidektomie 5-062.6 41 39
5-063.4
--------------------------------------------
SCHILDDRÜSEN-CARCINOM
Hemithyreoidektomie 5-061.0 21 25
Thyreoidektomie 5-063.0 30 32
Lymphadenektomie 5-402.0 38 40
5-403.00
--------------------------------------------
HYPERPARATHYREOIDISMUS
pHPT 5-066.0 21 14
5-067.0
--------------------------------------------
Gesamt 972 1056
Wenn man diese Zahlen mit anderen Krankenhäusern in München und Umgebung vergleicht, kann das Krankenhaus Maria Theresia in Bereich der Schilddrüse sehr gute Zahlen vorweisen.
Links
[Bearbeiten]Bekannte Schilddrüsenexperten im deutschsprachigen Raum
[Bearbeiten]in alphabetischer Reihenfolge:
Achtung: die folgende Liste ist weder vollständig, noch wertend,
noch sauber überprüft, noch peer reviewt.
Achtung: Es gibt keinen allgemeinen Konsens, wer sich Experte im Allgemeinen,
bzw. Schilddrüsenexperte im besonderen nennen darf.
- Dr. med. Katharina Binz
- Stockerstrasse 42 8002 Zürich Telefon: 01 281 14 04 Fax: 01 281 13 81
- Dr. med. Fridolin Caduff
- Rathausstrasse 24 4410 Liestal Telefon: 061 921 10 00
- Dr. med. Mirjam Christ-Crain Kantonsspital Basel Endokrinologie, Diabetologie und klinische Ernährung
- Petersgraben 4 4056 Basel Telefon: 061 265 25 25
- Professor Karl-Michael Derwahl
- St. Hedwig-Krankenhaus Berlin, Große Hamburger Straße 5 - 11 10115 Berlin
- Telefon: 0 30 - 23 11 25 03
- http://www.prof-derwahl.de
- PD Dr. med. Johannes W. Dietrich
- Sektion Diabetologie, Endokrinologie und Stoffwechsel
- Universitätsklinik St. Josef-Hospital Bochum und Klinik Blankenstein Hattingen
- Gudrunstraße 56, 44791 Bochum, NRW
- Fernruf: (02 34) 5 09 - 32 71
- http://www.endokrinologie.org
- Dr. med. Reimar Fritzen
- Endokrinologische Gemeinschaftspraxis am Aachener Platz, Aachener Straße 196, 40223 Düsseldorf, NRW
- http://www.endo-duesseldorf.de
- Prof. Dr. Roland Gärtner, Medizinische Klinik Innenstadt, Universität München
- Ziemssenstr. 1, D-80336 München, BY
- Fernruf: 089-5160-2330
- http://www.klinikum.uni-muenchen.de/Medizinische-Klinik-Innenstadt/de/01Klinik/04Mitarbeiter/02Bereichsleiter/Gaertner_Roland/index.html
- PD Dr. Steffen Hering, Mathias-Spital Rheine
- Frankenburgstr. 31 - 48431 Rheine, NRW
- Fernruf: 05971 42-0
- https://www.mathias-spital.com/fachkliniken/medizinische-kliniken/medizinische-klinik-iii-diabetologie-endokrinologie-und-nephrologie/
- Alexander Horn, Medizinische Klinik I, Klinikum Weiden, BY
- Dr. med. Ernst Iff
- Schänzlistrasse 6 4500 Solothurn Telefon: 032 624 50 40 Fax: 032 624 50 41
- Prof. Dr. George J. Kahaly, Mainz, RP, Endokrine Orbitopathie (EO)
- Prof. Dr. Wolfram Karges, Universitätsklinikum Aachen, NRW
- Prof. Dr. Harald H. Klein, MVZ für Diagnostik und Therapie Bochum
- Bergstr. 26, 44791 Bochum, NRW
- Fernruf: 0234 955 40 100
- https://endokrinologieprofklein.de/
- Prof. Dr. Jochen Kußmann,
- Klinik für Endokrine Chirurgie, Schön Klinik Hamburg-Eilbek, Dehnhaide 120, 22081 Hamburg
- Tel.: 040-2092-7101 Fax: 040-2092-7102
- Prof. Dr. Armin E. Heufelder, München, BY
- Endokrinologe
- Prof. Dr. med. Lothar-Andreas Hotze, Mainz-Kastel, RP
- Nuklearmediziner
- Prof. Dr. Ulrich Loos, Universität Ulm und KreLo Medical Diagnostics GmbH
- Endokrinologe
- Sedanstr. 14
- 89077 Ulm. BW
- http://www.krelo-med.de/
- Gynter Mödder
- Max-Planck-Straße 27a, 50858 Köln (Junkersdorf), NRW
- PD Dr. med. Beat Müller
- Kantonsspital Basel
- Endokrinologie, Diabetologie und klinische Ernährung
- Petersgraben 4 4056 Basel
- Telefon: 061 265 50 78
- Dr. med. Tarek Stanarius (geb. Mustafa)
- Universitätsklinikum Halle, Experimentelle Chirurgie und Onkologie, Martin-Luther-Universität, Halle, ST
- Telefon: 0345 5571332
- Prof. Dr. C. Renate Pickardt, München, BY
- Endokrinologin
- http://www.endokrinologiemuenchen.de
- Prof Dr. Christoph Reiners
- Leiter der nuklearmedizinischen Abteilung der Universität Würzburg, BY
- Experte für die Diagnostik und Behandlung von Schilddrüsenkrebs
- Leiter der nuklearmedizinischen Abteilung der Universität Würzburg, BY
- Prof. Dr. Dr. Jürgen Ruhlmann
- Münsterstrasse 20, 53111 Bonn, NRW
- Tel.: (0228) 90 81 100
- http://www.mcbonn.de
- Prof. Dr. Mattias Schott
- Universitätsklinikum Düsseldorf
- Moorenstraße 5
- 40225 Düsseldorf, NRW
- http://www.uniklinik-duesseldorf.de/endokrinologie
- Chefärztin: Prof. Petra-Maria Schumm-Draeger, Krankenhaus München-Bogenhausen, 81927 München, BY
- Dr. med. Alexander Viardot
- Kantonsspital Basel Endokrinologie, Diabetologie und klinische Ernährung Petersgraben 4 4056 Basel Telefon: 061 265 25 25
- Prof.Dr. Cuong Hoang-Vu
- Universitätsklinikum Halle, Martin-Luther-Universität, Halle, ST
- Telefon: 0345 5571332
- Hermann Wagner, Innere Abt., Medizinische Klinik I, Klinikum Weiden, Weiden, BY
- Prof. Dr. med. Frank Weber
- Klinik für Allgemein-, Viszeral- und Transplantationschirurgie
- Sektion Endokrine Chirurgie
- Universitätsklinikum Essen
- http://www.uk-essen.de/index.php?id=2118
- und viele mehr
Sektion Schilddrüse der DGE Deutsche Gesellschaft für Endokrinologie
[Bearbeiten]- Sprecher:
- Prof. Dr. Markus Luster, Marburg
- Beirat:
- PD Dr. Joachim Feldkamp, Bielefeld
- Prof. Dr. Dr. Dagmar Führer, Essen
- Prof. Dr. Heiko Krude, Berlin
- Prof. Dr. Thomas Musholt, Mainz
- Prof. Dr. Matthias Schott, Düsseldorf
- Prof. Dr. Christine Spitzweg, München
Ungeordnet
[Bearbeiten]- Prof. Dr. med. Holger Palmedo
- Kompetenznetz Schilddrüse Bonn Rhein-Sieg,
- Überörtliche Gemeinschaftspraxis für Radiologie und Nuklearmedizin, PET-CT-Zentrum Johanniterkrankenhaus Bonn
- holger.palmedo@gmx.de
- Kompetenznetz Schilddrüse Bonn Rhein-Sieg,
- Dr. med. Charlotte Michaeli
- Kugelherrenstr. 1, 35510 Butzbach
- Tel: 06033/65543
- http://www.michaeli-praxis.de
- Prof. Dr. med. Andreas Türler
- Evangelische Kliniken Bonn gGmbH, Johanniter-Krankenhaus;
- Kompetenzzentrum für Schilddrüsen- & Nebenschilddrüsenchirurgie (DGAV), Bonn
- Evangelische Kliniken Bonn gGmbH, Johanniter-Krankenhaus;
- Prof. Hans Jürgen Biersack
- Nuklearmedizin
- Universitätsklinik Bonn
- Frau Korman
radiologische Gemeinschaftspraxis in Köln am Ebertplatz
- Dr. Michael Herzau
Praxis für Radiologie und Nuklearmedizin Zeitzer Strasse 20 07743 Jena
- Dr. Hans-Joachim Kröhne
Praxis für Innere Medizin / Endokrinologie Ambulantes Medizinisches Zentrum Ernst-Abbe-Platz 3-4 07743 Jena
- Herr Matthias Männel / Dr. Matthias Richter
Praxis für Nuklearmedizin / Radiologie Ambulantes Medizinisches Zentrum Ernst-Abbe-Platz 3-4 07743 Jena
- Prof. Ulrich A. Müller
Leiter der Abteilung Endokrinologie / Stoffwechselerkrankungen Klinik für Innere Medizin III Universitätsklinikum Jena Bachstrasse 18 07740 Jena
- PD Dr. Dirk Sandrock
Chefarzt der Klinik für Nuklearmedizin Klinikum Chemnitz gGmbH Flemmingstraße 2 09116 Chemnitz
- Dr. Martin Freesmeyer
Leiter der Klinik für Nuklearmedizin Universitätsklinikum Jena Bachstrasse 18 07740 Jena
- Dr. Nils Morgenthaler, Prof. Dr. W.A. Scherbaum
- Dr. Paul Banga (London)
Forschen über die SD an verschiedenen Projekten
- Prof. Dr. R. Paschke, Dipl.-Biol. P. Wonerow
- Untersuchungen zur Molekularbiologie der TSH-Rezeptoraktivierung
- TSH-Rezeptormutationen
- PD. Dr. med. J. Feldkamp, Internist, Bielefeld;
- Dr. med. M. Beyer, Internist, Nürnberg;
- Prof. Dr. med. H.G. Bohnet, Gynäkologe, Hamburg;
- Dr. rer. nat. Ch. Eckert-Lill, Apothekerin, Berlin;
- Prof. Dr. med. P.E. Goretzki, Chirurg, Neuss;
- Prof. Dr. med. A. Grüters, Pädiaterin, Berlin;
- Prof. Dr. med. F. Grünwald, Nuklearmediziner, Frankfurt/Main;
- Prof. Dr. med. R. Hehrmann, Internist, Hannover;
- Prof. Dr. med. M.B. Ranke, Pädiater, Tübingen;
- Dr. med. habil. W. Reske, Internist, Dresden;
Chirurgen
[Bearbeiten]- Prof. Dr. Martin Büsing
- Klinikum Vest-Knappschaftskrankenhaus Recklinghausen, Chirurg. Klinik 02361/563401 http://www.darmchirurgie.de
- Prof. Dr. Heinz J. Buhr
- Berlin Uniklinik Benjamin Franklin, Chirurg. Klinik 1 030/84 45 25 41 http://www.medizin.fu-berlin.de/chi/
- Weitere Mitarbeiter : PD Dr. med. Germer, Dr. med. Mann
- Prof. Dr. med. Dr. h.c. mult. Henning Dralle
- Essen Uniklinikum, Allgemein-, Viszeral- und Transplantationschirurgie, Sektion Endokrine Chirurgie, 0201/723 8120, http://www.uk-essen.de/
- Prof. Dr. U. Finke, Sankt-Katharinen-Krh, 60389 Frankfurt. www.sankt-katharinen-ffm.de
- Prof. Dr. Peter E. Goretzki
- Düsseldorf 02 11/ 8 11 73 52 Uniklinikum, Klinik fr Allgemein- u. Unfallchirurgie
- http://www.chir.uni-duesseldorf.de/
- Prof. Dr. Jochen Kußmann,
- Klinik für Endokrine Chirurgie, Schön Klinik Hamburg-Eilbek, Dehnhaide 120, 22081 Hamburg
- Tel.: 040-2092-7101 Fax: 040-2092-7102
- http://www.schoen-kliniken.de/ptp/kkh/eil/faz/endo-chirurgie/
- Prof. Dr. Wolfram Lamadé,
- Klinik für Allgemein- und Viszeralchirurgie
- Spezielle Tumorchirurgie, Endokrine Chirurgie
- HELIOS Spital Überlingen GmbH, Härlenweg 1 - 88662 Überlingen a.B.
- Tel.: +49 7551 9477-3502
- Fax: +49 7551 9477-443502
- http://www.helios-kliniken.de/ueberlingen
- PD Dr. C. Nies
- Prof.Dr.K.-H.Schultheis Florence Nightingale Krankenhaus 40489 Düsseldorf-Kaiserswerth Tel.00492114092504
- Sekr.: Tel. 06421-28-62506 Vorbildliche Op Statistik im Web abrufbar im Jahr 1999 ca 350 SD OPs
- Dr. Katrin Schultz, St.Hedwig-Krankenhaus Berlin, Große Hamburger Str. 5-11, 10115 Berlin
in Pension: *Prof. Dr. J. Schumann Frankfurt am Main 0 69/1 56 32 21 St. Marien Krankenhaus,
- Prof Dr med Arnold Trupka, Klinikum Starnberg, Endokrine Chirurgie, Tel 08151-182270; www.endokrine-chirurgie.de
- Prof. Dr. Peter Wagner Rosenheim 0 80 31/36 32 21
- Dr. med. Christian Vorländer Frankfurt am Main 0 69/ 1 50 04 11 Bürgerhospital Frankfurt am Main, Klinik für Endokrine Chirurgie
- Prof. Dr. med. Frank Weber
- Klinik für Allgemein-, Viszeral- und Transplantationschirurgie, Sektion Endokrine Chirurgie, Universitätsklinikum Essen
- http://www.uk-essen.de/index.php?id=2118
- Prof. Dr. Hubertus J. C. Wenisch Potsdam 03 31/ 2 41 52 02 Klinikum Ernst v. Bergmann,
- Chefarzt Dr. Günter Haselow St. Elisabeth Krankenhaus Geilenkirchen http://www.krankenhaus-geilenkirchen.de/
Pathologen
[Bearbeiten]- K.W. Schmid und S.-Y. Sheu Institut für Pathologie, Universitätsklinikum Essen,
- C. Ensinger,Pathologisches Institut, Universität Innsbruck, Österreich
- M. Tötsch, Institut für Pathologie, Universitäts-Hospital Genf, Schweiz
- Prof. Dr. H.-J. Holzhausen, Institut für Pathologie der Universität Halle-Wittenberg, Halle
- Prof. Dr. Klaus Wolfgang Kaserer...Reisnerstraße 5/3/2 ...1030 Wien Labor Kaserer, Salzer & Beer Wien
Pensioniert oder verstorben
[Bearbeiten]- Hans Wilhelm Bansi
- Prof.Dr.med Peter Pfannenstiel
- Prof. Dr. Dr. Fritz Spelsberg München 0 89/ 7 27 62 24 Krankenhaus Martha-Maria,
Liste von SD Spezialisten im Internet
[Bearbeiten]Leider nicht mehr verfügbar. Eventuell bei archive.org nachschauen.
Vereine und Gesellschaften
[Bearbeiten]Vereine und Gesellschaften
[Bearbeiten]- Sektion Schilddrüse der Deutschen Gesellschaft für Endokrinologie
- http://www.endokrinologie.net/profil/gremien/sektionen/schilddruese/schilddruese.html
- Deutsche Gesellschaft für Autoimmun-Erkrankungen
- http://www.autoimmun.org/erkrankungen/hashimoto_thyreoiditis.html
- Deutsche Gesellschaft für Nuklearmedizin e.V
- Schilddrüsen-Initiative Papillon
- Arbeitskreis Jodmangel
- Österreichische Gesellschaft für Nuklearmedizin
- Österreichische Schilddrüsengesellschaft
Geschichte der Schilddrüsenforschung
[Bearbeiten]
Übersicht
[Bearbeiten]Das Verständnis für die Funktion der Schilddrüse entwickelte sich erst langsam. Bis in die zweite Hälfte des 19. Jahrhunderts wurde sie als „Nebendrüse der Atemwege“ betrachtet, deren Funktion unklar war.[10]
Der Dubliner Arzt Robert Graves beschrieb 1835 in seiner Arbeit „Palpitation of the heart with enlargement of the thyroid gland“ als erster die Symptomkonstellation der später im englischsprachigen Raum nach ihm benannten Krankheit (Graves’ disease): Palpitationen, Struma und Exophthalmus. Als Ursache dieser Symptomatik nahm Graves eine Herzerkrankung an.
Unabhängig hiervon beschrieb Carl Adolf von Basedow 1840 in Merseburg in seiner Publikation „Exophthalmus durch Hypertrophie des Zellgewebes in der Augenhöhle“ ebenso die Symptomtrias von Struma, Exophthalmus, und Tachykardie (auch als Merseburger Trias bezeichnet). Zur Therapie empfahl er die Einnahme von jodidhaltigem Mineralwasser. Im deutschsprachigen Raum setzte sich die Bezeichnung Basedowsche Krankheit durch.
Die Bestimmung der Basedowschen Krankheit als einer Krankheit der Schilddrüse erfolgte allerdings erst 1886 durch den Leipziger Neurologen Paul Julius Möbius.[11][12]
George R. Murray führte 1891 die erste erfolgreiche Therapie des Myxödems mit Schilddrüsenextrakten durch.[11]
1896 isolierte Eugen Baumann eine unlösliche, nicht aus Proteinen bestehende Substanz, in der sich fast das gesamte in der Schilddrüse vorhandene Jod wiederfand – das sogenannte Jodothyrin (oder auch Thyreojodin) – und charakterisierte es als den wirksamen Bestandteil der Schilddrüse.[13]
1899 fand Adolph Oswald das Thyreoglobulin. [14]
Robert Hutchison stellte 1898 in seiner Arbeit über die Physiologie der Schilddrüse das Wissen seiner Zeit dar. Man wusste den Jodgehalt des Kolloids der Follikel abzuschätzen und stellte ausschließlich die jodhaltigen Bestandteile als aktiv dar. Damalige Versuche hatten gezeigt, dass die intravenöse Gabe des Kolloides keinerlei Wirkung auf Blutdruck oder Herztätigkeit ausübte. Man hatte jedoch nach Injektion von Schilddrüsenextrakten Blutdruckabfälle festgestellt. Tierversuche ergaben, dass das Blut nach Injektion des Kolloides in den Gefäßen nicht verklumpte, dass ein Warmhalten nach operativer Schilddrüsenentfernung keine Verzögerung des Auftretens oder Änderung des Verlaufes aktuer Symptome erbrachte, obwohl man keine Giftstoffe in Galle oder ZNS ausmachen konnte, jedoch die orale Gabe von Schilddrüsengewebe den Mortalitätsrate senkte. Darüber hinaus stellte man bei den Versuchen fest, dass weder die operative Entfernung von Hoden bzw. Eierstöcken, noch die orale Gabe von Nebenschilddrüse einen kurativen Einfluss auf das Myxödem hatten.[15]
Jodothyrin diente Ende des 19. und Anfang des 20. Jahrhunderts zu Versuchzwecken.[16] Aus der gegensätzlichen Wirkung unterschiedlicher Schilddrüsenextrakte auf den Kreislauf entwickelte sich um die Jahrhundertwende ein damals als polemisch bezeichneter Disput.[17] 1909 konnte John H. King feststellen, dass Jodothyrin einen eigenständigen, dem Extrakt der gesamten Schilddrüse überlegenen, verzögernden Effekt auf den Kohlenhydratstoffwechsel hat.[18]
1911 beschrieb Harry E. Alderson die gegensätzlichen Auswirkungen von Unter- und Überfunktion der Schilddrüse auf die Haut, sowie Möglichkeiten der Behandlung. Als wirksam im Sinne einer Schilddrüsenstimulation beschrieb er Extrakte der ganzen Schilddrüse, Jod und jodhaltige Substanzen, Arsen, Salicylate, Phosphor, Alkohol, Pilocarpin, Tee, Kaffee, Fleisch, sexuelle Betätigung, Gebärmutterleiden, Schwangerschaft und große emotionale Aufregungen. Als wirksam im Sinne einer Minderung der Schilddrüsenfunktion beschrieb er Opioide, Bromide, Hypnotika im Allgemeinen, Glycerophosphate aus der Linde, Calcium, Milch, getreidereiche Ernährung und sexuelle Enthaltung.[19]
Lewellys F. Barker bezeichnete Jodothyrin 1913 als das Hormon der Schilddrüse und rechnete es zu den sympathikotrophen Substanzen endokrinen Ursprungs. Als Wirkungen beschrieb er eine Beschleunigung der Herzfrequenz, eine Erweiterung der Lidspalte, den Exophthalmus sowie eine vermehrtes Ansprechen der Pupille auf Adrenalin.[20]
Die Entdeckung des Schilddrüsenhormones Thyroxin wird Edward Calvin Kendall zugeschrieben. Er hatte aus Jodothyrin einen aktiven Anteil herauskristallisiert und ihn Thyroxin genannt.[21]
Zur Diagnose einer Schilddrüsenerkrankung im Blut wurden in dieser Zeit indirekte Parameter wie Blutgerinnung und Differentialblutbild verwendet.[22]
1922 beschrieb Henry Stanley Plummer einen mittels der Lugolschen Lösung erreichten Rückgang von Hyperthyreosezeichen bei Patienten mit Morbus Basedow, das sogenannte „Plummern“. [23]
Emil Abderhalden und Ernst Wertheimer zeigten 1929, dass Muskelgewebe eine Thyroxinlösung in weit größerem Ausmaß aufnahm als Lebergewebe, konnten jedoch nicht feststellen, „was aus dem von den Geweben aufgenommenen Thyroxin wird.“[24]
Noch 1930 wurde über die Entstehung des Thyroxins im Organismus vermutet, dass es sich aus zwei Molekülen Dijodtyrosin zusammensetzen könnte.[25]
1933 beschrieben I. Abelin und A. Florin, dass Schilddrüsenhormone den Grundumsatz stark erhöhen, einen Glykogen- und Fettschwund veranlassen sowie Herz- und Atemfrequenz beschleunigen.[26]
Die künstliche Herstellung des Thyroxins wurde erstmals 1927 von Charles Robert Harington in London durchgeführt.[11]
Im Jahre 1952 wurde erkannt, dass Thyroxin-bindendes Globulin das Haupttransportprotein für Schilddrüsenhormone im Blut ist. (Robbins, Rall 1952).
1965 meldete Beverley E. P. Murphy sein Patent zur direkten Messung von Thyroxin in Körperflüssigkeiten an, das am 3. Dezember 1968 von der Patentbehörde angenommen wurde. Bis zu diesem Zeitpunkt waren nur indirekte Schilddrüsenfunktionstestungen, wie etwa die Messung des absoluten Jodgehaltes oder des proteingebundenen Jodes im Blut durchgeführt worden.[27]
1986: Reaktorunfall in Tschernobyl. Dieser führte zu einem starken Anstieg des Schilddrüsenkrebses in der Region Gomel. ( siehe http://leifi.physik.uni-muenchen.de/web_ph09_g8/geschichte/09tschernobyl/gesundheit.htm )
Stoffsammlung chronologisch
[Bearbeiten]Paracelsus war der erste, der die Kropferkrankung auf Mineralien im Trinkwasser zurückführte. Allerdings meinte er, daß dabei das Blei den entscheidenden Einfluß habe.
Geschichte der Chirurgie der Schilddrüse
[Bearbeiten]| 1614 | Felix | Platter | (1536-1614) | Basel | Erste Beschreibung einer malignen Struma |
| 1791 | Pierre-Joseph | Desault | (1744-1795) | Erste erfolgreiche Entfernung eines Strumalappens | |
| 1800 | J.A.W. | Hedenus (sen) | 8.10.1800 wird die erste 'Totalextirpation des Kropfes' durchgeführt | ||
| 1885 | J.v. | Mikulicz | (1850-1905) | Beschreibung der subtotalen Schilddrüsenresektion | |
| 1909 | Theodor | Kocher | (1841-1917) | Bern | Pionier der modernen Schilddrüsenchirurgie, erhält den Nobelpreis für seine Arbeiten über "Physiologie, Pathologie und Chirurgie der Schilddrüse" |
Quellen
[Bearbeiten]- ↑ 1,0 1,1 Richtlinie „Strahlenschutz in der Medizin“ (zur StrlSchV) bmub.bund.de, bmu.de (PDF; 841 kB)
- ↑ 2,0 2,1 2,2 F. Grünwald, C. Menzel: Radioiodtherapie. In: T. Kuwert, F. Grünwald, U. Haberkorn, T. Krause: Nuklearmedizin. Stuttgart / New York 2008, ISBN 978-3-13-118504-4.
- ↑ 3,0 3,1 Robertson IS. Dosimetry of radionuclides. In: Falk S (Hrsg.). Thyroid disease. New York: Raven 1997. Zitiert nach: F. Grünwald, C. Menzel. Radioiodtherapie. In: T. Kuwert, F. Grünwald, U. Haberkorn, T. Krause. Nuklearmedizin. Stuttgart, New York 2008 ISBN 978-3-13-118504-4
- ↑ Hall P, Boice JD Jr, Berg G, Bjelkengren G, Ericsson UB, Hallquist A, Lidberg M, Lundell G, Mattsson A, Tennvall J, et al. Leukaemia incidence after iodine-131 exposure. Lancet. 1992 Jul 4;340(8810):1-4. PMID 1351599
- ↑ Ron E, Doody MM, Becker DV, Brill AB, Curtis RE, Goldman MB, Harris BS 3rd, Hoffman DA, McConahey WM, Maxon HR, Preston-Martin S, Warshauer ME, Wong FL, Boice JD Jr. Cancer mortality following treatment for adult hyperthyroidism. Cooperative Thyrotoxicosis Therapy Follow-up Study Group. JAMA. 1998 Jul 22-29;280(4):347-55. PMID 9686552
- ↑ Homepage der American Thyroid Association; zuletzt eingesehen am 13. März 2008
- ↑ 7,0 7,1 7,2 7,3 Verfahrensanweisung zur Radioiodtherapie (RIT) beim differenzierten Schilddrüsenkarzinom
- ↑ 8,0 8,1 8,2 Chow S.M.: Side effects of high-dose radioactive iodine for ablation or treatment of differenciated thyroidcarcinoma, Hong Kong College Radiologist, 2005, (:127 - 135; zuletzt eingesehen am 13. März 2008
- ↑ Handelman D.J., e.a.: Azoospermia after iodine-131 treatment for thyroid carcinoma, British Medical Journal, 1980, 281:1527; zuletzt eingesehen am 13. März 2008
- ↑ J. Hyrtl: Lehrbuch der Anatomie das Menschen. Braumüller Hofbuchhändler. Wien, 1863. S.666
- ↑ 11,0 11,1 11,2 G. Bettendorf (Hrsg.): Zur Geschichte der Endokrinologie und Reproduktionsmedizin. Springer Verlag, Berlin 1995. S.27
- ↑ W. Gerabek, B. Haage, G. Keil, W. Wegner (Hrsg.): Enzyklopädie Medizingeschichte. Verlag de Gruyter, Berlin 2004. ISBN 978-3110157147
- ↑ E. Baumann: Über das Thyrojodin. In: Münchn Med Wschr 43 (1896/2): 309.
- ↑ A. Oswald. Zeitschr. f. physiol. Chem. 27: 14, 1899.
- ↑ R. Hutchison: Further Observations on the Chemistry and Action of the Thyroid Gland. In: J Physiol. 1898 July 26; 23(3): 178–189.
- ↑ O. von Fürth, K. Schwarz: Über die Einwirkung des Jodothyrins auf den Zirkulationsapparat. In: Pflügers Archiv European Journal of Physiology, Volume 124, Numbers 3-5 / August 1908, Verlag Springer Berlin/Heidelberg; ISSN 0031-6768 (Print) 1432-2013 (Online)
- ↑ A. G. Barbbra: Influence of Iodine, Sodium Iodide, and Iodothyrin on the Circulation. Pflüger’s Archiv, 1900, 79, S.312-318
- ↑ J. H. King: The influence of the thyroid on carbohydrate metabolism. J Exp Med. 1909 September 2; 11(5): 665–672.
- ↑ H. E. Alderson: The Skin as Influenced by the Thyroid Gland. Cal State J Med. 1911 June; 9(6): 240–243.
- ↑ L. F. Barker: The clinical significance of the autonomic nerves supplying the viscera, and their relations to the glands of internal secretion. Can Med Assoc J. 1913 August; 3(8): 643–657.
- ↑ R. B. Welbourn: The History of Endocrine Surgery. Greenwood Publishing Group, 1990. S.36. ISBN 0275925862
- ↑ An epitome of current medical literature. Br Med J. 1914 June 20; 1(2790): E97–E100.
- ↑ H. S. PLUMMER, W. M. BOOTHBY: Collected Papers. Mayo Clinic 15: 565, 1923.
- ↑ E. Abderhalden, E. Wertheimer: Studien über das Verhalten von Thyroxin im tierischen Organismus. Pflügers Archiv European Journal of Physiology, Springer Berlin/Heidelberg, ISSN 0031-6768 (Print) 1432-2013 (Online), 221:1, 1929, S.82-92
- ↑ A. T. Cameron: Some notes on our present knowledge and ignorance of throid function. Can Med Assoc J. 1930 February; 22(2): 240–246.
- ↑ I. Abelin, A. Florin: Nichtschilddrüsenstoffe mit Schilddrüsenwirkung. Naunyn-Schmiedeberg's Archives of Pharmacology, Verlag Springer Berlin/Heidelberg, ISSN 0028-1298 (Print), 1432-1912 (Online), 171:1, 1933, S. 443-456
- ↑ Patentschrift des United States Patent Office 3.414.383 pdf
Literatur
[Bearbeiten]Ungeordnet
[Bearbeiten]- Karl A. v. Basedow (1799-1840) Exophthalmus durch Hypertrophie des Zellgewebes in der Augenhöhle
- Casper's Wochenschrift 1840
- Beitrag zur Geschichte der Schilddrüse
- Zeitschrift Langenbeck's Archives of Surgery Verlag Springer Berlin / Heidelberg
- ISSN 1435-2443 (Print) 1435-2451 (Online) Heft Volume 116, Number 1 / Dezember 1912 Seiten 628-642
- Walther E. von Rodt1 chirurgischen Universitätspoliklinik Bern, Bern, Schweiz
- Veröffentlichungen der Schweiz. Gesellschaft für Geschichte der Medizin und der Naturwissenschaften SGGMN 1-40
- Band 19:
- Bornhauser, Sigmund: Zur Geschichte der Schilddrüsen- und Kropfforschung im 19. Jahrhundert (unter besonderer Berücksichtigung der Schweiz).
- 1951. 173 S.
- Band 19:
- Veröffentlichungen der Schweiz. Gesellschaft für Geschichte der Medizin und der Naturwissenschaften SGGMN 1-40
- Band 26:
- Tröhler, Ulrich: Der Schweizer Chirurg J. F. de Quervain (1868-1940).
- Wegbereiter neuer internationaler Beziehungen in der Wissenschaft der Zwischenkriegszeit.
- 1973. X, 137 S. 1 Abb.
- Zur Geschichte der Endokrinologie
- Springer-Lehrbuch ISSN 0937-7433 Verlag Springer Berlin Heidelberg Copyright 2007
- ISBN 978-3-540-37702-3 (Print) ISBN 978-3-540-37703-0 (Online)
- Bernhard Kleine und Winfried G. Rossmanith
- The History of Clinical Endocrinology: A Comprehensive Account of ... Von Victor Cornelius Medvei
- Veröffentlicht 1993 Taylor & Francis 551 Seiten ISBN 1850704279
- Sanitätsrat Dr. Karl Adolf von Basedow : (28. 3. 1799 - 14. 4. 1854) ; Kreisphysikus von Merseburg / Herbert Broghammer
- Broghammer, Herbert Verleger: Herbolzheim : Centaurus-Verl.-Ges. Erscheinungsjahr: 2000
- Umfang/Format: 188 S. ; 21 cm ISBN 3-8255-0309-7
- Broghammer, Herbert Verleger: Herbolzheim : Centaurus-Verl.-Ges. Erscheinungsjahr: 2000
Singer C, Underwood EA. A short history of medicine, 2nd ed. Oxford, Oxford University Press, 1962:519–34.
Bernard C. Piqure diabetes. Memorna societa de biologica, 1849, 1:80–92.
Hughes AF. A history of endocrinology. Journal of the history of medicine and allied sciences, 1977, 32:292–313.
King TW. Observations on the thyroid gland. Guy’s Hospital report, 1856, 1: 429–47.
Gley E. Sur les fonctions du corps thyroide. CR Società Biologica, 1891, 48:429–35.
Reverdin JL. Accidents consécutifs à l’ablation totale du goitre. Reviera medica suisse rom, 1882, 2:539.
Rehn L. Uber die extirpation des Kropfs bei morbus Basedowii. Berlin Klinica Wescher, 1884, 21:163–6.
Mackenzie HWG. A case of myxoedema treated with great benefit by feeding with fresh thyroid glands. British medical journal, 1892, 2:940–1.
Baumann E. Uber das normale Vorkommen Von Jod in Thierkorper. Hoppe-Seyler’s Zeitschrift fur physio-logische Chemie, 1895–1896, 21:319–30.
Hutchison R. The chemistry of the thyroid gland and the nature of its active constituents. Journal of physiology, 1896, 20:474–96.
Oswald A. Die Eiweisskorpor der Schilddruse. Hoppe-Seyler’s Zeitschrift fur physiologische Chemie, 1899, 27: 14–21.
Gross J, Pitt-Rivers R. Tri-iodothyronine in relation to thyroid physiology. Recent progress in hormone research, 1954, 10:109–24.
Kendall EC. The isolation of a compound containing iodine in the thyroid. Journal of the American Medical Association, 1915, 64:2042–3.
Harrington CR, Barger G. Constitution and synthesis of thyroxine. Biochemistry journal, 1927, 21:169–81.
Marie P. Acromegaly. Brain, 1890, 12:59–81.
Crowe SJ, Cushing H, Homans J. Experimental hypophysectomy. Bulletin of the Johns Hopkins Hospital, 1910, 21: 121–69.
Collip JB, Anderson EM. Studies on the thyrotropic hormone of the anterior pituitary. Journal of the American Medical Association, 1935, 104:965–6.
Hoskins RG. The thyroid–pituitary apparatus as a servo (feed-back) mechanism. Journal of clinical endocrinology, 1949, 9:1429–31.
Harris GW. Natural control of the pituitary gland. Physiological review, 1948, 28: 139–79.
Greer M. Evidence of a hypothalamic control of pituitary release of thyrotrophin. Proceedings of the Society of Experimental and Biological Medicine, 1951, 77:603–8.
Saffran M, Schally AV, Benfey BG. Stimulation of the release of corticotropin from the adenohypophysis by a neurohypophysial factor. Endocrinology, 1955, 57: 439–49.
Parry CH. Collections from the unpublished medical writings of the late Caleb Hillier Parry (volume 2). London, Underwoods, 1825:111.
Chatin M. Presence de iode dans les eaux pluviales, les plantes des Antilles et des cotes de la Mediterranee. CR Academa Scienca, 1853, 37:723–4.
Paracelsus M. De generative stultorum. Liber theophrasti. In: Omnia opera tractatus. Rome, 1603, volume 1.
McCarrison R. Observations on endemic goitre. Lancet, 1908, 2:1275–80.
Chisney AM, Clawson TA, Webster B. Endemic goiter in rabbits. Bulletin of the Johns Hopkins Hospital, 1928, 43:261–75.
Coindet JF. Iodine: on its application as a medicine. Quarterly journal of science, 1821, 11:408.
Marine D, Lenhart CH. Observations and experiments. Journal of experimental medicine, 1910, 12:311–20.
Marine D, Kimball OP. The prevention of simple goitre in man. Archives of internal medicine, 1920, 25:661–74.
Curling TB. Two cases of absence of the thyroid body, and symmetrical swellings of fat tissue at the sides of the neck, connected with defective cerebral development. Medico-chirurgical transactions, 1850, 33:303–6.
Gull WO. On a cretinoid state supervening in adult life in women. Transactions of the Clinical Society of London, 1873, 7:180–5.
Ord WM. On myxoedema, a term proposed to be applied to an essential condition in the cretinoid affection occasionally observed in the middle-aged women. Medico-chirurgical transactions, 1878, 61:57–78.
Murray G. Notes on the treatment of myxoedema. British medical journal, 1891, 2:796–7.
Riedel B. Vorstellung eines Kraken mit chronischer Strumitis. Ver Deutsch Ges Chirurgica, 1897, 26:127–31.
Hashimoto H. Zur Kenntniss der lympho-matosen Veranderung der Schilddruse (struma lymphomatosa). Archiv fur klinische Chirurgie, 1912, 97:219–25.
De Quervain F, Giordanengo G. Die akute and subacute nicht Eiterige. Thyroiditis. Mitt Grenzgeb Medica Chi-rurgica, 1936, 44:588–93.
Graves RJ. Newly observed affection of the thyroid gland. London medical and surgical journal, 1835, 7:516–7.
Von Basedow CA. Exophthalmus durch Hypertrophie des Zellgewebes in der Augenhöhle. Wochenschrift für die gesammte Heilkunde, 1840, 6:197–204.
Adam DD, Beavan DW. The presence of abnormal thyroid stimulator in the blood of thyrotoxic patients. Journal of clinical endocrinology and metabolism, 1962, 68: 154–65.
Astwood EB. Treatment of hyperthyroidism with thiourea and thiouracil. Journal of the American Medical Association, 1943, 122:78–85.
Sawin CT, Becker DV. Radioiodine and the treatment of hyperthyroidism: the early history. Thyroid, 1997, 7:163–76.
Adolf Oswald
[Bearbeiten]- Oswald Adolph
- geb 1870 Sulz (Elsass) 26.02.1870, Zof.1892 (Nr.1770),
- stud.auch in Berlin u.Würz- burg, Staatsexamen 1895 in Basel,
- Basel (Akad.kat.: imm.14.10.89 - 25.04.92, iterum als Dr.phil.24.04.94-1896) ab mit Zgn. 30.09.1893; (prom. 17.10.1893, StAZ U 110 e.4)
- Dr.med. (Diss.1897 üb.den Jodgehalt der Schilddrüsen)) und Dr.phil.II, Diss. "Der Rüsselapparat der Prosobranchier" (VZU 1558),
- 1900 PD in Zürich f. innere Medizin, Habil.schr. "Über die chemische Beschaffenheit u.die Funktion der Schilddrüse" (J´verz.1900/01 Nr.12),
- 1919 Tit.prof., Hormonforscher, Kunstmaler u.Alpinist,
- gestorben Zürich 22.07.1956: UFS 1983 S.692 ; V´j.schr.Naturf.Ges.Zch.1956 S.226 f.; Amodio 158 f.
- geb 1870 Sulz (Elsass) 26.02.1870, Zof.1892 (Nr.1770),
verheiratet mit Amalie Honegger (1880- 1958), E: Fr. A. O´, Gartenstr.107, Basel (Vater Seidenindustrieller)
- Habiltationsschrift:
- Ueber die chemische Beschaffenheit und die Function der Schilddrüse / Adolph Oswald
- Verfasser: Oswald, Adolf Daniel *1870-1956*
- Erschienen: Strassburg : Trübner, 1900 Umfang: 61 S. ; 8"
- Hochschulschrift: Zürich, Univ., Diss., 1900
- Anmerkung: 4 in: Zürich, Habilitations-Schriften. 1900-O1
- Ueber die chemische Beschaffenheit und die Function der Schilddrüse / Adolph Oswald
- Über die Wirkung der Schilddrüse auf den Blutkreislauf II. Mitteilung
- Zeitschrift Pflügers Archiv European Journal of Physiology Verlag Springer Berlin / Heidelberg
- ISSN 0031-6768 (Print) 1432-2013 (Online) Heft Volume 166, Numbers 3-4 / Dezember 1916
- Seiten 169-200
- Adolf Oswald Pharmakologischen Institut der Universität Zürich, Schweiz
- Zeitschrift Pflügers Archiv European Journal of Physiology Verlag Springer Berlin / Heidelberg
- Die Beziehungen Zwischen Schilddrüse und Nervensystem
- Zeitschrift Journal of Molecular Medicine Verlag Springer Berlin / Heidelberg
- ISSN 0946-2716 (Print) 1432-1440 (Online) Heft Volume 4, Number 22 / Mai 1925 Seiten 1053-1055
- A. Oswald Zürich
- Physiological Action of Substances from the Thyroid. By E. VON CYON and AD. OSWALD (Pflüger’s Archiv, 1901, 83, 199-206).
- The Combination of Iodine in Iodothyreoglobulin, and some Observations on Iodothyrin.
- ADOLF OSWALD (Arch. exp.Path. Pharm., 1908, 60, 115-130).
- The degradation of iodothyreoglobulin by pancreatin and barium hydroxide solution was studied. By means of the former, a small amount of a substance was obtained, which deposited from the digest, and was goluble in alkalis, but insoluble in acids ; it contained 3-4*5% iodine, and was in many respects similar to Baumann's iodothyrin ; the greater part of the iodine found in the digest was not in combination with organic substances. By scission with barium hydroxide, also, only a small amount of an organic iodine compound was obtained, which was soluble in acids, and was probably unchanged thyreoglobulin.
- ADOLF OSWALD (Arch. exp.Path. Pharm., 1908, 60, 115-130).
- Oswald, Adolf:
Titel: Chemische Konstitution und pharmakologische Wirkung, ihre Beziehungen zu einander bei den Kohlenstoffverbindungen. Eine Pharmakologie der Kohlenstoffverbindungen bekannter Konstitutionen. EA. Verlag: Berlin, Borntraeger, 1924. Beschreibung: X, 892 S., 2 Bll. Lex.-8°, OHLederband. Gewicht in [g]: 3000
- Oswald, Adolf:
Titel: Lehrbuch der chemischen Pathologie. Verlag: Leipzig. Verlag von Veit & Comp. 1907 Beschreibung: OHldr., gr.8°, 614 Seiten. Zustand: Bibliotheksexemplar, etw. berieben, bestossen, innen tadellos. Gewicht in [g]: 600
- Oswald, Adolf.
Titel: Die Schilddrüse in Physiologie und Pathologie. Leipzig, Veit & Comp. Verlag: 1916 Beschreibung: . Mit 10 Abb. 3 Bll., 88 S., 1 Bl. Gr.-8°. OBroschur. - Umschlag etwasfleckig und angerändert, Stempel auf Titel; unaufgeschnittenes, breitrandiges Exemplar. Bemerkung: [Medizin, Pharmazie, Psychologie; 1916; Pathologie; Physiologie; Schilddrüse;]
- Cyon, Elie & Oswald, Adolf:
- Ueber die physiologischen Wirkungen einiger aus der Schilddrüse gewonnener Producte.
- Pflüger's Arch., 83. - Bonn, E.Strauss, 1901, 8°, pp.199-206, 1 Tafel, OBrosch.
- First edition - author's off-print from the "Archiv for die gesamte Physiologie".
- Oswald, Adolf:
- Über jodierte Spaltungsprodukte des Eiweißes.
- Beitr. chem. Phys. Path., 3/9-10. - Braunschweig, Fr.Vieweg & Sohn, 1903, 8°, pp.391-416, OBrosch; mit eigenhändiger **Widmung "Herrn Prof.Dr. v.Bunge,
- Aus dem chemischen Laboratorium der medizinischen Klinik Zürich.
Elias von Cyon
[Bearbeiten]Cyon, Elias von. 1898. Physiologische Beziehungen zwischen den Herznerven und der Schilddrüse. Centralblatt für Physiologie 11: 279-280, 357-361
Cyon, Elias von. 1898. Beiträge zur Physiologie der Schilddrüse und des Herzens. Archiv für die gesammte Physiologie des Menschen und der Thiere 70: 126-280
Cyon, Elias von. 1898. Jodothyrin und Atropin: Vorläufige Mittheilung. Archiv für die gesammte Physiologie des Menschen und der Thiere 70: 511-512
Robert Hutchison
[Bearbeiten]Chemical Assistant to.thc Professor of Physiology, University of Edinburgh.
- Robert Hutchison
- Br Med J. 1896 March 21; 1(1838): 722–723. PMCID: PMC2406478
- Preliminary Note on the Active Substance in the Thyroid
- Br Med J. 1896 March 21; 1(1838): 722–723. PMCID: PMC2406478
- Robert Hutchison
- Br Med J. 1898 July 16; 2(1959): 142–145. PMCID: PMC2434086
- The Pharmacological Action of the Thyroid Gland
- Br Med J. 1898 July 16; 2(1959): 142–145. PMCID: PMC2434086
Links
[Bearbeiten]- Klassische Beschreibung der Basedowschen Erkrankung
- Die Hashimoto Erkrankung und Dr. Hakaru Hashimoto
- Einiges zum Thema Geschichte der Schilddrüsenmedizin
- Das Kropfspital in Wien
- Emil Theodor Kocher Begründer der Schilddrüsenchirurgie
- Eine historische Recherche zur Ord-Thyreoiditis
- Geschichte der Schilddrüsenhormon -Therapie
- Julius Wagner-Jauregg 1857 - 1940
- "Myxödem und Kretinismus" (im Handb.d. Psych., Spez. T, 2, l), Leipzig und Wien 1912,
- Leben und Wirken des Carl Adolph von Basedow,
- Die Kranheiten der Schilddrüse ein Lehrbuch von 1901
- Eiselsberg, Anton Freiherr von
Stichworte zum Thema Schilddrüse
[Bearbeiten]
Alphabetische Liste von Stichwörtern zum Thema Schilddrüse
[Bearbeiten]Ein Tipp: Geben Sie das Stichwort zusammen mit dem Wort Schilddrüse in eine Suchmaschine oder in Wikipedia ein.
A
[Bearbeiten]- Akropachie
- Alkoholbehandlung heißer Knoten
- Amiodaron und Schilddrüse
- Antikörper
- mikrosomale
- schilddrüsenspezifische
- TRAK
- MAK
- Antriebsarmut
- Atrophie
- Autoimmunkrankheit
- Autoimmunthyreoiditis
- Autonomes Adenom
- Autonomie
B
[Bearbeiten]- Basedowsche Krankheit
- Bradykardie
C
[Bearbeiten]- Calcitonin
- Carbimazol
- CEA-Spiegel
- Chemotherapie
- Computertomographie
- Cortison
- Cordarex
- CRP
- C-Zellen
- C-Zell-Hyperplasie
- C-Zell-Karzinom
D
[Bearbeiten]- Dalrymple-Zeichen
- Dejodase
- Dijodthyrosin
- Doxorubicin
- Ductus thyreoglossus
- Durchfall
E
[Bearbeiten]- Echokardiografie
- Echogenität
- endokrine Orbitopathie
- Entwicklungsverzögerung
- Epithelkörperchen
- Euthyreose
- Exophthalmus
F
[Bearbeiten]- Familienanamnese
- Farbdopplersonographie
- Feinnadelpunktion
- Follikelhyperplasie
- Follikelhypertrophie
- Follikelzellen
- follikulär
- fT4-Index
- fT3
- fT4
G
[Bearbeiten]- Gammakamera
- Ganzkörperszintigraphie
- Globulin, thyroxinbindendes
- Glucocorticoidtherapie
- Graefe-Zeichen
- Grundumsatz
H
[Bearbeiten]- Hashimoto-Thyreoiditis
- Heiserkeit
- Hemithyreoidektomie
- Hormon
- Hyperthyreose
- Amiodaron-induziert
- angeborene
- fetale
- bei Autonomie
- HCG-induziert
- jodinduziert
- nichtimmunogene, familiäre
- postpartale
- transiente
- Hyperthyreosis factitia
- Hyperzirkulation
- Hypoparathyreoidismus
- Hypophyse
- Hypophysentumor, TSH-produzierender
- Hyporeflexie
- Hypothyreose
- Amiodaron-induziert
- angeboren
- erworben
- fetal
- iatrogen
- periphere
- postpartale
- primäre
- sekundäre
- tertiäre
I
[Bearbeiten]- Immunglobulin
- Immunhyperthyreose
- Immunsuppressivum
- Immunthyreopathie
- In-vitro
- In-vivo
- Irenat
- Isthmus
J
[Bearbeiten]- Jod
- Jod-123
- Jod-131
- Jodausscheidung im Urin
- Jodbedarf
- Jodgehalt
- Jodid
- Jodierung
- Jodination
- Jodisation
- Jodisationsdefekt
- Jodisationshemmstoff
- Jodmangel
- Jodmangelstruma
- Jodtabletten
- Jodzufuhr
- Jodaufnahme
K
[Bearbeiten]- Kalter Knoten
- Knoten
- Knotenkropf
- Kolloid
- Koma
- hypothyreot
- hyperthyreot
- Kontrastmittel, jodhaltig
- Krise, thyreotoxische
L
[Bearbeiten]- L-Thyroxin
- Levothyroxin
- Lidschlag
- Liothyronin
- Lithium
- Lobektomie
- Lobus pyramidalis
- Low-T3-Syndrom
- Low-T4-Syndrom
- Lymphadenektomie
- Lymphknoten
M
[Bearbeiten]- Magnetresonanztomographie
- Maligne, Malignom
- Marine-Lenhart-Syndrom
- Medikamentenanamnese
- Metastasen
- Mikrokarzinom, papillär
- Morbus Addison
- Morbus Basedow
- Myxödem
N
[Bearbeiten]- Nebennierenrindeninsuffizienz
- Neoplasie
- Nervus laryngeus recurrens
- Neugeborenenhypothyreose
- Neugeborenenstruma
O
[Bearbeiten]- Obstipation
- Orbitadekompression
- Orbitafettresektion
- Orbitopathie
P
[Bearbeiten]- Palliativ
- Panhypopituitarismus
- Pentagastrin
- Perchlorat
- Pertechnetat
- PET
- Plasmapherese
- Plummern
- Pluriglanduläre Insuffizienz
- Polresektion
- Positronenemissionstomographie
- Präalbumin, thyroxinbindendes
- Propylthiouracil
- Punktion
Q
[Bearbeiten]- deQuervain-Thyreiditis
R
[Bearbeiten]- Radiochemotherapie
- Radiojodtest
- Radiojodtherapie
- Radionuklid
- Rekurrensparese
- Resektion
- reverses T3
- Retrobulbärbestrahlung
- Riedel-Struma
- Röntgenuntersuchung
S
[Bearbeiten]- SD
- Schilddrüse
- Schilddrüsenadenom
- Schilddrüsenatrophie
- Schilddrüsendystopie
- Schilddrüsenektopie 42, 44
- Schilddrüsenhormone
- Schilddrüsenhormonresistenz, periphere 65 f
- Schilddrüsenkarzinom
- anaplastisches
- differenziertes
- follikuläres
- medulläres
- familiäres
- onkozytäres
- papilläres
- metastasierendes
- Schilddrüsenknoten
- Schilddrüsensarkom
- Schluckbeschwerden
- Schmerz
- Schmidt-Syndrom
- Schwangerschaft
- Schwangerschaftshyperthyreose
- Selen
- Sick euthyroid syndrome
- Sick thyroidea syndrome
- Skelettszintigraphie
- Somatostatin
- Sonographie
- Speicheldrüse
- Speisesalz
- Stellwag-Zeichen
- Stillzeit
- Strahlentherapie
- Struma
- Struma diffusa
- Struma nodosa
- euthyreote Struma
- retrosternale Struma
- Struma maligna
- Strumaoperation
- Strumaprophylaxe
- Strumaresektion
- Suppressionsszintigraphie
- Sympathikus
- Szintigraphie
T
[Bearbeiten]- T3
- T4
- TAK
- Tetrajodthyronin
- Tg
- Tg-AK
- Thiamazol
- Thiouracile
- T3-Hyperthyreose
- Thyreoglobulin
- Thyreoidea
- Thyreoideastimulierendes Hormon
- Thyreoidektomie
- Thyreoiditis
- Thyreostatikum
- Thyreotropin-releasing-Hormon
- Thyroxin
- thyroxinbindendes Präalbumin
- TPO-Antikörper
- TRAK
- Transportprotein
- TRH-Test
- Trijodthyronin
- TSH
- TSH-Rezeptor
- TSH-Rezeptor-Autoantikörper
- T4-T3-Konversion 5
- Tumormarker
- Tumornachsorge
U
[Bearbeiten]- Uptake
V
[Bearbeiten]- Volumenmessung
W
[Bearbeiten]- Wachstumsfaktoren
Z
[Bearbeiten]- Zellen
- Zyklus
- Zyste
Abkürzungen
[Bearbeiten]
Abkürzungen
[Bearbeiten]Wenn man sich mit der Schilddrüse beschäftigt und darüber nachliest, stößt man auf zahlreiche Abkürzungen, die wichtigsten sind hier augelistet:
Abkürzung Bedeutung ---------------------------------------------------------- DJT 3,5 –Dijodtyrosin FT3 freies Trijodthyronin FT4 freies Thyroxin im Blut HCG Humanes Chorion Gonadotropin HVL Hypophysenvorderlappen ICD 10 International Classification of Diseases 10 KeV KiloElektronenVolt µg ein mikro Gramm = ein millionstel Gramm MAK Mikrosomale Antikörper siehe TPO MJT 3 -Monojodtyrosin MW Molekulargewicht NIS Natrium-Iodid Symporter, Blut > Iod > SD PBI Protein-gebundenes Jod rT3 reverses T3 SD Schilddrüse SDH Schilddrüsenhormone T3 Trijodthyronin T4 Tetrajodthyronin = Thyroxin TAK Thyreoglobulin Antikörper TBA Thyroxin- bindendes Albumin TBG Thyroxin bindendes Globulin ( Transportprotein im Blut ) TBPA Thyroxin – bindendes Präalbumin Tc Technetium TRAK TSH-Rezeptor Antikörper TPO Threoidea Peroxidase Antikörper TSH ThyreoideaStimulatingHormone TRH ThyreotropinReleasingHormone 10^-9 ein Milliardstel (1:1 000 000 000) 10^-12 ein Billionstel (1:1 000 000 000 000)
Fragen zum Thema Schilddrüse
[Bearbeiten]
Fragen zum Thema Schilddrüse
Hier können Sie Ihre Fragen zum Thema Schilddrüse eingeben:
Mononukleose und Hashimoto Thyreoditis
[Bearbeiten]- Gibt es einen Zusammenhang zwischen der Mononukleose und der Hashimoto Thyreoditis ?
Erhöhter TSH Wert , Was tun ?
[Bearbeiten]Bei mir wurde ein erhöhter TSH-Wert und damit eine Schilddrüsenunterfunktion festgestellt. Die autoimmune Form konnte jedoch anhand der anderen Blutwerte und des Ultraschallbefundes ausgeschlossen werden. Mein Internist hat mir Jodtabletten verschrieben. Reicht das oder muss ich Thyroxin einnehmen?
Antwort: Zur Beantwortung dieser Frage braucht man alle Ihre Schilddrüsenwerte :
TSH wie hoch ? T3 erniedrigt ? T4 erniedrigt ?
Außerdem sollte ein guter Schilddrüsen Ultraschall gemacht werden, mit der Fragestellung, ob eine zu kleine oder zu grosse Schilddrüse vorliegt und ob eine Schilddrüsenentzündung erkennbar ist .
Gibt es gute websites/Informationen über Schilddrüsenkrebs bei Tieren?
[Bearbeiten]Antwort: Recherchieren Sie doch selbst einmal und geben Sie ihre Antwort und gefundenen Links hier ein. Siehe zb http://www.wer-weiss-was.de/tiere/wer-kann-mir-etwas-naeheres-zu-schilddruesenkrebs-be
Welche Funktion hat der N.Laryngeus recurrens ?
[Bearbeiten]Antwort
[Bearbeiten]
Der Nerv versorgt die Stimmbänder. Wenn er geschädigt wird, dann bekommt man eine Stimmbandlähmung. Es resultiert eine Heiserkeit, manchmal auch eine Atemnot. Da der Nerv sehr eng hinter der Schilddrüse verläuft und sehr klein und schlecht zu sehen ist, kann er bei einer Schilddrüsenoperation verletzt werden.
Physiologie
[Bearbeiten]- Gibt es eine circadiane Rhythmik des freien SD-Hormon spiegels T3 oder T4 wie beim Cortison?
Hormonersatz bei der Unterfunktion
[Bearbeiten]- Kann man die Schilddrüsentabletten (Thyroxin) auch am Abend zum Schlafen einnehmen?
- Die Tageszeit der Einnahme ist beliebig, da Thyroxin mit einer Halbwertszeit von 8 Tagen eher als Depot für die Bildung von T3 fungiert. Wichtig ist, dass die Einnahme mindestens 30 Minuten vor bzw. 5 h nach einer Mahlzeit erfolgt, da die Nahrung im Magen eine verminderte Aufnahme des Thyroxin bewirkt. Es sind auch die Wechselwirkungen mit evtl. zum gleichen Zeitpunkt zu nehmenden Medikamenten zu beachten.
ACHTUNG: Dies gilt nur für die Einnahme von Thyroxin, also T4! Bei der Medikation mit T3 oder Kombinationspräparaten T4 / T3 ist durch die schnelle Bioverfügbarkeit des T3-Hormons und dem damit schnell eintretenden Wirkungseintritt eine Einnahme nach dem Aufwachen sinnvoll.
Abnehmen ohne Schilddrüse?
[Bearbeiten]Kann man ohne Schilddrüse abnehmen?
Antwort
[Bearbeiten]Wieso nicht? Man muss nur einen ausreichenden Hormonersatz durchführen. Das muss man aber sowieso, ob man abnehmen will oder nicht. Ohne Schilddrüse kann man nicht leben.
Autonomes Adenom
[Bearbeiten]Mit großem Interesse habe ich den Bericht über die percutane AlkoholInjektion gelesen. Vor etwa 14 Jahren entdeckte man in meinem linken Schilddrüsenlappen eine Zyste. Um die Zyste wuchs in den Jahren ein autonomes Adenom bis auf ca. 4 cm unter ärztlicher Aufsicht an. Die Zyste ist noch die Basis dieses autonomen Adenoms (wurde vor kurzem punktiert). Nun ist der Nuklearmediziner der Meinung, dass man für meine Schilddrüse nichts mehr hormonell tun könne und gab die Indikation zur Operation. Mein Adenom prodoziert mal Hormone und mal nicht. Bislang hatte ich L-Tyroxin eingenommen. Mal habe ich eine Überfunktion und mal eine Unterfunktion. In zwei Kliniken habe ich mich über Risiken und Nutzen der Operation aufklären lassen und bin zum Entschluss gekommen, dass ich mich nicht operieren lassen möchte. Das Risiko der Stimmbandschädigung und sei es auch nur eine vorübergehende Hemiparese würde für mich das berufliche AUS bedeuten und habe auch derzeit nicht die Zeit mich ins Krankenhaus zu legen. Käme für mich die percutane Alkohol Injektion in Frage? Wohin könnte ich mich wenden?
Antwort: Die einfachste Behandlung des Schilddrüsenüberfunktion ist immer noch die Therapie mit Thiamazol. Diese funktioniert auch bei einem oder mehreren autonomem Knoten ganz gut.
Eine Alkoholbehandlung ist vor allem bei einem einzelnen Knoten eine gute Behandlung. Man braucht dazu einen erfahrenen Ultraschalldoktor, der auch gezielte Punktionen vornehmen kann. Wer das in Göttingen kann, weiß ich leider nicht. Auch vor einer Operation braucht man nicht so viel Angst haben, wenn man sich einen Operateur mit mehr als 30 Schilddrüsenoperationen / Jahr heraussucht und mit ihm schriftlich vereinbart, dass er nur den autonomen Knoten > entfernt und die restliche Schilddrüse belässt. Dann ist die Gefahr einer Verletzung der Nervus recurrens oder eine Entfernung der Nebenschilddrüsen sehr gering. Nicht ganz klar, ist mir Ihre bisherige Thyroxinbehandlung. Sie scheint mir unnötig und kontraindiziert.
Hashimotothyreoditis
[Bearbeiten]Welchen Einfluss hat die niedrigdosierte Gabe von T4 ( zB Thyroxin 50 mikrog / Tag ) auf den Verlauf einer beginnenden Hashimotoerkrankung ?
[Bearbeiten]Nicht selten gibt es Patienten mit einer initialen Hashimotoerkrankung. Die AK sind hoch, TSH ist leicht erhöht, T3 und T4 sind aber noch normal. Was soll man tun ? Kann bei so einer Konstellation extern zugeführtes T4 das Fortschreiten zu einer Unterfunktion verzögern oder beschleunigen ?
Hat die Jodversorgung etwas mit der Thyreoiditishäufigkeit insbesondere mit der Häufigkeit der Hashimotothyreoiditis zu tun?
[Bearbeiten]- Gängige Medizinische Lehrmeinung: Die Autoimmunerkrankungen (Basedow und Hashimoto Thyreoiditis) der Schilddrüse haben nichts oder sehr wenig mit der Jodversorgung zu tun. Dazu gibt es eine lange medizinische Diskussion über Jahrzehnte. Die Länder mit Trinkwasserjodierung und einer einigermaßen brauchbaren Häufigkeitsstatistik der Schilddrüsenkrankheiten zeigen, dass es keinen echten Anstieg der Krankheitszahlen nach Einführung der Jodierung gegeben hat. Der Entstehungsmechanismus ist weitgehend unabhängig vom Jod Benutzer:Rho
- Literatur dazu:
- Lit 1: :
- Thyroid. 2003 Feb;13(2):199-203.
- Introduction of iodized salt to severely iodine-deficient children does not provoke thyroid autoimmunity: a one-year prospective trial in northern Morocco.
- Zimmermann MB, Moretti D, Chaouki N, Torresani T.
- The Human Nutrition Laboratory, Swiss Federal Institute of Technology, Zurich, Switzerland. michael.zimmerman@ilw.agrl.ethz.ch
- lit2
- J Clin Endocrinol Metab. 1999 Feb;84(2):561-6.
- The spectrum of thyroid disorders in an iodine-deficient community: the Pescopagano survey.
- Aghini-Lombardi F, Antonangeli L, Martino E, Vitti P, Maccherini D, Leoli F, Rago T, Grasso L, Valeriano R, Balestrieri A, Pinchera A.
- Department of Endocrinology, University of Pisa, Italy.
- Literatur dazu:
- Andere Meinung: Das kann man nicht so apodiktisch sagen. Die Iodversorgung beeinflusst die Häufigkeit von Hashimoto- und Basedow-Erkrankungen nur nicht linear. Vermutlich werden Thyreoiditiden bei zu hoher Iodeinnahme (> 500 ug/d) verursacht. Einige Einzelstudien: siehe lit1 [2] [3] Ausführliche Darstellung: [4]. --w:Benutzer:MBq Disk Bew 17:14, 1. Sep 2006 (CEST)
- lit1:
- N Engl J Med. 2006 Jun 29;354(26):2783-93.
- Comment in: N Engl J Med. 2006 Jun 29;354(26):2819-21.
- Effect of iodine intake on thyroid diseases in China.
- Teng W, Shan Z, Teng X, Guan H, Li Y, Teng D, Jin Y, Yu X, Fan C, Chong W, Yang F, Dai H, Yu Y, Li J, Chen Y, Zhao D, Shi X, Hu F, Mao J, Gu X, Yang R, Tong Y, Wang W, Gao T, Li C.
- Department of Endocrinology
- lit2
- Thyroid. 2003 May;13(5):485-9.
- Comment in: Thyroid. 2003 Dec;13(12):1187; author reply 1188.
- High prevalence of autoimmune thyroiditis in schoolchildren after elimination of iodine deficiency in northwestern Greece.
- Zois C, Stavrou I, Kalogera C, Svarna E, Dimoliatis I, Seferiadis K, Tsatsoulis A. Division of Endocrinology, Department of Medicine, University of Ioannina, Greece.
- lit3
- J Endocrinol Invest. 2003;26(2 Suppl):43-8. Links
- Improvement of iodine deficiency after iodine supplementation in schoolchildren of Azerbaijan was accompanied by hypo and hyperthyrotropinemia and increased title of thyroid autoantibodies.
- Markou KB, Georgopoulos NA, Makri M, Vlasopoulou B, Anastasiou E, Vagenakis GA, Kouloubi K, Theodosopoulos N, Lazarou N, Veizis A, Sakellaropoulos G, Vagenakis AG.
- Department of Medicine, Division of Endocrinology, University of Patras Medical School, University Hospital, Patras, Greece.
- lit4
- lit1:
- Kommentar zur Dosis: Ein Jodeinnahme von > 500 mikrog/ Tag ist viel zu viel und unnötig . Standarddosis sind 100 - 200 mikrog/ Tag in der Kropfvorbeugung Benutzer:Rho
Als Umweltfaktor ist im Wesentlichen die Iodversorgung zu nennen: umso höher die tägliche Iodaufnahme ist, umso häufiger entwickelt sich eine Hashimoto-Thyreoiditis bei erblicher Veranlagung. Stimmt diese Aussage ?
[Bearbeiten]Diese Aussage findet sich auf der Internetseite von Prof. Dr. Karl-Michael Derwahl. Wie ist diese Aussage belegt ?
Wie müsste eine Untersuchung ausschauen die den Zusammenhang zwischen Jodierung und Autoimmunerkrankungen der SD klärt?
[Bearbeiten]Man müsste 1000 Patienten mit einer Struma diffusa, die man mit Jod behandeln möchte randomisieren. Eine Hälfte erhält Plazebo, die andere erhält Jodid. Dann schaut man nach ein oder 2 Jahren nach, ob in der behandelten Gruppe die Zahl des Hashimoto- oder des Basedowfälle angestiegen ist. So eine saubere Arbeit existiert wohl bislang nicht. Interessant sind auch Beobachtungen aus Ländern, in den einen generelle Jodierung eingeführt wurde (Schweden, Schweiz etc). Kam es zum Zeitpunkt der Jodierung zu vermehrten Autoimmunerkrankungen?
Eine recht gute Literaturstelle zum Thema ist folgende:
- Th. Rink, H.-J. Schroth, L.-H. Holle, H. Garth:
- Effekte von Jodid und Schilddrüsenhormonen bei der Induktion und Therapie einer Thyreoiditis Hashimoto.
- Nuklearmedizin 1999; 38:144-9
- Effekte von Jodid und Schilddrüsenhormonen bei der Induktion und Therapie einer Thyreoiditis Hashimoto.
Keine Lust mehr Tabletten einzunehmen
[Bearbeiten]Was passiert, wenn ein Patient, der an einer hochgradigen Schilddrüsenüberfunktion gelitten hat (Basedow bekannt), dessen Schilddrüse auch schon radioaktiv zerstört wurde, seine verordneten Schilddrüsen-Tabletten nicht einnimmt?
Antwort: Er bekommt wahrscheinlich innerhalb einiger Wochen eine Schilddrüsenunterfunktion. Das sollte man vermeiden und deswegen sollte er die Tabletten brav weiter einnehmen. Manchmal passiert auch gar nichts, wenn eine ausreichende Restfunktion der eigenen Schilddrüse vorhanden ist.
SD und Gedächtnis
[Bearbeiten]Gibt es einen Zusammenhang zwischen der Gedächtnisleistung und der Funktion der Schilddrüse?
Bereits bei der Hirnreifung im Kindesalter sind die Schilddrüsenhormone beteiligt. Auch eine Schilddrüsenunterfunktion wirkt sich negativ auf das Gedächtnis aus. Auch eine Überfunktion beeinträchtigt das Gehirn meist im negativen Sinne.
SD und Uran
[Bearbeiten]Was hat das Uran mit der Schilddrüse zu tun. Einige Soldaten die im Balkankrieg im Einsatz waren und mit Uranmunition in Kontakt kamen müssen sich Schilddrüsen Untersuchungen unterziehen. warum? was hat die Schilddrüse mit dem Uran zu tun?
Hashimoto und Nebenschilddrüse
[Bearbeiten]Ist von der Hashimoto-Erkrankung auch die Nebenschilddrüse betroffen? Falls ja, was tun?
Bei der Hashimotokrankheit ist die Nebenschilddrüse nicht betroffen. Es gibt allerdings Patienten die mehrere Autoimmunerkrankungen kombiniert haben. Dabei gibt es dann sicher auch den seltenen Fall einer Autoimmunerkrankung der Schilddrüse und der Nebenschilddrüse.
Den Ausfall der Nebenschilddrüse muss man mit der Gabe von AT 10 Dihydrotachysterol oder Rocaltrol behandeln. Zusätzlich wird die Calciumzufuhr erhöht.
Thyroxin zur Kropftherapie
[Bearbeiten]Frage
[Bearbeiten]Ich bin 19 Jahre alt und vor ca. 4 Jahren wurde bei mir eine leichte Kropfbildung festgestellt. Mir wurde daraufhin Jod verordnet. Vor ca. 3 Jahren hat die Kasse dieses dann nicht mehr bezahlt, sodass mein Arzt mir vorschlug, L-Thyroxin einzunehmen, was noch bezahlt wird. So nehme ich nun schon seit 3 Jahren täglich eine halbe L-Throxin 50 (also 25 µg). Meine Mutter hat nun gehört, dass dieses Medikament Gedächtnisstörungen verursachen kann. Ist das Medikament in meinem Fall überhaupt angebracht oder soll ich nicht lieber die "sanftere", (wenn auch teurere Variante), einer Jod-Ergänzung bevorzugen.
Antwort
[Bearbeiten]Das Verhalten Ihrer Krankenkasse ist kurzsichtig und aus medizinischer Sicht falsch.
Es reicht für Sie wahrscheinlich völlig aus, wenn Sie Jodtabletten einnehmen. Diese kosten nicht viel. Machen Sie doch einfach einen Probekauf bei der Apotheke. Sie brauchen kein Rezept.
Aber auch die Einnahme der geringen Menge Thyroxin, die ihr Arzt Ihnen verordnet hat, ist nicht verkehrt. Thyroxin in dieser Dosis bremst etwas die Kropfbildung, macht aber noch keine Überfunktion. Außerdem enthält das Molekül auch Jod. Nach dem Abbau wird das Jod vom Körper auch noch genutzt.
Nennen Sie doch bitte die Quelle, nach der Thyroxin Gedächtnisstörungen verursachen soll. Diese Quelle ist wahrscheinlich falsch. Außerdem sind die Nebenwirkungen des Thyroxins entscheidend von der Dosis abhängig. In der niedrigen Dosis die Sie einnehmen ist eine Überfunktion sehr unwahrscheinlich.
Wichtig ist für Ihre Frage auch die Höhe ihrer Schilddrüsenwerte im Blut.
Jod und Thyroxin kombiniert Wann sinnvoll?
[Bearbeiten]Wann ist die kombinierte Gabe von Jod und Thyroxin sinnvoll?
Die Kombination beider Stoffe ist eigentlich nur selten notwendig. Man kann es geben, wenn unter alleiniger Jodgabe ein Kropf ohne Knoten nicht ausreichend kleiner wird. Meist reicht die alleinige Jodgabe aus.
Bei einer Unterfunktion der Schilddrüse ist Thyroxin notwendig. Die zusätzliche Jodgabe bringt in der Regel nichts.
Offizielle Anwendungsempfehlung laut gelber Liste:
Euthyreote Struma ohne gleichz. Funktionsstör., wenn neben Schilddrüsenhormon eine zusätzl. Iodgabe angezeigt ist. Rezidivprophylaxe nach operierter od. m. Radioiodid behandelter Schilddrüse.
siehe Diskussion zu dieser Seite
Gesamt T3 , Gesamt T4
[Bearbeiten]Viele Labore bestimmen nur noch das Freie T3 und das Freie T4 und bieten Gesamt T3, T4 nicht mehr an. Gibt es dennoch eine Indikation für die Bestimmung von Gesamt T3,T4?
Sind erhöhte Schilddrüsenantikörper immer ein Zeichen einer Krankheit?
[Bearbeiten]Bei einer Blutuntersuchung wurden folgende Werte festgestellt:
- der tsh-wert ist normal.
- TAK 267 ( normal < 100 )
- TPO-AK über 600. ( normal < 80 )
Was kann man aus diesen Werten schlussfolgern?
Antwort:
[Bearbeiten]Vorhandene Antikörper gegen Thyreoglobulin (TGAK) und Thyreoperoxidase (TPO-AK) bedeuten noch nicht, dass eine Autoimmunerkrankung, die vorrangig die Schilddrüse betrifft, vorliegt.
Allerdings ist der Teil der Gesunden, die Antikörper aufweisen, sehr klein. Gelegentlich finden sich Antikörper auch bei anderen Schilddrüsenerkrankungen.
Die Wahrscheinlichkeit ist dennoch hoch, dass sich eine Autoimmunerkrankung (Hashimoto Thyreoiditis, Morbus Basedow) entwickeln kann. Besonders die Hashimoto Thyreoiditis kann auch seronegativ verlaufen. Es sind dann keine Antikörper bzw. keine erhöhten Antikörper nachweisbar.
Die Antikörper stellen eine Reaktion auf den Zerstörungsprozess der Schilddürse dar und sind selbst nicht pathogen.
Erhöhte, und wie im Beispiel deutlich erhöhte Antikörper, belegen dagegen eine Autoimmunerkrankung!
Die Schilddrüsenwerte selbst müssen in dem Zusammenhang jedoch nicht außerhalb der Norm liegen, Symptome können dennoch auftreten. In jedem Fall empfiehlt sich eine Sonographie.
Bei Morbus Basedow müssen zwingend die TRAK (TSH-Rezeptorantikörper) bestimmt werden. Diese sind als einzige der genannten Antikörper pathogen und wohl mitverantwortlich für die Entstehung einer endokrinen Orbitopathie.
Kann eine große Joddosis eine erloschene Schilddrüse reaktivieren?
[Bearbeiten]Vorgeschichte: Ich nahm täglich 100 Mikrogramm L-Thyroxin, wegen Hashimoto-Erkrankung. Dann, nach zweimaligem Herzkatheter mit Kontrastmittel, war der TSH-Wert nicht mehr messbar. Jetzt, neun Wochen später, benötige ich immer noch Carbimazol. Ich bin unsicher bezüglich der weiteren Vorgehensweise, zumal eine KHK besteht. Welche diagnostischen Maßnahmen wären empfehlenswert? CL, Bobingen
Antwort
[Bearbeiten]Die wichtigste Maßnahme in so einer etwas verworrenen Situation heißt:
Kurzfristige Kontrollen von TSH, T3 und T4 und dem entsprechende Anpassung der Therapie. (Kontrollen beispielsweise alle 2 Wochen). Die Therapieanpassung kann in Form einer Reduktion oder Erhöhung der Dosis von Carbimazol erfolgen. Falls sich langsam wieder eine Hypothyreose einstellt muss Carbimazol wieder komplett abgesetzt werden und die Thyroxinsubstitution muss wieder begonnen werden. Die Therapie sollte wegen des Herzens auch durch einen Betablocker zb Bisoprolol 2,5 oder 5 mg pro Tag ergänzt werden. Statt Carbimazol könnte man auch Thiamazol geben.
Die Erklärung für so einen Zustand ist nicht so einfach:
Offensichtlich war die Schilddrüse eben doch noch nicht völlig erloschen. Denn bei einer späten ausgebrannten Hashimotothyreoiditis findet sich eigentlich nur noch narbiges Restgewebe. Da wäre eine Reaktivierung eigentlich unerklärbar.
Es gibt Mischbilder der Hashimoto- und der Basedowerkrankung. Vielleicht liegt so etwas vor. Außerdem kann es im Verlauf der Hashimotoerkrankung vorübergehend auch zu einer Hyperthyreose kommen, allerdings meist am Anfang der Krankheit. Offensichtlich wurde durch die exszessive Jodgabe durch das Kontrastmittel die Entzündung der Schilddrüse noch einmal verstärkt. Eine letzte Möglichkeit besteht noch darin, dass sich zusätzlich zur Hashimotoerkrankung ein autonomes Adenom in der Schilddrüse befindet, welches durch die Jodgabe dekompensiert ist.
Alle Erklärungsversuche ändern aber zunächst einmal nichts am therapeutischen Vorgehen: Kurzfristige Kontrollen von TSH, T3 und T4 und dem entsprechende Anpassung der Therapie.
Vielleicht können Sie Ihre Befunde und den Verlauf weiter in diesem Buch dokumentieren. Das wäre recht interessant.
Weiterer Verlauf nach 7 Monaten
[Bearbeiten]Nach Gabe von Carbimazol 10 mg /d über ca. 2 Monate jetzt nach 7 Monaten wieder Normalwerte von TSH, T3, T4 und wieder Substitution von 50 mikrog L-Thyroxin / Tag
Wie erfolgt die Hormonversorgung mit Schilddrüsenhormonen bei angeborenere Hypothyreose vor der Geburt?
[Bearbeiten]Ist Jodmangel weltweit die häufigste vermeidbare Ursache für geistige Retardierung?
[Bearbeiten]Dies wird im Herold/Innere Medizin 2008 behauptet. Müsste es nicht vielmehr heißen: Die unbehandelte angeborene Hypothyreose ist weltweit die häufigste vermeidbare Ursache für geistige Retardierung. Der Jodmangel führt eigentlich nur in extremen Fällen zu einer Hypothyreose.
Quelle dazu:
Im Abstract sind allerdings auch keine echten Daten genannt.
Wachstumsdynamik heißer Knoten
[Bearbeiten]
Gibt es heiße Knoten, die unkontrolliert aktiv sind und an Hand des TSH Spiegel noch nicht erkennbar sind ?
Die Frage ist für einen einzelnen heißen Knoten leicht zu beantworten: Es hängt einfach von der Größe und Aktivität des heißen Knotens ab.
Ist der Knoten noch sehr klein ( unter 1 cm ), dann sind die Blutwerte noch normal.
Wird der Knoten langsam größer, dann bremst er die restliche SD und der TSH Spiegel sinkt ab. Die T3 und T4 Werte sind zu diesem Zeitpunkt noch normal. Woher die Hypophyse weiß, dass der Knoten vorhanden ist und die TSH Produktion reduziert, das ist bis heute nicht klar. Wahrscheinlich sind die T3, T4 Spiegel über den ganzen Tag betrachtet, eben doch schon etwas zu hoch.
Wird der Knoten noch größer ( so etwa ab 2 - 3 cm ) , dann kann die Hypophyse Ihre Produktion nicht mehr weiter drosseln , die restliche SD ist fast stillgelegt und der heiße Knoten produziert jetzt auch eindeutig messbar zuviel T3 und T4 . Dann muss man den Knoten auch dringend behandeln.
Der zeitliche Verlauf des Wachstums ist dabei sehr langsam und zieht sich meist über mehrere Jahre hin.
Calcitoninspiegel bei jedem kalten Knoten ?
[Bearbeiten]Soll man bei jedem kalten Knoten der Schilddrüse den Calcitoninspiegel bestimmen ?
Jodinduzierte Hyperthyreose
[Bearbeiten]Kann man durch eine hochdosierte Jodgabe wie z.B. die Gabe eines Röntgenkontrastmittels bei einer primär normalen Schilddrüse eine Hyperthyreose auslösen? Gibt es dazu einen überzeugenden Fallbericht? Wie kann man die Wirkung des Jods dabei erklären?
Bei mir wurde durch Jodkontrastmittel eine Hashimoto ausgelöst.
Das würde mich auch interessieren, insbesondere wie eine Schilddrüsenentzündung behandelte wird, die durch Radoiojod ausgelöst wurde. Nach Herzkathederdiagnostik mit Jodkontrastmittel hatte ich 6 Mon. danach eine Haschimoto und weiß nicht wie die behandelt werden kann. Wer weiss was?
Hashimoto heilbar ?
[Bearbeiten]In welchem Prozentsatz der Fälle heilt eine Hashimotothyreoiditis aus ? Was sind die besten Aktivitätsparameter der Erkrankung ?
Wie kann man die zelluläre Aufnahme von T3 blocken ?
[Bearbeiten]Die molekularen Mechanismen der zellulären Aufnahme des Schilddrüsenhormons L-T3 sind unklar. Dies ist einer der Gründe, warum für die effektive Behandlung einer Schilddrüsenüberfunktion durch spezielle Einflussnahme auf die lokale Schilddrüsenhormonwirkung z.B. am Herzmuskel, bisher kein wirksames und beim Menschen einsetzbares Medikament verfügbar ist. Kann man die Aufnahme mit Calciumantagonisten blocken ?
Thiamazol Therapie, TSH Spiegel bei 6
[Bearbeiten]Bei einem Patienten mit Hyperthyreose, der unter einer Therapie mit 5 mg Thiamazol steht, wird bei einer Kontrolle ein TSH Wert von 6 festgestellt. Welche Konsequenz soll aus dem Wert gezogen werden.
Antwort: Offensichtlich ist Thiamazol leicht überdosiert, hat die Schilddrüse zu stark gebremst und eine leichte Hypothyreose verursacht. Dies ist am leicht erhöhten TSH Spiegel erkennbar. Als Konsequenz des Wertes wird man Thiamazol pausieren oder auf 2,5 mg / Tag reduzieren. Weitere Kontrollen des TSH Wertes sind alle 4 Wochen notwendig.
Spezielle Diät zum Gewichtabnehmen bei Sd-Unterfunktion ?
[Bearbeiten]Bei einer jungen Frau wurde eine Schilddrüsenunterfunktion festgestellt. Trotz Tabletten, Diät und Sport kann sie ihr Übergewicht nicht verlieren ? Gibt es eine spezielle Ernährung oder ein paar hilfreiche Rezepte in diesem Fall ?
Antwort: Das Wichtigste bei einer Schilddrüsenunterfunktion ist die dauerhafte und richtig dosierte Einnahme von Schilddrüsenhormonen.
Eine spezielle Diät gibt es wohl nicht. Auch die Frage, ob man jodarm oder jodreich essen soll, ist wahrscheinlich bis jetzt nicht geklärt. Wahrscheinlich spielt die Jodeinnahme keine große Bedeutung mehr, wenn man genügend Thyroxin schluckt. Es bleibt also nichts anderes übrig als viel Sport zu treiben und möglichst wenig zu essen. Dann klappt das schon mit dem Abnehmen. Außerdem kann man die Thyroxindosis so hoch wählen , daß man knapp an die Überfunktion hinkommt, d.h. Daß der TSH Spiegel an der unteren Grenze liegt. Aufpassen muß man dann aber, daß man keine Herzrhythmusstörungen bekommt oder leicht psychisch überdreht wird.
Versehentliche Überdosierung von Thyroxin
[Bearbeiten]Jemand hat eine leichte Schilddrüsenunterfunktion und wird mit einer niedrigen Dosis Thyroxin behandelt. Durch eine zu hohe Dosis ist er in eine Schilddrüsenüberfunktion gekommen. Thyroxin wurde daraufhin pausiert. Nach sieben Tagen verspürt der Patient immer noch Symptome einer Überfunktion. Wie lange dauert es bis Thyroxin sich abbaut ? Wie eng hängt der Thyroxinspiegel mit den subjektiv empfundenen Symptomen zusammen?
Antwort
[Bearbeiten]Das Thyroxin hat im Körper – an Thyroxin-bindendes Globulin gebunden – eine Halbwertszeit von etwa acht Tag. Es kann also schon ein paar Tage dauern bis die Symptome abklingen. Sie können die Symptome durch Betablocker, ein abendliches Schlafmittel und viel Sport reduzieren. Ausserdem sollten Sie die Überfunktion durch Messung ihres Pulses , ihres Blutdrucks, ihrer Körpertemperatur und ihrer Zittrigkeit zb durch eine Schreibprobe jeden Tag dokumentieren. Das ganze ist nicht lebensbedrohlich und wird bald besser werden. Sie können natürlich ihren T4 Spiegel messen und die Überfunktion auch so objektivieren.
Wie steuert man die Thyroxindosis bei der Hypothyreose ? An welchen Parameter soll man sich halten: TSH, T3, T4. ?
[Bearbeiten]Bei einer älteren Frau wird eine Schilddrüsenunterfunktion mit 150 mikrog Thyroxin / Tag behandelt. Sie wird wegen Luftnot und einer Tachyarrhythmie ins Krankenhaus eingeliefert. Im Labor fällt ein unterdrückter sehr niedriger TSH Spiegel auf . Der T4 Spiegel ist leicht erhöht. Der T3 Spiegel ist leicht erniedrigt.
- Liegt hier eine Hyperthyreose vor ?
- Hängt die Tachyarrhythmie mit der Thyroxintherapie zusammen ?
- Wie steuert man die Thyroxindosis bei der Hypothyreose ?
- An welchen Parameter soll man sich bei der Dosierung von T4 halten: TSH, T3, T4. ?
Antwort
[Bearbeiten]Pathologiefragen Schilddrüsenkrebs
[Bearbeiten]In einer Patho-Klausur wurde folgende Frage gestellt:
Welche Aussage trifft zu?
- Beim Schilddrüsenkarzinom findet man
- A) zytologische Besonderheiten wie Milchglaskerne, indirekte Kerneinschlüsse, dachziegelartige Kernlagerung
- (Milchglaskerne ja, Rest nein, daher falsch?)
- B) praktisch keine Knochenmetastasen
- (falsch)
- C) oft Psammomkörper
- (ja, beim papillären SD-CA)
- D)nicht selten einen hochdifferenzierten, an normales Schilddrüsengewebe oder Adenomgeweben erinnernden histologischen Bau
- (stimmt aber meines Erachtens auch..)
- E)üblicherweise keine Thyreoglobulinsynthese und keine Radiojodspeicherung
- (Radioiod stimmt, aber Thyreoglobulin wird gebildet, oder? also auch falsch ?
- A) zytologische Besonderheiten wie Milchglaskerne, indirekte Kerneinschlüsse, dachziegelartige Kernlagerung
Was sind hier korrekte Antworten ?
Die Fragestellung ist ungenau formuliert. Es gibt verschiedene histologische Typisierungen: - differenzierte SD Ca (follikuläres Ca, Papilläres Ca) - medulläres SD-Ca - undifferenziertes SD-Ca Am häufigsten sind die differenzierten Ca die meistens Thyreoglobulin synthetisieren und eine Radiojodspeicherung aufweisen (deshalb auch die elegante Möglichkeit einer Radiojodszintigraphie und -therapie). Die medullären und undifferenzierten Ca haben keine Radiojodspeicherung und keine Thyreoglobulinsynthese. Histologisch gibt es je nach Typ verschiedene Erscheinungsbilder. Also: richtig sind A, C, D
Adressen
[Bearbeiten]Antwort auf Fragen zu Untersuchung und Behandlung bietet das Forum Schilddrüse an: über
- info@forum-schilddruese.de
- forum-schilddruese.de unter http://schilddruese.de/
- telefonisch zwischen 8.00 und 16.00 Uhr unter der Telefonnummer 069/63803727.
Sehr viele Fragen finden sich auch hier:
Man kann in diesem Gästebuch auch seine Fragen eingeben.
Links
[Bearbeiten]- Siehe auch http://www.jodmangel.de/fragen_und_antworten/
- Siehe auch http://www.schilddruesenselbsthilfe.de/forum/index.html
- Siehe auch http://www.forum-schilddruese.de/fragen_antworten.php
- Siehe auch http://www.schilddruesenforum.at/index.php
- Siehe auch http://www.ht-mb.de
Wiederholung und Prüfungsvorbereitung Schilddrüse
[Bearbeiten]Zurück zur Schilddrüse
Wiederholungsfragen zum Thema Schilddrüse
[Bearbeiten]Was versteht man unter T3 ?
Was versteht man unter T4 ?
Was ist ein Hormon ?
An welchen Endorganen entfalten die Schilddrüsenhormone ihre Wirkung ?
Was ist TSH ?
Was ist TRH und wo wird es gebildet ?
Welche Symptome hat man bei einer Überfunktion der Schilddrüse ?
Welche Symptome hat man bei einer Unterfunktion der Schilddrüse ?
Was ist ein kalter Knoten ?
Was ist ein heißer Knoten ?
Was ist ein warmer Knoten ?
Welche Kriterien sprechen für die Bösartigkeit eines Schilddrüsenknotens ?
Was ist eine Thyreoiditis ? Welche Formen gibt es ?
Was ist der Morbus Basedow ?
Was sind Schilddrüsenantikörper ?
Wozu braucht die Schilddrüse Jod ?
Wieviel Jodatome sind im T3 ?
Wieviel Jodatome sind im T4 ?
Wie wird ein Jodmangel festgestellt ?
Wie wird ein Jodmangel behandelt ?
Warum gibt es in der Schilddrüse so viele Knoten ?
Welche Zeichen eines Knoten sprechen für eine Bösartigkeit ?
Warum gab es in der Umgebung von Tschernobyl vermehrt Schilddrüsenkrebs ?
Wie kann man den Schilddrüsenkrebs behandeln ?
Welche Untersuchungsmethoden der Schilddrüse kennen Sie ?
Was ist ft3 und ft4 ?
Was versteht man unter einer Recurrensparese ?
Fallbeispiele
[Bearbeiten]Fall1
[Bearbeiten]Junge Frau, 26 Jahre, stellt sich wegen verdicktem Hals vor, der einer Freundin aufgefallen sei. Sonst habe sie keinerlei Beschwerden. Die Patientin ist 60kg schwer und 162cm groß. Der einzige auffällige Befund in der körperlichen Untersuchung ist die bei Reklination sichtbar verdickte Schilddrüse. Weitere Befunde: Im Ultraschall findet sich ein errechnetes Schilddrüsenvolumen von 32ml (normal 20ml). Im rechten Schilddrüsenlappen sieht man einen echogleichen, kleinen Knoten mit etwa 0.5cm Durchmesser Labor: TSH = 3,5uU/ml innerhalb der Normwerte
Fragen: Welche Diagnose liegt vor? Welche Therapie soll man beginnen? Mit welchem Ziel? Welche Probleme können bei der Therapie auftreten?
Fall2
[Bearbeiten]Eine 77jährige Patientin stellt sich wegen Abgeschlagenheit vor. Zudem sei ihr Gesicht immer so verquollen, vor allem morgens. Die körperliche Untersuchung ergibt eine Sinusbradykardie mit 55/min. Die Patientin wirkt verlangsamt, ihr Gesicht aufgeschwemmt. Routinemäßig bestimmen sie die SD-Werte mit, die Schilddrüse war nicht palpabel: Das TSH ist erhöht, die SD-Hormone reduziert. Zusätzlich fällt im Labor eine deutliche Hypercholesterinämie, sowie eine CK-Erhöhung auf. Die Autoantikörper gegen Thyreoperoxidase sind deutlich erhöht, die gegen TSH-Rezeptor normal. Sie veranlassen ein Sono der Schilddrüse, das eine deutlich echoarme und inhomogene kleine Schilddrüse zeigt.
Fragen: Welche Diagnose liegt vor ? Welche Therapie soll begonnen werden? Welche Laborkontrollen sind notwendig und wann? Welche Komplikationen sind möglich?
Fall3
[Bearbeiten]Bei einer 32-Frau in der 7ten Schwangerschaftswoche wird bei einem Routinescreening ein TSH-Spiegel von 12uU/ml gemessen. Die freien T3 und T4-Werte sind leicht reduziert, die Autoantikörper gegen Thyreoperoxidase sind erhöht, die gegen TSH-Rezeptor normal. Die Schwangerschaft ist bisher komplikationslos verlaufen. Beschwerden hat die Schwangere nicht. Sie hat auch keine Struma.
Fragen: Welche Diagnose liegt vor ? Welche Besonderheiten in der Therapie sind zu beachten im Vergleich mit der Patientin in Fall 2?
Fall4
[Bearbeiten]Eine aufgeregte 37-Jährige kommt in ihre Praxis, die sich deutlich unwohl fühlt: Innerhalb der letzten 2 Monate habe sie ungewollt etwa 7kg Gewicht verloren und wiegt jetzt bei 163 cm Körpergröße 52kg. Sie schwitze vermehrt und sei übernervös. Ihre Hände zittern und zudem habe sie letzte Woche auch noch Durchfall bekommen. Besonders beunruhigt habe sie, dass sie seit drei Tagen beim Autofahren Probleme habe, weil sie Doppelbilder sehe. Vor Ihnen sitzt eine schlanke Patientin mit Fingertremor, Exopthalmus und Struma. Beim Blick nach oben kann der rechte Bulbus nicht folgen. Beim Blick nach unten ist beidseits über der Iris die Sklera zu sehen. Die Konjunktiven sind gerötet, zusätzlich bestehen mäßige Lidödeme. Im Labor ist das TSH nahezu nicht nachweisbar, die freien Schilddrüsenhormonwerte sind erhöht. Autoantikörper gegen Thyreoperoxidase sowie gegen TSH-Rezeptor sind erhöht.
Fragen: Diagnose? Ursache? Therapie?
- Wie ist die Dosierung der Medikamente zu Beginn und im Verlauf einiger Wochen
- Was ist Ihr Behandlungsziel?
- Woran ist eine korrekte Dosierung erkennbar. Was ist die Problematik dabei?
- Welche Nebenwirkungen der Therapie gibt es und wie gehen Sie mit diesen um bzw beugen ihnen vor und welche Laborwerte sind dafür hilfreich?
- Was passiert bei einer Überdosierung?
Fall5
[Bearbeiten]Eine 75-jährige Patientin in deutlich reduziertem Allgemein- und Ernährungszustand wird verwirrt und desorientiert über die Notaufnahme aufgenommen: Sie ist leicht tachykard (105/min) und hat Fieber mit 39,5°C, sowie Durchfälle. Das Labor weist allerdings keinerlei Entzündungszeichen auf, Leukozyten, CRP und Lactat sind normal. Dagegen sind die freien SD-Werte stark erhöht (fT3 16ng/l, fT4 20ng/l), das TSH ist <0,01uU/ml, die Schilddrüsensonographie zeigt eine mäßig vergrößerte Struma nodosa.
Frage: Welche Verdachtsdiagnose? Wie Therapieren sie und was sind dabei Gemeinsamkeiten und die Unterschiede zu Fall 4?
Lösungsvorschläge zu den Fallbeispielen
[Bearbeiten]Fall1
[Bearbeiten]- Diagnose: Struma nodosa euthyreot, wahrscheinlich ein Jodmangelstruma
- Therapie: L-Thyroxin und Jod zur Verkleinerung der Struma
- Thyroxin: 1-1,5ug x kg Kgew → Beginn mit 50 oder 75ug, Zieldosis: 60 bis 90ug, abhängig von der Klinik der Patientin → Laborkontrolle: nach 4-6 Wo TSH, bei UAW natürlich früher
- Jod: Bedarf 100-200ug → Überdosierung kaum möglich
- Ziel: Verkleinerung der Struma durch Thyroxin- und Jod-Kombitherapie, halbjährliche Kontrollen des Sonobefunds und TSH, bei Remission Auslassversuch, ausschleichen nicht notwendig
- Probleme: Die Dosierung des Thyroxin muss herabgesetzt werden, sobald der Patient hyperthyreoseartige Nebenwirkungen wie Durchfall, Herzrasen etc. Thyroxin darf zudem nur nüchtern, nur mit einem Schluck Wasser eine halbe Stunde vor dem Frühstück eingenommen werden, sonst ist die Resorption evtl gestört.
Fall2
[Bearbeiten]- Diagnose: ausgeprägte Hypothyreose bei Hashimoto-Thyreoiditis
- Therapie: L-Thyroxin 1-1,5ug x kg Kgew → Beginn mit 50ug und aufbau zur Zieldosis: abhängig von der Klinik und unter Kontrolle des TSH
→ kein Jod notwendig, triggert evtl den Autoimmunprozess
- welche Laborkontrollen wann: 4 bis 6 Wochen nach Therapiebeginn TSH Kontrolle, wenn eingestellt ½ bis jährliche Kontrollen des TSH und der Hormonwerte, Dosis immer an Klinik der Patientin orientieren
- Komplikationen: Arzneimttel UAW bei zu hoher Dosierung des Thyroxins. Assoziiert mit Hashimoto sind andere Autoimmunerkrankungen wie Diabetes oder CEDs wahrscheinlicher
Fall3
[Bearbeiten]- Diagnose: Hashimoto bedingte Hypothyreose in der Schwangerschaft,
- Therapie und Besonderheiten:
Thyroxin in 'Schwangerendosis' also mindestens 1,5ugx kg Kgew, sollten zügig erreicht werden → schnell aufdosieren und nach 14 Tagen kontrollieren, danach bis zur 20ten Woche alle 4 Wochen Kontrolle und ggf Anpassung der Thyroxindosis, im 3ten Trimenon sinkt der Bedarf wieder etwas. Betreuung durch Endokrinologen anstreben, die kritischste Phase für das Kind ist das erste Trimenon, aber T3 ist in jeder Entwicklungsphase wichtig. TSH: im 1.Trimenon TSH < 2,5uU/ml im 2. und 3.Trimenon TSH < 3,5uU/ml in Ordnung, insgesamt sollte das TSH im unteren Normbereich sein Jod: ist trotz Hashimoto hier empfohlen, nicht aber bei Patientinnen die Kinderwunsch haben und noch nicht schwanger sind
- Nach der Schwangerschaft: muss die Dosis des Thyroxin an das nun verminderte Gewicht angepasst werden, sonst droht der Mutter eine Überdosierung, das Jod sollte abgesetzt werden.
Fall4
[Bearbeiten]- Diagnose: Hyperthyreose vom Typ Basedow mit endokriner Orbitopathie
- Ursache: Antikörper gegen den TSH-Rezeptor der Schilddrüsen-Zellen → stimulierung, wachstum und Hormonausschüttung vermehrt
- welche weitere Diagnostik: Augenärztliche Vorstellung zur Therapie der Orbitopathie, denn diese kann auch nach besserung der Hyperthyreose beststehen bleiben
- Therapie: Thyreostatika, Thiamazol (1,6fach potenter) oder Carbimazol
- Wie ändert sich die Dosierung im Verlauf:
Thiamazol: → Einstieg mit 20 oder 40mg abhängig von Schwere, hier 40mg, also 20mg 2-0-0, kein Einschleichen Carbimazol: 60mg, Problem hierbei ist die geringe dosis pro Tablette (10mg) also 6-0-0 → sobald TSH und die Hormonwerte im Normbereich sind oder die Dynamik des Werteabfalls einen weiteren erwarten lässt, kann mit der Dosisreduktion begonnen werden, um die Therapie wenn mit möglichst kleiner Erhaltungsdosis durch zu führen. → nach c.a. 1 Jahr sollte spätestens ein sukzessiver Auslassversuch erfolgen Ist der Auslassversuch nicht erfolgreich, sollte sich der Patient überlegen, eine definitive Therapie durchführen zu lassen, mit Radiojod oder Thyreodektomie.
- Woran korrekte Dosierung messbar und welche Problematik dabei? Zu Beginn alle 2 Wochen, dann in etwas größeren Abständen TSH, T4 und T3 bestimmen. Problem: die Hormonwerte entwickeln sich zu Beginn von Patient zu Patient unterschiedlich schnell und können bei der gleichen Dosis beim nächsten Mal schon zu stark supprimiert sein → Dynamik mitbeurteilen
- Welche Nebenwirkungen der Therapie und welche Laborwerte regelmäßig kontrollieren:
Schwerste Nebenwirkung ist die Agranulozytose, deswegen immer BB Kontrollen wenn TSH Kontrolle und Patienten über Warnsymptome (vermehrte Infektentwicklung) aufklären. Problem: der Abfall der Granulozyten verläuft u.U schlagartig, weswegen die BB-Kontrollen vorher auch ganz normal sein können. Des Weiteren sollten immer auch die Leberwerte mit kontrolliert werden, da die Leberfunktion unter Therapie gestört werden kann, Allergien sind auch möglich.
- Was tun bei UAW? Bei Agranulozytose müssen die Medikamente sofort abgesetzt werden, bei einem hohen Hyperthyreoserisiko kann überbrückend Perchlorat oder Lithium gegeben werden, ansonsten sollte man sobald wie möglich eine Radiojodtherapie oder Op anstreben.
- Gefahr bei Überdosierung? Hypothyreose-Symptome: Obstipation, Müdigkeit, etc, aber auch Leberschädigung
- Cave: Kontraindikation von Thyreostatika in der Schwangerschaft, hier früher Propylthiouracil empfohlen
Fall5
[Bearbeiten]- Diagnose: Autonomie
- Therapie: Thyreostatika (Thiamazol 20 oder 40mg) nur überbrückend, ziel ist entweder eine RJT oder die OP sobald als möglich.
- welche Laborkontrollen wann: zügig nach Einstieg Kontrolle (2-3 Wo), sobald TSH und die Hormonwerte im Normbereich sind oder die Dynamik des Werteabfalls einen weiteren erwarten lässt, kann mit der Dosisreduktion begonnen werden, um die Therapie wenn mit möglichst kleiner Erhaltungsdosis durch zu führen.
- Komplikationen: siehe Fall 4
Bücher und Zeitschriften zum Thema Schilddrüse
[Bearbeiten]Zurück zur Übersicht

Bücher
[Bearbeiten]Patientenratgeber
[Bearbeiten]Es gibt eine Vielzahl guter Patientenratgeber . Einer ist hier genannt.
- Krankheiten der Schilddrüse --Ratgeber Schilddrüse--
- Mödder, Gynter
- 3., aktualisierte u. erw. Aufl., 2003, VIII, 176 S., 43 illus., 3 in Farbe, Softcover
- ISBN: 978-3-540-43423-8
- Mödder, Gynter
Fachbücher
[Bearbeiten]- Schilddrüsenkrankheiten - Diagnose und Therapie
- Prof. Dr. med. P. Pfannenstiel, Prof. Dr. med. L.A. Hotze und Dr. med. B. Saller
- 4. neu bearbeitete und erweiterte Auflage, 382 Seiten Berliner Medizinische Verlagsanstalt, 1999
- ISBN 3-88040-206-X
- Gut lesbar, umfassend, ein Klassiker
- Prof. Dr. med. P. Pfannenstiel, Prof. Dr. med. L.A. Hotze und Dr. med. B. Saller
- Die Schilddrüse in Klinik und Praxis
- von Fritz Spelsberg (Autor), Thomas Negele (Autor), Michael M. Ritter (Autor)
- Preis: EUR 69,95
- Gebundene Ausgabe: 214 Seiten
- Verlag: Karl F. Haug Fachbuchverlag (Mai 2000) ISBN-10: 3830450133 ISBN-13: 978-3830450139
- Thyroid Disease: A Case-based and Practical Guide for Primary Care
- von Brams (Autor)
- 168 Seiten Verlag: Springer, Berlin; Auflage: 1 (30. August 2005)
- Sprache: Englisch ISBN-10: 1588295346 ISBN-13: 978-1588295347
- Thyroid Cancer
- von H.-J. Biersack (Autor), F. Grünwald (Autor)
- "Two of the main features of thyroid malignancy are its rarity and its excellent prognosis in the overwhelming number of cases ..." (mehr)
- Preis: EUR 139,05
- Gebundene Ausgabe: 363 Seiten Verlag: Springer, Berlin; Auflage: 2nd ed. (Juni 2005)
- Sprache: Englisch ISBN-10: 3540223096 ISBN-13: 978-3540223092
- Atlas der Schilddrüsenchirurgie. Ein chirurgisch-klinisches Lehrbuch
- von Ernst Gemsenjäger (Autor)
- Preis: EUR 57,95 Gebundene Ausgabe: 146 Seiten
- Verlag: Huber, Bern; Auflage: 1 (April 2005)
- Sprache: Deutsch ISBN-10: 3456841035 ISBN-13: 978-3456841038
- Schilddrüse 2005: Henning-Symposium, 17 - Konferenz Uber Die Menschliche Schilddruse
- von Rainer Hehrmann (Autor), Oswald Ploner (Autor)
- Preis: EUR 84,00
- 450 Seiten Verlag: Gruyter; Auflage: 1. A. (Juli 2006)
- Sprache: Deutsch ISBN-10: 3110189410 ISBN-13: 978-3110189414
- Hauptthema war die Hypothyreose
- Radiojodtherapie.Bei benignen und malignen Schilddrüsenerkrankungen. 1999. X, 142 S. m. 51 z.
- Bell, Eberhard; Grünwald, Frank:
- Tl. farb. Abb. 24 cm. Gebunden. 412gr. ISBN: 3-540-65913-7, -SPRINGER, BERLIN-49.95 EUR
- Bell, Eberhard; Grünwald, Frank:
Ältere Bücher, immer noch interessant zu lesen
[Bearbeiten]- Die Krankheiten der Schilddrüse (Gebundene Ausgabe)
- von Karl Oberdisse (Autor), Erich Klein (Autor), Dankwart Reinwein (Autor)
- Gebundene Ausgabe: 664 Seiten
- Verlag: Thieme; Auflage: 2.überarb. u. erw. Aufl. (1980)
- ISBN-10: 3133836021 ISBN-13: 978-3133836029
Ein sehr umfassendes Schilddrüsenbuch aus dem Jahr 1980. Aus heutiger Sicht fehlt natürlich einiges. Trotzdem teilweise noch sehr spannend zu lesen.
Zeitschriften
[Bearbeiten]- THYROID
- Organ der American Thyroid Association
- CLINICAL THYROIDOLOGY
- Klinische Schilddrüsenforschung Online
- Nuklearmedizin
- Schattauer Verlag
- Organ der Deutschen Gesellschaft für Nuklearmedizin, Organ der Österreichischen Gesellschaft für Nuklearmedizin, Organ der Schweizerischen Gesellschaft für Nuklearmedizin, Journal of the German, Austrian and Swiss Societies of Nuclear Medicine
- Allgemeine Daten:2007 Band 46 (6 Hefte jährlich) ISSN 0029-5566
- Schriftleiter: O. Schober (verantwortlich)
- Sektionseditoren:
- Chr. Eilles (Endokrinologie, Gesundheitsökonomie)
- Schattauer Verlag
- Ultraschall in der Medizin
- European Journal of Ultrasound
- The American Thyroid Association
- The Journal of Nuclear Medicine
- European Journal of Nuclear Medicine
- New England Journal of Nuclear Medicine
- Clinical Nuclear Medicine
- Nuclear Medicine Communications
- Nuklearmedizin
- Thyroid
- Clinical Endocrinology & Metabolism
- Endocrine Reviews
- European Journal of Endocrinology
- Clinical Endocrinology
- Radiology
- RadioGraphics
- Radiological Society of North America
- Radiography
- American Journal of Roentgenology
- Seminars in Nuclear Medicine
Referiert
[Bearbeiten]Links zum Thema
[Bearbeiten]Zurück zur Übersicht

Links zum Thema Schilddrüse
[Bearbeiten]Wikipedia
[Bearbeiten]Deutsch
[Bearbeiten]- Sehr gute SD Seite – Prof. Dr. Hotze
- Umfassendes Schilddrüsenportal
- Gutes Teamwork: Info's zu SD-Erkrankungen von Ärzten & Patienten, Special: alternative Therapien
- links und Infos sowie eine Arztübersicht
- Prof. Dr. Mödder
- Sehr übersichtliche Seiten zum Thema SD – Dr. Proschek
- Forum Schilddrüse
- Infoline Schilddrüse
- Hashimoto Forum
- Infos zu Hashimoto und der Nebennierenschwäche
- Spezielle SD-Infoseiten für Ärzte
- Umfangreiches SD-Portal
- Netdoktor Hyperthyreose
- Netdoktor Hypothyreose
- Überblickseiten zum Schilddrüsenkrebs von der Deutschen Krebshilfe
- Das Wartezimmer
- Selbsthilfe-Forum für Schilddrüsenkrebs - Ohne Schilddrüse leben e.V.
- Beschäftigt sich vor allem mit Schilddrüsenkrebs
- Schöne Übersicht zum Thema SD-Feinnadelbiopsie
- Aufklärung vor SD-Operationen mit schönen Bildern
- Elektronenmikroskopische Bilder der Schilddrüse
- Firma Merck
- Firma Henning
- Firma Sandoz
- Schilddrüsenliga
- SD-Selbsthilfe Bodensee
- Selbsthilfegruppe für autoimmune SD-Erkrankungen Österreich
- Der Verein "Die Schmetterlinge e. V." kümmert sich um schilddrüsenkranke Kinder und deren Eltern und/oder Angehörigen.
- Netzwerk und Informationsportal von Patienten
- SHG Bielefeld
- Laborwerte SD
Englisch
[Bearbeiten]- http://www.thyroidmanager.org/
- Komplettes Online Lehrbuch über die Schilddrüse in Englisch
- http://www.thyroid.about.com/health/thyroid/
- http://www.meddean.luc.edu/lumen/MedEd/medicine/endo/thyroid/thycont.htm
- http://www-med.stanford.edu/school/DGIM/Teaching/Modules/hypothyroidism.html
- http://thyroid.miningco.com
- http://www.thyroid.com
- http://www.thyroid.org
- http://www.cf.ac.uk/uwcm/md/ETA.html
- http://www.glandcentral.com
- http://www.synthroid.com
- http://www.icb2.usp.br/~lats
- http://xanadu.mgh.harvard.edu/receptor/trrfront.html
- http://www.thyroid.org/journal/journal.htm
- http://www.med.Virginia.EDU/~jtd/iccidd
- http://www.io.com/thyroid
- http://www.Emissary.Net/thyroid/thyrbc.html
- http://www.hsc.missouri.edu/medicine/thyroid/thyindex.html
- https://www.lats.org/index.asp
- Latin American Thyroid Society - Südamerikanische Schilddrüsen Gesellschaft
- Beverly
- http://www.thyroid-info.com
- (Hashimoto Encephalopathy, USA)
- http://www.thyroid-info.com
- Dawn:
- Gail:
- Graham:
- Janie:
- Lyn:
- Mary (Shomon)
- http://thyroid.about.com (USA)
- Nora (Norway)
- Sheila
- http://tpa-uk.org.uk (UK)
Französisch
[Bearbeiten]
Patientenseiten
[Bearbeiten]- Ansgar:
- Ben:
- Dagi (Flensburger SHG)
- Hans:
- Inken:
- http://www.hashimoto-selbsthilfe.de (Bielefelder SHG)
- Kerstin:
- Kro: Schweizer SHG
- Leni:
- Maria: Grazer SHG
- Natascha:
- Nicole:
- Nirvana:
- Norbert:
- Rita:
- Susanne:



















