Medizinische Mikrobiologie: Arenaviridae
Arenavirus
[Bearbeiten]Lassa-Virus
[Bearbeiten]| Lassa-Virus | ||||||||||
|---|---|---|---|---|---|---|---|---|---|---|
 | ||||||||||
| Systematik | ||||||||||
| ||||||||||
| Morphologie | ||||||||||
| umhüllt, helikal | ||||||||||
Das Lassafieber ist eine meldepflichtiges virales hämorrhagisches Fieber. Es wurde 1969 zum ersten Mal beschrieben, als in Nigeria eine amerikanische Missionsschwester starb, eine weitere erkrankte und zur Behandlung in die USA ausgeflogen wurde. Das Virus wurde nach der Stadt Lassa benannt, in der die erste Krankenschwester gearbeitet hatte. In New York City traten unter Wissenschaftlern, die das Virus isolierten, zwei Laborinfektionen auf, einer der Infizierten ist infolge der Erkrankung verstorben.
Erreger: Der Erreger des Lassa-Fiebers ist ein behülltes Einzel(-)Strang-RNA-Virus mit hoher Virulenz und gehört zu Gattung Arena-Virus (Familie Arenaviridae). Zur selben Virenfamilie gehören auch die Erreger des Junin-Fiebers und des Machupo-Fiebers. Sie alle werden der höchsten biologischen Sicherheitsstufe 4 zugeordnet. Vom Lassa-Virus sind bisher vier serologische Subtypen bekannt: Typ Nigeria, Sierra Leone, Liberia und Typ Zentralafrikanische Republik.
Serologische Daten lassen vermuten, dass zumindest in Westafrika etwa 90 bis 95% aller Infektionen inapparent verlaufen könnten.
Als natürlicher Reservoirwirt für das Lassa-Virus ist neben anderen Kleinnagern hauptsächlich die Natal-Vielzitzenmaus (Mastomys natalensis) festgestellt worden.
Vorkommen: Man findet das Lassa-Virus endemisch in den westafrikanischen Ländern Senegal, Gambia, Mali, Guinea, Liberia, Sierra Leone, Elfenbeinküste, Ghana, Burkina Faso und Nigeria. Daneben ist es auch in weiteren tropischen Ländern wie der Zentralafrikanische Republik und Namibia festgestellt worden. In den genannten Gebieten sind bis zu 15% der Vielzitzenmäuse mit dem Virus infiziert. Verwandte nicht-humanpathogene Viren gibt es auf dem ganzen afrikanischen Kontinent.
Übertragung: Das Lassa-Virus wird durch die in afrikanischen Häusern weit verbreitete Natal-Vielzitzenmaus (Mastomys natalensis) per Kontaktinfektion bzw. Schmierinfektion über die Ausscheidungen der Tiere auf anschließend vom Menschen verzehrte Lebensmittel übertragen. Daneben können die Viren auch über Tröpfcheninfektion, Wundinfektion und durch Sekrete direkt von Mensch zu Mensch wie auch durch Geschlechtsverkehr übertragen werden. Vor dem Krankheitsausbruch ist lediglich über das Blut eine Übertragungsmöglichkeit durch infizierte Menschen festgestellt worden.
Bisher ging man von einem saisonalen Anstieg der Inzidenz während der Trockenzeit von Januar bis März aus. In Sierra Leone hingegen wurde ein Epidemiegipfel im Übergang zur Regenzeit (Mai bis November) beobachtet.
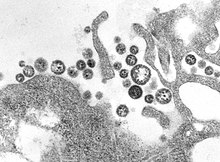
Diagnose: Testung auf Erreger in der Rachenspülflüssigkeit, im Pleura- oder Aszitespunktat oder durch Titeranstieg in der Komplementbindungsreaktion. Diese Untersuchungen sind nur in Labors mit speziellen Sicherheitseinrichtungen durchführbar.
Differentialdiagnostisch kommen Malaria, Influenza, Typhus und septisches Fieber in Frage.
Krankheitsverlauf/Symptome: Die Inkubationszeit des Lassa-Fiebers beträgt zwischen 6 und 21 Tagen, meist 7 bis 10 Tage.
Nach einem schleichendem Krankheitsbeginn mit Abgeschlagenheit, grippeähnlichen Muskel- und Gliederschmerzen, Übelkeit und Kopfschmerzen entsteht ein Dauerfieber (Kontinuafieber) von ca. 40°C. Ab dem 3. bis 7. Tag stellen sich zuerst Entzündungserscheinungen im Rachen ein später dann weißliche Plaques und Ulzerationen. Die Patienten sind stark allgemeinreduziert und apathisch. Die Zervikallymphknoten sind vergrößert und druckdolent.
Ab dem 7. Tag entsteht oft ein makulo-papulöses Exanthem (fleckiger Hautausschlag mit kleinen erhabenen Knötchen) im Gesicht, am Hals und an den Armen beginnend, das sich dann auf den ganzen Körper ausbreitet. Um die gleiche Zeit treten kolikartige Bauchschmerzen auf, der Stuhl ist von breiiger Konsistenz bis hin zu Durchfall. Erbrechen ist aufgrund des schlechten Allgemeinzustandes möglich. Gelegentlich kommt es zur generalisierten Lymphknotenschwellung. Die Krise tritt zwischen dem 7. und 14. Tag ein. Die Nahrungsaufnahme ist wegen der Ulzerationen und Schwellungen erschwert; auch die Atmung kann beeinträchtigt sein. Die meisten Patienten weisen eine Hepatosplenomegalie auf. Zur hämorrhagischen Diathese kommt es aufgrund der verminderten Gerinnungsfaktoren bei normaler Thrombozytenzahl und erhöhter Permeabilität der Kapillaren durch Wandschädigungen. Auf die Nierenbeteiligung weisen eine Proteinurie und Mikrohämaturie hin. Nach einer kurzen Entfieberung nach dem 5.-7. Tag kann es zu einem neuerlichen Fieberanstieg nach weiteren 3-5 Tagen kommen. Die Prognose ist ernst und die Letalität liegt für hospitalisierte Patienten bei etwa 15%, bei schwangeren Frauen bei etwa 50%.
Komplikationen: Zwischen dem 5. und 8. Tag des Ausbruchs des Lassa-Fiebers stellt die hämorrhagische Diathese eine gefürchtete Komplikation dar. Des Weiteren die Pneumonie, unter Umständen mit Begleitpleuritis und Erguß. Sie tritt häufig in der zweiten Woche auf und ist in einigen Fällen die Todesursache gewesen. Zu nennen sind noch Meningismus, Verwirrtheitszustände, Benommenheit. Die Rekonvaleszenz ist deutlich verzögert und Kreislaufprobleme können noch lange nach der Erkrankung anhalten.
Therapie: Eine spezifische Therapie ist nicht bekannt. Innerhalb der ersten sechs Tage der Erkrankung war das Virostatikum Ribavirin (oral, intravenös oder als Immunplasma) erfolgreich. In anderen 6 Fällen wurde Rekonvaleszentenserum gegeben, welches bei 5 dieser 6 Fälle ebenfalls erfolgreich war. Bei Ebola-Fieber reduziert die Gabe von Humanplasma mit ebolaspezifischen Antikörpern die Virämie. Dazu kommen fiebersenkende Mittel und die intensivmedizinische Überwachung und Versorgung.
Vorbeugung: Gegen die Erkrankung existiert bislang keine Schutzimpfung zur Vorbeugung, an der Entwicklung eines Impfstoffes wird jedoch gearbeitet.[1]
Zur Verhinderung einer Infektion sind allgemeine Hygieneregeln zu beachten und ein enger, ungeschützter Umgang mit erkrankten Personen und deren Körperausscheidungen zu vermeiden.
Statistik: Schätzungen zufolge kommen in Westafrika jedes Jahr etwa 100.000-300.000 Fälle von Lassa-Fieber vor, etwa 70% verlaufen subklinisch. Die Sterblichkeitsrate rangiert zwischen 2% in den Dörfern, 16% in den Krankenhäusern und 30% bei schwangeren Frauen. In Westafrika kam es mehrfach zu Ausbrüchen in Krankenhäusern vor allem in Nigeria, Liberia und Sierra Leone häufig mit Todesfällen unter dem medizinischen Personal.
Gesetze: Nach § 6 Meldepflichtige Krankheiten des IfSG sind virusbedingte hämorrhagische Fieber mit Namen meldepflichtig.
Literatur und Weblinks:
Lymphozytisches Choriomeningitis-Virus (LCMV)
[Bearbeiten]| Lymphozytisches Choriomeningitis-Virus | ||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Systematik | ||||||||||||
| ||||||||||||
| Morphologie | ||||||||||||
| umhüllt, helikal | ||||||||||||
Krankheitsbilder: Das LCM-Virus kann bei Immunkompetenten eine leichte bis mittelschwere, meist unkomplizierte virale Meningitis auslösen. Bei Immunsupprimierten kann die Infektion zum Tode führen. Erregerreservoir ist die Hausmaus, allerdings können auch andere Nager wie z.B. Hamster und Meerschweinchen infiziert sein und das Virus mit dem Urin ausscheiden. Das New England Journal of Medicine berichtet 2006 von 8 Organtransplantierten, die sich in zwei Clustern über eine Organspende infiziert hatten und von denen 7 Patienten zwischen dem 9. Tag bis zweieinhalb Monate nach Organerhalt verstorben sind. Bei einem der zwei Organspender konnte ein LCMV-positiver Hamster als Infektionsquelle eruiert werden.
Standardmäßig werden Organspender auf Syphilis, HIV, HBV und HCV getestet, für LCMV gibt es keinen geeigneten Schnelltest. Daher sollte in der Anamnese nach entsprechenden Haustieren gefragt werden, aufgrund des Spendermangels wäre dies allerdings keine absolute Kontraindikation für eine Explantation.[2]
Quellen
[Bearbeiten]- ↑ Forschungsbericht: Charakterisierung der zellulären und humoralen Immunantwort bei der humanen Lassavirusinfektion
- ↑ Fischer SA et al. “Transmission of lymphocytic choriomeningitis virus by organ transplantation.”. N Engl J Med, 354(21):2235-49, May 25 2006. PMID:16723615
