Medizinische Mikrobiologie: Rhabdoviridae
Rhabdoviridae
[Bearbeiten]| Rhabdoviridae | ||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Systematik | ||||||||||||
| ||||||||||||
| Morphologie | ||||||||||||
| umhüllt, helikal | ||||||||||||

Viren der Familie Rhabdoviridae (griech. rhabdos = Stab) . All diese Viren sind behüllte Einzel(-)Strang-RNA-Viren mit meist stäbchen- oder geschossförmiger Gestalt.
Systematik: Zu den Rhabdoviren gehören die Gattungen Vesiculovirus, Lyssavirus, sowie Cytorhabdovirus, Ephemerovirus, Novirhabdovirus und Nucleorhabdovirus.
Zu den Vesiculoviren gehört das Vesicular-Stomatitis-Virus (VSV), welches bei Tieren die Stomatitis vesicularis (Mundschleimhautentzündung mit Bläschenbildung) auslöst und auch auf den Mensch übertragbar ist.
Lyssavirus
[Bearbeiten]| Lyssavirus | ||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
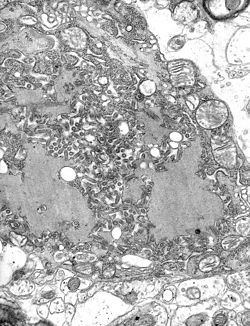 | ||||||||||||||||||||||||
| Systematik | ||||||||||||||||||||||||
| ||||||||||||||||||||||||
| Morphologie | ||||||||||||||||||||||||
| umhüllt, helikal | ||||||||||||||||||||||||
Zu den Lyssaviren gehört das bei Tier und Mensch die Tollwut verursachende Rabiesvirus, das australische Fledermaus-Lyssavirus, das Duvenhage-Virus, zwei europäische Fledermaus-Lyssaviren, das Lagos-Fledermausvirus, sowie das Mokola-Virus.
Tollwut ist eine seit Jahrtausenden bekannte Virusinfektion, die bei Tieren und Menschen eine akute lebensbedrohliche Enzephalitis (Gehirnentzündung) verursacht. Synonyme sind die Begriffe Lyssa, Rabies und Rage. Früher benutzte man auch das Synonym Hydrophobie (Wasserfurcht).
Das Virus kann die meisten warmblütigen Tiere betreffen, ist aber unter Nicht-Fleischfressern selten. Das stereotypische Bild eines infizierten („tollwütigen“) Tieres ist der „verrückte Hund“ mit Schaum vor dem Mund, aber auch Katzen, Frettchen, Füchse, Dachse, Waschbären, Backenhörnchen, Stinktiere und die Fledertiere - Vampire-Fledermaus (Desmodus rotundus bzw. Desmodus sp.); bei insektenfressenden Fledertieren meist Fledermäuse (Microchiroptera) und fruchtfressenden Fledertieren meist Flughunde (Megachiroptera sehr selten) - können tollwütig werden beziehungsweise die klassische Tollwut oder eine andere Form übertragen. Hauptüberträger ist der Fuchs. Eichhörnchen, andere Nagetiere und Kaninchen werden sehr selten infiziert. Vögel bekommen sehr selten Tollwut, da ihre Körpertemperatur höher liegt als es für eine optimale Vermehrung des Virus notwendig ist. Tollwut kann sich auch in einer so genannten „paralytischen“ Form zeigen, bei welcher sich das angesteckte Tier unnatürlich ruhig und zurückgezogen verhält.
Zwischen 40.000 und 70.000 Menschen sterben jährlich an Tollwut, die meisten in Osteuropa, Asien (80%) und Afrika, wo Tollwut endemisch ist. Die Hälfte der Todesfälle weltweit betrifft Kinder und Jugendliche unter 15 Jahren.[1] Ungefähr 10 Millionen Menschen werden jährlich behandelt nach einem Verdacht, sich der Tollwut ausgesetzt zu haben.[2]
Erreger: Die Tollwut wird durch geschossförmige, behüllte Einzel(-)Strang-RNA-Viren, der Gattung Lyssaviren aus der Familie der Rhabdoviridae verursacht. Derzeit werden sieben Genotypen unterschieden:
- Genotyp 1: Rabiesvirus (RABV) = Tollwutvirus. Dieses Virus ist das klassische Tollwutvirus.
- Genotyp 2: Lagos-Fledermausvirus = Lagos bat virus (LBV)
- Genotyp 3: Mokola-Virus (MOKV)
- Genotyp 4: Duvenhage-Virus (DUVV)
- Genotypen 5 und 6: Europäisches Fledermaus-Lyssavirus = European bat lyssavirus (EBLV 1, 2)
- Genotyp 7: Australisches Fledermaus-Lyssavirus = Australian bat lyssavirus (ABLV)
Ausgenommen Genotyp 2 sind bei allen anderen oben aufgezählten Genotypen Tollwutfälle beim Menschen beschrieben.
Alle bekannten Tollwutviren werden durch Trockenheit, Sonnenlicht und bestimmte Desinfektionsmittel sehr schnell inaktiviert.

Übertragung: Das Virus ist im Speichel eines tollwütigen Tieres vorhanden, der Infektionsweg führt fast immer über Bissverletzungen. Aber auch kleinste Verletzungen der Haut und Schleimhäute können das Eindringen des Virus per Schmier- bzw. Kontaktinfektion ermöglichen. Außer bei der Organtransplantation (3 Fälle in den USA zu Beginn des Jahres 2004 und 3 Fälle in Deutschland Anfang 2005), ist die Übertragung von einer Person zur nächsten bislang nicht beobachtet worden.
Krankheitsverlauf und Symptome: Das Virus dringt im Wundgebiet in die peripheren Nerven ein und wandert Richtung ZNS. Sollte das Virus durch den Biss direkt in die Blutbahn gelangen, kann es das Zentralnervensystem auch sehr schnell erreichen. Nur während der mehr oder minder langen Frühphase, ist noch eine Impfung möglich. Sobald das Virus in die Nerven eingedrungen ist, ist eine Impfung nicht mehr wirksam.

Die Periode zwischen der Infektion und den ersten grippeartigen Symptomen (Inkubationszeit), kann bis zu zwei Jahre dauern, normalerweise sind es jedoch 3 bis 12 Wochen. Es wurden jedoch auch Inkubationszeiten von bis zu 10 Jahren glaubhaft dargelegt.
Das Virus verursacht eine Enzephalitis mit den typischen Symptomen. Eine Myelitis (Rückenmarksentzündung) ist ebenfalls möglich. Bei der Übertragung durch einen Biss in Arm oder Bein äußern sich häufig zuerst Schmerzen an der gebissenen Extremität. Sensibilitätsverlust entsprechend der Hautdermatome ist regelmäßig beobachtet worden. Daher werden viele, vor allem atypische Krankheitsverläufe, zunächst als Guillain-Barré-Syndrom falsch eingeschätzt. Bald danach steigern sich die zentralnervösen Symptome, wie Lähmungen, Angst, Verwirrtheit, Aufregung, weiter fortschreitend zum Delirium, zu anormalem Verhalten, Halluzinationen, und Schlaflosigkeit. Die Lähmung der hinteren Hirnnerven (Nervus glossopharyngeus, Nervus vagus) führt zu einer Rachenlähmung, verbunden mit einer Unfähigkeit zu sprechen (bei Hunden "heiseres Bellen") oder zu schlucken - dies ist während späterer Phasen der Krankheit typisch. Die Schluckstörung wird fälschlicherweise auch als "Hydrophobie" bezeichnet. Auch der produzierte Speichel kann nicht mehr abgeschluckt werden und bildet den Schaum vor Mund oder Maul.
Die Erkrankung kann auch in der "stummen" Form verlaufen, bei der ein Teil der genannten Symptome fehlt. Jedoch findet sich unabhängig von der Verlaufsform bei der Bildgebung mit dem Kernspintomographen eine Aufhellung in der Region des Hippocampus und am Nucleus Caudatus. Fast immer tritt 2 bis 10 Tage nach den ersten Symptomen der Tod ein.
Krankheitsverlauf beim Tier: Nach einer Inkubationszeit von meist 2 bis 8 Wochen treten die ersten Symptome auf und nach 1-7 Tagen tritt der Tod ein.
Erkrankte Haushunde können dabei besonders aggressiv und bissig werden, sind übererregt, zeigen einen gesteigerten Geschlechtstrieb und bellen unmotiviert („rasende Wut“). Später stellen sich Lähmungen ein, die zu heiserem Bellen, Schluckstörungen (starkes Speicheln, Schaum vor dem Maul), Heraushängen der Zunge führen und infolge Lähmung der Hinterbeine kommt es zum Festliegen. Die Phase der „rasenden Wut“ kann auch fehlen und die Tollwut gleich mit den Lähmungserscheinungen beginnen („stille Wut“). Es kommen auch atypische Verläufe vor, die zunächst einer Gastroenteritis gleichen.
Bei der Hauskatze gleicht das klinische Bild dem des Hundes. Häufig zieht sich eine erkrankte Katze zurück, miaut ständig und reagiert aggressiv. Im Endstadium kommt es zu Lähmungen.
Beim Hausrind zeigt sich eine Tollwut zumeist zunächst in Verdauungsstörungen, es kommt zu einer Atonie und Aufgasung des Pansens und Durchfall. Insbesondere bei Weidehaltung muss die Tollwut immer als mögliche Ursache für Verdauungsstörungen in Betracht gezogen werden. Später stellen sich Muskelzuckungen, Speicheln, ständiges Brüllen und Lähmungen der Hinterbeine ein. Bei kleinen Wiederkäuern wie Schafe und Ziegen dominiert die „stille Wut“, es können aber auch Unruhe, ständiges Blöken und ein gesteigerter Geschlechtstrieb auftreten.
Beim Hauspferd kann die Tollwut als „rasende Wut“ mit Rennen gegen Stallwände und Koliken oder als „stille Wut“ mit Apathie auftreten. Die „stille Wut“ kann mit einer Bornaschen Krankheit verwechselt werden.
Beim Hausschwein dominieren Aufregung, andauerndes heiseres Grunzen, Zwangsbewegungen und Beißwut.
Bei Vögeln ist die Krankheit sehr selten und äußert sich in ängstlichem Piepen, Bewegungsstörungen und Lähmungen.
Bei Wildtieren führt eine Tollwut häufig zum Verlust der natürlichen Scheu vor dem Menschen. Im Endstadium kommt es zu Lähmungen der Hinterbeine.
Therapie: Es gibt keine spezifische Therapie. Nach einer Infektion und Überschreitung der Frist für eine Nachimpfung wurde in letzter Zeit eine Behandlung mit antiviralen Medikamenten, Virustatika, und zeitgleichem künstlichem Koma zur Stoffwechselreduzierung versucht. Diese Therapieversuche waren jedoch bisher nicht erfolgreich, da nur einige wenige Patienten eine solche Behandlung mit schwersten Gehirnschäden überlebten. Als erster Mensch, der eine solche experimentelle Therapie nach einer Infektion weitestgehend ohne schwerwiegende Folgeschäden überstanden hat, gilt die US-Amerikanerin Jeanna Giese. Am 12. Mai 2006 starb ein Jugendlicher in Houston, Texas, an Tollwut als Folge eines Fledermausbisses, bei dem diese experimentelle Therapie ebenfalls angewendet wurde.
Vorbeugung: Die Erkrankung kann durch rechtzeitige Impfung verhindert werden. Louis Pasteur entwickelte 1885 die erste Tollwut-Impfung und rettete damit das Leben von Joseph Meister, der von einem tollwütigen Hund gebissen worden war. Heutige Impfstoffe sind relativ schmerzlos und werden in den Arm, ähnlich wie eine Grippe- oder Wundstarrkrampf-Impfung verabreicht. Sie bestehen aus inaktivierten Viren, welche in menschlichen (humanen) diploiden Zelllinien oder Hühnerfibroblasten angezüchtet werden.
Eine Impfung kann auch Stunden nach einem Biss noch erfolgreich sein. Für eine nachträgliche Impfung bleibt mehr Zeit, wenn die Wunde relativ weit vom Kopf entfernt ist und durch den Biss keine venösen Blutgefäße verletzt worden sind. Das Robert-Koch-Institut gibt folgende Richtlinie für die postexpositionelle Impfung vor:
| Grad der Exposition | Art der Exposition | Immunprophylaxe | |
|---|---|---|---|
| durch ein tollwutverdächtiges oder tollwütiges Wild- oder Haustier | durch einen Tollwut-Impfstoffköder | ||
| I | Berühren / Füttern von Tieren, Belecken der intakten Haut | Berühren von Impfstoffködern bei intakter Haut | keine Impfung |
| II | Knabbern an der unbedeckten Haut, oberflächliche, nicht blutende Kratzer durch ein Tier, Belecken der nicht intakten Haut | Kontakt mit der Impfflüssigkeit eines beschädigten Impfstoffköders mit nicht intakter Haut | Impfung |
| III | Jegliche Bissverletzung oder Kratzwunden, Kontamination von Schleimhäuten mit Speichel (z. B. durch Lecken, Spritzer) | Kontamination von Schleimhäuten und frischen Hautverletzungen mit der Impfflüssigkeit eines beschädigten Impfstoffköders | Impfung und einmalig simultan mit der ersten Impfung passive Immunisierung mit Tollwut-Immunglobulin (20 IE / kg Körpergewicht) |
Es sollte versucht werden, das tollwutverdächtige Tier zu fangen und zu isolieren (nicht töten!), da es in Quarantäne verbracht unter veterinärmedizinischer Kontrolle beobachtet werden kann. Tritt nach 10 bis 14 Tagen keine Tollwut auf, war das Tier nicht kontagiös. Falls das Tier erkrankt, kann eine Virusdiagnostik durchgeführt werden. Bei der infizierten Person kann erst nach Ausbruch der Krankheit eine Diagnose gestellt werden.
es besteht die Möglichkeit der aktiven Immunisierung mit einem Totimpfstoff. Dieser wird in mehreren Dosen im Abstand von einigen Tagen bis Wochen in den Oberarm injiziert. Der genaue Impfplan ist präparatabhängig. Die Impfung muss ein Jahr nach dem ersten Impfzyklus einmal wiederholt und danach alle 5 Jahre aufgefrischt werden.
Bei einer Verletzung durch ein tollwutverdächtiges Tier wird zunächst eine passive Immunisierung mit fertigen Antikörpern gespritzt. Gleichzeitig wird mit der aktiven Impfung begonnen. Außerdem muss der Tetanus-Schutz kontrolliert werden. Hilfreich ist auch ein gründliches Waschen der Wunde mit Wasser und Seife, um so viel infektiöses Material wie möglich zu entfernen.
Mythos und Geschichte: In früheren Zeiten war die Tollwut von Mythen, Aberglauben und Irrtümern umgeben und schürte, da die Krankheit fast unweigerlich zum Tod führte, die Ängste und die Phantasien der Menschen. Auch dass die Tollwut vermeintlich durch Wölfe übertragen wurde, trug zur Legendenbildung bei, der Ursprung des Werwolfsglaubens z.B. wurzelt in der Tollwuterkrankung der Menschen. Bereits in der Antike befassten sich Aristoteles und Euripides mit der Krankheit, in der griechischen Götterwelt waren Artemis, Hekate, Aktaion und Lykaon Verkünder, Verbreiter oder Opfer der Tollwut. Sirius, Hauptstern im Sternbild des Großen Hundes, verdankt seinen Namen der Legende, Wegbereiter der Seuche zu sein, im Hochsommer – an den Hundstagen (an denen Sirius in Sonnennähe steht; man nahm früher an, Sonne und Sirius würden in dieser Zeit zusammenwirken) – wurden Hunde, die man mit der Verbreitung der Tollwut in Verbindung brachte, malträtiert und geopfert. Im Mittelalter wurde, ausgehend von Augustinus, der Ursprung der Tollwut beim Teufel gesucht, der heilige Hubertus gilt seit dieser Zeit als Schutzpatron gegen die Tollwut.
Verbreitung und Bekämpfung: Das Tollwut-Virus überlebt in weiträumigen, abwechslungsreichen, ländlichen Tierwelt-Reservoiren. Die obligatorische Impfung von Tieren ist in ländlichen Gebieten weniger wirksam. Besonders in Entwicklungsländern ist es möglich, dass Tiere nicht in Privatbesitz sind; ihre Tötung kann unakzeptabel sein. Schluck-Impfstoffe können in Ködern sicher verteilt werden. Letzteres hat die Tollwut in ländlichen Gebieten Frankreichs, Ontarios, Texas, Floridas und anderswo erfolgreich zusammenschrumpfen lassen.
Um die Verbreitung der Krankheit zu bekämpfen, besteht für den grenzüberschreitenden Reiseverkehr mit kleinen Haus- und Heimtieren (Hunde, Katzen, Frettchen) eine allgemeine Impfpflicht gegen Tollwut. Die von Land zu Land sehr unterschiedlichen zusätzlichen Bestimmungen werden für die Verbringung von Tieren innerhalb der Europäischen Union mit der Einführung des EU-Heimtierausweises ab dem 4. Oktober 2004 vereinheitlicht.
Tollwut ist in vielen Teilen der Welt endemisch, und einer der Gründe für Quarantänezeiten im internationalen Tiertransport war der Versuch, die Krankheit aus unverseuchten Gebieten fernzuhalten. Inzwischen erlauben jedoch viele Industriestaaten, allen voran Schweden, Haustieren unbeschwertes Reisen zwischen den Territorien, sofern die Tiere durch eine entsprechende Abwehrreaktion vorweisen können, gegen Tollwut geimpft worden zu sein.
Deutschland: In Deutschland zeigt die Bekämpfung der Tollwut große Erfolge. Während noch im Jahr 1980 insgesamt 6.800 Fälle gemeldet wurden, waren es im Jahr 1991 noch 3.500, im Jahr 1995 nur 855, im Jahr 2001 noch 50 und 2004 noch 12 gemeldete Fälle. Mit 5 Fällen 2004 am stärksten von der Tollwut befallen ist der Fuchs. Zur Bekämpfung der Tollwut werden in den letzten Jahren so genannte Impfköder entweder von Jagdausübungsberechtigten ausgebracht oder, wie in einzelnen Bundesländern, großflächig aus Flugzeugen abgeworfen.
2004 wurden in Deutschland Tollwutfälle bei Tieren aus den Bundesländern Baden-Württemberg, Berlin, Hamburg, Hessen, Niedersachsen, Rheinland-Pfalz und Schleswig-Holstein gemeldet.
Am 4. Dezember 2005 wurde in Berlin bei einer von Kindern gefundenen, kranken und später verstorbenen Breitflügelfledermaus (Eptesicus serotinus) von Tierärzten des Instituts für Lebensmittel, Arzneimittel und Tierseuchen (ILAT) in Berlin die Tollwut festgestellt. Bei den bei Fledermäusen vorkommenden Tollwuterregern handelt es sich um eigenständige Virustypen. Sie werden als European Bat Lyssavirus (EBL) mit den Varianten 1 und 2 oder Europäisches Fledermaus-Tollwutvirus bezeichnet. Die Fledermaustollwut ist eine eigenständige Erkrankung, die von der Fuchstollwut abzugrenzen ist. Über die Medien erfolgte eine dringende Aufforderung an alle möglichen Kontaktpersonen, sich vorsorglich Impfen zu lassen.
Österreich: Das Österreichische Bundesland Tirol gilt als tollwutfrei (Juni 2005).
Schweiz: Die Schweiz gilt seit 1999 als tollwutfrei. Die Krankheitsfreiheit wurde durch eine gezielte Fuchsimpfkampagne erreicht.
Großbritannien: Von Großbritannien, das strenge Regulierungen bei der Einfuhr von Tieren hat, wurde angenommen, dass es von der Tollwut völlig frei sei, bis 1996 eine einzelne Wasserfledermaus entdeckt wurde, die mit einem tollwutartigen Virus infiziert war, das gewöhnlich nur bei Fledermäusen vorkommt - dem europäischen Fledermaus-Lyssavirus 2 (EBL2). Es gab keine weiteren bekannten Fälle bis September 2002, als in Lancashire eine weitere Wasserfledermaus positiv auf EBL2 getestet wurde. Ein Fledermaus-Schützer, der von der angesteckten Fledermaus gebissen worden war, erhielt eine Postexpositionsbehandlung, woraufhin er nicht an Tollwut erkrankte.
Im November 2002 wurde David McRae, ein Fledermaus-Schützer aus Guthrie, Angus, Schottland, der, wie man glaubte, von einer Fledermaus gebissen worden war, die erste Person, die in Großbritannien seit 1902 an Tollwut verschied. Er starb an der Krankheit am 24. November 2002.
In Großbritannien trugen Hundelizenzen, Tötung von Straßenhunden, Maulkorbpflicht und andere Maßnahmen zur Ausrottung der Tollwut am Anfang des 20. Jahrhunderts bei. In letzter Zeit ist auch die großangelegte Impfung von Katzen, Hunden und Frettchen in einigen Industrieländern bei der Bekämpfung von Tollwut erfolgreich gewesen.
USA: Seit der Entwicklung von wirksamen Impfstoffen für Menschen und Immunglobulin-Behandlungen ist die Zahl der Todesopfer der Tollwut in den USA von 100 oder mehr pro Jahr am Anfang des 20. Jahrhunderts, auf 1-2 pro Jahr gefallen, die größtenteils von Fledermaus-Bissen herrühren.
Am 2. Juli 2004 meldete dpa, dass in den USA die Tollwut von einem Organspender auf die Empfänger übertragen worden war. Drei Patienten, die verseuchte Organe transplantiert bekommen hatten, waren an der Krankheit gestorben. Der Organspender hatte sich durch eine Fledermaus mit dem tödlichen Virus angesteckt, wie die US-Seuchenüberwachungsbehörde CDC in Atlanta berichtet hatte.
Am 12. Mai 2006 starb ein 16-jähriger Schüler in Houston, Texas, an Tollwut nach einem nächtlichen Biss einer Fledermaus, die offenbar durch das offene Fenster flog.
Australien: Australien ist einer von wenigen Teilen der Welt, wo Tollwut nie eingeschleppt worden ist. Jedoch kommt das australische Fledermaus-Lyssavirus natürlicherweise sowohl bei insektenfressenden als auch bei fruchtfressenden Fledermäusen (Flugfüchsen) der meisten Festland-Staaten vor. Wissenschaftler glauben, dass das Virus in Fledermaus-Bevölkerungen überall in der Reihe von Flugfüchsen Australiens gegenwärtig ist.
Indien: Indien ist eines der Länder, in denen viele Tollwutfälle (Indien: ca.30 000/Jahr) bei Menschen bekannt sind. Die Dunkelziffer dürfte weit darüber liegen. Die Übertragung erfolgt dort überwiegend durch Bisse freilaufender Hunde (auch auf dem Land!). Da eine Immunglobulin-Behandlung nicht verfügbar ist, wird fast ausschließlich mit der Postexpositionsmethode behandelt, die möglicherweise nicht so gute Heilungschancen wie die kombinierte Methode verspricht. Bei einem längeren Aufenthalt sollte also an eine vorherige Aktivimpfung gedacht werden (Reisemedizin).
Meldung vom 22. Februar 2005: Nachrichtenmeldungen zufolge haben sich in Deutschland Anfang 2005 drei Empfänger von Organspenden mit Tollwut infiziert. Die Organspenderin hatte sich wahrscheinlich bei einem Indien-Urlaub infiziert und das Virus über die Organe weitergegeben. Fraglich ist, ob die Spenderin schon Anzeichen einer Tollwutinfektion gezeigt hatte, die als Folge Ihres Kokainkonsums fehlinterpretiert worden war.
Sechs Menschen erhielten Organe der Spenderin. Die Empfängerin der Lunge erlag der Infektion am Morgen des 20. Februar 2005, der 70-jährige Nierenempfänger am 21. Februar 2005. Auch der Nieren-Pankreas-Empfänger erlag der Krankheit trotz einer neuartigen Therapie am 7. April 2005. Man vermutet, dass die Erkrankung sich durch die für eine erfolgreiche Transplatation notwendige Immunsuppression sehr schnell ausbreiten konnte.
Die anderen drei Empfänger zeigen bis jetzt keinerlei Symptome. Sie sind aktiv und passiv geimpft, ihre Prognose ist gut. Zwei der Organempfänger haben ein Hornhauttransplantat erhalten, so dass die nötige Immunsuppression und der Operationsstress relativ gering sind, was ein frühzeitiges Ausbrechen der Erkrankung verhindert hat. Der Empfänger der Leber ist vor zirca 15 Jahren gegen Tollwut geimpft worden, so dass die Erkrankungen nicht ausbrechen konnte (Stand: 22. Februar 2005).
Weblinks:
Quellen
[Bearbeiten]- ↑ . “Fernreisende sind schlecht zu Tollwut informiert”. Ärzte Zeitung, 30.04. 2003.
- ↑ WHO - Rabies
