Medizinische Mikrobiologie: Togaviridae
Togaviren (Togaviridae) sind einzel(+)-strängige, behüllte RNA-Viren mit einem Durchmesser von 60-70nm. Die Reifung der Viren (Maturation) erfolgt an Plasmamembranen. Zu den Togaviren zählen die Gattungen der Alphaviren (bei denen die Krankheitserreger unter anderem durch blutsaugende Gliederfüßer auf den Mensch und Tiere übertragen werden) und Rubiviren (Erreger der Röteln).
Alphaviren
[Bearbeiten]| Alphaviren | ||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Systematik | ||||||||||||||||||||||||
| ||||||||||||||||||||||||
| Morphologie | ||||||||||||||||||||||||
| umhüllt, ikosaedrisch | ||||||||||||||||||||||||
Das Alphavirus (früher: Arbovirus A) ist eine Virus-Gattung der Togaviridae. In diese Gattung sind etwa 20 umhüllte und positiv-einzelsträngige RNA-Viren mit einem Durchmesser von ca. 60 bis 70nm eingeordnet. Die Virushülle besitzt charakteristische Spikes aus Glycoproteinen. Sie vermehren sich im Zytoplasma und die Nukleinsäure allein ist bereits infektiös.
Alphaviren kommen weltweit vor. Die Krankheitserreger werden vor allem durch Stechmücken (z.B. Anopheles) übertragen (daher der alte Name Arbovirus als Akronym für arthropod(s) born viruses). Alphaviren können beim Menschen endemisch, epidemisch und sporadische Erkrankungen hervorrufen. Dabei überwiegen gutartige fieberhafte Infekte, die zum Teil mit Exanthem und Gelenkentzündung (Polyarthritis) einhergehen. Bei Tieren kommen aber auch letale Infektionen mit Beteiligung des Zentralnervensystems vor (Enzephalomyelitis-Viren der Pferde, deren Krankheitsbilder zu den anzeigepflichtigen Tierseuchen gehören).
Humanpathogene Alpha-Viren Viren sind das Chikungunya-Virus, das Ross-River-Virus, das O'Nyong-nyong-Virus, das Mayaro-Fieber-Virus, das Sindbis-Virus, das Semliki-Forest-Virus, das Mucambo-Virus und das Everglades-Virus.
Tierpathogene Viren sind (bei Pferden) das das Eastern Equine Encephalomyelitis Virus (EEE-Virus), das Western Equine Encephalomyelitis Virus (WEE-Virus), das Venezuelan Equine Encephalomyelitis Virus (VEE-Virus) und bei Nagetieren und Vögeln das Highlands J-Virus.
Chikungunya-Virus
[Bearbeiten]Chikungunya-Fieber ist ein durch Viren ausgelöstes endemo-epidemisches tropisches Hämorrhagisches Fieber. Chikungunya heißt "der gekrümmt Gehende" und ist ursprünglich Kisuaheli. Im Deutschen wird die Krankheit auch „Gebeugter Mann“ genannt. Diese Erkrankung ist bislang nicht meldepflichtig.
Erreger: Das Chikungunya-Fieber wird durch das Chikungunya-Virus (CHIKV) ausgelöst. Das krankheitverursachende Virus ist ein behülltes Einzel(+)-Strang-RNA-Virus und gehört zur Gattung Alphavirus aus der Familie der Togaviridae. Außerdem gehört das Virus zur Gruppe der Arboviren und ähnelt denen, welche das Denguefieber und Gelbfieber auslösen und ist eng mit dem das O'nyong'nyong-Fieber verursachendem O'nyong'nyong-Virus verwandt.[1]. Als Reservoirwirte sind bislang Meerkatzen, Paviane und Nager festgestellt.[2]
Vorkommen: Das Chikungunya-Fieber ist erstmals 1952 in Tansania bekannt geworden. Später ist dieses Fieber sowohl in Westafrika wie auch in Indien, Südostasien und auf den Philippinen ausgebrochen. Die Bevölkerung in diesen Regionen hat sich jedoch als weitgehend immun gegen diesen Krankheitserreger erwiesen. Mittlerweile hat es sich zusammen mit der Asiatischen Tigermücke Aedes albopictus auf nahezu allen Kontinenten ausgebreitet. Seit etwa zehn Jahren sind auch Europa und Inseln im Pazifik und im Indischen Ozean betroffen. Im letzten Auftrittsgebiet der Inseln vor Ostafrika fehlt den dortigen Bewohnern und den Urlaubern aus Europa eine Immunität.
Übertragung: Das Chikungunya-Fieber kann nach Expertenmeinung theoretisch durch den Stich verschiedener Stechmücken der Gattungen Anopheles, Aedes, Culex und Mansonia übertragen werden. Als eindeutiger Vektor ist allein die ursprünglich aus Ostasien stammende Asiatische Tigermücke Aedes albopictus (seit neuerem auch Stegomyia albopicta) nachgewiesen.[3] Auch diese nur etwa 5mm große, schwarz-weiß gestreifte und sehr aggressive Mücke, die am Tage sticht und dies teilweise sogar durch die Kleidung hindurch, hat sich weltweit ausgebreitet und überträgt neben dem Chikungunya-Fieber auch noch das Dengue-Fieber, Gelbfieber, West-Nil-Fieber und weitere Krankheiten. Diese Mückenart kommt mittlerweile nur in den heißen Sommermonaten auch in Südeuropa vor, doch sind hier bislang noch keine mit dem Chikungunya-Virus infizierten Exemplare festgestellt worden.
Das Chikungunya-Fieber kann nicht direkt von Mensch zu Mensch weitergegeben werden.
Diagnose: Ein serologischer Test für Chikungunya ist von der Universität Malaya in Kuala Lumpur, Malaysia erhältlich.
Krankheitsverlauf und Symptome: Nach einer Inkubationszeit von zwei bis zehn Tagen entwickeln die Betroffenen in der Regel hohes Fieber mit Kopf- und schweren Gelenkschmerzen mit hoher Berührungsempfindlichkeit, so dass sie sich kaum noch aufrecht halten können. Andere häufige Symptome sind Erschöpfung, Hautausschlag und Atembeschwerden. Normalerweise klingt diese Erkrankung nach etwa zwei Wochen von selbst wieder ab und es bleiben auch keine Schäden zurück. Nach überstandener Krankheit kommt es zu lebenslanger Immunität.
Komplikationen: Die oben geschilderten Symptome können gelegentlich wiederkehren und bis zu neun Monate anhalten. Weiterhin können durch das hohe Fieber gelegentlich starke neurologische Störungen, Hirnhautentzündungen oder sogar Gehirnschäden verursacht werden. Ein schwerer Krankheitsverlauf kann auch zu einer paraviralen Arthritis führen. Auf La Réunion kam es durch diese Erkrankung sogar zu mehreren Todesfällen (siehe unten).
Therapie: Bisher gibt es keine kausale Therapie. Schmerzen können z.B. mit Paracetamol behandelt werden.
Vorbeugung: Es existiert bislang kein Impfstoff. Einzig wirksame vorbeugende Gegenmaßnahmen sind die Bekämpfung der Mücken, geschlossene Kleidung und Moskitonetze bei Nacht. Die Mückenbekämpfung in tropischen Regionen ist schwierig, da diese Insekten besonders zur Regenzeit dort auftreten, wo eine chemische Bekämpfung kaum möglich ist, ohne die Fauna nachhaltig zu schädigen.
Geschichte: Die Krankheit wurde das erste Mal im Jahre 1952 in Tansania und Uganda beschrieben.
Im Jahre 1999 gab es einen Ausbruch von Chikungunya in Malaysia, bei dem 27 Personen betroffen waren. Seit Dezember 2005 grassiert auf der französischen Insel La Réunion eine Chikungunya-Epidemie. Es sind dort nach Angaben der Behörden bislang 186.000 Personen infiziert und es gab bis Anfang März 2006 bereits 93 Todesfälle. Dies wird dadurch begünstigt, dass das Virus dort bislang unbekannt war und die Bevölkerung keine Immunität besitzt. Die wirtschaftlichen Auswirkungen der Epidemie auf die vom Tourismus abhängige Insel können schwerwiegend sein. In Mauritius waren im Jahre 2005 3.500 Personen betroffen. Es gab auch Fälle auf der Komoreninsel Mayotte und in Madagaskar und auf den Seychellen.
In Deutschland wurden bereits Patienten ärztlich behandelt, die sich zuvor im Urlaub in einer entsprechenden Region infiziert hatten. Die Erkrankung kann in Deutschland allerdings nicht übertragen werden, da die Überträgermücke hierzulande noch nicht vorkommt und das Chikungunya-Fieber wie oben schon erwähnt nicht direkt von Mensch zu Mensch weitergegeben werden kann.
Ross-River-Virus
[Bearbeiten]Das Ross-River-Virus (RRV) ist ein Arbovirus aus der Familie der Togaviridae (Genus Alphavirus). Es ist in Australien, auf Papua Neu-Guinea und den benachbarten Inseln endemisch und führt jährlich zu mehreren tausend Erkrankungen (sog. epidemische Polyarthritis).
Geschichte: Das Krankheitsbild ist seit den 1930er Jahren bekannt, die erste Isolation des Virus erfolgte in den 1960er Jahren. Seitdem hat sich das Virus weiter ausgebreitet, vermutlich weil durch verstärkte Migration neue und damit nicht immune Bevölkerungsgruppen betroffen waren. Endemische Gebiete finden sich in South Australia, im Northern Territory, in Queensland, Victoria und New South Wales. Eine weitere Ausbreitung ist theoretisch möglich, da die das Virus verbreitenden Vektoren (Stechmücken) auch auf anderen Kontinenten vorkommen.
Infektionsweg: Die Übertragung erfolgt durch Stechmücken der Familien Aedes, Culex und Mansonia. Das Reservoir sind vermutlich Kleinsäuger.
Klinik: Nach einer Inkubationszeit von 3 bis 9 Tagen kommt es zu plötzlich einsetzenden, symmetrischen Gelenk- und Muskelschmerzen sowie Gelenksteifigkeit, leichte Temperaturerhöhung, Müdigkeit, Abgeschlagenheit, Lethargie, Hautausschläge und Kopfschmerzen. Die Erkrankung ist selbstlimitierend, Symptome können jedoch auch Monate bis Jahre andauern.
Therapie: Eine Impfung oder spezifische Therapie gibt es nicht, die Therapie ist symptomatisch. In den betroffenen Gebieten ist Schutz vor Stechmücken ratsam.
O'Nyong-nyong-Virus
[Bearbeiten]Das O´nyong-nyong-Fieber wird durch das gleichnamige Virus ausgelöst. Das ss(+)RNA-Virus gehört zur Gattung der Alphaviren aus der Familie der Togaviren. Es besteht eine Verwandtschaft zum Chikungunya-Virus. Der Name bedeutet "Gelenkbrechen".
Vorkommen: Ost- und Zentralafrika. Das Virus wurde in Kenia, Malawi, Mozambique, Tansania, Uganda, Senegal und in der Zentralafrikanischen Republik festgestellt. Auch Touristikgebiete sind betroffen. Die Krankheit tritt sporadisch als Epidemie auf. Zwischen den Epidemien können oftmals 10 bis 20 Jahre liegen, dabei liegt die Durchseuchung in der Bevölkerung bei bis zu 80%. Das Virus wurde erstmals während einer großen Epidemie zwischen 1959 und 1962 in Uganda nachgewiesen. Damals erkrankten zwei Millionen Menschen. Es wird ein extrahumanes Reservoir vermutet.
Übertragung: O'nyong-nyong ist eine Arbovirusinfektion. Die Übertragung erfolgt durch Stechmücken (Anopheles gambiae und Anopheles funestus). Die Mücken sind dämmerungsaktiv, ihre Verbreitung ist an das Vorhandensein von stehenden Gewässern gebunden.
Diagnose: Typische Reiseanamnese, Antikörpernachweis im Blut, Klinik. Verwechslungen mit Chikungunya sind möglich.
Krankheitsverlauf und Symptome: Die Inkubationszeit beträgt 8–11 Tage. Die Krankheit beginnt plötzlich mit Schüttelfrost, hohem Fieber, Kopfschmerzen und Lymphadenitis. Es besteht eine Leukopenie mit relativer Lymphozytose. Charakteristisch sind die ausgeprägten, symmetrischen Gelenkschmerzen (Polyarthralgien), die über mehrere Wochen bestehen können. Nachfolgend makulopapulöser Ausschlag in ca. 60% der Fälle. Enantheme der Wangen- und Gaumenschleimhaut können auftreten. Die Symptome bilden sich nach 2 Wochen zurück. Inapparente Infektionen (ohne Krankheitsgefühl) sind häufig. Es bleibt eine lang anhaltende Immunität zurück. Tödliche Verläufe sind nicht bekannt.
Therapie: Eine kausale Therapie oder Impfung gibt es nicht, die Behandlung erfolgt symptomatisch.
Vorbeugung: Konsequenter Schutz vor Mückenstichen: Repellentien, Moskitonetze, helle, lange Kleidung, Vermeidung von Außenaufenthalten während und nach der Dämmerung.
Mayaro-Fieber-Virus
[Bearbeiten]Sindbis-Virus
[Bearbeiten]Das Sindbis-Virus löst das Sindbis-Fieber (Karelisches Fieber, Okelbokrankheit, Pogosta-Krankheit) aus. Die Übertragung erfolgt durch nachtaktive Stechmücken (Culicidae). Das Virusreservoir sind Vögel, eine Übertragung von Mensch zu Mensch durch Stechmücken ist möglich.
Vorkommen: Afrika, Asien, Nord- und Osteuropa
Klinik: Grippeähnlich, Inkubationszeit 4 Tage, Fieber, Kopf- und Gelenkschmerzen, Exanthem vor allem an Hand- und Fußsohlen. Der Verlauf ist gutartig.
Weblinks: Medizin.de - Ockelbo´sche Krankheit: Arbovirose Skandinaviens (28.10.2005)
Semliki-Forest-Virus
[Bearbeiten]Mucambo-Virus
[Bearbeiten]Everglades-Virus
[Bearbeiten]Rubiviren
[Bearbeiten]Rubellavirus
[Bearbeiten]| Rubellavirus | ||||||||||
|---|---|---|---|---|---|---|---|---|---|---|
 | ||||||||||
| Systematik | ||||||||||
| ||||||||||
| Morphologie | ||||||||||
| umhüllt, ikosaedrisch | ||||||||||
Das Rötelnvirus (Rubella-Virus) ist der Erreger der als harmlosen Kinderkrankheit bekannten "Röteln" und der Verursacher der gefürchteten Rötelnembryopathie bei Infektion in den ersten Schwangerschafts-Wochen.
Der Erreger gehört zur Familie der Togaviridae. Es handelt sich um ein genetisch stabiles, behülltes, einzel(+)-strängiges RNA-Virus mit einer Größe von 50–70nm, dessen Kapsid von einer weiten, faltigen Lipidhülle mit Strukturproteinen (der Toga) umgeben ist. Der einzige Wirt des weltweit verbreiteten Virus ist der Mensch. Die Übertragung erfolgt mittels Tröpfcheninfektion.
Häufigkeit: Die Rötelninfektionskrankheit ist weltweit verbreitet mit eher niedriger Ansteckungsgefahr. Da der Mensch der einzige Wirt des Virus ist, bekommt sie in dichteren Populationsgebieten hohe Bedeutung. Die unvollständige Durchimpfung der Bevölkerung kann zu sporadischen und epidemischen Infektionen bei Kindern, Jugendlichen und auch Erwachsenen führen. Bei Vorschuluntersuchungen von 2000 bis 2002 waren rund 86% der Kinder geimpft. Vor der Verfügbarkeit von Röteln-Impfungen behalf man sich zum Teil mit so genannten Rötelnpartys, damit sich die eingeladenen jungen Mädchen vor einer möglichen Schwangerschaft ansteckten. Die Ständige Impfkommission empfiehlt eine Schutzimpfung aller Kinder ab dem zwölften Lebensmonat, eine Wiederholungsimpfung möglichst im zweiten Lebensjahr, der Mindestabstand zur ersten Impfung beträgt einen Monat, außerdem eine Impfung aller seronegativen Erwachsenen (kein IgG nachweisbar).
Übertragung: Das Virus wird per Tröpfcheninfektion übertragen. Eine Woche vor Ausbruch des Exanthems bis eine Woche nach Exanthemausbruch ist der Patient infektiös.
Symptome: Nach einer Inkubationszeit von 14 bis 16 Tagen bilden sich bei 50% der Infizierten zunächst im Gesicht gerötete, einzelstehende Hauteffloreszenzen, die sich als kleinfleckiges makulöses oder makulopapulöses Exanthem auf den Stamm und die Extremitäten ausbreiten und den Masern ähneln, allerdings sind sie blasser und konfluieren kaum. Die Hauterscheinungen bilden sich meist nach etwa drei Tagen zurück. Begleitend tritt oft eine erhöhte Temperatur bis 39°C auf. Hinzu kommen eventuell Gliederschmerzen, Arthritis, Lymphknotenschwellung am Hinterkopf, Nacken und hinter den Ohren sowie eine Vergrößerung von Leber und Milz.
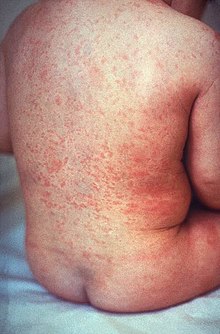
Die Symptome der Röteln bei Erwachsenen sind häufig stärker ausgeprägt als bei einer Rötelninfektion in der Kindheit, unterscheiden sich aber nicht wesentlich. Vor allem Gelenkbeteiligungen kommen bei Erwachsenen häufiger vor.
Komplikationen: Eine Rötelninfektion während der ersten Wochen der Schwangerschaft kann zu schweren Fehlbildungen des Ungeborenen führen (Rötelnembryopathie). Daher gehört die Untersuchung auf Röteln zur Mutterschaftsvorsorge. Mögliche Fehlbildungen sind Innenohrschwerhörigkeit, Rötelnkatarakt, Herzfehler, Gefäßfehlbildungen (offener Ductus Botalli, Septumdefekte und Fallot'sche Tetralogie), Spina bifida aperta und Enzephalomeningitis.
Diagnostik: Die Diagnostik in Bezug auf die Immunität gegenüber einer Rötelninfektion wird über den Nachweis von ausreichenden Titern an spezifischen Antikörpern im Serum durchgeführt. Der Nachweis des Rötelnvirus erfolgt durch die Isolation von Viren oder durch den Nachweis von viraler RNA. Man unterscheidet drei Möglichkeiten des Infektionszustandes:
- Immunität liegt vor, wenn eine Infektion durchgemacht wurde – diese führt zumeist zu einer lebenslangen Immunität – oder eine Impfung erfolgte und ausreichend hohe IgG-Antikörper in zwei verschiedenen Labortests (z.B. ELISA oder HAH) nachweisbar sind.
- Eine Primärinfektion liegt bei entsprechenden klinischen Symptomen und dem Nachweis von IgM-Antikörpern vor.
- Von einer Reinfektion spricht man, wenn IgM-Antikörper in zwei methodisch verschiedenen Labortests nachweisbar sind und gleichzeitig IgG-Antikörper für eine früher abgelaufene Rötelninfektion sprechen, diese Infektion verläuft überwiegend harmlos.


Differentialdiagnose: Masern, Scharlach, Infektiöse Mononukleose, Drei-Tage-Fieber, Ringelröteln u.a.m. Die Unterscheidung anhand des Exanthems ist oft schwierig.
Behandlung: Keine kausale Therapie. Bei starkem Fieber können fiebersenkende Mittel verabreicht werden, bei starkem Krankheitsgefühl wird Bettruhe empfohlen.
Prophylaxe: Die aktive Lebend-Impfung wird zumeist in der Kombination mit dem Masern-Mumps-Rubella (MMR)-Impfstoff durchgeführt. Eine postexpositionelle passive Impfung bei Schwangeren ist möglich.
Krankheitsbild Rötelnembryopathie: Bei der Rötelnembryopathie (auch Embryopathia rubeolosa, Congenitales Rubella-Syndrom (CRS) oder Gregg-Syndrom) handelt es sich um mögliche Folgeerkrankungen einer Röteln-Infektion während der Schwangerschaft. Die Infektion der Mutter kann auch subklinisch verlaufen. Die Wahrscheinlichkeit von kindlichen Schäden beträgt dabei 90%(!) bei einer Infektion in den ersten 8 Schwangerschaftswochen und 25%–35% bei einer Infektion während des zweiten Trimesters.
Der australische Augenarzt Sir Norman McAllister Gregg (1892-1966) beschrieb 1941 erstmals ein Fehlbildungssyndrom bei Neugeborenen, das, wie er erkannte, auf eine Rötelninfektion der Mutter während der Schwangerschaft zurückzuführen war. Man findet Innenohrschwerhörigkeit, Katarakt, Mikrophthalmie, Angiokardiopathien und intrauteriner Wachstumsretardierung (IUGR) auch psychomotorische Entwicklungsstörungen, welche häufig kombiniert mit der Mikrozephalie auftreten, sowie hypo- und aplastische Milchzahnanlagen. Die Infektion der Frucht im ersten Trimenon kann eine Indikation für einen Schwangerschaftsabbruch sein. Dieses Fehlbildungssyndrom gilt auch für andere pränatale Virusinfektionen (Mumps, Varizellen).
Außer dem genannten Syndrom kann es zur Fehl- und Frühgeburt kommen.
Pathogenese und Infektionsweg: Das Virus wird von der erkrankten Mutter diaplazentar auf den Embryo/Feten übertragen. Eine Rötelnerkrankung während der Schwangerschaft kommt nur zustande, wenn die Schwangere keinen ausreichenden IgG-Antikörper-Titer besitzt.
Epidemiologie: In Deutschland beträgt die Anzahl seronegativer Frauen im gebärfähigen Alter 4 bis 7%, sodass bei durchschnittlich 800.000 Geburten pro Jahr 30.000 Neugeborene durch eine pränatale Rötelninfektion gefährdet sind. Bei einer Rötelninfektion in den ersten zehn SSW besteht eine 90%ige Gefahr der Schädigung des Kindes, bis zur 17. SSW sinkt das Risiko auf 11 bis 33% und nach der 17. Woche auf ca. 4%.
Prophylaxe und Diagnostik: Bei geplanter Schwangerschaft sollte der Impfstatus, beziehungsweise IgG-Ak-Titer gegen Röteln überprüft werden, gegebenenfalls sollte eine Impfung erfolgen. Häufig ist die Schwangerschaft jedoch nicht geplant. Im Rahmen der Mutterschaftsvorsorge werden Röteln-Antikörper bei allen Schwangeren bestimmt. Als grenzwertig werden Titer von 1:8 und 1:16 angesehen, bei 1:32 oder höher nimmt man einen ausreichenden Schutz an. Sind keine Antikörper nachweisbar, sollte die werdende Mutter den Kontakt zu rötelninfizierten Personen meiden. Bei Personen, die aufgrund ihres Berufs (Kindergärtnerinnen, Lehrerinnen etc.) vermehrt mit Viren in Kontakt kommen könnten, ist evtl. auch eine mehrfache Immunglobulingabe in der Frühschwangerschaft angezeigt. Liegt ein unzureichender IgG-Ak-Titer vor und bestand Rötelnkontakt beziehungsweise der Verdacht auf eine Infektion, kann mit dem Einverständnis der Schwangeren eine pränatale Diagnostik durch eine Amniozentese oder eine Nabelschnurpunktion erfolgen. Im Blutserum eines rötelninfizierten Fetus lassen sich zu 94% IgM-Antikörper ab der 22. SSW nachweisen.
Ab der Geburt sind bei allen Neugeborenen mit Rötelnembryopathie selbst gebildete IgM-Antikörper und auch größtenteils von der Mutter stammende IgG-Antikörper vorhanden. Im Blut der Neugeborenen sind Viren vorhanden, die Kinder sind somit ansteckend. IgM-Antikörper können nicht über die Plazenta von der Mutter auf das Kind übertragen werden, sie sind deshalb immer Ausdruck einer konnatalen Infektion (Nachkommen werden bereits infiziert geboren).
Therapie: Nach einer Rötelnexposition sollte sofort der IgM/IgG-Immunstatus (HHT, ELISA) geprüft werden. Wenn nach einer Woche (maximal 10 Tage) bereits Röteln-Antikörper nachweisbar sind, dann bedeutet dies, dass die Schwangere eine früher erworbene Immunität besitzt und dass es zu keiner akuten Infektion kommt. Exponierte schwangere Frauen, die keine Antikörper besitzen können innerhalb von 48 Stunden nach Kontakt mit dem Virus ein Röteln-IgG-Ak-Serum (Röteln-Hyperimmunglobulin) erhalten. Danach ist die Wirkung unsicher, ab dem 5. Tag nach Exposition wirkungslos. Da die Röteninfektion eine Inkubationszeit von etwa 2-3 Wochen hat, ist die passive Immunisierung beim Auftreten von Symptomen (Rötelnexanthem) nicht mehr möglich.
Weblinks: RKI - Röteln
Quellen
[Bearbeiten]- ↑ PMID 15891138
- ↑ http://arbmed.med.uni-rostock.de/bkvo/m3104.htm
- ↑ http://zdf.de/ZDFheute/inhalt/7/0,3672,3905287,00.htm
