Biochemie und Pathobiochemie: Valin-, Leucin- und Isoleucin-Stoffwechsel
Allgemeines
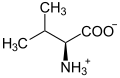
[Bearbeiten]Die essentiellen, proteinogenen Aminosäuren Leucin, Valin und Isoleucin besitzen eine aliphatische, verzweigte, lipophile Seitenkette.
Abbau der verzweigtkettigen Aminosäuren
[Bearbeiten]| ⇓ | Subst. | (⇑) | ⇓ | Subst. | (⇑) | ⇓ | Subst. | (⇑) | Co. | Enzym | EC/EG | Erkr. | |||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
|
|
|
|||||||||||||||||||
| α-KG | α-KG | α-KG | Pyrid- oxal- Phos. | Verzweigtkettige- Aminosäuren- Transaminase | 2.6.1.42 Tr | ||||||||||||||||
|
|
|
|||||||||||||||||||
| CoA-SH, NAD+
CO2, NADH/H+ |
CoA-SH, NAD+
CO2, NADH/H+ |
CoA-SH, NAD+
CO2, NADH/H+ |
Thiamin- P2 | Verzweigtkettige- α-Ketosäuren- Dehydrogenase- Komplex | 1.2.4.4 Ox | MSUD I | |||||||||||||||
| 2.3.1.168 Tr | MSUD II | ||||||||||||||||||||
| FAD | 1.8.1.4 Ox | MSUD III | |||||||||||||||||||
|
|
|
|||||||||||||||||||
| A
AH2 |
|
A
AH2 |
A
AH2 |
|
A
AH2 |
A
AH2 |
|
A
AH2 |
FAD | 1) Isovaleryl-CoA- Dehydrogenase
2) Butyryl-CoA- Dehydrogenase 3) Acyl-CoA- Dehydrogenase |
1.3.8.4 Ox
|
| |||||||||
|
|
|
|||||||||||||||||||
| ATP, HCO3-
ADP, Pi |
Biotin | Methyl-crotonoyl- CoA-Carboxylase | 6.4.1.4 Lig | MCC1-Def., MCC2-Def. | |||||||||||||||||
|
|||||||||||||||||||||
| H2O
|
1.
|
H2O
|
H2O
|
2.
|
|
H2O
|
2.
|
|
1) Methyl- glutaconyl-CoA- Hydratase
2) Enoyl-CoA- Hydratase |
4.2.1.18 Ly
4.2.1.17 Ly |
1) MGA1
| ||||||||||
|
|
|
|||||||||||||||||||
| H2O | 3-Hydroxy- isobutyryl-CoA- Hydrolase | 3.1.2.4 Hyd | |||||||||||||||||||
|
|||||||||||||||||||||
| NAD+ | 1.,2.
|
NAD+ | 2.,3.
|
NAD+ | 1) 3-Hydroxy- isobutyrat- Dehydrogenase
2) 3-Hydroxy- acyl-CoA- Dehydrogenase 3) 3-Hydroxy- 2-Methylbutyryl- CoA- Dehydrogenase |
1.1.1.31 Ox
|
| ||||||||||||||
|
|
||||||||||||||||||||
| CoA-SH, NAD+
CO2, NADH/H+ |
1.
|
CoA-SH
|
2., 3.
|
1) Methyl- malonat- semialdehyd- Dehydrogenase
2) Acetyl-CoA-C-Acetyltransferase 3) Acetyl-CoA- C-acyltransferase |
1.2.1.27 Ox
2.3.1.9 Tr
2.3.1.16 Tr |
1) MMSDHD
| |||||||||||||||
|
|
||||||||||||||||||||
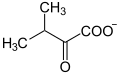
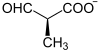
Der Abbau der drei essentiellen verzweigtkettigen Aminosäuren ist sehr ähnlich, zu Anfang steht bei allen eine Transaminierung gefolgt von einer Dehydrierenden Decarboxylierung. Danach folgt die Dehydrierung der zweiten C-C-Bindung.
Der weitere Abbau gestaltet sich wie folgt:
1) L-Leucin-Abbauweg: Methylcrotonoyl-CoA (3-Methylbut-2-enoyl-CoA) wird unter ATP-Verbrauch carboxyliert und dann hydratisiert. Das Endprodukt β-Hydroxy-β-methylglutaryl-CoA (HMG-CoA) kann in die Ketonkörperbiosynthese (und darüber zu Acetyl-CoA abgebaut) oder in die Cholesterinbiosynthese eingeschleust werden.
2) L-Valin-Abbauweg: Methylpropenoyl-CoA wird hydratisiert, CoA-SH wird abgespalten, dann wird es zu Methylmalonatsemialdehyd dehydriert (= oxidiert). Dieses kann über Propionyl-CoA zu Succinyl-CoA abgebaut und in den Citratzyklus eingeschleust werden.
3) L-Isoleucin-Abbauweg: Methylbutenoyl-CoA wird hydratisiert, dehydriert und unter Verwendung eines Coenzym A in Acetyl-CoA und Propionyl-CoA gespalten.
Literatur
[Bearbeiten]- Harris RA, Joshi M, Jeoung NH, Obayashi M. “Overview of the molecular and biochemical basis of branched-chain amino acid catabolism”. J. Nutr., 135:1527S–30S, June 2005. PMID 15930464.
Weblinks
[Bearbeiten]
| Allgemeine Hintergrundfarbe für Substrate | Hintergrundfarbe Reaktionspfeile | „Schlüsselenzyme“ | |
| Energiereiche Phosphate Reduktionsäquivalente | CO2 / HCO3− C1-Reste Stickstoff |
Abk.: Tr.: Transkriptionelle Regulation, Tl.: Regulation der Translation, Lok.: Regulation über die Enzymlokalisation, Kov.: Regulation durch kovalente Modifikation, All.: Allosterische Regulation, Koop.: Kooperativer Effekt, Co.: Cofaktoren, EC: Enzymklassifikation, EG: Enzymgruppe (Oxidoreductase, Transferase, Hydrolase, Lyase, Isomerase, Ligase), Erkr.: Assoziierte Erkrankungen.
Haben Ihnen die Informationen in diesem Kapitel nicht weitergeholfen?
Dann hinterlassen Sie doch einfach eine Mitteilung auf der Diskussionsseite und helfen Sie somit das Buch zu verbessern.