Pathologie: Tumoren des Nervensystems
Buch-Navigation
In diesem Kapitel finden Sie die Tumoren des Nervensystems, sortiert nach der aktuell gültigsten Klassifikation der WHO (2007).
Allgemeines
[Bearbeiten]Klassifikation nach Lokalisation:
- Intraaxial (im Hirnparenchym) - extraaxial (außerhalb der Pia mater).
- Infratentoriell (Rautenhirn) - supratentoriell (Großhirn).
Korrelation mit der Altersverteilung:
- Kinder: I. Allg. eher infratentoriell - Pilozytisches Astrozytom, Medulloblastome, Ependymome.
- Erwachsene: Eher supratentoriell - Astrozytome, Oligodendrogliome, Meningeome, Metastasen.
Klassifikation nach der Dignität: Die WHO teilt Hirntumoren in vier verschiedene Malignitätsgrade ein (WHO I°-IV°).
Klassifikation nach Histopathologie (WHO):
- Neuroepitheliale Tumoren
- Tumoren der peripheren Nerven
- Tumoren der Meningen
- Keimzelltumoren
- Tumoren der Sellaregion
- Metastatische Tumoren
Einteilung in Ausbreitungsmuster:
- Diffus-infiltrativ: Astrozytome und Oligodendrogliome ab °II, Gliomatosis cerebri, primäre ZNS-Lymphome.
- Diskret-infiltrativ bzw. lokalisiert: Pilozytisches Astrozytom, pleomorphes Xanthoastrozytom, Astroblastom, Ependymom, Choroidplexuspapillom, Hämangioblastom u.a.m.
Klinik: Neurologische Ausfallssymptome, Persönlichkeitsveränderungen, Morgendliche Kopfschmerzen mit Übelkeit und schwallartigem Erbrechen (Hirndruck, Dehnung der Meningen) mit Reaktion auf Liquordruckschwankungen (Aufsetzen, Bücken, Pressen). Epileptische Anfälle (in 50 % Erstsymptom), zerebrale Herdsymptome, Zeichen der Einklemmung.
Neuroepitheliale Tumoren
[Bearbeiten]Tumoren, die vom Hirnparenchym ausgehen, werden als neuroepitheliale Tumore bezeichnet. Zu diesen zählen:
- Astrozytome
- Oligodendrogliome
- Ependymome
- Neuronale Tumore
- Tumore des Plexus choroideus und des Pinealisparenchyms
- bestimmte embryonale Tumore
Molekulardiagnostik
[Bearbeiten]Bestimmte Genveränderungen haben bei glialen Tumoren eine große diagnostische und prognostische Bedeutung. Dazu zählen insbesondere Mutationen von IDH, H3F3A, ATRX und TERT sowie der Methylierungsstatus von MGMT.
Tabelle Verteilung von häufigen Mutationen in neuroepithelialen Tumoren (Quelle: Balss et al. Acta Neuropathol 2008; 116:597-602):
| Tumor | IDH1 | Tp53 | EGFR (Amplifikation) |
|---|---|---|---|
| primäres Glioblastom | 7% | 17% | 37% |
| sekundäres Glioblastom | 88% | 88% | 0% |
| Astrozytom II | 79% | 52% | 0% |
| Astrozytom III | 62% | 43% | 5% |
| Oligodendrogliom II | 71% | 10% | 0% |
| Oligodendrogliom III | 67% | 13% | 0% |
| Oligoastrozytom II | 78% | 23% | 0% |
| Oligoastrozytom III | 78% | 27% | 0% |
| Gliomatosis cerebri (type 2) | 42% | 10% | 0% |
- Rolle der Isocitratdehydrogenase
- häufigste Mutation bei Astrozytomen, Oligodendrogliomen und den daraus entstehenden sekundären Glioblastomen.
- Zytosolische IDH1 Mutationen sind weitaus häufiger als mitochondriale IDH2 Mutationen.
- Das Fehlen einer IDH1 R132 oder IDH2 R172 Mutation in höhergradigen Tumoren ist mit kürzeren Überlebenszeiten verbunden.
- Die Mutationen sind dabei aber sehr ungleich verteilt, mit Abstand am häufigsten wird ein Aminosäureaustausch IDH1 R132H beobachtet, weshalb für diese spezifische Mutation mittlerweile entsprechender Antikörper für die Immunhistochemie entwickelt wurde.
- Verteilung der IDH Mutationen in Hirntumoren (Quelle: Hartmann et al. Acta Neuropathol 2009, 118:469-474):
- IDH1: R132H (61,7 %), R132C (2,9 %), R132S (1,1 %), R132G (1,0 %), R132L (0,2 %), R132V (>0,1 %), R100Q( >0,1 %).
- IDH2: R172K (2 %), R172M (0,6 %), R172W (0,5 %), R140 (bisher nur AML).
- IDH2 Mutationen sind in Oligodendrogliomen häufiger anzutreffen.
- Die IDH1 R132C Mutation findet sich gehäuft in astrozytären Tumoren.
- Patienten mit einem IDH-mutiertem Glioblastom sind mit einem Alterschnitt von 48 Jahre deutlich jünger (IDH-Wildtyp Glioblastome: 61 Jahre) und zeigen mit 27 Monaten ein deutlich verlängte mittlere Überlebenszeit (IDH-Wildtyp Glioblastome: 12 Monate). [1]
- Rolle der Methylguanin-Methyltransferase (MGMT)
- Epigenetischer Marker: Methyliert bedeutet Protein inaktiv/ nicht vorhanden, unmethyliert bedeutet Protein aktiv/ vorhanden.
- Der Reparaturmechanismus von MGMT kann die durch Radio-Chemo-Therapie erwünschte DNA-Schädigung antagonisieren.
- Glioblastome mit einer Hypermethylation der MGMT-Promotorregion zeigen ein längeres Überleben als unethylierte GBM.
- Methylierte höhergradige Gliome zeigen ein besseres Ansprechen auf Radiochemotherapie.
- Bestimmung erfolgt durch MSP-PCR, MLPA, Pyrosequenzierung oder Methylierungsarrays. IHC ist nicht zuverlässig.
- Medulloblastome und Meningeome zeigen nur selten eine MGMT-Promotormethylierung.
- Rolle des ATRX-Status (Alpha Thalassemia/Mental Retardation Syndrome X-Linked)
- ATRX is notwendig für normale Telomerhömostase, die Tumormutation führen zu einer veränderten Telomerlänge .
- Inaktivierende Veränderungen in 7% der adulten GBMs und 14-31% of pädiatrischen GBMs [2]
- Der ATRX Verlust ist mit einem astrozytärem Phänotyp assoziert (kein LOH1p/19q)[3]
- ATRX Verlust (nuklär) kann mittels IHC erfasst werden.
- Rolle des Epidermal Growth Factor Receptor (EGFR)
- EGFR ist das am häufigsten (40 %) überexprimierte und amplifizierte Gen in Glioblastomen.
- EGFRvIII ist das häufigste Rearrangement (50-60 % der EGFR-amplifizierten GBM) und führt zu einem permanent aktivierten Rezeptor.
- Der Nachweis einer EGFR-Amplifikation in niedriggradigen Astrozytomen indiziert einen schlechteren Verlauf.
- Allerdings sprechen diese Tumore generell nicht besser auf Therpaie mit Tyrosinkinase-Inhibitoren an, weshalb Co-Faktoren wie AKT und PTEN derzeit in Kombination mit EGFR untersucht werden.
- Rolle der Tp53 Mutationen
- 53 % aller diffusen Astrozytome, 39% aller Oligoastrozytome und 8 % aller Oligoandrogliome Grad II WHO haben eine Tp53 Mutation.
- Am häufigsten sind die Mutationen in CpG-Inseln lokalisiert.
- In 75 % der Astrozytome Grad II WHO tritt die Tp53-Mutation mit einer IDH1/2 Mutation kombiniert auf.
- 53 % aller diffusen Astrozytome, 39% aller Oligoastrozytome und 8 % aller Oligoandrogliome Grad II WHO haben eine Tp53 Mutation.
- Rolle des LOH 1p/19q
- Prognostisch relevanter Marker für besseres Überleben und Ansprechen auf PCV-Therapie.
- 17 % aller diffusen Astrozytome, 44% aller Oligoastrozytome und 78 % aller Oligodendrogliome zeigen einen LOH1p/19q.
- In 65 % der Oligodendrogliome tritt die 1p/19q-Codeletion mit einer IDH1/2 Mutation kombiniert auf.
- LOH1p/19q und ATRX Verlust treten in der Regel nur sich gegenseitig ausschliessend auf.
- Bestimmung über Mikrosatelliten-PCR oder Array-Technologien.
Astrozytome
[Bearbeiten]Astrozytome leiten sich histomorphologisch von den Astrozyten ab und stellen die häufigsten Neoplasien des ZNS dar, gefolgt von den Hirnmetastasen und den Meningeomen. Grad I-Astrozytome (pilozytische Astrozytome) stellen eine eigene Entität dar. In die Grade II bis IV werden die restlichen Astrozytome - nach der Diagnose eines Astrozytoms - nach 4 Kriterien eingeteilt:
1) Kernatypien, 2) Mitosen, 3) Mikrovaskuläre Proliferation, 4) Nekrosen.
Prognostische Faktoren: 1) Alter über 40 Jahre, 2) Tumor größer als 5cm, 3) Kontrastmittelaufnahme, 4) Tumor wächst über die Mittellinie, 5) Neurologische Ausfälle. Liegen drei oder mehr dieser Kriterien vor, ist von einem kürzeren Verlauf auszugehen.
WHO-Grading der Astrozytome:
| WHO °I | (Juveniles) Pilozytisches Astrozytom | Subependymales Riesenzellastrozytom | |
| WHO °II | Diffuses Astrozytom | Pleomorphes Xanthoastrozytom | Pilomyxoides Astrozytom |
| WHO °III | Anaplastisches Astrozytom | Gliomatosis cerebri | |
| WHO °IV | Glioblastom | Gliosarkom | Riesenzellglioblastom |
Derzeitige therapeutische Standards (Oktober 2010):
- WHO II: Abwarten, bei Rezidiv Resektion, Radiotherapie, Chemotherapie
- WHO III: Resektion, Chemotherapie (Nitosourea, Temozolomid), Bestrahlung
- WHO IV: Resektion, Chemotherapie (Temozolomid), Bestrahlung, bei Rezidiv Chemotherapie (Nitosourea bzw. Temozolomid) oder Bestrahlung oder Angiognesehemmer (Bevacizumab)
Weblinks: KEGG: Glioma - Homo sapiens (human)
Pilozytisches Astrozytom
[Bearbeiten]WHO: Grad I
Syn.: Low grade Astrozytom (unpräzise!), juveniles pilozytisches Astrozytom (JPA), Optikusgliom (bei Beteiligung des N. opticus)
Ep.: Kinder und Jugendliche.
Lok.: Kleinhirn, Chiasma opticum/Sehnerv, Hirnstamm.
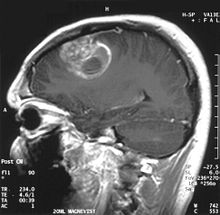
BG.: KM-affin.
Genetik: Pilozytische Astrozytome können bei einer Neurofibromatose Typ 1 auftreten. Abberante Expression des BRAF-Onkogens (Duplikationen, Fusionen oder Punktdeletionen) werden in 60-80% der pilozytischen Astrozytome beobachtet, sind aber selten in diffusen Astrozytomen.
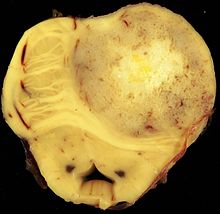
Makro: Eher lokalisiert, selten Hirninfiltration erkennbar.
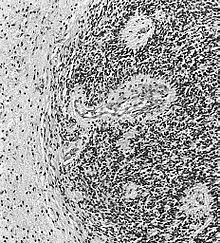
Histo: Biphasisches Muster, ROSENTHAL'sche Fasern, eosinophile Granularkörperchen (rundliche, ovale oder nierenförmige eosinophile Objekte), haarbüschelartiges Pilem, hyaline Gefäße. Gefäßproliferate können ebenfalls auftreten, sind aber kein Zeichen von Malignität.
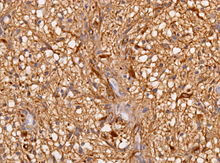
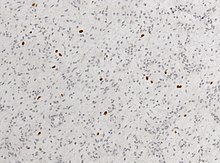
Immuno: Kräftige Expression von GFAP. Der MIB-1 Proliferationsindex ist meist gering (1-5 %).
DD: Diffuses Astrozytom Grad II, Oligodendrogliom.
Prg.: Gut, wenn operabel.
Sonderformen: Pilozytisches Astrozytom mit Anaplasiezeichen (entspricht vom biologischen Verhalten einem WHO III)
Pilomyxoides Astrozytom (PMA)
[Bearbeiten]WHO: Grad II.
Def: Variante eines Pilozytischen Astrozytoms.
Ep: geringer Anteil der pilozytischen Astrozytome, meist Neugeborene oder Kinder.
Lo: hypothalanisch, chiasmatisch, thalamisch.
Genetik: Einzelfälle mit NF1 bekannt.
Makro: Gelatinös.
Histo: prominente mucoide Matrix, angiozentrisches Arrangement der bipolaren Tumorzellen. Keine Rosenthal-Fasern oder EGBs.
Immuno: GFAP, S-100, Vimentin, selten Synaptophysin, MIB-1: 2-20 %
Prognose: Aggressiverer Verlauf als pilozytisches Astrozytom, höheres Rezidivrisiko, Liquoraussaat möglich.
Diffuses Astrozytom
[Bearbeiten]WHO: Grad II.
Ep.: Häufigkeitsgipfel bei jungen Erwachsenen (30-40 Lj.), 10-15 % aller astrozytären Neoplasien.
Lok.: Meist in den Großhirnhemisphären (bei Kindern häufiger im Hirnstamm oder Thalamus), Fälle des Kleinhirns sind selten.
MRT: Keine KM-Aufnahme (außer nach Radiotherapie), Kalzifikationen oder zystische Veränderungen möglich.
Genetik: Fälle in Li-Fraumeni-Syndrom und Morbus Ollier bekannt, Bis zu 80% der Tumore zeigen TP53- und IDHR132H Mutationen. Eine Promotor-Methylierung von MGMT wird in 50 %, von p14ARF in 30 % der Fälle beobachtet.
Makro: Diffuser Prozess ohne klare Abgrenzung. In Kortex-Nähe Auflösung der sichtbaren Mark-Rinden-Grenze. Im Hirnstamm gelegene Tumoren führen zur diffusen Vergrößerung mit Vergröberung des Oberflächenreliefs und evtl. Umschließung der A. basilaris.
Mikro: Tumor mit diffuse Hyperzellularität, geringen bis moderaten Kernatypien, astrozytäre Differenzierungsmerkmale (fibrillär oder gemistozytisch), eosinophile Zytoplasmaausläufer. mikrozytische aufgelockerter fibrillärer Hintergrund, keine signifikante mitotische Aktivität.
Histologische Varianten:
- Fibrilläres Astrozytom (Mikrozystische Formationen, schmales, kaum erkennbares Zytoplasms).
- Protoplasmatisches Astrozytom (seltenste Form, oft mucoide Degeneration, kleine Zellfortsätze, kaum GFAP).
- Gemistozytisches Astrozytom (mind. 20% Gemistozyten: breites eosinophiles Zytoplasma, exzentrischer Kern, oft perivaskuläre lymphozytäre Infiltrate).
Immuno: Tumorzellen sind GFAP, S-100 und Vimentin positiv, WT1 und MAP2 können fokal in den Zellfortsätzen beobachtet werden. IDH1R32H finden sich in 60-80 % der Tumoren, p53 kann in einzelnen Fällen sehr extensiv ausfallen. MIB-1 +/- 2 % (Proliferationsmarker). Bcl-2 wird oft in Gemistozyten beobachtet.
SF: Nicht-pilozytisches tectales Gliom, periaquaedukal, eher diffus, langsam wachsend, nicht KM-affin.
DD.:
- Reaktive Gliose (z.B. bei Demyelinisierung)
- Pilozytisches Astrozytom - Eher lokalisiert, KM-affin!
- Astrozytom °III - + Mitosen (Kriterium 2).
- Gliomatosis cerebri
- Oligodendrogliom
Prg.: Mittleres Überleben: 6-8 Jahre. Nicht selten nach einigen Jahren Transformation zum Astrozytom °III oder °IV. Sehr ungünstig sind Hirnstamm- und Thalamusgliome. Ausgedehnte Tumore, gemistozytische Varianten, p53-Mutationen und MIB-1 Proliferation über 5% zeigen ungünstigere Verläufe. Jüngere Patienten haben oft eine bessere Prognose. IDH-Mutationen haben eine diagnostische, und dahingehend eine prognostische Relevanz, dass IDH wildtyp Astrozytome ein biologisches Verhalten ähnlich dem eines Glioblastoms zeigen (N Engl J Med 2015; 372:2481-2498).
Anaplastisches Astrozytom
[Bearbeiten]malignant astrocytoma (unpräzise)
WHO: Grad III.
Ep.: Häufigkeitsgipfel zwischen 40-50 Lebensjahr, entweder de novo oder durch Progression aus einem diffusem Anstrozytom (WHO II). Männer leicht überrepräsentiert.
Lok.: Großhirnhemisphären (bei Kindern auch Hirnstamm oder Thalamus).
MRT: KM-affin!
Genetik: Tp53 (70 %), IDH1 (65 %) und PTEN (20 %) Mutationen. Selten EGFR-Amplifikation. LOH 10q (40-50 %), 17p (50-60 %), 19q (40-50 %), 22q (30 %).
Makro: Vergrößerung infiltrierter Strukturen, Gewebe kann weicher und opaker imponieren.
Mikro: Stärkere Hyperzellularität, Zunahme der Kernatypien einschließlich multinukläre Tumorzellkerne, Prominentere Nukleolen, Mitosen. Keine Gefäßproliferation oder Nekrosen.
Immuno: MIB-1 typischerweise zwischen 5-10 %,ansonsten entspricht das Immunprofil dem diffusen Astrozytom WHO Grad II.
SF: Glioneuronaler Tumor mit Neuropil-Inseln: Mikronoduli mit NeuN-positiven Tumorzellkernen (NeuN kann in neoplastischen Zellen auch negativ sein) und Synaptophysin-positivem Neuropil. Prognose ansonsten gleich.
Prg.: Deutlich ungünstiger als bei Grad °II, Üblicherweise Progression zum Glioblastom. Ältere Patienten und Fälle mit EGFR-Amplifikation zeigen einen ungünstigeren Verlauf. IDH-Wildtyp-Tumore haben eine schlechtere Prognose als Glioblastome mit nachgewiesener IDH-Mutation.
Glioblastom (GBM)
[Bearbeiten]WHO: Grad IV.
Syn.: Highgrade Astrozytom, Glioblastoma multiforme (GBM).
Ep.: Häufigster primärer Hirntumor (15 % aller intrakraniellen, 70 % aller astrozytären Tumoren. Häufigkeitsgipfel in der 6. Dekade aufwärts. Inzidenz: 3/100.000, Männer leicht überrepräsentiert.
Lok.: Meist subkortikal in den Großhirnhemisphären, typischerweise frontotemporal, bei Kindern häufiger im Hirnstamm. Kleinhirn und Rückenmark nur selten.
BG.: Ring- oder girlandenförmiges KM-Enhancement (höchste Zelldichte) mit zentraler Nekrose und perifokalem Ödem (entspr. der Tumorinfiltration). (DD.: Abszess, Metastase).
Einteilung:
- Primäres Gliobastom (95 %) - de novo.
- Sekundäres Glioblastom (5 %)- Entstanden aus einem präexistenten Astrozytom (WHO II oder III).
Genetik: Primäre und sekundäre Glioblastome zeigen große genetische Unterschiede. Sekundäre Glioblastome zeigen das typischerweise ein genetisches Profil mit IDH1 (75 %) und p53 (81 %)-Mutationen, welches auch bei diffusen Astrozytomen (WHO II und III) beobachtet wird. Nekrosen werden nur in 50 % der IDH-mutierten primären Glioblastome (3,5 %) beobachtet.
Primäre Glioblastome zeigen folgende genetische Eigenschaften:
- EGFR Amplifikation (40 %), davon 50 % EGFRvIII-assoziert
- PTEN Mutationen (25 %)
- P53 Mutationen (25 %) bzw. MDM2 Amplifikation (10 %)
- p16INK4a (31 %)
- NF1 Mutationen (14 %)
- PI3KR Mutationen (10 %)
- ERBB2 Mutationen (8 %)
Sowohl primäre als auch sekundäre Glioblastome zeigen typischerweise einen LOH10q, p14ARF-Alterationen. Methylierung der MGMT-Promotorregion ist in beiden Gruppen mit einem besserem Therapieansprechen auf Temozolomid und damit längerem Überleben assoziert.
Molekulare Subklassen: Glioblastome lassen sich anhand Genexpressionsmuster in proneural, mesenchymal oder proliferative Tumore einteilen. Rezidivtumore zeigen in der Regel einen mesenchymalen Typ (Phillips et al. Cancer Cell 2006).
Makro: Bunte Schnittfläche, gelbliche Nekrosen, hämorrhagische Stippchen, diffus infiltrierend, bevorzugt Wachstum entlang von Nervenbahnen (z.B. Corpus callosum), oft zur Gegenseite wachsend (sog. Schmetterlingsglioblastom), expandierend.
Mikro: Diffuser infiltrativer Prozess, Hyperzellularität, Endothelproliferate, strichförmige bis geografische Nekrosen (Koagulationsnekrose, betrifft Parenchym und Gefäße, kaum Immunozyten, DD: Infarkt), in deren Randbereich erhöhte Zelldichte mit palisadenförmiger Anordnung der Zellkerne, Mitosen, keine Nukleolen, fibrillärer Hintergrund. Das histologische Bild ist sehr variabel. Evtl. perivaskuläre Lymphozyteninfiltrate.
IHC: Meist GFAP +, MIB-1 > 9 %.
Prg.: Nicht heilbar, Lebenserwartung je nach Therapie zwischen Monaten und Jahren. Alter des Patientens zum Diagnosezeitpunkt ist der stärkste prognostische Faktor. IDH1-mutierte Glioblastome haben eine deutlich bessere Prognose. Nekrosen und unmethylierter MGMT-Status sind mit einem kürzeren Überleben assoziert.
Gewebemuster („Tissue patterns“):
Bestimmte morphologische Veränderungen werden nur als Gewebeuntereinheiten angesehen, dar sie sich zwar morphologisch vom konventionellen Glioblastom unterscheiden, aber prognostisch keinen Unterschied machen.
Dazu zählen:
- Kleinzelliges Glioblastom (small cell glioblastoma)
- Glioblastom mit oligodendroglialer Komponente
- Glioblastom mit Granularzellkomponente
- Glioblastom mit epithelialer Metaplasie
Hingegen zeigen Varianten deutliche Unterschiede die eine eigenständige Gruppierung berechtigen. Dazu zählen:
Riesenzellglioblastom
[Bearbeiten]WHO: IV.
Ep: 5 % aller Glioblastome, Mittleres Alter: 40 Jahre, auch Kinder bekannt.
Genetik: De novo, p53 Mutation 75-90 %, PTEN mutationen (30 %), keine p16INK4a Verluste: hybrides Profil zwischen klassischen primären und sekundären Glioblastomen.
Makro: Geringeres infiltratives Wachstum.
Histo: Zahlreiche zum Teil bizarre, mehrkernige Riesentumorzellen mit Lipidvakuolen, verstärkte Akkumulation eines retikulären Netzwerkes, häufig atypische Mitosen. Häufig Nekrosen, während Gefäßproliferate nur in einer Minderheit der Tumore beobachtet werden.
Immuno: Riesenzellen zeigen eine variable Expression von GFAP,sind positiv für p53, EGFR.
Prognose: Etwas besser als klassische Glioblastome.
 |
Gliosarkom
[Bearbeiten]WHO: IV.
Ep: Altersverteilung identisch zu klassischen Glioblastomen.
Genetik: gliale und sarkomatöse Anteile zeigen die gleichen genetischen Veränderungen. p53 (23 %) und PTEN Mutationen (38 %), p16INK4a Deletionen (37 %), aber so gut wie keine EGFR Amplifikationen.
Makro: Derbe Läsion.
Histo: Gliale Anteile wie bei konventionellem Glioblastom sowie sarkomatöse Anteile mit dicht gepackten Bündeln an spindeligen Tumorzellen, welche reichlich Kollagen aufweisen. Die sarkomatösen ANteile lassen sich in einer Retikulinfärbung gut darstellen.
Immuno: Gliale Anteile: GFAP positiv, sarkomatöse ANteile GFAP negativ.
DD: Glioblastom mit Desmoplasiezeichen (Meningeale Infiltration.)
Prog: In manchen Studien etwas besser als Glioblastom, in anderen Studien keine Unterschiede.
Gliomatosis cerebri (GC)
[Bearbeiten]WHO: Grad III.
Synonym: Astrocytosis cerebri.
Lokalisation: Großhirn (75 %), Kleinhirn (30 %), Hirnstamm (50 %), Rückenmark (9 %).
Ep: Typischerweise zwischen dem 30-40 Lebensjahr, allerdings sind Fälle aus allen Altersgruppen beschrieben.
Einteilung:
- Typ 1: klassische Form (rein diffus): primäre CG.
- Typ 2: mit solideren Tumoranteilen (Tp53-Mutationen, IDH1 Mutationen): sekundäre CG.
Histologie: diffus angehobene Zelldichte, meist elongierte Kerne mit geringer Pleomorphie und astrozytärer Morphologie, selten Mitosen.
Immuno: Tumorzellen zeigen variable Expression für GFAP und S-100. MIB-1 < 1-30 %.
Die Diagnose einer Gliomatosis cerebri ist nur in Zusammenschau mit der radiologischen Bildgebung oder postmortalem Sampling entsprechender Regionen möglich, da definitionsgemäß 3 oder mehr Lappen von einem diffus wachsenden glialen Tumor befallen sein müssen.
Komplikationen: Kognitive Ausfälle.
DD: Reaktive Astrogliose, Infiltrationszone eines diffusen Astrozytoms/Glioblastoms.
Pleomorphes Xanthoastrozytom (PXA)
[Bearbeiten]WHO: Grad II.
Ep: Weniger als 1 % der astrozytären Neoplasien.
Lok: 90 % supratentoriell. Der Tumor ist meist im Temporallappen lokalisiert.
Genetik: In 65 % BRAF V600E Mutationen, oft kombiniert mit homozygoten Deletionen von p16ink4a, zusätzlich p53 Mutationen bekannt, Einzelfälle im Rahmen einer NF1 beobachtet.
Makro: oberflächlich mit überwiegend leptomeningealer Ausbreitung in den Subrachnoidalraum, in der Hälfte der Fälle als Knötchen innehalb einer Zyste. Scharfe Demarkierung des Tumors zum darunterliegenden Hirnparenchym.
Histo: Faszikuläres Arrangement der Tumorzellen, welche Lipidisierungen aufweisen könne. Bizarre Astrozytenformationen tragen zu dem pleomorphen Erscheinungsbild bei. Perivaskuläre Lymphozytenansammlungen und Eonsinophilic granular bodies (EGB) werden oft gesehen, sind aber nicht spezifisch für einen PXA. In der Retikulinfärbung Umscheidung einzelner oder ganzer Tumorgruppen sichtbar. In Kryostatschnitten können Lipidanteile mit Ölrot sichtbar gemacht werden. Anaplastische Formen mit Gefäßproliferaten, Nekrosen und mehr als 5 Mitosen/10 HPF sind Einzelfälle.
Immuno: Die Tumorzellen sind positiv für GFAP und S-100. Ganglienzellen können im Tumor auftreten und lassen sich entsprechend mit Synaptophysin, MAP2 und Neurofilament darstellen. CD34 wird regelmäßig im Tumor exprimiert. MIB-1: 1 %.
Prognose: 5-Jahres-Überlebensrate: 81 %.
Komplikationen: Rezidivierende Tumore können maligne Transformationen durchlaufen.
DD: Gangliogliom, Riesenzellglioblastom, Pilozytisches Astrozytom, Malignes fibröses Histiozytom.
Subependymales Riesenzellastrozytom (SEGA)
[Bearbeiten]Subependymal giant cell astrocytoma
WHO: Grad I.
Epidemiologie: Kinder und junge Erwachsene.
Lokalisation: Meist intraventrikulär, von Zellen unterhalb des Ependyms ausgehend.
Genetik: Als autrosomal-dominanter Erbgang im Rahmen einer Tuberösen Sklerose (Morbus BOURNEVILLE-PPRINGLE) auftretend. Bis zu 50 % der TSC-Fälle sind Neumutationen. Einzelne sporadische Fälle sind beschrieben.
Makro: Kompakt aufgebauter, gut vaskularisierter, verkalkender Tumor.
Histo: Astrozytäre Riesenzellen mit pinkfarbenem Zytoplasma und exzentrisch gelegenen vesikulären Kernen, daneben polygonale bis fusiform imponierende gliale Tumoranteile, stellenweise auch ganglioid imponierende Zellen. Mitosen sind selten. Mastzellen können einen nicht unwesentlichen Anteil am Tumor ausmachen.
Immuno: Variable Expression von GFAP, S-100, Synaptophysin und Neurofilament. Der MIB-1 Proliferationsindex ist sehr gering.
Komplikation: Störung des Liquorabflusses.
Prognose: gut, auch bei subtotaler Entfernung.
DD: Gemistozytisches Astrozytom, Riesenzellglioblastom
 | ||
 |
 |
 |
Oligodendrogliome
[Bearbeiten]Oligodendrogliome werden von der WHO in zwei Gruppen eingeteilt:
- °II: Diffuses Oligodendrogliom
- °III: Anaplastisches Oligodendrogliom
Oligoastrozytome werden unter dem Punkt „Gemischte Gliome“ vorgestellt.
Oligodendrogliom
[Bearbeiten]WHO: Grad II.
Ep.: Erwachsenenalter (40-50 Lj.), 5-6 % aller Gliome.
Lok.: Meist Großhirnhemisphären, bevorzugt kortikal und frontal (50-60 %).
BG: Oft vergleichsweise gut abgegrenzt. Wenig Ödem. Verkalkungen.
Genetik: In 80 % der Tumoren: LOH1p/19q, in mehr als 90% der adulten Tumore: IDH1-Mutation (Fehlen schließt jedoch ein Oligodendrogliom nicht aus), diese haben meist zusätzlich eine Methylierung von MGMT. EGFR Amplifikation ist typischerweise nicht vorhanden.
Klinik: 2/3 der Pat. haben epileptische Anfälle.
Makro: Weicher, gelatinöser Tumor, häufig mit fokalen Verkalkungen.
Mikro: Monotone Zellen mit kleinen runden Kernen, sichtbaren Nukleolen, häufig artifiziellem perinukleären Halo und sichtbaren Zellgrenzen („Spiegeleier“). Kapillaren begrenzen Tumorzellen und Tumorzellhaufen in geometrischem Muster (Honigwabenstruktur, „chicken wire“). Gleichförmige Zelldichte. Häufig Verkalkungen. Im Kortex können perineuronale Satellitose und perivaskuläre sowie subpiale Akkumulation neoplastischer Zellen auffallen. Evtl. Palisaden, evtl. mikrozystische Veränderungen, evtl. Minigemistozyten (plumpe astrozytär anmutende Zellen mit eosinophilem hyalinem evtl. fibrillärem Plasma, die allerdings oligotypische montone Kerne und kaum Zellfortsätze aufweisen).
Immuno: S-100 +, Vimentin: variabel, MBP -, Zytokeratine -, p53 meist -, MAP2 und Olig-Expression sind nicht spezifisch für Oligodendrogliome. MIB-1 meist unter 5 %, Minigemistozyten und gliofibrilläre Oligodendrozyten: GFAP + Fälle mit fokal neuronaler Differenzierung (NeuN +, Synaptophysin +) bekannt.
Prg.: Bessere Prognose und geringere Progression als beim Astrozytom (10-JÜR: 50 %). Prognostische Faktoren: LOH 1p/19q, Patientenalter, Pleomorphie, Zelldichte, Kern-Plasma-Relation, MIB-1-Index.
DD: Demyelinisierungen, DNT, klarzelliges Ependymom, Neurozytom .
Anaplastisches Oligodendrogliom
[Bearbeiten]WHO: Grad III.
Ep: 1 % aller Hirntumoren, 20 % aller Oligodendrogliome, typischerweise zwischen 45-55 Lj. Progression von WHO Grad II bekannt.
Genetik: 2/3 LOH 1p/19q, Deletionen von CDKN2A auf 9p21 in 1/3, In weniger als 10 % EGFR und MDM2-Amplifikationen bekannt.
Makro: Zirkumskript bis diffus. Verwaschene Mark-Rinden-Grenze, expandierendes Wachstum.
Histo: Bild wie Oligodendrogliom WHO II, jedoch zunehmende Pleomorphie, höhere mitotische Aktivität und evtl. Gefäßproliferate und Nekrosen.
Prg: Mittleres Überleben: 3,5 Jahre, Alter, 1p/19q-Status, Mitosen, Nekrosen, mikrovaskuläre Proliferationen als prognostische Faktoren.
 |
 |
 |
Mischgliome
[Bearbeiten]- Oligoastrozytom; NOS (WHO II)
- Anaplastisches Oligoastrozytom; NOS (WHO III)
Ep: Je nach Tumorregister beträgt der Anteil der Mischgliome 1,5-9 %. Pat. sind typischerweise zwischen 35-45 Jahre.
Histo: Gemischte Tumoren enthalten sowohl Anteile eines Astrozytoms als auch eines Oligodendroglioms. Anhand ihrer genetischen Veränderungen können Sie als Astrozytome (IDH mutiert & ATRX Verlust) oder Oligodendroglioma (IDH mutiert und 1p/19q Codeletion) reklassifiziert werden.
In die Gruppe der Mischgliome werden daher nur noch Tumore eingeteilt, für die noch keine genetische Untersuchung erfolgt ist bzw. deren molekulares Profil nicht eindeutig ist.
Immuno: GFAP, Vimentin, WT1 in astroglialen Anteilen. MIB-1 typischerweise unter 6 %.
Prg + Genetik: 5-J-ÜL.: 58%. Ein LOH1p/19q in Mischgliomen (30-50% der Fälle) ist wie bei Oligodendrogliomen ein prognostisch günstiger Marker, während p53-Mutationen wie bei Astrozytomen mit einem schlechterem Überleben assoziert sind. Nahezu alle Mischgliome sind IDH1/2 mutiert.
DD: DNT, Glioblastom mit oligodendroglialer Komponente, demyelinisierende Erkrankungen.
 |
 |
Ependymale Tumoren
[Bearbeiten]Zu den ependymalen Tumoren zählen Subependymom, myxopapilläres Ependymom, während das Ependymoblastom zu den embryonalen Tumoren gerechnet wird.
Ependymom
[Bearbeiten]ependymoma
WHO: Grad II.
Ep.: Hauptsächlich Kinder, dort 8-12% aller intrakraniellen Tumore 5% aller neuroepithelialen Tumore, bzw. 50% aller spinalen Gliome.
Lok.: Bei Kindern eher infratentoriell am Kleinhirn am Boden des 4. Ventrikels, bei Erwachsenen eher supratentoriell oder im zerviko-thorakalen Spinalkanal. Selten Tumore der Ovarien bekannt.
Genetik: Spinale Ependymome treten gehäuft bei Neurofibromatose Typ 2 auf. Einzelfälle bei NF1 und Turcot-Syndrom bekannt. 30% der Ependymome haben Deletionen bei 22q. Supratentorielle Ependymome zeigen gehäuft LOH auf Chr.9. Keine EGFR-Amplifikation oder LOH1p/19q bekannt.
Makro: exophytisch wachsend, relativ umschrieben, Zysten möglich. Tumor demarkiert sich relativ scharf vom ZNS.
Mikro: Relativ monomorphes Zellbild, moderate Zelldichte, perivaskuläre Pseudorosetten mit kernfreien Räumen, echte ependymale Rosetten mit zentralem Lumen, selten ependymale Kanäle mit säulenartig aufgereihten Tumorzellen um ein zentrales Lumen. Wenige Mitosen, Regressive Veränderungen mit Blutungen und Verkalkungen sowie Herde mit hoher Zelldichte möglich. Kleinere Nekrosen sind laut aktueller WHO-Klassifikation auch noch mit einem WHO Grad II kompatibel.
Varianten:
- Zellulär (meist extraventrikulär).
- Papillär (seltenste Variante mit epithel-ähnliche, glatte Oberfläche).
- Klarzellig (Oligo-ähnliches Zellbild, meist supratentoriell bei Kindern).
- Tanyzytisch (meist spinal, lange bipolare Zellausläufer).
Immuno: GFAP- und WT1-positive Fortsätze, Perinukläre EMA-positive "dots". Tumorzellen können mit S-100 und Vimentin dargestellt werden. Variable Positivität für EMA und Nestin. Ependyme des 3. Ventrikels können TTF-1-positiv sein. Kein Nachweis einer IDH1 R132H-Mutation.
Prg.: Histologisch benigne, aber je nach Lage inoperabel. MIB-1 unter 4% sind mit einer besseren Prognose assoziert. 5-Jahres Überleben: 55 %.
DD: Pilozytisches Astrozytom (tanyzytische Variante), anaplastisches Ependymom.
Anaplastisches Ependymom
[Bearbeiten]anaplastic ependymoma
WHO: Grad III.
Ep: Häufiger in Kindern, als bei Erwachsenen, meist in der hinteren Schädelgrube.
Genetik: Verlaufsformen von WHO II nach WHO III bekannt. LOH Chr. 9 und 13 werden mit der Progression in Verbindung gebracht.
Histo: Schmale Pseudorosetten. Erhöhte Zelldichte, Mitosen, Gefäßproliferate, Nekrosen.
Immuno: GFAP fällt oft geringer als bei den WHO II Ependymomen aus.
Prognose: Alter unter 3 Jahre, leptomeingeale Aussaat, inkomplette Resektion und ausgeprägte Anaplasiemerkmale sind mit einer schlechteren Prognose assoziert.
Myxopapilläres Ependymom
[Bearbeiten]WHO: Grad I.
Ep.: Langsam wachsender Tumor des jüngeren Erwachsenenalters (Peak: 20-30. Lj), 10 % aller ependymalen Tumoren.
Genetik: Bisher keine typischen Veränderungen bekannt.
Lok.: Häufig am Filum terminale, dort der häufigste intramedulläre Tumor. Selten thorakal oder ventrikelnah. Ektope Tumoren im Bereich der subkutanen Gewebes der sacrococcygealen Region bekannt.
Makro: Gut abgrenzbar, oft abgekapselt.
Histo: Kubisch elongierte Tumorzellen, ependymale Rosetten, perivaskuläre Pseudorosetten, Alcian-blau-positive mucinöse Ablagerungen, sklerosierte Gefäße. Selten Koexistenz mit Lipomen.
IHC: Die Tumoren sind S-100 und Vimentin positiv und zeigen GFAP-positive Fortsätze. Pan-CK ist negativ MIB-1: 1-2%.
Komplikation: Störung der Liquorabflusswege.
Prognose: Bei kompletter Resektion „en bloc“ gut.
DD: Schwannom, Paragangliom, Ependymom, Chordom.
Subependymom
[Bearbeiten]WHO: Grad I.
Ep: Langsam wachsender Tumor aller Altersgruppen mit Schwerpunkt 45-75. Lebensjahr, 8 % aller ependymalen Neoplasien. Männer sind doppelt so häufig betroffen, wie Frauen.
Lokalisation: Überwiegend im 4. Ventrikel (50 %), Fälle in den Seitenventrikeln (40 %), 3. Ventrikel, Septum pellucideum und intraspinal sind beschrieben.
Bg: Scharf begrenzt, nodulär, ohne Enhancement.
Genetik: Derzeit keine spezifischen Veränderungen bekannt.
Makroskopie: Exophytisches Wachstum, derbe bis kalkharte Knötchen.
Histo: Tumorzell-Clustering isomorpher Kerne vor einem fibrillärem Hintergrund. Geringe mitotische Aktivität. Sklerosierende Gefäße, mikrozystische Auflockerungen, Kalzifikationen und Hämosiderinablagerungen möglich. Tumore der Seitenventrikel können auch kleinere Zysten aufweisen. Gemischte Subebendymome/Ependymome sind bekannt.
Immunhistochemie: Variable GFAP-Expression. Der MIB-1 Proliferationsindex beträgt zwischen 0 und 1,5 %.
Prognose: besser als bei konventionellen Ependymomen, Zufallsbefunde bei Autopsien beschrieben.
Tumoren des Plexus choroideus
[Bearbeiten]Plexustumore machen 2-4 % der Tumoren unter 15 Jahre, 10-20 % der Tumore im ersten Lebensjahr aus. Verteilung: 50% Seitenventrikel, 5 % III. Ventrikel, 40 % IV. Ventrikel, 5 % multipel. Plexuspapillome sind 5 mal häufiger als Plexuskarzinome.
Plexuspapillom
[Bearbeiten]WHO: Grad I.
Epidemiologie: 0,5 % der Hirntumoren, überwiegend Kinder und Jugendliche.
Lokalisation: Seitenventrikel, 3. und 4. Ventrikel.
Genetik: Meist sporadisch, Einzelfälle bei Li-Fraumeni oder Aicardi-Syndromen bekannt.
Makro: Blumenkohlartig.
Histo: Papilläre Formationen aus kubischem bis hochprismatischem Epithel, Mitosen sehr selten. Seltene onkozytäre, glanduläre und muzinöse Formen bekannt.
Immuno: Nachweis von Synaptophysin, Kir 7.1, EAAT-1, Vimentin, Podoplanin, pan-Zytokeratin, in 75% CK7+/CK20- Kombination, GFAP in 25-50% der Plexuspapillome, 75% Transthyretin,
DD: Normaler Plexus choroideus, atypisches Plexuspaillom, Ependymom.
Komplikationen: Liquoraufstau.
Prognose: Nach Operation gut.
Atypisches Plexuspapillom
[Bearbeiten]WHO: Grad II.
Ep: 15 % der Plexustumoren.
Histo: Zwei oder mehr Mitosen auf 10 high power fields, erhöhte Zelldichte und Pleomorphie, fokale Nekrosen möglich, ansonsten Bild wie bei Plexuspapillom Grad I WHO.
Immuno: Der MIB-1 Proliferationsindex ist oft höher als bei Plexuspapillomen Grad I WHO.
DD: Plexuspapillom, Ependymom.
 |
Plexuskarzinom
[Bearbeiten]WHO: Grad III.
Epidemiologie: 0,5 % aller Hirntumoren, bevorzugt im Kindesalter auftretend.
Genetik: Vereinzelt im Zusammenhang mit LI-FRAUMENI-Syndrom beschrieben.
Histo: Oft solides Wachstum und erhöhte Zelldichte, Kernpleomorphie, Kernatypien, Mitosen (mehr als 5/10 HPF), Nekrosen, ZNS-Infiltration.
Immuno: Plexuskarzinome sind positiv für pan-CK, EAAT-1, Kir7.1, seltener S-100, GFAP (2 0%).
Komplikationen: Hirndruck durch Liquoraufstau, Infiltration des Hirnparenchyms. Metastasen.
Prognose: Abhängig von Operationsmöglichkeit und Ansprechen auf Chemotherapie.
DD: AT/RT, papilläres Meningeom, Karzinom-Metastasen.
 |
Gliale Tumoren unbekannter Herkunft
[Bearbeiten]Astroblastom
[Bearbeiten]WHO: Noch kein Grad zugeteilt.
Ep: Rarität, sowohl im Kindes auch Erwachsenenalter bis 30. Lj. auftretend.
Lok: Superfizieller glialer Tumor.
Makro: groß, zystisch, deutliche Abgrenzung zum ZNS (pushing margin).
Histo: Vasozentrischem Wachstum, die unipolare plumpen Zellfortsätze sind auf die hyalinisierten Gefäße ausgerichtet. Anaplastische Formen mit Mitosen und Pseudopalisaden-Nekrosen sind beschrieben. Der Tumor darf definitionsgemäß keine Anteile eines konventionellen diffusen Astrozytoms/Ependymoms haben, auch sind die Zellfortsätze kürzer als bei Ependymomen und zeigen keinen fibrillären Aspekt.
Immuno: GFAP positiv, Synaptohysin negativ, fokal EMA/panCK. MIB-1: 1-18 %.
DD: Ependymom, PGNT, Papilläres Meningeom.
Chordoides Gliom des 3. Ventrikels
[Bearbeiten]WHO: Grad II.
Ep: Seltener Tumor im Erwachsenenalter.
Lok: Ursprungszelle möglicherweise subkomissurale Ependymzellen des 3. Ventrikels.
Makro: Solider Tumor an der Wand des 3. Ventrikels mit scharfer Grenze zum ZNS.
Histo: Uniforme, epitheloid imponierende Zellen mit uniformen Kernen in Strängen inmitten einer schwach basophilen, muzinösen Matrix. Zwischen den neoplastischen Zellen können prominente lymphoplasmazytische Infiltrate mit RUSSEL-Körperchen auftreten.
Immuno: GFAP und S-100 positiv, fokal EMA an der Zelloberfläche möglich. MIB-1: 0-2 %.
Komplikationen: endokrine Störungen, komplette Resektion an dieser Lokalisation nicht immer möglich.
DD: Chordom, Chordoides Meningeom.
Angiozentrisches Gliom
[Bearbeiten]auch als angiocentric neuropithelial tumor bezeichnet.
WHO: Grad I.
Ep: Epilepsie-assozierter, langsmer Tumor der Hemisphären bei Kinder/jungen Erwachsenen.
Lok: Meist superifiziell cerebral, kein KM-Enhancement. Die Lokalisation des Tumors passt nicht zu Ependymomen (Ursprung: Radiale Glia?).
Histo: monomorphe, bipolare spindelige Zellen mit Orientierung um Gefäße (entlang oder pseudopapillär wie bei Ependymomen): Schwannomähnlich. Myxoide Matrix, Tumor eher zellarm, kann aber hierfür viele Mitosen aufweisen.
Immuno: GFAP, EMA dots, negativ für neuronale Marker, MIB-1: 1-5 %.
Neuronale und gemischt neuronal-gliale Tumoren
[Bearbeiten]Gangliozytom
[Bearbeiten]WHO: Grad I.
Ep: Kinder und junge Erwachsene, zusammen mit Gangliogliomen 0,4 % aller ZNS-Tumore.
Lok: Bevorzugt supratentoriell mit Prädilektion des Temporallappens.
Makro: Umschriebener Tumor als Knötchen innerhalb einer Zyste.
Histo: große neuronale Zellen unterschiedlichen Kalibers vor feinem fibrillärem Hintergrund. Gliazellen des normalen Kortex fehlen und geben daher dem Tumor ein hypozelluläres Erscheinungsbild. Perivaskuläre Lymphozytenansammlungen und Eosinophilic granular bodies (EGB) können vorkommen.
Immuno: Nachweis neuronaler Antigene in den Tumorzellen.
DD: Hamartom, Gangliogliom, Gangliozytom des Kleinhirns (Lhermitte-Duclos).
 |
Desmoplastisches infantiles Astrozytom/Gangliogliom
[Bearbeiten]WHO: Grad I.
Ep: Kleinkindesalter (1-24 Monate).
Lok: Supratentorielle Lokalisation: Kortex/Dura („meningeozerebrales Astrozytom“).
Makro: Großer zystischer Tumor, Kortikale Zyste mit xanthochromer Flüssigkeit, Tumor nur extrazerebral.
Histo: prominentes desmoplastisches Stroma (fibroblast-like) mit Nachweis von Retikulin. Darin einliegend Astrozyten (DIA) bzw. neuronale Komponente (DIG: klein, runde Kerne, wenig Perikaryon), scharfe Demarkierung vom Kortex.
Immuno: GFAP +, MAP2 +, MIB-1 meist unter 2 %, bei DIG: Synatophysin positiv.
Prognose: Gut nach Resektion.
DD: Solitärer fibröser Tumor, Gliosarkom, Astrozytom mit Desmoplasiezeichen.
Dysembryoplastischer neuroepithelialer Tumor (DNT)
[Bearbeiten]WHO: Grad I.
Ät: Benigner, epilepsie-assozierter, kortikaler Tumor mit komplexem Aufbau mit oft stabilem Verlauf.
Ep: DNTs machen 10-15 % aller Epilepsie-chirurgischen Eingriffe aus, Kinder - Erwachsene (30 Lj.), Männer überrepräsentiert.
Lok: Prädilektion für den Temporallappen (50 %), ansonsten meist kortikal, selten Kleinhirn oder Hirnstamm, in 80 % mit kortikaler Dysplasie assoziert.
Klinik: Epilepsien.
Genetik: Fälle bei NF1 bekannt. Keine TP53 Mutationen bekannt.
Makro: Zystisch, viskös, meist nur intrakortikal, Kalzifikationen, Exophytisches Wachstum, Deformation des überliegenden Calvariums möglich.
Histo (Einteilung):
- Einfache Form: Nur glioneuronales Element: zur Kortexoberfläche ausgerichtete Säulen aus axonalen Bündeln, welche von Oligodendroglia-ähnlichen Zellen gesäumt werden. Die Neurone "schwimmen" hierbei in der umgebenden blassen-eonionophilen Matrix.
- Komplexe Form: Gliaknötchen (astrozytär, oligodendroglial oder neuronal, vaskuläre Proliferate) und glioneuronales Element.
- Unspezifische Variante: Solitäres Gliaknötchen ohne glioneuronales Element, nur in Kombination mit Klinik und Bildgebung diagnostizierbar.
Immuno: MIB-1: 0-8 %.
Wikipedia: DNT.
DD: Oligondendrogliom, Gangliogliom, pilozytisches Astrozytom, diffuses Astrozytom.
Gangliogliom
[Bearbeiten]WHO: Grad I.
Ep: häufigste Entität bei Epilepsie (1% aller Hirntumoren, 25-30 % aller Epilepsiechirurgischen Eingriffe), Peak: 10 Lj.
Genetik: In ~ 20 % BRAF V600E Mutationen. Gain of Chr. 7, aber keine EGFR oder p53 Mutationen. Assoziation mit COWDEN-Syndrom.
Makro: Zystische Läsion mit wandständigem Knötchen.
Histo: Kombination aus neuronal differenzierten multipolaren, dysplastischen Zellen wie bei einem Gangliozytom mit zusätzlicher glialer Komponente. Die gliale Komponente kann sowohl das Bild eines pilozytischen Astrozytoms als auch eines diffusen Astrozytoms aufweisen. Retikulin-positive Abschnitte möglich. Charakteristisch sind Kalzifikationen, Eosinophilic granular bodies (EGB) und lymphozytäres Cuffing der Gefäße.
Immuno: Neuronale Zellen: NeuN, MAP2, Neurofilament, Synaptophsin. 70-80 % der Gangliogliome sind CD34 positiv, auch perineuralen Satellitenzellen. Gliale Anteile: GFAP positiv, MAP2 selten positiv. MIB-1: 1-2 %.
Prognose: sehr gut: 94 % der Patienten sind über 7.5 Jahre Rezidivfrei.
DD: Pilozytisches Astrozytom/Diffuses Astrozytom mit ortsständigen Neuronen, PXA.
Anaplastisches Gangliogliom
[Bearbeiten]WHO: Grad III.
Histo: Neuronale-Zellkomponente wie bei Gangliozytom/gliom sowie gliale Komponente mit Anaplasiezeichen wie bei Anaplastischen Astrozytom/Glioblastom. Nekrosen.
 |
 |
Zentrales Neurozytom / Extraventrikuläres Neurozytom
[Bearbeiten]WHO: Grad II.
Ät: Intraventrikulärer neuronaler Tumor, von subependymalen neuroglialen Vorläuferzellen ausgehend.
Ep: Peak um das 30 Lj. Weniger als 0,25 % aller intrakraniellen Tumoren.
Lok: Intraventrikulär, typischerweise Sietenventrikel (Foramen monro) SF: extraventrikuläres Neurozytom.
Genetik: 1 Fall bei VHL bekannt. Keine 1p/19q-Deletionen.
Makro: Umschrieben, Kalzifikationen, selten Blutung, extraventrikuläre Neurozytome: zystisch mit wandständigem Knötchen.
Histo: Monomorphes Zellbild der rundlichen bis ovoiden Kerne, welche ein feines Salz-und-Pfeffer-Sprenkelungsmuster des Kernchromatins aufweisen. Das ansonsten ruhige Zellbild wird gelegentlich durch kernfreie Räume (Neuropil-Inseln) aufgelockert. Oligodendrogliom-ähnliches Zellbild, Gefäßproliferate möglich.
Immuno: Synaptophysin +, NeuN +. Bei einer erhöhten MIB-1 Proliferationsrate von über 2 % werden die Tumoren als atypische Neurozytome bezeichnet.
Komplikation: Liquorabflußstörung.
Prognose: Die 5-Jahres-Überlebensrate nach Operation beträgt 81 %.
DD: Oligodendrogliom, Ependymom, SEGA, Plexuspapillom, Pineozytom.
Zerebelläres Liponeurozytom
[Bearbeiten]WHO: Grad II (früher [WHO 2000]: Grad I).
Ep: Peak: 50 Lj.
Lokalisation: Kleinhirn, selten intraventrikulär.
Genetik: 20 % TP53 missense-Mutationen, keine 17q Isochromosomen.
Histo: Neuronal differenzierter Tumor mit dem Bild eines Neurozytoms mit zusätzlich lipomatösem Erscheinungsbild einiger Tumorzellen.
Immuno: Synaptophysin +, NSE +, MAP2 +, GFAP: fokal, MIB: 1-3 %.
Prognose: Gut, allerdings 62 % Rezidive.
DD: Medulloblastom mit lipomatöser Differenzierung (Alter, Proliferation).
  |
Papillärer glioneuronaler Tumor (PGNT)
[Bearbeiten]WHO: Grad I.
Ep: Tumor des Kindesalter, der aus a) perivaskulären Gliazellen und b) Neurozyten besteht. Er wurde früher als Variante des Ganglioglioms angesehen.
Lok: Tumor der cerebralen Hemisphären, v.a temporal.
Makro: Solide bis zystisch.
Histo + Immuno: Pseudopapillärer Tumor mit einschichtigen kleinen kuboiden zellen (GFAP+), welche hyaline Gefäße bedecken. Die äußeren Zellen zeigen neuronale Differenzierung mit vesikulären Kernen bis hin zu Ganglienzell-Differenzierung (NeuN+, Neurofilament+, NSE+ aber Chromogranin-). Im Randbereich Rosenthal-Fasern, Hämosiderin, Kalzifikationen. MIB-1: 1-2 %.
Prognose: gut
 |
 |
 |
 |
 |
Rosetten-bildender glioneuronaler Tumor des IV. Ventrikels (RGNT)
[Bearbeiten]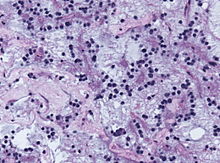 |
 |
WHO: Grad I
Ät: Benigner Mischtumor mit neurozytärer und astrozytärer (pilozytischer) Differenzierung mit fraglichem Ursprung der subependymalen Platte des 4. Ventrikels.
Ep: Tumor der Erwachsenen (30 Jahre), früher als DNT des Kleinhirns klassifiziert, aus dem infratentoriellen Ventrikelsystem stammend.
Lok: Tumor des 4. Ventrikels,
Histo: biphasischer Tumor mit neurozytärer + glialer Differenzierung, neurozytische Rosetten, perivaskuläre Pseudorosetten, Syn+, MAP2+ glialer Anteil: pilozytisches Astrozytom ohne Mitosen und Nekrosen. GFAP +, MIB-1: 1-3 %.
Prg: Abhängig von dem operativen Eingriff.
Paragangliom
[Bearbeiten]WHO: Grad I (spinales Paragangliom).
Ät: eingekapselter neuroendokriner Tumor der autonomen Ganglien im Erwachsenen, meist sporadisch, aber Fälle in verschiedenen genetischen Zusammenhängen bekannt (s.u.).
Ep: 40-70 Lj. Männer leicht überrepräsentiert. In Höhengebieten wie Peru ist die Inzidenz von Paragangliomen der Karotiden bis zu 10fach erhöht.
Genetik: Auftreten bei Von Hippel Lindau (VHL), Multiple endocrine neoplasia (MEN type 2), NF1. Paragangliome des Kopf-Hals-Bereiches haben meist Succhinat-Dehydrogenase-Untereinheit D Mutationen (SDHD), während Phaeochromozytome meist Untereinheit B Mutationen (SDHB) aufweisen. Bei spinalen Paragangliomen bisher eine SDHD-Mutation beschrieben.
Pathogenese: Tumore mit SDHB und SDHD Muatationen weisen deutlich höhere VEGF und HIF-2a-Spiegel auf.
Lok:
- Cauda equina, Filum terminale (Spinales Paragangliom).
- Karotiden (Chemodektom).
- jugulotympanisch (Glomustumor)-> pulsatiler Tinnitus.
- Nebennierenrinde, Aortenbogen (Phäochromozytom): Hypertension, Diarrhoe.
Histo: Zellballen-Architektur (type I chief cells), spindelig imponierende sustentikuläre Zellen (type II) S-100, Kapillaren, öfters ausreifende Ganglienzellen (gangliozytische Paragangliome), feines Sprenkelungsmuster der Chief-Zellkerne, eosinophiles granuläres Zytoplasma. Mitosen und Nekrosen möglich.
SF: Melanotisches Paragangliom.
Immuno: Synaptophysin, Chromogranin A, NF, 5-HT, paranuklär CK; MIB-1 unter 2 %.
Prognose: Paraaortale Phäochromozytome haben hohes Metastasierungsrisiko (30-40 %), Karotiden (Schädelbasis): 2-9 % , Glomus-TU: 5 %, spinale Paragangliome: 4 % Rezidive.
Tumoren des Pinealis (Parenchym)
[Bearbeiten]Nur 15-25 % aller Tumoren in der Pinealisregion sind Pinealisparenchymalen Ursprunges.
Pineozytom
[Bearbeiten]WHO: Grad I.
Ep. Tumor des Pineozyten im Erwachsenenalter, 20 % aller Pinealistumoren.
Lok: Glandula pinealis.
Makro: umschrieben, selten Kalzifikationen oder Zysten, meist unter 3cm im Durchmesser.
Histo: pineozytäre Rosetten, moderate Dichte des Tumors aus runden bis ovalen, uniformen Zellen mit flächigem Wachstum, kurze Zellfortsätze. Das Kernchromatin ist lockerer als bei einem Pineoblastom. Die Mitosen sind gering (unter 1/10 HPF), Ganglienzellen möglich.
Immuno: Syaptophysin, Neurofilament, NSE, PGP 9.5, Chromogranin, retinales S-Antigen werden vom Tumor exprimiert.
Ko: Kompression Aqädukt, Hirnstamm und Kleinhirn, Parinaud-Syndrom
Prg: gut, keine Metastasen, 5J-ÜL: 86-100%
 |
 |
 |
Pinealisparenchymtumor intermediärer Differenzierung (PPTID)
[Bearbeiten]WHO: Noch nicht festgelegt, biologisches Verhalten entspricht WHO II oder III.
Ep: alle Altersgruppen, 50 % aller Pinealisparenchym-Tumoren.
Lok: Glandula pinealis.
Histo: Milde bis moderate Atypie und mitotische Aktivität, keine pineozytäre Rosetten, vereinzelt Homer-Wright-Rosetten.
Immuno: Synaptophysin +, NSE +, Chromogranin A +, MIB-1 typischerweise zwischen 3-10 %.
Beurteilung des biologischen Verhaltens durch Differenzierung von Mitosen und Neurofilament-Immunhistochemie möglich. Nach Jouvet et al. entsprechen Tumore unter 6 Mitosen / 10 HPF oder Tumoren mit mehr als 6 Mitosen / 10 HPF aber vorhandener Neurofilament-Expression einem WHO Grad II, Tumoren mit über 6 Mitosen und Fehlen von Neurofilament einem WHO Grad III.
Klinik: wie Pineozytom.
Prg: 5-JÜL: 39-74 %, Metastasen sind extrem selten.
Pineoblastom
[Bearbeiten]WHO: Grad IV.
Ep: 30-40 % der Pinealistumoren, meist Kinder, Jugendliche, Assozitation mit bilateralen Retinoblastomen („pineal anlage tumour“) möglich.
Lok: Glandula pinealis.
Genetik: RB1-Mutationen, POU4F2-Überexpressionen bekannt.
Histo: Der Tumor imponiert zelldicht, formlos als klein rund-und blauzelliger Tumor mit reichlich Mitosen. HOMER-WRIGHT-Rosetten, FLEXNER-WINTERSTEIN-Rosetten (neurozytische Rosetten), selten können auch Fleuretten (Photorezeptor-Differenzierung) beobachtet werden. Hämorrhagien, Nekrosen, leptomeningeale Infiltration möglich.
Immuno: Synaptophysin, NSE, Neurofilament, retinal S-Ag können im Tumor vorkommen. Der MIB-1 Proliferationsindex ist in der Regel hoch.
Komplikation: Dissemination der Tumorzellen über den Liquor.
Prg: 5-Jahres-Überlebensrate: 58 %.
DD: Medulloblastom.
Papillärer Tumor der Pinealisregion (PTPR)
[Bearbeiten]WHO: Grad II oder III je nach Pleomorphie.
Lok: Pinealistumor, Herkunft: am ehesten Zellen des subkomissuralen Organs (SCO).
Ep: Erwachsene, früher oft als Ependymom der Pinealisregion klassifiziert.
Histo: Ependymal imponierender Tumor mit papillärem Aufbau und Nachweis epithelialer Markern. Die Zellen haben ein klares Zytoplasma, runde-ovale Kerne und sind von hyalinen Gefäße umgeben. PAS-positive Einschlüsse, Nekrosen sind möglich. Je nach WHO-Grad: 0-4 bzw. 5-10 Mitosen/10HPF.
Immuno: NF negativ, GFAP und Synaptophysin kann fokal vorhanden sein, Kir 7.1 ist negativ, Zytokeratine sind positiv.
Prg: 5-J-ÜL: 73 %.
Pinealiszyste
[Bearbeiten]Ep.: Häufig, Pravalenz ca. 23 %.
Makro: Hohlraum, meist < 0,5 cm.
Histo: Pseudozyste.
Klinik: Benigne. Meist asymptomatisch.
Embryonale Tumoren
[Bearbeiten]Medulloblastom
[Bearbeiten]engl. medulloblastoma, veraltet: cerebelläres Neuroblastom.
WHO: Grad IV.
Ät: Embryonaler Tumor des Kleinhirns, undifferenziert oder mit überwiegend neuronaler Differenzierung. Frühchen haben ein höheres Risiko für die Entstehung eines Medulloblastoms. Histogenese a) externe Körnerzellschicht oder b) subependymale Matrix.
Ep.: V.a Kleinkinder (Peak um das 7. Lj.), selten im Erwachsenenalter, 65 % männlich, Inzidenz: 0,5 %/100.000.
Genetik: Auftreten bei Li-Fraumeni (p53), Gorlin-Syndrom (PTCH1), Turcot-Syndrom (APC), Rubinstein-Taybi-Syndrom (CBP). 30-40 % der Medulloblastome haben ein Isochromosom 17q, Amplifikation von MYC/MYCN (5-10 %), daneben SHH (8 %: PTCH, SMO, SUFU)-Mutationen und Wnt (4-10 %; CTNNB1 mit nuklärer Nachweis von beta-Catenin) und TP53-Mutationen (15 %) in sporadischen Fällen.
Lok.: 75 % Kleinhirnwurm, axial. Tumoren der Hemisphäre sind öfters desmoplastisch und haben ein älteres Patientenkollektiv.
Makro: Mittelliniennah, bunte Schnittfläche, selten Nekrosen.
Mikro: Zelldichter, knotiger Tumor, hyperchromatische Kerne, hohe Kern-Plasma-Relation, wenig bis viele Mitosen, Apoptosen. Primitive, kleine, runde- bis karottenartige Zellen. Neuroblastäre (Homer-Wright)-Rosetten (40%). Endothelproliferate. Selten spongioblastäres Bild oder einzelne Ganglienzellen.
Immuno: Neuronale Diff: Synaptophysin +, Neurofilament +, MAP2 +, NSE +, Chromogranin A +, Glial: GFAP +, Vimentin +, MIB-1: 20-90 %.
Subtypen:
- Desmoplastisches/noduläres Medulloblastom: pale islands: Retikulin-freie Areale mit reduzierter proliferativer Aktivität
- Medulloblastom mit extensiver Nodulariät (MBEN): traubenähnliche Bildgebung, „streaming“ der Tumorzellen
- Anaplastisches Medulloblastom: Viele Mitosen, Zellkernumhüllung, reichlich Apotosen
- Großzelliges Medulloblastom (2-4 %): reichlich eosinophiles Zytoplasma, oft Mischform mit anaplastischem Medulloblastom
Differenzierungsvarianten:
- Myogen (Medullomyoblastom): glattmuskuläre Anteile, Myosin +, Myoglobin +, Desmin +.
- Melanotisch (Melanozytisches Medulloblastom): S100 +.
Molekulare Stratifizierung:
- Wnt (15 %): um 10 Lj. fast immer klassisches Medulloblastom, selten großzellig/anaplastisch, oft Monosomie Chromosom 6, nukläre Expression von ß-catenin, DKK-Expression, sehr gute Prognose bei Fehlen von "high risk"-Faktoren.
- SHH (25 %): Kleinkinder und Erwachsene, Immuno: GAB1-positiv. MYCN-Amplifikationen. Gains auf 3q, losses auf 9q/10q Desmoplastisch/nodulär (gute Prognose bei Kindern), 50% der Anaplastisch/großzelligen Tumore (schlechte Prognose).
- Non-Wnt/SHH (60 %): um 8. Lj. meist klassisch, häufig Isochromosom 17q, 50% der Anaplastisch/großzelligen Tumore (bei MYC-Amplifikation sehr schlechte Prognose), häufig metastasierend.
Kompl.: Kerzenwachsartige Abtropfmetastasen z.B. an der Cauda equina.
Prg.: Früher letal, heute deutlich bessere Prognose (5-J-ÜL: 70%)
- high risk: Alter unter 3 J., Resttumor größer als 1,5cm, Ausbreitung über den Liquorraum oder Metastasen zum OP-Zeitpunkt
- low risk: desmoplastisch/noduläre Medulloblastome oder Kinder mit klassischen Medulloblastomen des Wnt-Pathways ohne MYC-Amplifikation.
DD: „Klein-rund und blauzellige Tumore“: U.a. Lymphom, EWING-Sarkom/peripherer PNET, kleinzelliges Karzinom, kleinzellige Varianten anderer Tumoren.
Primitive neuroektodermale Tumoren des zentralen Nervensystems (CNS-PNET)
[Bearbeiten]Die primitiven neuroektodermale Tumore des ZNS stellen eine heterogene Gruppe von Tumoren dar, die bevorzugt im Kindesalter auftreten.
ZNS PNET, nicht näher spezifiert (NOS)
[Bearbeiten]alt: supratentorieller PNET
WHO: Grad IV.
Als nicht näher spezifizierte primitive neuroepitheliale Tumoren des ZNS (CNS-PNET, NOS) werden alle embryonale Tumore mit neuronaler, glialer, myogener oder melanozytärer Differenzierung zusammengefasst, die nicht einer anderen Entität innerhalb dieser Gruppe zugeordnet werden können.
Ep: Peak: 5 Lj.
Makro: Überwiegend solide, weich. Nekrosen möglich.
Histo: Undifferenziert, klein-rund-und-blauzellig, HOMER-WRIGHT-Rosetten, fibrilläre Zonen möglich, Kalzifikationen.
Genetik: In 12 % der adulten PNET sind IDH1 Mutationen beschrieben worden. Pädiatrische PNET zeigen solche Mutationen nicht.
DD: Peripherer PNET.
 |
Medulloepitheliom / ETMR
[Bearbeiten]WHO: Grad IV.
Epidemiologie: Kleinkinder (5 Monate - 6 Jahre), supra- und infratentoriell.
Genetik: 19q13.42-Amplifikation (wie auch andere ETMR)
Histo: Tubuläre oder trabekuläre Zellstränge, deren Bild an das embryonale Neuralrohr erinnert. PAS-positive Basalmembran auf retikulärem Netzwerk. Mitosen besonders luminal.
Immuno: Neuronale, gliale oder mesenchymale Differenzierung möglich. MIB-1: bis zu 50 %, Nestin +; GFAP -; SYN -; S100 -; INI-1 +; LIN28A +
Prg: Sehr schlecht, aber Langzeitüberleber bekannt.
DD: Medulloblastom, Ependymoblastom, Neuroblastom, Plexus-choroideus-Karzinom.
 |
 |
 |
Ependymoblastom & ETANTR / ETMR
[Bearbeiten]WHO: Grad IV.
Ät: Ependymoblastome, Medulloepitheliome und Embryonal tumors with abundant neuropil and true rosettes (ETANTR) werden aufgrund ihrer genetischen Übereinstimmung als embryonal tumor with multilayered rosettes (ETMR) zusammengefasst.
Inzidenz: Sehr selten, meist Kleinkinder und Neugeborene.
Genetik: ETANTR und Ependymoblastome zeigen eine Amplifikation von 19q13.42. Diese Stelle kodiert für zahlreiche miRNAs.
Histo: Klein rund-und-blauzelliger Tumor mit mehrreihigen (ependymoblastären) Rosetten. Bei ETANTR zusätzlich feinfibrilläres Neuropil, einzelne unreife Neuronen. Immunhistochemie: LIN28+
Prognose: Schlecht.
ZNS Neuroblastom
[Bearbeiten]Sympathischer neuroektodermaler Tumor.
Ep.: 80 % treten vor dem 5. Lebensjahr auf.
Lok.: Nebennierenmark, Grenzstrang.
Genetik: CDKN2A-Deletionen, RASSF1A-Amplifikationen.
Makro: Expansiv, abgekapselt.
Histo: Klein-rund und blauzelliger Tumor, HOMER-WRIGHT-Rosetten, neuronale Differenzierung. (Synaptophysin +)
Prg.:
- Hohe Spontanheilungsrate.
- Ungünstig sind Amplifikationen des Onkogens n-myc.
 |
 |
ZNS Ganglioneuroblastom
[Bearbeiten]Epidemiologie: Kleinkinder, meist unter dem 5. Lebensjahr.
Lokalisation: Paraspinaler Grenzstrang, selten im ZNS und im Rückenmark.
Histo: Klein rund und blauzelliger, neuroblastärer Tumor mit Nachweis von Ganglienzelldifferenzierung.
 |
Atypischer teratoider/rhabdoider Tumor (AT/RT)
[Bearbeiten]WHO: Grad IV
Ep.: 2 % aller kindlichen Hirntumore, tritt insbesondere bei Kleinkindern unter 2 Jahren auf.
Ursprung: bösartiger embryonaler Tumor unklarer Herkunft.
Genetik: Mutationen des SMARCB1 (INI1/hSNF5) oder SMARCA4 (BRG1)-Gens. 25 % der Pat. haben Keimbahnmutationen. Der Tumor kann familiär gehäuft bei dem sogenannten Rhabdoid-Prädispositions-Syndrom auftreten.
Lok.: Bevorzugt hintere Schädelgrube, kann aber auch in den Großhirnhemisphären auftreten.
Makro: Bunte Schnittfläche, äußerlich wie ein Medulloblastom imponierend.
Histo: Zellreich, solide bis papillär aufgebaut. Spektrum von primitiven, kleinen, runden, blauen Zellen bis zu rhabdoiden Zellen mit exzentrischem Kern und prominenten Nukleolen reichend. Viele Mitosen. Nekrosen.
Immuno: Je nach neuronaler, glialer oder epithelialer Differenzierung Nachweis von GFAP, Synaptopyhsin, Neurofilament, pan-Zytokeratin. Die fehlende nukläre Expression von INI-1 in den Tumorzellen ist charakteristisch.
Kompl.: Rasches Tumorwachstum.
Prg.: Sehr schlecht. Trotz Hochdosis-Chemotherpie und Bestrahlung liegt die Letalität nach zwei Jahren über 83 %.
DD: Medulloblastom, CNS-PNET und andere klein-rund-und blauzellige Tumore, Plexuskarzinom.
Tumoren der peripheren Nervenscheiden
[Bearbeiten]Schwannom
[Bearbeiten]Syn.: Neurinom, Neurilemmom.
WHO: Grad I.
Ät. benigner, eingekapselter Tumor der Schwannzellen (periphere Markscheidenglia), in 90% sporadisch auftretend.
Ep+Lok: Peak: 40-60 Lj, in Kindern selten, meist kutan/subkutan (asymptomatisch).
Genetik: 4% in Neurofibromatose Typ 2 (NF2), 5% mutipel ohne NF2, 60% der Schwannome haben inaktivierende Mutationen im NF2 Gen (Merlin) oder einen Verlust des entsprechenden Genabschnittes auf Chr. 22q. Melanotische Schwannome treten vor allem beim Carney-Komplex (PRKAR1A Mutationen auf Chr. 17q) auf.
Makro: Fischfleischartig, weich, blass
Mikro: Kerne länglich ausgezogen, angeschrägte Zytoplasmaausläufer.
- Antoni-A-Muster: In länglichen Zügen angeordnet (fischzugartig, Lattenzaunmuster). Verocay-bodies. Zelluläre Schwannome bestehen meist aus dichten Antoni A-Regionen ohne Verocay bodies.
- Antoni-B-Muster: Aufgelockerter, myxoider, weniger Zellen. Zellkerne etwas pleomorpher, hyperchromatischer. Evtl. eingestreute Entzündungszellen. In Akustikusneurinomen sind Antoni B Regionen oft prädominierend.
ELMI: Luse-Körperchen: lange Kollagenstränge.
Subtypen:
- Zellulär (hohe Zelldichte bei Antoni-A ohne Verocay-Bodies, weniger als 4 Mitosen /10 HPF)
- Plexiform (meist kutan, multipel bei NF2 oder Schwannomatosen)
- Melanotisch (Nachweis von perizellulärem Retikulin, psammomatöse FOrmen mit Carney-Complex assoziert).
Immuno: S-100 +, Kollagen IV +, Laminin +, Calretinin +, fokal GFAP möglich, p53 gering. Im Randbereich oft Neurofilament-positive Axone.
SF: Akustikusneurinom (AKN) - klinisch inkorrekte Bezeichnung eines Schwannom des N. vestibularis (HN VIII). Gehäuft bei Neurofibromatose 2 (dann meist beidseitig). Kl.: Hypakusis, Schwindel, Gleichgewichtsstörung, periphere Fazialisparese ipsilateral, Geschmacksstörungen.
Prg: gut, da Nervenerhaltende Resektionen möglich. Zelluläre Schwannome haben erhöhtes Rezidivrisiko, 10 % aller melanotischen Schwannome zeigen maligne Verläufe).
DD: Je nach Lokalisation Leiomyom, Sarkom, GIST.
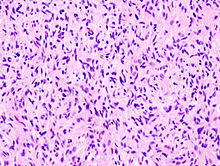
Neurofibrom
[Bearbeiten]WHO: Grad I.
Ät: Benigne Tumoren aus peripheren Perineural-, Schwannzellen und Fibroblasten.
Ep: Häufig, meist sporadisch auftretendes soliäres Knötchen, multipel bei NF1. Alle Altersgruppen und Geschlechter gleichermaßen betroffen.
Lok: Meist kutan, intraneural peripherer Nerven oder plexiforme Vergrößerung der Nervenabgänge und spinale Nervenwurzeln. Hirnnerven sind nicht betroffen.
Genetik: Häufigster Tumor bei der Neurofibromatose Typ 1 (Morbus VON RECKLINGHAUSEN) (erblich). Neurofibrome sind selten bei NF2 und Schwannomatosen. Verluste auf 17q (NF1), selten auch 19q, 22q.
Histo: Diffuses intraneurales Konglomerat aus Schwannzellem, Perineural-ähnlichen Zellen und Fibroblasten in einer Alcianblau-positiven Matrix („shredded carrots“), diese können vom Epineurium abgekapselt bleiben. Große Neurofibrome können Pseudo-MEISSNER-Körperchen oder melanotische Zellen aufweisen. Blutgefäße sind in der Regel nicht hyalinisiert (DD Schwannom).
Immuno: S-100 + (weniger als bei Schwannomen), fokal EMA (weniger als bei Perineuriomen), diffus eingestreute Neurofilament-positive Axone. MIB-1: 2 - 3 %.
Subtyp:
- Plexiformes Neurofibrom: Multiple und große plexiforme Neurofibrome sind mit NF1 assoziert, meist spinale Wurzeln und Nervenplexus mit multinodulären Knötchen („bag of worms“). Größere Neurofibrome können zentral noch relativ intakt imponierendes Nervenbündel zeigen.
Prg: Maligne Transformation in 5 % der größeren Neurofibrome möglich.
 |
 |
 |
Perineuriom
[Bearbeiten]Ät: Tumor aus neoplastischen Perineuralzellen.
WHO:
- Intranneurales Perineuriom (von Endoneurium umgeben): Grad I
- Weichteil-Perineuriom: Grad I-III (benigne - perineurialer MPNST)
Ep: selten, weniger als 1 % der Nervenscheidentumore, meist im frühen Erwachsenenalter.
Klinik: Muskelschwäche.
Genetik: kein Zusammenhang mit NF1, Fälle mit Beckwidth-Wiedmann-Syndrom bekannt, Monosomie 22 (aber selten NF2 Deletionen).
Makro: segmentale Vergrößerung der Nerven.
Histo: konzentrische Schichten (Pseudo-onion bulbs), Myelinscheiden oft fehlend, extensive Hyalinisierung möglich. Selten Mitosen. Bei Weichteilperineuriomen: lamellierte wavy cells, Mitosen in Abhängigkeit vom WHO Grad.
Immuno: Vim+, EMA+, Axone: NF+,S-100+, bei Weichteilperineuriomen: CD34 -, S-100 -, fokal EMA +.
Prog: Selten maligne Formen (MPNST-Transformation), deren Prognose etwas besser als MPNST.
 |
Maligne periphere Nervenscheiden-Tumoren (MPNST)
[Bearbeiten]WHO: II bis IV.
Ep: 5 % aller Weichteiltumoren, junges bis mittleres Erwachsenenalter, typischerweise 40 - 60. Lj., in NF1: 20 - 30 Lj.
Lok: Meist mittlere oder größere Nerven, N. ischiadicus am häufigsten involviert.
Ät: Entstehen aus Neurofibromen oder de novo, 10 % sind strahleninduziert (Latenzzeit: 15 Jahre).
Genetik: 50% der MPNST wird bei der Neurofibromatose Typ I beobachtet, 2 - 5 % aller NF1-Patienten können einen MPNST entwickeln. Ein Großteil der Tumoren hat Deletionen auf 17p und Mutationen von p53.
Histo: Fischgräte-Muster wie bei Sarkomen, Mitosen, Nekrosen, hohe Zelldichte, hyperchromatische Kerne 3x größer als bei Neurofibromen.
Immuno: 50 - 70 %: S-100 +, p53 in den meisten Tumoren +, p27 und p16 meist -. MIB-1: 5 - 65 %.
Subtypen:
- Epitheloider MPNST (weniger als 5 %), keine NF1-asszitation, oft aus Schwannomen.
- Glandulärer MPNST, in 75 % mit NF1, meist mit dem Bild von Intestinalepithel.
- Tumore mit myogener Differenzierung: Triton-Tumore, 60 % der Fälle haben NF1.
- Melanotischer MPNST bzw. Melanotisch psammomatöser MPNST bei CARNEY-Komplex.
Prg: 5-Jahres-Überlebensrate: 34 %.
DD: Fibrosarkom, Synovialsarkom, zelluläres Schwannom.
Nervenscheidenmyxom
[Bearbeiten]Myxomatöses Perineuriom, Neurothekom
WHO: keine Gradierung
Lok: meis kleinere kutane Nerven
Histo: multilobulärer, myxoider Tumor mit lockeren, spindelzelligen Nestern, S-100+
 |
Granularzelltumor des Nervens
[Bearbeiten]WHO: Grad I.
Ät. Tumor von den Schwannzellen peripherer Nerven ausgehend.
Ep: Mittleres bis höheres Lebensalter, bis zu 10 % multipel.
Lok: Subkutanes Gewebe von Kopf und Hals, 25 % Mund und Zunge, 15 % viszeral, 5 % gastrointestinal.
Histo: fächiges Wachstum polyhedraler bis elongierter granulärer, PAS-positiver Tumorzellen.
Immuno: S-100, CD68 und alpha-Antichymotrypsin positiv.
Sekundäre Nerventumoren
[Bearbeiten]Adenoid-zystische-Karzinome infiltrieren meist den perineuralen Zwischenraum und wachsen hier entlang des Nervens und können so starke Schmerzen verursachen.
Hämatopoietische Neoplasien können ebenfalls mit einer diffusen Infiltration von Nerven manifestieren.
Periphere neuroblastäre Tumore
[Bearbeiten]Olfaktorius-Neuroblastom
[Bearbeiten]Syn: Ästhesioneuroblastom
Olfaktorius-Neuroepitheliom
[Bearbeiten]Sympathisches Neuroblastom
[Bearbeiten]neuroblastoma
Ep: 6-10 % aller Tumore im Kindesalter.
Ät: Neuroendokriner Tumor des Kindesalters.
Lok: Nebennieren, entlang der Wirbelsäule, im Kopf-, Hals- und Nackenbereich sowie im Brust-, Bauch- und Beckenraum entlang des zervikalen, thorakalen und abdominalen Grenzstranges sowie in den Paraganglien.
DD: Rhabdomyosarkom, EEWING-Sarkom, WILMS-Tumor.
Prg: N-myc amplifikationen haben eine schlechte Prognose, genetische Sonderform 4S kann in bis zu 80% spontan eine Regression zeigen.
 |
 |
Phäochromozytom
[Bearbeiten]Siehe im Kapitel Nebenniere.
Paragangliom
[Bearbeiten]Ursprung: Sympathische oder parasympathische Ganglien.
Histo:
- Neuroendokrine Morphologie (monomorphe Tumorzellen, monomorphe runde Zellkerne mit „Salz-und-Pfeffer-Chromatin“.
- Rasenartig oder nestförmig („Zellballen“) mit Bindegewebssepten
 |
 |
 |
 |
 |
Ganglioneurom
[Bearbeiten]Lok: Sympathische Ganglien des Mediastinum, Retroperitoneum und Becken.
Genetik: Diffuse Läsionen werden im Rahmen einer MEN IIb beobachtet, selten im Rahmen einer NF1.
Makro: homogen, solide, dünne Pseudokapsel.
Histo: reife autonome Ganglienzellen welche von unmyelinisierten Axonen und begleitenden Schwannzellen umgeben sind. Neuroblasten eines Neuroblastoms liegen nicht vor.
Immuno: Axone+Ganglien: Neurofilament, Synaptophysin, NSE, Schwann-Zellen: S-100. Nachweis von VIP möglich.
 |
 |
DD: Neurofibrom, Ganglioneuroblastom.
Tumoren der Meningen
[Bearbeiten]Meningotheliale Tumoren (Meningeome)
[Bearbeiten]Ursprung: Arachnoidea-Deckzellen.
Ep: Inzidenz 4.4/100.000, mittleres Diagnosealter: 63 Jahre, Zufallsbefunde bei Autopsien bis zu 2%, Metastasen sind sehr selten, obwohl Gefäßinfiltration öfters beobachtet wird. Männer haben zweifach höheres Risiko für Grad II und Grad III Tumoren.
Genetik: Häufigster Tumor nach Schwannomen in Neurofibromatose Typ II, selten Fälle bei Gorlin-, Cowden-, LiFraumeni-Syndrom sowie MEN Typ 1 beschrieben. 40-70% der sporadischen Meningeome sowie nahezu alle NF-2 assozierten Meningeome weisen eine Mutation in Merlin-Gen (22q12.2) auf. Diese Muatationen sind in fibroblastischen, psammomatösen und transitionalen Varianten häufiger anzutreffen. KLF4 (K409Q)-Punktmutationen werden nur bei sekretorischen Meningeomen beobachtet. AKT1 (E17K)-Mutationen sind mit meningeothelialen und transitionalen Varianten assoziert. Anaplastischen Meningeome zeigen häufiger Verluste auf Chr. 9p21 (p16ink4a, p14ARF) und eine Hypermethylation von TIMP3 und NDRG2.
Makro: Gut abgegrenzter, an der Dura haftender Tumor. Gefäßinvasion ist kein Zeichen von Malignität.
Mikro: Klassisch Zwiebelschalenkonfigurationen = konzentrische Schichtungsfiguren, Verkalkungen (Psammom-Körperchen), Lochkernzellen, uniformes Zellbild mit pseudozynzytialem Erscheinungsbild. Spektrum reicht von mesenchymal dominierenden Eigenschaften (fibroblastär mit kollagenem Stroma) bis epithelial (EMA-Expression, sekretorische Ablagerungen).
Immuno: Vimentin +, EMA fokal bis flächig +, CD34 und S-100 schwach + (bevorzugt fibröser Subtyp), GFAP -, CK18 und CD99 kann positiv sein.
WHO-Grading:
- °I: Gut differenziertes Meningeom (80 %), Rezidivrisiko: 3 %.
- °II: Atypisches Meningeom (16-18 %), Rezidivrisiko: 40 %.
- °III: Anaplastisches (malignes) Meningeom (1-2%), Rezidivrisiko: 70-90 %.
Meningeome können eine Progression von WHO I nach III durchlaufen, die meisten Rezidive behalten jedoch den WHO Grad bei. Meningeome, die an der Schädelbasis lokalisiert sind, weisen signifikant seltener atypische oder anaplastische Formen auf.
Subtypen (morphologische Kriterien müssen in mehr als 50% der Tumorzellen vorliegen):
- Meningothelial (WHO °I)
- Fibrös (fibroblastisch, WHO °I)
- Transitional (gemischt, WHO °I)
- Psammomatös (WHO °I)
- Angiomatös (WHO °I)
- Mikrozystisch (WHO °I)
- Sekretorisch (WHO °I)
- Lymphoplasmazyten-reich (WHO °I)
- Metaplastisch (WHO °I)
- Klarzellig (WHO °II)
- Chordoid (WHO °II)
- Papillär (WHO °III)
- Rhabdoid (WHO °III)
Prg.: Je nach Grading und Lokalisation (problematisch: Tuberkulum sellae, Clivus, lateraler Keilbeinflügel).
WHO Grad I Meningeome
[Bearbeiten]Def: Keine Atypiekriterien für WHO II/III erfüllt, keine Hirninvasion.
Diagnostik: häufigste Form: meningeotheliale Variante. Psammomatöse Formen kommen bevorzugt im thorakalen Spinalkanal vor. Mikrozystische Meningeome entsprechen vom histologischen Bild eher Arachnoidatrabekel als Arachnoidadeckzellen. Metaplastische Meningeome können sowohl Knochen, Knorpel, Fett oder xanthomatöse Anteile aufweisen. Sekretorische Meningeome zeigen in der PAS-Färbung sekretorische Ablagerungen (Pseudopsammomkörper) und weisen in der Regel reichlich Mastzellen auf.
Atypische Meningeome
[Bearbeiten]WHO: Grad II.
Diagnostikkriterien:
- 4 oder mehr Mitosen auf 10 HPF.
- Vorliegen von drei oder mehr Atypiekriterien: a) flächenhaftes Wachstum, b) erhöhte Zelldichte, c) prominente Nukleolen, d) Hohe Kern-Plasmarelation, e) spontane Nekrosen (keine Embolisationsnekrosen)
- histologische Subvariante: a) chordoid (mucinreich) oder b) klarzellig (glykogen-reich, extensive interstitielle Kollagendeposits).
- WHO Grad I Tumoren mit Zeichen von Hirninfiltration werden biologisch analog WHO II gewertet, sind jedoch keine atypischen Meningeome 'per se', da auch atypische Meningeome Zeichen einer ZNS-Invasion zeigen können.
 |
 |
 |
 |
 |
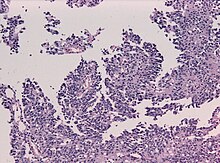
Anaplastische Meningeome
[Bearbeiten]WHO: Grad III.
Genetik: 67 % der Tumore zeigen eine Hypermethylation von TIMP3. Alterationen auf Chr. 9p21 (mit Verlusten von p16ink4a, p14ARF und CDKN2B) sowie eine reduzierte Expression von E-cadherin und Familienmitgliedern der 4.1B-Proteinfamilie ist mit einem aggressiveren Verlauf der Meningeome verbunden.
Diagnostikkriterien:
- 20 oder mehr Mitosen auf 10 HPF.
- Vorliegen eines morphologisch anaplastischen Zellbildes, welches einem Karzinom oder Sarkom entspricht (EMA-Nachweis oder Progression aus einem WHO I/II Meningeom).
- histologische Subvariante: a) papillär (Ependymom-ähnliche Pseudorosetten) oder b) rhabdoid (exzentrische Kerne).
 |
 |
 |
Mesenchymale, nicht-meningotheliale Tumoren
[Bearbeiten]Hämangioperizytom
[Bearbeiten]WHO: Grad II oder III (<5Mit/10HPF, Zelldichte, Pleomorphie, Nekrose, Blutung).
Ep: 2-4 % aller meningealen Tumore (öfters extrakraniell als intrakraniell).
Klinik: Hypoglykämien (IGF-Sekretion), Osteomalazien (Phostpaturie).
Histo: Zelldichter, monotoner Tumor mit nur wenig fribrösen Anteilen, irreguläre Gefäße („staghorn“-Sinusoide), klares Zytoplasma, blande runde bis ovale Nuclei. Retikulin um jede Zelle.
Genetik: NAB2-STAT6 Fusionstranskripte
Immuno: STAT6 (nuklär), CD34 (variabel), EMA (fokal), Vimentin +, CD99 +, SMA +, CD31 -, S-100 -, PgR -.
DD: SFT (homogenere CD34 Expression, aber auch NAB2-STAT6), Meningeom (niedrigerer MIB1, genetisch LOH 22q, die bei Hämangioperizytomen nicht vorkommen).
Prg: Rezidviert fast immer (85-90 %), kann metastasieren. 15-JÜL 43 %, 5-ÜL: 85 %.
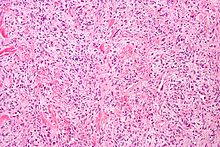
Solitärer fibröser Tumor
[Bearbeiten]Lok: Tumor der kranialen und spinalen Meningen im Erwachsenenalter.
Ät: Kontinuum mit Hämangioperiztyomen wird diskutiert, da beide eine NAB2-STAT6 Genfusion aufweisen
Histo: Spindelzellige Tumorfaszikel mit kollegenen Bündeln.
Immuno: CD34 +, bcl-2, EMA -, S-100 -, STAT6 nuklär
 |
Andere nicht-meningotheliale Tumoren
[Bearbeiten]Die nachfolgend aufgelisteten mesenchymalen Tumore treten bevorzugt in der Dura auf:
- Lipom (0,4 % intrakraniell, meist Corpus callosum, Kleinhirnbrückenwinkel, Conus medullaris bei thethered cord)
- Angiolipom
- Hibernom
- Liposarkom (intrakraniell)
- Fibromatose
- Fibrosarkom
- Malignes fibröses Histiozytom
- Leiomyom
- Leiomyosarkom
- Rhabdomyom
- Rhabdomyosarkom
- Chondrom
- Chondrosarkom
- Osteom
- Osteosarkom
- Osteochondrom
- Hämangiom
- Epitheloides Hämangioendotheliom
- Angiosarkom
- Kaposi-Sarkom
 |
Primäre melanozytäre Läsionen
[Bearbeiten]- Diffuse Melanozytose
- Melanozytom
- Maligne Melanome
- Meningeale Melanomatose
Malignes Melanom
[Bearbeiten]Ep: Primär im ZNS sehr sehr selten (0.005/100.1000), diese dann meist leptomeningeal, der Großteil der Melanome sind Metastasen, diese meist im Parenchym loklaisiert.
Histo: Epitheloid – spindelzellig Läsionen mit ausgeprägten Atypiemerkmalen und angiozentrischem Wachstum (5/Mit/10 HPF). Melanotische und amelaontische Tumoren möglich.
Immuno: HMB45, MelanA (MART1), MITF, S-100 positiv.
Melanozytom
[Bearbeiten]Ursprung: Leptomeningeale Melanozyten (besonders ventrale Dura Hirnstamm).
Ep: meist Erwachsene (45-50 Lj.), extramedullär, intraduraler Tumor.
Histo: Reichlich melanozytäre Zellen, oft spindelzellig, meist gut umschrieben, zytologisch blande, keine Nekrosen, keine ZNS-Invasion, 0-1 Mitosen/10 HPF.
Immuno: S-100, HMB45, MelanA, MIB: 0-2 %, Kollagen IV nur um Blutgefässe, nicht um einzelne Zellen (→ sonst DD: Schwannom), EMA+ panCK: negativ.
Lymphome und hämatopoetische Neoplasien
[Bearbeiten]Ep: 2 % der intrakraniellen Tumore sind Lymphome, davon entstehen 80 % primär im ZNS, 10-15 % infolge eines systemischen Lymphombefalls.
Ät: EBV-Nachweis in 15-20 % der immunkompetenten, nahezu 100 % der immunsupprimierten Patienten.
Klinik: fokale neurologische Defizite, kognitiver Abbau, Augenbeteiligung in 15-25%, spontane Regressionen möglich (oft Ansprechen auf Steroide).
- Maligne Lymphome.
- Plasmozytom.
- Granulozytisches Sarkom.
Diffus großzelliges B-Zell-Non-Hodgkin-Lymphom
[Bearbeiten]Die Prognose, das genetische Profil sowie der klinische Verlauf der cerebralen Lymphome unterscheidet sich von systemischen B-Zell-Neoplasien.
Ep: Peak zwischen 60-70LJ, meist Männer, Inzidenz steigend.
Ät: Meist de novo, selten Entstehung aus Marginalzonen-Lymphom oder follikulärem Lymphom.
Lok: 60 % supratentoriell, 20-40 % multipel, selten extraneurale Beteiligung.
Histo: Blastäre Zellkerne (so groß/größer wie Kerne eines Makophagens oder doppelter Durchmesser eines Lymphozytenkerns) meist perivaskulär und in der Gefäßwand einliegend. Dazwischen Makrophagen und Lymphozyten eingestreut. Nach Steroidgabe: zahlreiche Schaumzellen
Varianten:
- Zentroblastisch (2-4 Nucleoli an der Kernmembran, polylobuliert), häufigste Variante, monomorph (nur Zentroblasten oder wenige Immunoblasten.
- Immunoblastisch (prominenter Nucleolus in der Kernmitte): mehr als 90 % der Zellkerne.
- Anaplastisch (bizarre Nucleoli), CD30 +.
- T-Zell-reich/Histiozytär.
Immuno:
- pan-B-Zell Nachweis: C19, CD20, CD22, CD79a
- Selten CD5 (sind aber im Ggs. Zu Mantelzell-Lymphomen CyclinD1 negativ)
- p53: 20-60 %, MUM-1: 90 %, bcl6: 60-80 %, CD10: 10-20 %
- Oft: bcl-2, aber kein Indiz für Vorliegen einer Translokation
Subgruppen (Hans classifier):
- Germinal Cell (GC-Subtyp): early germinal stage (BCL6 +/CD10 +), bzw. late germinal stage (BCL6 +/CD10 -/MUM1 -).
- Activated B-Cell-Subtyp (ABC-Subtyp): BCL6-/CD10 - oder BCL6 +/CD10 -/MUM1 + in einigen Studien schlechteres Survival als in der GC-Gruppe.
 |
 |
 |
Niedriggradiges B-Zell Non-Hodgkin-Lymhom
[Bearbeiten]Ep: Frauen überwiegen (4:1).
Lok: Fast immer Dura-basiertes MALT-Lymphom (mucosa-associated lymphoid tissue, marginal zone B cell lymphoma), lymphoplasmazytisches Lymphom.
Histo: Lymphoide Follikel, meist ohne angozentrisches Wachstum, Kerne kleiner aber Nucleoli, Amyloid-Deposits möglich (Light chain deposition disease: LCDD).
Immuno: CD19 + , CD20 +, CD79a +, CD3 -, CD10 -, selten CD5 +.
Plasmozytome
[Bearbeiten]Lok: Selten sind rein extraossäre Lokalisationen möglich, diese können dann inkrakraniell als noduläre oder plaque-ähnliche Läsionen auftreten.
Histo: Exzentrischer bzw. Uhrenförmiger Kern, perinuklärer Halo, multinukläre Tumorzellen möglich.
Immuno: EMA +, CD79a +, CD56 +, CD38 +, CD20 -.
siehe hierzu: Plasmozytom.
 |
Posttransplantations-Lymphoproliferative Erkrankung
[Bearbeiten]Posttransplantations-Lymphoproliferative Disorder (PTLD)
Ep: Bis zu 25 % aller extranodalen Fälle können im ZNS auftreten, meist 5 Monate – 2 Jahre nach Transplantation, pädiatrische Fälle weisen ein höheres Risiko auf.
Histo: Durabasiertes B-Zell-Lymphom, meist EBV-assoziert.
Sekundäre Lymphome
[Bearbeiten]ZNS-Metastasen bei:
- Lymphoblastisches Lymphom.
- Burkitt-Lymphom.
- Hodgkin-Lymhom (selten).
Siehe hierzu Kapitel Lymphatisches System.
Histozytäre Läsionen
[Bearbeiten]Gruppe neoplastischer Läsionen entweder aus Langerhans-Histiozyten oder Makrophagen.
Langerhans-Zell-Histiozytose (Hand-Christian-Schüller-Erkrankung, Abt-Letter-Siewe, eosinophiles Granulom)
[Bearbeiten]Lok: Hypothalamus, Infundibulum, Chiasma opticum, Choroid Plexus, seltener cerebral
Klinik: Diabetes insipidus, Hirnnervenausfälle, Ataxien.
Makro: Gelblich-weißlich, meist Dura-basiert.
Histo: Langerhans-Zellen, Plasmazellen, Lymphozyten, Makrophagen, Eosinophile Granulozyten, selten Touton-Riesenzellen.
Immuno: S-100 +, CD1a +, CD207 + (Langerin), CD68 +, MIB-1: 4-16 %.
Nicht-Langerhans-Histiozytosen
[Bearbeiten]- Rosai-Dorfman-Erkrankung (CD11c +, CD68 +, CD1a -, S-100 +/-, Emperipolese).
- Erdheim-Chester-Erkrankung (CD1a -, CD68 +, S100 -).
- Juveniles Xanthogranulom (CD1a -, CD11c +, CD68 +, S-100).
- Histiozytäres Sarkom(CD68 +, CD163 +, CD11c +).
Tumoren unklarer Histogenese
[Bearbeiten]- Hämangioblastome wurden früher fälschlicherweise als angioblastäre Meningeome eingestuft.
Kapilläres Hämangioblastom
[Bearbeiten]WHO: Grad I.
Syn.: LINDAU-Tumor.
Ep: Langsam wachsender vaskulärer Tumor des jüngeren Erwachsenenalters,meist sporadisch, multiple Tumore in VHL oder POEMS (siehe Genetik).
Lok: 80 % cerebellär, 10 % medullär, 7 % RM, aber nur < 2 % supratentoriell.
Genetik: Auftreten in VON-HIPPEL-LINDAU-Syndrom, Castleman-Syndrom (POEMS).
Klinik: Polyzythämie durch Erythopoietin-Produktion im Tumoren.
Einteilung:
- Retikulärer Subtyp.
- Zellulärer Subtyp.
Makro: Wandständiges Gefäßknäuel (sogenannter Nidus) in einer Pseudozyste, zystisch, gelblich
Mikro: Zahlreiche Kapillaren, helles Stroma mit Vakuolen (Ölrot), rund-ovale Kerne. Retikulin: Clustering, Nukläre Pleomorphie , Hyalinisierung, intratumorale Blutungen möglich, gut abgrenzbarer Tumorrand. Beim selteneren zellulären Subtyp Anordnung der stromalen Tumorzellen in Ballen.
Immuno: Gefäße: CD31, Stroma: NSE, S-100, CD56, VEGF, MIB1: 0-2 %
BG: Pseudozyste mit wandständigem KM-affinem Nidus, Pseudozystenwand ohne KM-Aufnahme.
Prg.: Gut, wenn operabel.
DD: Klarzelliges Nierenzellkarzinom (EMA +, CK +, CD10 +)
Wikipedia: Hämangioblastom
 |
 |
Keimzelltumoren
[Bearbeiten]Inzidenz der Keimzelltumore zeigt eine geographische Variabilität: Europa: 0,3-0,6 % aller intrakraniellen Tumore, in Japan: 2-3 % aller intrakraniellen Läsionen. In 80-90% der Fälle sind die Patienten unter 25 Jahre mit Peak um 10-14 Lj. Männliche Patienten haben eine Prädilektion für die Pinealisregion.
Genetik: Assozitation mit Klinefelter (beta-HCG: Gonadotrophin erhöht), DOWN-Syndrom (Germinome).
Klinik: Vorzeitige Pubertät durch neoplastische Synzytiotrophoblasten.
Einteilung: Meist Mischformen (25-32 %), Reine Tumore fast immer nur Germinome oder Teratome.
Entstehungshypothesen:
- Migration primoderialer Keimzellen in die Pinealis
- Misfolding des Neuralrohres
- Entstehung aus pluripotenten Stammzellen
Germinom
[Bearbeiten]Synonyme: Seminom (Hoden), Dysgerminom (Ovarien).
Ep: 40-50 % aller Keimzelltumoren.
Lok: Pinealis, suprasellär, entspricht dem Seminom des Hodens bzw. dem Dysgerminom des Ovars.
Germinome/Seminome/Dysgerminome kommen entlang der embryonalen Keimzellanlagen vor: Pinealis (Epiphyse), hinteres Mediastinum, retroperitoneal, Keimdrüsen.
Histo: kohäsives Wachstum, große runde Tumorzellen mit blassem Zytoplasma und prominente Nukleolen inmitten eines lymphozytenreichen Stromas (meist T-Zellen). Der Tumor kann auch hinter einem ausgeprägten granulomatösen Bild zurücktreten. Oft Mitosen, aber keine Nekrosen. Selten syncytiotrophoblastäre Riesenzellen (beta-HCG +, Subtyp mit schlechterer Prognose).
Immuno: Nachweis von PLAP, C-KiT und Oct4 im Tumor. MIB-1 sehr hoch.
Ko: Ausbreitung über Meningen oder ventrikuloperitoneale Shunts möglich.
Prg.: Unbehandelt hochmaligne, sehr gutes Ansprechen auf Chemotherapie und Bestrahlung (5-Jahres-Überlebensraten: 80-93 %).
Klinik: werden nicht immer biopsiert (ß-HCG und AFP-Bestimmung im CSF), Evtl. Kopfschmerzen, Diabetes insipidus. Labor: AFP (Dottersack: fetale Hepatozyten und Intestinum) oder Teratom, betaHCG (Synzytiotrophoblasten) → Chorion Carcinom oder Mischtumor mit Germinom, PLAP: Germinome.
Embryonales Karzinom
[Bearbeiten]Ep: 3-5 % aller Keimzelltumoren.
Histo: große Zellen, vesikuläre Kerne, Makronukleoli, glasiges Zytoplasma, Anordnung in papillären Strängen, Acini oder cribiform, Mitosen, oft Nekrosen, embryonale Kavitäten („Discs“).
Immuno: CD30 +, OCT4 +, CK +, alpha-FP -, beta HCG -, PLAP +/-, C-KIT -.
Prg: Schlechte Prognose.
 |
 |
Dottersacktumor
[Bearbeiten]Syn: yolk-sac tumor.
Ep: 2% aller Keimzelltumore, aus dem Dottersack-Endoderm.
Histo: sog. „endodermaler Sinus“: epitheliale Reihen in muzinöser Matrix (extra-embryonale Mesoblasten), Schiller-Duval-Bodies (primitive Glomeruli), retikuläre Varianten: eosinophile Mikrozysten, hyaline Globuli: PAS+, Diastase-fest. Reichlich Mitosen, Nekrosen selten.
Immuno: alpha-FP +, CK +, CD30 -, OCT4 -, beta-HCG -.
Prg: Schlechte Prognose.
 |
 |
Chorionkarzinom
[Bearbeiten]Ep: 2 % aller Keimzelltumoren.
Histo: basophiles Zytoplasma, Blutseen, Nekrosen
- multinukleäre Synzytiotrophoblasten: beta-HCG +, HPL +
- mononukleäre Zytotrophoblasten: PLAP +/-.
Immuno: CD30 -, OCT4 -, CKIT - alpha FP -.
Prg: Schlechte Prognose.
Teratom
[Bearbeiten]Subtypen:
- Reifes Teratom
- Unreifes Teratom
- Teratom mit maligner Transformation
Histo:
- reifes Teratom: differenziert: Epitheliale Zysten, glioneuronale Inseln, Plexus, Knorpel, Knochen.
- unreifes Teratom (häufiger): Hyperzelluläres Gewebe aus fetalen mesenchymalen Zellen, glanduläre
- malignes Teratom: Tumorzellen mit Carcinom / Sarkom-Anteilen.
 |
 |
Gemischte Keimzelltumoren
[Bearbeiten]Tumoren der Sellaregion
[Bearbeiten]Hypophysenadenom
[Bearbeiten]Dieser häufigste Tumor der Sellaregion wird in einem eigenen Kapitel der Endokrinologie abgehandelt.
Kraniopharyngeom
[Bearbeiten]WHO: Grad I.
Subtypen:
- Adamantinomatös (Kinder und Erwachsene): häufig CTNNB1 Mutationen
- Papillär (Erwachsene): in ca. 80% BRAF (V600E) mutiert
Ep.: Zweigipfelige Häufungskurve: Vorwiegend Kinder und Erwachsene um das 40. Lebensjahr.
Ursprung: Plattenepithelreste der Rathke-Tasche (Embryologische Einstülpung des embryonalen Vorderdarms als Anlage der Adenohypophyse).Man geht davon aus das Epithel der Zahn-Primordien als Ausgang für das adamantinomatöse, das Epithel der Wangenschleimhaut Ausgang für das papilläre Kraniopharyngeom dient.
Lok.: Suprasellär (Im Bereich der Sella turcica).
Makro: Zystischer Tumor mit maschinenölartiger Flüssigkeit in den Zysten.
Histo: (Adamantinomatös): Trabekuläre Anordnung von Plattenepithel mit benignen basaloide Zellreihen, fibröses Material, u.U. Tumorzapfen im benachbarten Hirngewebe, Gliose mit reaktiven Rosenthalfasern im Nervengewebe. Hornablagerungen („wet keratin“) im Tumor. (Papillär): Gering differenzierte Plattenepitehliale Strukturen, keine Keratindeposits, keine Verkalkungen. Proliferierende Zellen gleichmäßiger verteilt.
IHC: Häufig nukläre Translokation von beta-catenin in adamantinomatösen Kraniopharyngeomen
Klinik: Sehstörungen (typisch bitemporale Hemianopsie), Wachstumsstillstand (STH-Mangel), Schwäche (ACTH-Defizit) und Blässe (MSH-Defizit), Polydipsie und Polyurie (ADH-Defizit).
Prg: 10-Jahres Überlebensrate: 64-96 %, Rezidivrisik vom Resektionsausmaß abhängig. Resttumoranteile größer als 5 cm haben eine deutlich schlechtere Prognose.
DD: Rathke'sche-Zyste, Karzinom-Metastasen
 |
 |
 |
 |
 |
Granularzelltumor
[Bearbeiten]Syn: Abrikossoff-Tumor, Choristom.
WHO: Grad I.
Ep: Seltener intra/suprasellärer Tumor im Erwachsenenenalter, von der Neurohypophyse ausgehend.
Klinik: Gesichtsfeldausfälle durch Kompression Chiasma opticum, selten Panhypopituitarismus.
Makro: Gut abgrenzbare Läsion, typischerweise 1-6cm groß ohne Nekrosen oder Blutungen
Histo: Dicht gepackte, polygonale Tumorezellen mit reichlich granulärem Zytoplasma, PAS-Diastase fest. kleine Nukleoli, perivaskuläre lymphozytäre Infiltrate. Selten Mitosen
Immuno: CD68 +, S-100 +, CK -, Chromogranin -, Synaptophysin - kein Nachweis von Hypophysenhormonen.
Prognose: Sehr gut.
 |
Pituizytom
[Bearbeiten]WHO: Grad I
Ät: Extrem seltener, spindelzelliger, glialer Tumor von Pituizyten der Neurohypophyse oder Infundibulums.
Makro: Umschrieben, kompakt.
Histo: Elongierte spindelige Tumorzellen in Faszikeln, fokal eosinophiles Zytoplasma, selten Mitosen, wenig interzelluläres Retikulin.
Immuno: TTF1+, Vimentin +, S-100 +, GFAP +/-, EMA +/-, kein Nachweis neuronaler, neuroendokriner, epithelialer oder hypophysärer Marker. MIB-1: 0,5-2 %.
 |
 |
Spindelzelliges Onkozytom (SCO)
[Bearbeiten]WHO: Grad I.
Ät: Onkozytäre, nicht endokrin aktive Neoplasie der Adenohypophyse im Erwachsenenalter, von follikulo-stellären Zellen ausgehend.
Ep: selten, weniger als 0,5 % aller intrasellären Neoplasien.
Klinik: Wie bei Hypophysenadenomen.
Histo: Bündel spineliger bis epitheloider Tumorzellen mit eosinophilem Zytoplasma, moderate Kernatypien, fokal Lymphozytäre Infiltrate möglich.
Immuno: Vimentin +, EMA +, S-100 +, GFAP -, CD34 -, neuronale und hypophysäre Marker negativ. MIB-1: 1-8 %.
Metastatische Tumoren
[Bearbeiten]Häufigste Tumore des ZNS mit Inzidenz bis zu 11/100.000 Fälle pro Jahr. Bis zu 25% aller Krebspatienten haben ZNS-Metastasen zum Todeszeitpunkt.
Ursprung (Erwachsene):
- Bronchialkarzinom (50 %).
- Mammakarzinom (15 - 20 %).
- Melanom/gastrointestinal/urogenital (5 - 10 %).
- Ursprung unbekannt (CUP: 10 %).
Ursprung (Kinder):
- Leukämie.
- Lymphom.
- Ewing-Sarkom/PNET.
- Rhabdomyosarkom.
Mikro/Makro: „Karzinomnarbe“, oft subkortikal an der Rinden-Mark-Grenze, ggf. Meningeosis carcinomatosa, Histologie entsprechend dem Ursprungsgewebe, perifokales Ödem. Häufig Blutungen bei Chorion-Karzinomen, Melanomen und Nierenzellkarzinomen. Proliferation oft höher als im Primärtumor. Differenzierung oft noch gut.
Klinik: Hirndruck, neurologische Ausfälle, Infarkte, Hämorrhagien.
Prognose: Pat. unter 65 Jahren und einem Karnofsky-Index über 70% haben eine bessere Prognose. Mittleres Überleben 6-12 Monate.
 |
 |
 |
Tumorsyndrome mit Beteiligung des Nervensystems
[Bearbeiten]Siehe hierzu auch den Abschnitt Phakomatosen im Kapitel angeborene ZNS-Erkrankungen.
Neurofibromatose Typ I
[Bearbeiten]periphere Neurofibromatose, Morbus Recklinghausen.
Allgemeine Informationen: NF1, Kapitel Phakomatosen.
- Dermale Neurofibrome (kutane Neurofibrome weisen mehr Mastzellen und Inflammation auf).
- Plexiforme Neurofibrome: 10 % Entartungsrisiko.
- Pilozytische Astrozytome des N. opticus (Optikusgliome) diese oft nicht progredient.
- selten diffuse Astrozytome WHO II,III sowie Glioblastome.
- MPNST, auch glanduläre MPNST oder Triton-Tumor: spindelzellig & rhabdomyoblastisch.
Neurofibromatose Typ II
[Bearbeiten]Syn.: Zentrale Neurofibromatose.
Allgemeine Informationen: NF2, Kapitel Phakomatosen
- Multiple Schwannome ab 30 Lj.: (sporadische Schwannome normalerweise ab 60 Lj.), leicht höhere Proliferationsaktivität.
- kutane Schwannome (plexiform, multilobulär „grapes“).
- Meningeome (50 % der NF2 haben multiple Meningeome, v.a Kinder, meist fibromatöser Subtyp).
- Gliome (80 % der NF2 Gliome sind spinal, 10% medullär, insgesamt 2/3 sind Ependymome (intramedullär),
seltener pilozytische Astrozytome.
- Schwannosen (entangled axons).
- Meningeoangiomatosis: multifokal, Gefäßassoziert.
- Cerbrale Hamartien/Mikrohamartome (S100+) intrakortikal.
- Periphere Neuropathien (axonal, sekundär durch kleine Schwannom-Tumorlets).
COWDEN-Syndrom
[Bearbeiten]Selten (1:250.000), autosomal-dominanter Erbgang mit Mutationen in PTEN (Supressor des PI3K/Akt/mTOR Pathway).
Welches auch ein Schlüsselregulator der ZNS-Entwicklung ist und deshalb im Nukleus+Zytoplasma der Neurone vorkommt.
Patienten mit COWDEN-Syndrom entwickeln im Verlauf Ihres Lebens multiple Hamartome aller 3 Keimblätter. Sie haben ein hohes Risiko im Laufe Ihres Lebens an Tumoren der Brust, Schilddrüse oder Endometrium zu erkranken.
- Major Kriterion: adult onset Lhermitte-Duclos disease (dysplastisches Gangliozytom des Cerebellums).
Dysplastisches Gangliozytom des Kleinhirns
[Bearbeiten]WHO: Grad I (allerdings von manchen Autoren eher als Hamartom als Neoplasie eingestuft).
Lokalisation: Kleinhirn.
Genetik: Auftreten im Rahmen des Cowden-Syndroms (Mutationen von PTEN).
Makro: Auflösung der Kleinhirnschichtung mit invertiertem Erscheinungsbild.
Histo: Dysplastische Purkinjezellen.
Komplikationen: Rezidive möglich.
 | ||
 |
 |
 |
oder feststellen, dass ein Fehlen kein substanzieller Verlust darstellt.
Von Hippel-Lindau-Syndrom
[Bearbeiten]retino-zerebelläre Angiomatose
Erbgang: autosomal-dominant, VHL-Keimzellmutationen (Chr. 3p25-26), 1:40.000, 3 exons Rolle bei der HIFalpha-VEGF Induktion als koordinierende Antwort bei Hypoxie, Angiogenese.
Mutationsabhängige Tumortypen.
- Type 1 : ohne Phäochromozytome.
- Type 2: Phäochromozytome, aber keine RCC.
- 2B: mit Phäochromozytome + RCCs.
- 2C: nur Phäochromozytome.
Prg: Lebenserwartung: 40-50J. Jährliches screening
Diagnose: Multiple kapilläres Hämangiom ZNS oder Retina (30 Lj.), oder Tumor + Verwandter mit VHL
Tumoren: Hämangiome im Kleinhirn, Hirnstamm oder RM
(sporadisch: fast nur KH)
supratentoriell sehr selten!
Stromazellen: Tumorzellen, Herkunft unklar (embryonal?).
plus andere Tumore: RCC (klarzellig), Phäochromozytome (10-20%), ELST, Pankreas-Tumore, Cystadenoma, der Adnexe oder Epidiymis
 |
LI-FRAUMENI-Syndrom
[Bearbeiten]Erbgang: autosomal-dominant, Hot-Spot Mutationen in Tp53 (17p13) bekannt, etwa 500 Familien p53: Tumorsupressor (MDM2 kontrolliert) Aufregulation im Nukleus: Zellzyklus-Arrest Apoptose mutierte Proteine haben längere HWZ (positive Immuno!)
Ep: Multiple Tumore im Kindesalter: Weichteiltumore (20 %), Mamma /28 %) und adrenocorticale (10 %) Tumoren, Hirntumoren (13 % aller LFS-Fälle haben Tumore des ZNS):
- 48 % Astrozytome
- 11 % Medulloblastome
- 15 % Plexustumore
- 3 % Ependymome
- 2 % Oligodendrogliome
Diagnose-Kriterium: Sarkom vor 45 Lj. + Verwandter mit Tumor vor 45.
Turcot-Syndrom
[Bearbeiten]Erbgang: autosomal dominant: zwei Formen bekannt
- mismatch replication (type 1), mit genomischer Instabilität, Immunhistochemie für involvierte Proteine möglich: PMS2m MLH1, MSH6. Tumoren: Glioblastome.
- Mutationen des APC-Komplexes (type 2). Tumoren: Colon-Carcinome (HNPCC, FAP), Medulloblastome (type 2), Glioblastome (10-30 Lj.).
Etwa 10 % der sporadisch auftretenden Medulloblastome haben ebenfalls Mutationen von beta-Catenin.
GORLIN-GOLZ-Syndrom
[Bearbeiten]naevoid basal cell carcinoma syndrome
Erbgang: autosomal dominant, 1:60.000, PTCH mutations (Chr. 9q22) → Shh pathway.
Neoplasien:
- 5-15% Medulloblastome (fast alle unter dem 5. LJ).
- → desmoplastisches Medullo unter 2 Jahre: diagnostisches Hauptkriterium.
- Multiple Basalzellkarzinome.
- Odontogene Keratozysten.
- selten Meningeome, Astrozytome, Kraniopharyngeome: diese evtl. Radiatio-induziert.
Rhabdoid Tumor Prädispositions-Syndrom
[Bearbeiten]Genetik:
- Keimbahnverlust INI1 (Chr. 22q11.2), auch bei sporadischen AT/RTs-> Zellzykluskontrolle.
- second hit: Monosomie Chr. 22. (SMARCB1,BAF47).
- selten: SMARCA4/BRG1 in einer Familie with rhabdoid tumor predisposition syndrome.
Ep: meist Kinder
Neoplasien:
- renale / extrarenale maligne rhabdoid Tumore (AT/RTs)
- selten: CPCs (umstritten!), CRINET
- Meningeome mit INI1 Verlust bekannt,meist in Kontext von NF2 (vermutlich ausgedehnte Deletionen)
Aber: rhabdoide Meningeome haben in der Regel regelhafte Expression von INI1.
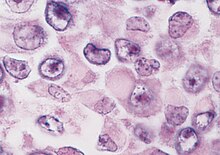 |
Noch ohne WHO Klassifikation:
[Bearbeiten]DOLN
[Bearbeiten]Diffuse oligodendroglial-like neoplasm
- Gliom mit expansivem, leptomengialen Wachstum.
- LOH1p und KIAA1549-BRAF Fusionen in den meisten Fällen.
| thumb|DOLN, HE Färbung | thumb|DOLN, HE Färbung | thumb|DOLN, HE Färbung |
CRINET
[Bearbeiten]Cribiform neuroepithelialer Tumor
- Meist vebtrikulär.
- Trabekulärer Aufbau, EMA-positiv
- INI1-Verlust
Literatur
[Bearbeiten]- World Health Organisation Classification of Tumours - Pathology & Genetics - Tumours of the Nervous System. IARCPress Lyon 2007
- Armed Forces Institute of Pathology Atlas of Tumor Pathology - Tumours of the Peripheral Nervous System - AFIP Washington 1997
- Russell & Rubinstein's Pathology of Tumors of the Nervous System
- Smears and Frozen Sections in Surgical Neuropathology: A manual
Buch-Navigation
- ↑ Nobusawa et al. IDH1 mutations as molecular signature and predictive factor of secondary glioblastomas. Clin Cancer Res. 2009;15:6002-7.
- ↑ Schwartzentruber J, Korshunov A, Liu XY, Jones DTW, Pfaff E, Jacob K, Sturm D, Fontebasso AM, Quang DAK, Tonjes M, Hovestadt V, Albrecht S, Kool M, Nantel A, Konermann C, Lindroth A, et al. Driver mutations in histone H3.3 and chromatin remodelling genes in paediatric glioblastoma (vol 482, pg 226, 2012). Nature. 2012; 484(7392):130-130
- ↑ author. “ATRX loss refines the classification of anaplastic gliomas and identifies a subgroup of IDH mutant astrocytic tumors with better prognosis.”. Acta Neuropathol, 126:443-51, Sep 2013. DOI:10.1007/s00401-013-1156-z.