Pathologie: Leber
Buch-Navigation
Folgen von Lebererkrankungen
[Bearbeiten]Leberzellzerstörung
[Bearbeiten]- Nekrose
- Apoptose - Vork.: Hepatitis.
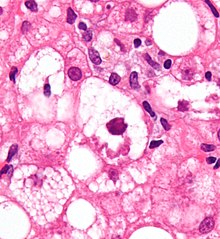
- Ballooning degeneration - Zellschwellung, vakuoliges (schaumiges) aufgehelltes Zytoplasma.
- -> COUNCILMAN-bodies - Schrumpfung, eosinophiles Zytoplasma. Vork.: Virushepatitis, hämaorrhagische Fieber (Gelbfieber), Steatohepatitis.
- -> MALLORY-bodies - Intrazytoplasmatische Einschlusskörperchen aus kondensierten Keratinfilamenten. Morph.: Erinnert an eine „verdrehte Strickleiter“. Vork.: Bei alkoholischer Hepatitis (ASH).
 |
 |
 |
 |
Leberfunktionsstörungen
[Bearbeiten]- Reduzierte Entgiftungs- und Ausscheidungsfunktion
- -> Kompromittierter Harnstoffzyklus -> Ammoniak-Anstieg -> Hepatische Enzephalopathie v.a. bei Eiweißexposition (Ösophagus-/Fundusvarizen-Blutung!)
- -> Gestörte Biotransformation
- -> Verzögerter Abbau von Androgenen -> periphere Umwandlung in Östrogene -> Gynäkomastie, Bauchglatze, andere endokrine Störungen
- -> Reduzierte Bilirubin-Ausscheidung -> Ikterus (Gelbsucht)
- Intrahepatische Cholestase -> Ikterus, Pruritus
- Reduzierte Synthesefunktion
- -> Albumin-Mangel -> Verringerter kolloidosmotischer Druck im Kapillarbett -> Ödeme, Aszites -> Hypotonie, Kollapsneigung, hepatorenales Syndrom, erektile Dysfunktion, Spontan-bakterielle Peritonitis (SBP)
- -> Mangel an Gerinnungsfaktoren (z.B. der Vitamin K-abhängigen Faktoren II, VII, IX, X) -> Störungen des extrinsischen Gerinnungssystems (Quick erniedrigt bzw. INR erhöht) -> Lebensbedrohliche Blutungen
- -> Reduzierte metabolische Funktion (Glycogenspeicherung, Gluconeogenese) -> Hypoglykämien
Pfortaderhochdruck
[Bearbeiten]- Erhöhung des intrahepatischen Gefäßwiderstandes -> Erhöhung des portalvenösen Blutdrucks
- -> Aszites -> Spontane bakterielle Peritonitis (SBP)
- -> Splenomegalie
- -> Aktivierung der Umgehungskreisläufe
- -> Caput medusae
- -> Ösophagus- und Fundusvarizen -> Lebensbedrohliche Blutungen
Aszites
[Bearbeiten]Syn.: Bauchwassersucht
Ät. und Pg.:
- Abflussstörungen -> Portale Hypertension:
- prähepatisch: Z.B. bei Portalvenenthrombose
- intrahepatisch: Z.B. bei Leberzirrhose
- posthepatisch: Z.B. bei BUDD-CHIARI-Syndrom oder Herzinsuffizienz
- Erniedrigter kolloidosmotischer Druck: Albuminmangel z.B. bei Leberzirrhose (Synthesedefizit) oder nephrotischem Syndrom (Verlust).
- Sekretion: Peritonealkarzinose durch sezernierende Adenokarzinome (maligner Erguss), Serositis.
Makro: Seröse Flüssigkeitsansammlung in der Bauchhöhle.
Cholestase
[Bearbeiten]Kann Ursache oder Folge von Lebererkrankungen sein.
Klinik: Ikterus (Gelbsucht), Pruritus (Juckreiz).
 |
Fehlbildungen der Leber
[Bearbeiten]- Agenesie (Rarität)
- Lageanomalien (bei situs inversus)
- abnorme Lappung
- Ektopes Lebergewebe
Fehlbildungen der Gallenwege
[Bearbeiten]- Kongenitale polyzystische Erkrankung des Kindes
- Kongenitale polyzystische Erkrankung des Erwachsenen
- Solitäre Leberzysten
- Kongenitale Leberfibrose
- Gallengangsmikrohamartome (VON-MEYENBURG-Komplex) - Subkapsulär, Bindegewebe mit eingelagerten Gallengängen.
- CAROLI-Syndrom: angeborene Leberzirrhose, zystische Dilatation der intrahepatischen Gallengänge, porto-portale Bindegewebssepten
Angeborene Stoffwechselstörungen
[Bearbeiten]Glycogenosen (GSD)
[Bearbeiten]glycogen storage disease
Ät.: Stoffwechseldefekte mit Ablagerung von Glycogen in Leber und/oder Muskel. Die Leber ist bei der GSD3 (Morbus CORI) betroffen.
Histo: Ballonierte hepatozyten mit hellem Zyplasma. Periportale Fibrose.
Klinik: Hepatopathie und/oder Myopathie, Hypoglykämie.
 |
 |
Hämochromatose (HFE)
[Bearbeiten]Primäre Siderosen
Syn.: , Eisenspeicherkrankheit
Ätiologie:
- Klassische hereditäre HFE: Autosomal-rezessive Mutation des HLA-H-Gens bzw. des HFE-Gens (6p21.3), adulte Form, Männer stärker betroffen (Eisenverlust bei Frauen über die Menstruation), bis zu 10 % der Bevölkerung sind heterozygote Träger der Mutation.
- HFE2A: Juvenile Hämochromatose (JH) durch Mutation des Hemojuvelin-Gens (HJV; 1q21).
- HFE2B: Juvenile Hämochromatose (JH) durch Mutation des hepcidin antimicrobial peptide-Gens (HAMP; 19q13).
- HFE3: Autosomal-rezessive Mutation im Gen des Transferrinrezeptors-2 (TFR2; 7q22).
- HFE4: Autosomal-dominante Mutation im SLC40A1-Gen (2q32), welches Ferroportin kodiert.
Pg: Ungebremste Eisenresorption Im GIT -> hohe Eisenspiegel, Akkumulation in den Organen -> Lipidoxidation und DNA-Interaktion.
Folgen der klassischen HFE: Die Leber kann in Form von Nekrosen, Fibrose, Zirrhose oder Entwicklung eines HCC betroffen sein. Weitere typische Manifestationen sind Diabetes mellitus, CMP, Bronzefärbung der Haut (fahlbraunes Hautkolorit), Arthritiden, Hypogonadismus, Hypothyreose.
Juvenile Formen: Beide Geschlechter betroffen, schwerer, Symptome vor dem 30. Lebensjahr: Hypogonadotroper Hypogonadismus, Herzversagen und/oder Arrhythmien, unbehandelt letal durch kardiale Komplikationen.
Labor: Ferritin > 700 ng/ml, Transferrin-Sättigung > 50 %.
Makro: Bräunliche Verfärbung zahlreicher Organe, zirrhotischer Umbau.
Histo: Nachweis der Eisenablagerungen mit der Eisenfärbung (Berliner Blau).
Weblinks: OMIM - Hemochromatosis, OMIM - Juvenile hemochromatosis (JH), OMIM - HFE3, OMIM - HFE4
 |
Morbus WILSON
[Bearbeiten]Syn.: Kupferspeicherkrankheit, hepatolentikuläre Degeneration
Ep.: Erstmanifestation oft schon vor dem 20. Lebensjahr.
Ät.: Mutation im Gen ATP7B (13q14.3-q21.1), das für ein Kupfer-Transportprotein (ATPase) kodiert. Autosomal-rezessiver Erbgang.
Pathogenese: Kupferablagerungen in Leber, Niere, ZNS -> Schädigung von Mikrotubuli und Mitochondrien.
Makro: Kleinknotiger, fibrotischer Umbau der Leber.
Klinik: Leberzirrhose, neurologisch-psychiatrische Symptome, Erhöhte Kupferkonzentration im Urin, S-Coeruloplasmin und S-Gesamtkupfer vermindert, KAYSER-FLEISCHER-Kornealring.
Weblinks: OMIM - Wilson disease
 |
Amyloidose
[Bearbeiten]Siehe Kapitel Degeneration.
 |
 |
 |
Zirkulationsstörungen
[Bearbeiten]Physiologie: Die Versorgung der Leber erfolgt zu 1/3 über die A. hepatica propria, zu 2/3 über die V. portae.
Prähepatische Einflußstörungen
[Bearbeiten]Ät.:
- Leberarterienkompression
- Portalvenenkompression
- Pfortaderthrombose
Folgen: Ösophagusvarizen, Splenomegalie, intestinale Kongestion (Stauung).
Schockleber
[Bearbeiten]Ät.: Linksvorwärtsinsuffizienz des Herzens.
Makro: Schlaffe weiche Leber.
Histo:
- Akut: Zentrolobuläre Schocknekrosen.
- Protrahiert: Zusätzlich zentrolobulär verschmählerte Leberzelltrabekel.
Intrahepatische Zirkulationsstörungen
[Bearbeiten]Verminderter Leberdurchfluss
[Bearbeiten]Ät.:
- Zirrhose
- Sinusoidokklusion
Folgen: Aszites, Ösophagusvarizen, Hepatomegalie, Transaminasen-Anstieg.
ZAHN'scher Infarkt
[Bearbeiten]Lokale Druckatrophie durch Stauungshyperämie, z.B. bei Rechtsherzinsuffizienz und gleichzeitiger lokaler Kompression kleiner Portalvenen im betroffenen Bereich, keine Nekrose.
Leber-Infarkt
[Bearbeiten]Meist hämorrhagisch (wg. doppelter Blutversorgung über Vasa publica und Vasa privata).
Posthepatische Abflußstörungen
[Bearbeiten]Folgen: Aszites, Hepatomegalie, Bauchschmerzen, Transaminasenanstieg
BUDD-CHIARI-Syndrom
[Bearbeiten]Thrombose der großen Lebervenen
Ät.: idiopathisch (30 %), Kollagenosen (SLE), myeloproliferative Erkrankungen
Mikro: Multiple, zentrolobuläre Nekrosen
Beim Budd-Chiari-Syndrom kommt es zu einer sich schnell (= akuten) oder langsam (= chronisch) entwickelnden Blutabflussstörung der Leber durch eine Thrombose in den Lebervenen oder der V. cava inferior. Klinisch besteht eine Lebervergrößerung, Schmerzen im rechten Oberbauch und Aszites (= Erguss der Bauchhöhle). Die Thrombose der Lebervenen entsteht im Rahmen einer allgemein erhöhten Thromboseneigung bei hämatologischen Grunderkrankungen, Mutationen von Genen der Blutgerinnungsfaktoren (insbesondere der Faktor V), Lupus erythematodes, Verwendung von Kontrazeptiva und malignen Tumoren. Die Thrombosen beim Budd-Chiari-Syndrom können aber auch beim direkten Verschluss von Lebervenen durch Tumoren oder Entzündungen entstehen. Ca. 30% der Patienten mit Budd-Chiari-Syndrom zeigen jedoch keine eindeutig identifizierbare Ursache (sog. „idiopathische“ Genese).
Vena-occlusive-disease
[Bearbeiten]Thrombosierung der kleinen intrahepatischen Venen
Ät.: Zytostatika, nach KM-Tx, nach Radiotherapie
Akute kardiale Leberstauung
[Bearbeiten]Ät.: Akute Rechtsherzinsuffizienz, z.B. bei fulminanter Lungenarterienembolie, Perikardtamponade, akutem inferioren Hinterwandinfarkt.
Makro: Geschwollene rote Leber. Von der frischen Schnittfläche fließt reichlich Blut ab.
Mikro: Hyperämie. Normale Architektur des Lebergewebes.
Chronische kardiale Leberstauung
[Bearbeiten]Ät.: Chronische Rechtsherzinsuffizienz z.B. bei Cor pulmonale aufgrund einer primären oder sekundären pulmonalen Hypertonie (COPD, rezidivierende Lungenarterienembolie), Klappenfehler z.B. Trikuspidal- oder Pulmonalstenose, Perikarditis constrictiva, altem Hinterwandinfarkt mit Rechtsherzbeteiligung, Pericarditis constrictiva.
Makro: Muskatnussleber (Schnittfläche: Hellbraunes Lebergewebe mit etwas eingesunkenen dunkelbraunen hyperämischen Zentralvenen). Vollbild: Herbstlaubleber (Wie Muskatnussleber plus gelblich verfettete Areale).
Mikro: Die Zentralvene ist gestaut, erweitert, erythrozytenreich, die Sinusoide sind perizentral erweitert, die Hepatozyten besonders perizentral komprimiert (Druckatrophie). Stauungsstraßen und läppchenzentral betonte Fibrose.
Kompl.: Zirrhose cardiaque durch die fibrotische Bindegewebsvermehrung.
 |
Akute Virus-Hepatitis
[Bearbeiten]Definition: Hepatitis < 6 Monate
Ät.:
- Virushepatitis: HAV 55 % HBV 35 %, HCV 10 %
- Virusbegleithepatitis: EBV, CMV, VZV u.a.m.
Verlauf:
- Infektion
- Latenzphase
- Prodromalstadium: 2-7 Tage, grippeähnlich, gastrointestinale Symptome
- Hepatische Organmanifestation: 4-8 Wochen, 2/3 anikterisch!
Verlaufsformen:
- Subklinisch
- Akute Hepatitis
- Carrier (gesunder Virus-Träger)
- Persistenz/Chronische Hepatitis (chronisch stabil <-> chronisch aggressiv)
Morphologie:
- Zellödeme (hydropisch geschwollene ballonierte Zellen) mit läppchenzentraler Betonung
- T-Zell-vermittelte eosinophile Leberzelldegeneration mit Koagulationsnekrosen (Councilman-bodies: Einzelzellnekrosen, extrazellulär)
- Proliferation der Kupffer-Stern-Zellen
- Lymphozytäre Infiltration der Leberläppchen
- Lymphohistiozytäre Infiltration der Portalfelder -> Mottenfraßnekrosen
- Im abklingenden Stadium Akkumulation von Ceroidpigment und Eisen in den Makrophagen
Formen der Nekrose:
- Disseminierte Einzelzellnekrosen
- Zentrale Nekrose
- Ausbreitung nach periportal -> Konfluierende brückenbildende Nekrosen
- Periportale Mottenfraßnekrosen
- Massive Nekrosen
Komplikationen:
- Cholestatische Verlaufsformen: Hepatitis mit intrahepatischem Verschlußsyndrom, S-AP+, LAP+, γGT+
- Protrahierter Verlauf: Transaminasenerhöhung > 3 Monate
- Fulminanter Verlauf: brückenbildende und multilobuläre Nekrosen (Hep.A. 0,1%, Hep.C 1%)
- Extrahepatische Manifestation: Kryoglobulinämie, Glomerulonephritis; 5-10% bei HBV)
- Viruspersistenz = chronische Hepatitis
- Chronisch persistierend (CPH) - Milchglaszellen
- Chronisch aggressiv (CAH) - Mottenfraßnekrosen
- Spätkomplikation: Leberzell-Ca
Folgezustände:
- Restitutio ad integrum
- Entzündliche Residuen (Aktivierung der Kupffer-Stern-Zellen, lymphohistiozytäre Portalfeldinfiltrate)
- Chronische Hepatitis
- Fibrose und Zirrhose
- Hepatocelluläres Karzinom (HCC)
Hepatitis A
[Bearbeiten]RNA-Virus
Übertragung: fäkal-oral
- Vermehrung nur in Leberzellen
- Kein chronischer Verlauf
Histo: Einzelzellnekrosen in periportaler Zone
Hepatitis B
[Bearbeiten]DNA-Virus
Übertragung: sexuell, Blut.
Mikro: Nekrosen in den Läppchenzentren, Milchglashepatozyten.
Verlaufsformen:
- Subklinisch 60 - 65 % -> 100 % Erholung
- Akute Hepatitis 20 - 25 % -> 99 % Erholung, < 1 % fulminant
- Carrier 5 - 10 % (Gesunder HBs-Ag-Träger: Evtl. Leberzellkarzinom)
- Persistierend 4 %
- -> 70 - 90 % Erholung
- -> 10 - 30 % Chronische Hepatitis -> Zirrhose, hepatozelluläres Karzinom (HCC)
 |
Hepatitis C
[Bearbeiten]RNA-Viren
Übertragung: Transfusion, i.v.Drogen (Spritzentausch), sexuell, z.T. unklar
Verlauf:
- Heilung 15 %
- Chronifizierung 85 %
- -> Stabil 80 %
- -> Zirrhose 20 % -> HCC
- Fulminant selten
Hepatitis D
[Bearbeiten]RNA-Virus
Braucht zur Replikation das HBs-Antigen des Hepatitis B-Virus
- Simultaninfektion: 90 % Heilung
- Fulminanter Verlauf häufiger
- Superinfektion: Meist chronischer Verlauf
Hepatitis E
[Bearbeiten]Nicht chronisch, hohe Letalität bei Infektion in der Schwangerschaft.
Chronische Hepatitis
[Bearbeiten]Dauer > 6 Monate
Ät.:
- Viral (Hepatitis B,C,D)
- Autoimmunologisch: Primär biliäre Leberzirrhose (PBC), Primär sklerosierende Cholangitis (PSC)
- Medikamentös-toxisch (α-Methyldopa, Isoniazid)
- Alkoholabusus
- Stoffwechselstörungen (Diabetes mellitus, Hämochromatose, Morbus Wilson, α1-AT-Mangel)
Folge: Leberfibrose, -zirrhose in 20-50 % nach 10-20 Jahren
Kompl.: HCC
Morphologische Diagnostik:
- Vorliegen einer Hepatitis und Hinweise für Chronizität - Überwiegend lymphozelluläre Infiltration mit P.m. in den Periportalfeldern, evtl. periportale Fibrose und Grenzzonenhepatitis (= Interfacehepatitis, früher: Mottenfraßnekrose).
- Aktivität (Grading) - Hierzu gibt es verschiedene Scores (z.B. Desmet-Scheuer-Score)
- Fibrosestadium (Staging) - Z.B. Mit dem Score nach Desmet et al.
- Ätiologie (in Zusammenschau mit den klinischen Daten) - Z.B. Milchglaszellen pathognomonisch für Hepatitis B. Oder z.B. klinischer (serologischer) Nachweis von HBs-Antigen.
Notwendige klinische Angaben zur Befundung von Leberstanzbiopsien:
- Labor: Leberwerte (GOT (AST), GPT (ALT), γ-GT, AP, γ-Globulin) und Autoantikörper.
- Mikrobiologie: Hepatitis-Serologie
- Anamnese (Beschwerden, Dauer, Alkohol/Drogen/Medikamente, Familienanamnese, Reiseanamnese, Berufsanamnese)
- Klinik/Vorerkrankungen: Z.B. Stoffwechselstörungen
Literatur:
- Schirmacher P et al. “Bioptische Diagnostik der chronischen Hepatitis - Ergebnisse einer evidenzbasierten Konsensuskonferenz der Deutschen Gesellschaft für Pathologie (DGP), der Deutschen Gesellschaft für Verdauungs- und Stoffwechselkrankheiten (DGVS) und des Kompetenznetzes Hepatitis (HepNet)”. Pathologe, 25(5):337-48, Sep 2004. PMID 15278290
- http://www.dgvs.de/media/leitlinie_biopt_diagnostik.pdf
Chronische Virushepatitis
[Bearbeiten]Ät.: HBV, HCV, HDV
Mikro:
- Portale Entzündung, Nekrosen (Grading)
- Fibrosierung, Zirrhose (Staging)
- Gallengangsproliferate
Bakterielle Hepatitis
[Bearbeiten]Erreger: E. coli, Streptokokken, Staphylokokken
Infektionswege: Hämatogen (arteriell, portalvenös), cholangiogen-aszendierend, traumatisch.
Morph.: Destruierend, abszedierend, konfluierend (-> Septikopyämie).
Parasitäre Lebererkrankungen
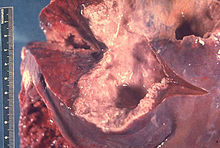
[Bearbeiten]Leberabszess bei Amöbiasis
[Bearbeiten]Ät.: Infektion durch Entamoeba histolytica (Magnaform).
Pg.: Komplikation der Amöbenruhr.
 |
Echinokokkose
[Bearbeiten]Echinococcus: Zysten (Hydatiden) aus Kapsel, parasitärer Keimschicht und Scolizes der Finnen.
2 Arten:
- Echinococcus granulosus - Hundebandwurm - Zystische Echinokokkose: Große, gekammerte, rundliche Hydatide.
- Echinococcus multilocularis - Fuchsbandwurm - Alveoläre Echinokokkose: diffus sich verzweigende Hydatide, schlechtere Prognose. Invasiv wachsend, kann metastasieren.
Th.: Kurativ: Chirurgische Resektion. Unterstützend/palliativ: Antihelminthika.
Die Erkrankung ist meldepflichtig!
Autoimmunhepatitis
[Bearbeiten]Ep.: 5 - 20 % aller chronische Hepatitiden, bes. Frauen (jung oder postmenopausal)
Ät.: T-Suppressorzell-Defekt: T-Zell-Rezeptor gegen Leberzellmembran-Ag (CYP450)
Klinik: IgG erhöht, ANA +, SMA +
Assoziation mit Immunerkrankungen wie Thyreoitiden, Vaskulitis u.a.
Medikamenteninduzierte Hepatitis
[Bearbeiten]Histo: variabel, z.B.:
- Eosinophilie
- Lymphozyten
- Granulome
 |
Eklampsie
[Bearbeiten]Metabolisch-toxische Leberschäden
[Bearbeiten]Lebergifte:
- Obligate Lebertoxine - Dosisabhängige Schädigung, vorhersagbare Wirkung
- Fakultative Lebertoxine - Keine dosisabhängige Schädigung, keine vorhersagbare Wirkung
- Primäre Lebertoxine - Schädigen direkt
- Sekundäre Lebertoxine - Schädigung durch Metabolite (Giftung, Biotransformation)
Manifestation eines Leberschadens: Leberzellnekrosen, Leberzellverfettung (groß-, kleintropfig), intrahepatische Cholestase, akute/chronische Hepatitis, granulomatöse Entzündung, Fibrose, Zirrhose.
Leberzellverfettung
[Bearbeiten]Syn: Steatosis hepatis
Ät.: Metabolisch (Diabetes, Überernährung), toxisch (Medikamente!), alkoholisch.
Makro: Die Leber ist gelblich verfärbt.
Histo:
- Zahlreiche Vakuolen, evtl. kribriformes (siebförmiges) Muster.
- Anzahl verfetteter Hepatozyten > 50 % = Fettleber
Kompl.:
- Alkoholische Steatohepatitis (ASH)
- Nicht-alkoholische Steatohepatitis (NASH).
- Leberfibrose/-zirrhose
 |
 |
 |
Alkoholtoxischer Leberschaden
[Bearbeiten]30 - 50 % aller Lebererkrankungen in Europa, USA
Schädigungsmechanismen:
- Giftung in der Leber: Alkohol -ADH-> Acetaldehyd (toxisch)
- Verschiebung des Redoxgleichgewichts (NADH-Anstieg)
- Induktion des mikrosomalen Ethanol-oxidierenden Systems (MEOS) -> Medikamenteninteraktionen
Mögliche Folgen:
- Alkoholische Steatosis hepatis
- Alkoholische Steatohepatitis (ASH)
- Alkoholische Leberfibrose und -zirrhose
Mikro: Siegelringzellen (zentrale Fettvakuole, an den Rand gedrängter Kern), alkoholisches Hyalin (hirschgeweihartig), MALLORY-Körperchen (intrazellulär), Leberfibrose (perivenuläre/perizelluläre Fibrose bis zur zentralen Sklerose, Maschendrahtfibrose), porto-portale/porto-zentrale Bindegewebssepten, unspezifisches entzündliches Bild, Cholestasezeichen.
Makro: Die Leber ist vergrößert, gelblich, teigig-weich
Kompl.: HCC, ZIEVE-Syndrom, extrahepatisch
Leberzirrhose
[Bearbeiten]Ät.: Alkoholabusus 60 - 70 %, chronische Hepatitis 10 - 15 %, biliär 5 %, Hämochromatose 5 %, andere Stoffwechselerkrankungen (Galaktosämie, Fruktose-Intoleranz, Glykogenosen, Morbus WILSON, α-1-Antitrypsinmangel) < 1 %, Toxine < 1 %, Leberstauung < 1 %, idiopathisch 10 %
Einteilung:
- Postnekrotische Leberzirrhose
- Posthepatitische Leberzirrhose
- Biliäre Leberzirrhose
- Pigmentzirrhose (Morbus WILSON, Hämochromatose)
- Fettzirrhose
Erscheinungsform:
- Kleinknotig </= 3 cm
- Großknotig > 3 cm
- Gemischt
Aktivität:
- Aktive Zirrhose (Leberzellnekrosen, Entzündung)
- Stationäre (inaktive) Zirrhose
Makro: Die Leber ist geschrumpft und hat eine höckrige Oberfläche.
Mikro: Bindegewebsvermehrung (EVG: BG violett), Bindegewebssepten, abgeschnürte Regeneratknoten. Die Zentralvene ist verschwunden, man findet Neoduktuli (Gallengangproliferationen).
Folgen:
- Ikterus
- Gerinnungsstörungen
- Hypalbuminämie -> Aszites, Hypotonie, Hepatorenales Syndrom
- Endokrine Störungen -> Gynäkomastie, Leberhautzeichen (Bauchglatze, Spider-Nävi, Weißnägel, Palmarerythem)
- Ammoniak-Anstieg -> Hepatische Enzephalopathie/Coma hepaticum
- Portale Hypertension -> Aszites, Splenomegalie, Aktivierung von Kollateralkreisläufen -> Ösophagusvarizen, Fundusvarizen, Caput medusae.
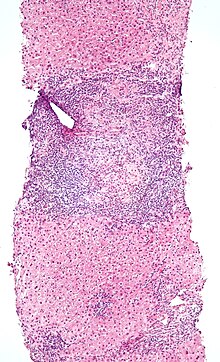
Chronisch destruierende nicht-eitrige Cholangitis - Primär biliäre Zirrhose (PBC)
[Bearbeiten]Ep.: 1 % der Zirrhosen, 95 % Frauen zwischen dem 40. und 60. Lj.
Ät.: Autoimmun, zytotoxische AK gegen Gallengangsepithel, Antimitochondriale Antikörper (AMA).
Stadieneinteilung 1 bis 4
Makro: Kleinknotiger, zirrhotischer Umbau.
Histo: Lymphohistiozytäre Infiltration mit Epitheloidzellgranulomen, Bindegewebssepten porto-portal und porto-zentral.
Klinik: Cholestase, Pruritus, Hypercholesterinämie.
Labor: Cholestase-Parameter (AP, GGT, Bilirubin) und IgM erhöht, > 90 % AMA.
Prg.: Ohne Transplantation schlecht.
 |
 |
 |
Primär sklerosierende Cholangitis (PSC)
[Bearbeiten]Entzündlich fibrosierender Prozess an den intra- und extrahepatischen Gallengängen
Ep.: w:m = 1:2, 25 - 40 Lj., familiäre Häufung, > 70 % Colitis ulzerosa!
Klinik: ANCA 80 %
Mikro: Periportal periduktuläre Fibrose, Bindegewebssepten mit lymphohistiozytärer Infiltration, Atrophie und Obliteration der Gallengänge.
Sekundär sklerosierende Cholangitis
[Bearbeiten]Ät.: Immunschwäche, rezidivierende Infekte, Gallenabflußstörungen, GvH-Reaktion
Tumoren der Leber
[Bearbeiten]RF: Vinylchlorid, Arsen, chron. HBV- und HCV-Infektion, Aflatoxine, Nitrosamine
Systematik der Lebertumoren:
- Epithelial
- Hepatozellulär - Fokale noduläre Hyperplasie (FNH), Adenom, Hepatozelluläres Karzinom (HCC)
- Cholangiozellulär - Cholangiom, Zystadenom, Zystadenokarzinom, Cholangiozelluläres Karzinom (CCC)
- Mesenchymal
- Benigne - Hämangiom, Fibrom, Lipom, Myom
- Maligne - Angio-, Fibro-, Lipo-, Leiomyosarkom
- Embryonale Tumore - Hepatoblastom
- Metastasen (30 % der Lebertumoren)
Gallengangshamartom (VON MEYENBURG-Komplex)
[Bearbeiten]Assoziation: Polyzystische Nierenerkrankung.
 |
 |
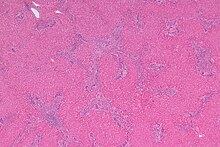
Fokale noduläre Hyperplasie (FNH)
[Bearbeiten]Ep.: w > m.
Ät.: Vermutlich reaktiv.
Makro: Zentrale sternförmige Narbe mit radiären Einziehungen.
Histo: Verlust der sinusoidalen Gliederung, lympho-histiozytäre Infiltration der Portalfelder. Gallengangsproliferate an der Grenze zum Normalgewebe.
IHC: Glutamin-Synthetase - Landkartenartige Anfärbung der Läsion.
Sono: Echoarm. KM: Radspeichenartiges Muster.
CT: Isodens.
MRT: Isointens.
Klinik: Meist asymptomatisch.
 |
 |
 |
Hepatozelluläres Adenom (HCA)
[Bearbeiten]RF: Anabole Steroide, hormonelle Kontrazeptiva.
Histo: Hepatozyten, nicht mehr als zwei Zelllagen, keine Portalfelder innerhalb der Läsion.
Subtypen:
- HNF1alpha-inaktiviertes resp. L-FABP-negatives Adenom - Verfettung, eher Frauen.
- beta-Catenin-positives Adenom - eher Männer, Atypien, kann maligne entarten.
- Inflammatorisches HCA - Lymphozytäre Infiltrate, Duktulusproliferate, CRP-Erhöhung, in 60 % gp130-Mutation.
IHC: Glutamin-Synthetase - Diffuse Reaktivität.
DD: FNH, HCC.
Hepatozelluläres Karzinom (HCC)
[Bearbeiten]Ep.: 90 % aller primären Lebertumoren, w:m = 1:5, 5. - 6. Dekade
- ca. 85 % auf dem Boden einer Leberzirrhose
- ca. 15 % ohne vorbestehende Leberzirrhose
In Afrika und Asien häufiger wegen der hohen HBV-Prävalenz.
Ät: Chronische virale Hepatitis B oder C, toxisch (Alkohol, Anabolika, Aflatoxine, DDT, Arsen, PVC), Stoffwechselerkrankungen (Glycogenosen, α1-AT-Mangel, Fructoseintoleranz, Mukoviszidose, Tyrosinämie Typ I), Hämochromatose, PBC, PSC.
Makro: Makronodulär, multizentrisch.
Histo: Evtl. gallebildend, nicht schleimbildend. Histologie sehr variabel. Ggf. fatty change, zahlreiche MALLORY-bodies.
Histologische Typen:
- Diffus
- Trabekulär
- Fibrolamellär
- Pseudoglandulär
- Szirrhös
- Solide
SF:
- Versilberung: Septen mehr als 2 Zelllagen dick.
IHC:
- Hepatocyte: +
- CD34: Darstellung von Tumorgefäßen (Sinusoide normalerweise negativ, CD34 positive Kapillaren nur in den Periportalfeldern).
Verhalten: Affinität zu venösen Gefäßen, hämatogene Metastasierung in die Lunge.
Tumormarker: α-Fetoprotein (AFP) (60 %), α1-Antitrypsin (< 10 %).
Therapie: Leberteilresektion, bei Leberzirrhose auch Lebertransplantation. Palliativ: Transarterielle Chemoembolisation (TACE).
 |
 |
 |
 |
 |
 |
 |
 |
Gallengangs-Zystadenom
[Bearbeiten]Morph.: Zystisch, multilobulär, polypös, regressive Veränderungen (Einblutung)
Zystadenokarzinom
[Bearbeiten]Ep.: Ältere Patienten
Ursprung: Gallengangszystadenom, kongenitale Gallengangszysten
Mikro: Karzinomatöse, teils intestinalisierte, biliäre Epithelauskleidung. Keine Gallebildung, oft schleimbildend.
Makro: Mehrkammerige Zysten mit papillären Einfältelungen
Met.: Lymphogen
Cholangiozelluläres Karzinom, intrahepatisch (CCC)
[Bearbeiten]Ep.: w:m = 1:1, 6. Dekade.
Ät.: Unbekannt.
Histo:
- Atypische Gallengangsepithelien
- Desmoplastische Stromareaktion
Tumor-Marker: CEA, EMA, Cytokeratin, kein α-Fetoprotein.
DD.: HCC
 |
 |
 |
 |
Angiomyolipom
[Bearbeiten]Solitärer fibröser Tumor
Morph.: Lokalisierte zelldichte Fibroblastenproliferation, knotig, gut begrenzt
Hämangiom
[Bearbeiten]Ep: häufigster benigner Tumor der Leber, w:m > 1
- die Häufigkeitsangaben schwanken je nach zugrundeliegender Untersuchungsmethode
- oft ein Zufallsbefund im Sono oder CT
Makro: Meist kavernös, subkapsulär, blutreich, schwammartig, zystisch, evtl. regressiv verändert, thrombosiert, sekundär entzündlich fibrosiert.
Histo: Große endotheltragende blutgefüllte Hohlräume, Thrombose, regressive Veränderungen.
Dignität: Benigne Proliferation von Blutgefässen in der Leber.
 |
 |
 |
Hämangiosarkom der Leber
[Bearbeiten]Syn.: Hämangioendothelsarkom
Ät.: Vinylchlorid, Arsen, Thorotrast (altes Röntgenkontrastmittel). Signaltumor!
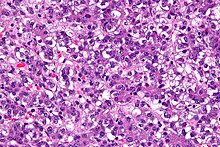
Hepatoblastom
[Bearbeiten]Maligner embryonaler Lebertumor.
Ep.: Kinder 1 - 4. Lj., 5 % der frühkindlichen Tumoren.
Assoziiert mit: Hemihypertrophie, Wilms-Tumor, FAP, Glycogenosen.
Histologische Typen:
- Epithelialer Typ (am häufigsten).
- Fetal - Ähnlich reifen Leberzellen, in Platten angeordnet.
- Embryonal - Kleine, dunkle Zellen, rosettenartige Anordnung.
- Anaplastischer Typ - Kleine undifferenzierte Zellen.
- Gemischter Typ - Epithelialer Typ mit primitiven mesenchymalen Strukturen (Herde von Osteoid, Knorpel, Stroma, Muskulatur).
Cave: Bis zu 5 Jahren nach Resektion noch Rezidive!
 |
 |
 |
Lebermetastasen
[Bearbeiten]- ca. 20 - 30 % aller Lebertumoren
- ca. 80 % aller bösartigen Lebertumoren (in Südostasien gibt es andere Zahlen, da dort das HCC viel häufiger ist)
Herkunft: Colon bis KANNENBÖHM'scher Punkt (Pfortaderabfluß), Lunge, Mamma, Magen, Melanom, Pankreas.
 |
Lebertransplantat
[Bearbeiten]Häufigste Indikation für eine Lebertransplantation: Leberzirrhose.
Komplikationen nach Lebertransplantation umfassen in erster Linie chirurgisch-transplantationstechnische Probleme (Konservierungs-/Reperfusionsschaden, Anastomoseninsuffizienzen, -strikturen), Abstoßungsreaktionen, opportunistische Infektionen und das Wiederauftreten der Grunderkrankung, die zur Transplantation führte.
Konservierungs-/Reperfusionsschaden
[Bearbeiten]Ät.: Ischämie, Hypoxie, Bildung freier Radikale (ROS) nach Reperfusion
Mikro: Ballonierung und Verfettung der Leberzellen, Cholestase
Primäres Transplantatversagen
[Bearbeiten]Ät.: Konservierungs-/Reperfusionsschaden, vorbestehende Schädigung
Zeitraum: In den ersten Stunden nach Tx
Mikro: Massive Nekrosen
Hyperakute Abstoßungsreaktion
[Bearbeiten]Ät.: Humoral (präformierte Antikörper)
Zeitraum: In den ersten Tagen nach Tx
Mikro: Intravasale Neutrophilen-Adhäsion und Thrombosierung, ausgeprägte Nekrosen
Akute Abstoßungsreaktion
[Bearbeiten]Ät.: Zelluläre Abwehrreaktion gegen das Spenderorgan (HLA-Antigene)
Zeitraum: Im 1. Monat nach Tx
Mikro:
- Portale gemischt-zelluläre Entzündung (neutrophile und eosinophile Granulozyten, Makrophagen, Lymphozyten und Plasmazellen)
- Gallengangsdestruktion und -inflammation
- Endothelitis, evtl. mit Thrombosierung der Zentralvenen und perivenulärer Nekrose
Chronische Abstoßungsreaktion
[Bearbeiten]Ät.: Zelluläre Abwehrreaktion gegen das Spenderorgan (HLA-Antigene)
Zeitraum: 2 bis 6 Monate nach Tx
Mikro:
- Obliterierende Arteriopathie - Entzündung und fibrosierende Wandverdickung mittelgroßer Arterien mit zunehmender Einengung des Lumens.
- Ductopenie - Zerstörung und Verlust der kleinen Gallengänge (> 30 % der Periportalfelder).
CMV-Infektion
[Bearbeiten]Ät.: Immunsuppression, größtes Risiko bei Tx eines infizierten Transplantats in einen seronegativen Empfänger.
Zeitraum: 1. bis 4. Monat nach Tx
Mikro: Mikroabszesse, evtl. nukleäre Viruseinschlußkörperchen
HSV-Infektion
[Bearbeiten]Ät.: Immunsuppression
Zeitraum: 1. bis 2. Monat
Mikro: Nekrosen (nekrotisierende Hepatitis), Viruseinschlußkörperchen
EBV-Infektion
[Bearbeiten]Zeitraum: 2. bis 6. Monat
EBV-assoziierte PTLD (post-transplant lymphoproliferative disorder)
[Bearbeiten]Ät.: Immunsuppression, EBV-Infektion/Reaktivierung
Zeitraum: Nach dem 6. Monat post Tx
Bakterielle Infektionen
[Bearbeiten]Ät.: Immunsuppression, Wunden, Katheter, Belastung durch Operation
Pg.: Wundinfektionen, Katheterinfektionen (z.B. Harnwegsinfektion, Venenkatheterinfektion)
Zeitraum: 1. Monat
Candida-Infektion
[Bearbeiten]Ät.: Immunsuppression
Zeitraum: 1. Monat (wg. Steroidhochdosistherapie)
Aspergillose
[Bearbeiten]Ät.: Immunsuppression
Zeitraum: 1. bis 4. Monat nach Tx
Cholestase
[Bearbeiten]Ät.: Z.B. Anastomosenstriktur
Ischämische Cholangiopathie
[Bearbeiten]Zeitraum: 1. bis 6. Monat nach Tx
Medikamentös-toxischer Schaden
[Bearbeiten]Ät.: Immunsuppressiva
Wiederauftreten der ursprünglichen Lebererkrankung
[Bearbeiten]- HBC
- HCV
- PSC
- PBC
- Ethyltoxischer Leberschaden, ASH
- NASH
- HCC
Literatur: Longerich T, Schirmacher P. “General aspects and pitfalls in liver transplant pathology”. Clin Transplant., 20(Suppl 17):60-8, 2006. PMID 17100703
Buch-Navigation
