Pathologie: Skelettmuskel
Buch-Navigation
Grundlagen
[Bearbeiten]Muskuläre Schäden können auf 3 Ebenen verursacht sein:
- Neuron -> Neurogene Muskelatrophie
- Neuromuskuläre Synapse -> Myasthene Syndrome
- Muskel -> Myopathie oder Myositis
Entsprechend dem unterschiedlichen Pathomechanismus lassen sich in der Histologie des Skelettmuskels neurogene von myopathischen Schäden unterscheiden.
Leitsymptome bei Myopathien:
- distal: myotone Dystrophien, okulopharyngeale Muskeldystrophie
- asymmetrisch: Fasioskapulohumerale Muskeldystrophie, Einschlusskörperchenmyositis, Glykogenose V
- paraspinal: Gliedergürteldystrophie, Glykogenose II
- Augenbeteiligung: Mitochondriale Myopathie, Okulopharyngeale Dystrophie
- Hypertophie: Myotonia congenita
- Pseudohypertrophie: Muskeldystrophien
- Lactatanstieg im Labor: Glykogenosen
Bei symptomfreien Patienten sollten andere Ursachen eines CK-Anstieges geprüft werden, bevor weitere invasive Diagnostik zur Erhebung von Muskelerkrankungen (hier nur in 20-30% erfolgreich) durchgeführt wird.
Idiopathische Hyper-CKämien:
- Sportliche Betätigung (bei Marathonläufen bis zu 50x über Norm)
- Muskuläre Injektionen
- Medikamente (Vor allem Diuretika, Cholesterinsenker, Psychopharmaka, Asthmatherapeutika, Lokalanästhetika)
- epileptische Anfälle
- Hypothyreose
- akute Psychosen
Muskeldiagnostik
[Bearbeiten]- Auswahl des zu biopsierenden Muskels
Indikationsstellung zur Biopsie durch den Neurologen, da bestimmte Erkrankungen wie Myasthenie oder Myotonie mit elektrophysiologischen Methoden nachgewiesen werden können. Der Muskel sollte erheblich betroffen sein, aber nicht völlig fettig degeneriert. Gegebenenfalls Auswahl mit Hilfe der bildgebenden Diagnostik. Keine Muskel, bei dem zuvor Injetionen oder eine Elektromygraphie durchgeführt wurde: Histologische Artefakte Bei Verdacht auf entzündliche Erkrankungen: Biopsie vor Beginn der immunsupressiven Therapie, da sonst Infiltrate mitigiert werden können.
- Art der Muskelbiopsie
Bei der offenen Biopsie wird nach örtlicher Betäubung ein Hautschnitt angelegt und der Muskel freigelegt. Danach wird eine Muskelgewebeprobe (ideal: 1 cm³) entfernt. Anschließend wird die Wunde nach Blutstillung durch Nähte verschlossen. Komplikationen bei der Entnahme wie Wundheilungsstörungen oder eine Infektion sind selten.
Weniger gebräuchlich ist die Stanzbiopsie, bei der nach örtlicher Betäubung mit einer Biopsienadel eine kleine Muskelgewebeprobe durch die Haut hindurch entfernt wird. Dieses Verfahren ist zwar weniger invasiv, allerdings kann auch nur weniger Muskelgewebe gewonnen werden.
Der Muskel sollte immer unfixiert in die Neuropathologie gesendet werden, da viele enzymhistochemische Färbungen nicht an formalinfixierten Präparaten durchgeführt werden. In der Regel wird ein Teil der Biopsie in Glutar für die Elektronenmikroskopie, ein Teil für molekulargenetische oder biochemische Untersuchungen in Stickstoff eingefroren. Was nicht für den diagnostischen Gefrierschnitt eingesetzt wird, kann in Formalin asserviert werden.
Eingesetzte Untersuchungstechniken in der Muskeldiagnostik:
- Histochemie
- Elektronenmikroskopie
- Immunhistochemie
Standardfärbungen: Die neuropathologische Untersuchung der Muskelprobe umfasst routinemäßig mehr oder weniger folgende Färbungen:
- Hämatoxylin-Eosin-Färbung (unter anderem Nachweis entzündlicher Infiltrate zum Beispiel bei Myositis)
- Elastika-van-Gieson-Färbung (EvG) (Nachweis einer Fibrose des endomysialen Bindegewebes zum Beispiel bei Myopathien)
- modifizierte Gomori-Trichrom-Färbung (Nachweis von Einschlusskörpern zum Beispiel bei der Nemalin-Myopathie)
- PAS-Färbung (Nachweis einer vermehrten Einlagerung von Glykogen zum Beispiel bei der McArdle-Krankheit)
- Ölrot-Färbung (Nachweis einer vermehrten Lipideinlagerung zum Beispiel bei Mangel der Carnitin-Palmitoyl-Transferase)
- Saure Phosphatase-Reaktion (Nachweis einer vermehrten Makrophagenaktivität zum Beispiel bei entzündlichen Myopathien)
- NADH-Reaktion (Darstellung des intermyofibrillären oxidativen Netzwerks und seiner Störungen zum Beispiel bei Central-Core-Myopathie)
- ATPase-Reaktion bei unterschiedlichen pH-Werten (Nachweis der verschiedenen Fasertypen und deren gestörtes Verteilungsmuster zum Beispiel bei chronisch-neurogener Schädigung)
- AMPDA-Reaktion (zum Nachweis/Auschluss eines MAD-Mangels)
- Phosphorylase-Reaktion (für Nachweis der entsprechenden Glykogenose)
Leitsymptome bei der Diagnostik:
- Entzündung: Polmyositis, Dermatomyositis, Granulomatöse Mysitis, Eosinophile Myositis, Makrophagenmyofaszitis
- Vakuolen: IBM, Morbus Pompe, HOKPP, Myofibrilläre Myopathie, Ceroidlipofuszinose, Medikamente
Histologie des Muskels bei Neuropathie: Elongierte atrophische Fasern, Fasertypengruppierung, feldförmig gruppierte Atrophie (entspr. je einer motorischen Einheit).
Histologie des Muskels bei Myopathie: Disseminierte Degeneration der Myozyten, zentrale Zellkerne, pathologische Kalibervariation, Zunahme von Fett- und Bindegewebe, Spaltbildung.
Leitfaden zur neuropathologischen Diagnostik von Muskelerkrankungen des Referenzzentrums für neuromuskuläre Krankheiten.
Neurogene Muskelatrophie
[Bearbeiten]Vorkommen bei:
- Spinale Muskelatrophie - Untergang der α-Motoneurone.
- Hereditäre spastische Paraparese (HSP) - Untergang des 1. Neurons.
- Amyotrophe Lateralsklerose (ALS) - Untergang der α-Motoneurone (2. Neuron) und der Pyramidenzellen (1. Neuron), Auftreten im Erwachsenenalter.
Histo:
- Angulär angeordnete atrophe Fasern.
- Gruppenatrophie.
- Fasertypen-Gruppierung.
- Targetoide.
Myasthene Syndrome
[Bearbeiten]Myasthenia gravis
[Bearbeiten]
Ep.: Prävalenz: 10/100.000, Inzidenz: 0,3-0,4/100.000/a.
Ät.: Polyklonale Autoantikörper gegen die α-Untereinheit nikotinerger ACh-Rezeptoren vom Muskeltyp (> 90 %) oder gegen MuskR (10 %). (MuskR ist eine muskelspezifische Rezeptortyrosinkinase, die für das Clustering der ACh-Rezeptoren zuständig ist.)
Ät. und Pg. der Autoantikörperbildung:
- Primäre Autoimmunerkrankung - Ät./Pg.: Im Thymus finden sich deplazierte ACh-Rezeptor-tragende Myoidzellen und ebenfalls deplazierte Keimzentren, also B-Zellen (lymphofollikuläre Hyperplasie) -> Antikörperinduktion gegen ACh-Rezeptor. Ep.: Bevorzugt junge Frauen, Assoziation mit HLA A1, B8, D33 und anderen Autoimmunerkrankungen wie Hashimoto-Thyreoiditis, Lupus erythematodes, rheumatoide Arthritis und rheumatischer Endokarditis.
- Paraneoplastisches Syndrom - Ät./Pg.: Epithelialer Thymustumor mit Expression ACh-Rezeptor-ähnlicher Oberflächenmoleküle -> Antikörper gegen ACh-R-Antikörper. Ep.: Bevorzugt ältere Männer, HLA DR2.
Pg.: Anti-Nikotinrezeptor-Antikörper, anti-MuskR-Antikörper
- -> Abdeckung der ACh-Bindungstasche
- -> Kreuzvernetzung der Rezeptoren -> Internalisierung und Abbau
- -> Komplementaktivierung
Mikro: Endomysiale Lymphozytenansammlungen.
Klinik: Betroffen sind vorwiegend Augen (Doppelbilder, Ptose (SIMPSON-Test: Zunahme der Ptose beim Versuch länger nach oben zu schauen), Abduktionsdefizit), Gesicht (Facies myopathica), Kaumuskeln und Oropharynx (Kauschwäche). Am restlichen Körper ist die Muskelschwäche proximal betont und betrifft die Arme stärker als die Beine. Zunahme im Tagesverlauf. Myasthene Krise: Näselende Dysarthrie, Schluckstörungen, Atemschwäche. Ansprache auf Cholinesterase-Hemmer (Edrophoniumchlorid, Prostigmin).
SF.: Transiente neonatale Myasthenie - Betrifft 10 - 20 % der Neugeborenen von Müttern mit Myasthenie. Ät.: Diaplazentar erworbene Antikörper.
Weblink: OMIM - Myasthenia gravis
Kongenitale Myasthenie
[Bearbeiten]Genetisch, sehr selten.
LAMBERT-EATON-Syndrom (LEMS)
[Bearbeiten]Ät.: Autoantikörper gegen präsynaptische Ca2+-Kanäle. In 60 % paraneoplastisch (kleinzelliges Bronchialkarzinom), 40 % idiopathisch.
EM.: Verlust der Doppelreihen (Typ. Anordnung der Ca2+-Kanäle), Rarifizierung.
Klinik: Beinbetontes myasthenes Syndrom (Treppensteigen!), autonom-anticholinerge Störungen (z.B. Mundtrockenheit). Anders als bei der Myasthenie kann eine wiederholte Innervation die Muskelkraft kurzfristig erhöhen (Fazilitation).
Myopathie
[Bearbeiten]Myotone Erkrankungen
[Bearbeiten]Einteilung: reine Myotonien (Ionenkanalerkrankungen), myotone Dystrophien (DM1 und DM2).
Myotonia congenita Thomsen
[Bearbeiten]Chloridkanalerkrankung (CLCN-1), bei Dauererregung: Muskelstarre, Warm-up-Phänomen bei klinischer Untersuchung, Graefe-Zeichen, dominanter Erbgang
Myotonia congenita Becker
[Bearbeiten]wie Thomsen, aber rezessiver Erbgang, späteres Manifestationsalter, transiente Symptomatik, mit 80% der Fälle die häufigere Myotonie.
Periodische Paralysen
[Bearbeiten]- hypokaliämische periodische Paralyse: CACNL1a3-Mutation des Kalziumkanals, bei chronischer Dauer: progrediente Myopathie
- hyperkaliämische periodische Paralyse SCN4A-Mutation des Natriumkanals: Paramyotones Bild
- Paramyotonia congenita: Myotonie unter Belastung und Kälte.
Myotone Muskeldystrophie DM1: (Morbus CURSCHMANN-STEINERT)
[Bearbeiten]Ep.: 5-10/100.000 (häufigste Muskelerkrankung im Erwachsenenalter, zweihäufigste Muskelerkrankung nach Duchenne)
Ät.: Instabile Expansion eines CTG-Trinukleotid-Repeats in der 3' nicht-translatierten Region des Myotonin-Protein-Kinase DMPK-Gens auf dem langen Arm von Chromosom 19 -> Generalisierter Membrandefekt mit erhöhter Natrium- und reduzierter Chloridleitfähigkeit.
Genetik: Autosomal-dominant mit hoher Penetranz, Repeat-Verlängerung v.a. bei maternaler Transmission. Antizipation.
Repeat-Muster:
- Normalbevölkerung: 4 - 30 CTGs
- „Prämutation“: 50 - 200 Tripletts, keine oder nur milde klinische Symptome.
- Manifestation: > 200 CTGs
- Kongenitale Form: > 1000 Tripletts im mutierten DMPK-Allel.
Mikro: Myopathisch: Kerninternalisierungen, Typ I Faseratrophie, Ringbinden, Vermehrung intrafusaler Fasern in Muskelspindeln. Selten "moth-eaten-fibers" und fibrotische Umbauvorgänge. Kompensatorische Typ II-Hypertrophie, neurogene Komponente mit angulär-atrophen Fasern bzw. kleinere Gruppen atropher Fasern möglich.
Klinik: Progressive Myotonie (verzögerte Muskelrelaxation), distal-extensorenbetont sowie facial (Facies myotonica). Sysarthire, evtl. auch Cataracta myotonica, Herzrhythmusstörungen (bis zur Herzschrittmacherpflichtigkeit), endokrine Störungen (Hodenatrophie, ovarielle Dysfunktion, Thyreose), geistige Retardierung (kortikale Atrophie und Läsionen der weissen Substanz), Beteiligung der glatten Muskulatur des Verdauungstrakts, Antriebsschwäche. Myotone Serienentladungen im EMG.
Formen: Kongenital - klassisch - milde (selten).
Weblink: OMIM - Dystrophia myotonica
DD: Narkolepsie, Myotonia congenita Thomson
Myotone Muskeldystrophie DM2: Ricker-Syndrom, PROMM
[Bearbeiten]Genetik: Expansion von CCTG-Repeats in ZNF9-Gen
Klinik: oft Muskelschmerzen. Proximale Hüftbeuger, selten Facies myopathica, Myotonie oft schwächer als bei DM1, CK nur leicht erhöht. EMG: pathologische Spontanaktivität.
Histo: überwiegend Typ II-Faseratrophie
 |
 |
DD: DM1 (Typ 1 Faseratrophie)
Dystrophinopathien
[Bearbeiten]Def: Erkrankungen durch Mutationen des Dystrophin-Gens. Bei out-of-frame-Mutationen oft schwerere Verläufe
Muskeldystrophie DUCHENNE (DMD)
[Bearbeiten]Ep.: 1:3500 Jungen. Beginn vor dem 5. Lebensjahr.
Ät.: Mutation im Dystrophin-Gen (Chr. Xp21: Expression in Herz, Hirn, Muskel), 2/3 der Fälle Deletion, 10% Duplikation. Kein brauchbares Genprodukt.
Genetik: X-chromosomal-rezessiv. 50-60 % de novo, 30 % vererbt von der Mutter, 10 % Keimzellmosaik.
Klinik: Proximale Muskelschwäche, initial besonders der unteren Extremität. Aufstehen aus der Hocke nur möglich mit auf den Oberschenkeln aufgestützten Händen (GOWER-Zeichen, Schwäche der glutealen Muskulatur). Progredienter Muskelschwund ab Kleinkindalter, Gangunsicherheit, Muskelschwäche, „Gnomenwaden“ (Pseudohypertrophie), Serum-CK stark erhöht (>10x), Kontrakturen, gelegentlich geistige Retardierung.
Mikro: Fibrotische Degeneration von Skelettmuskulatur und Herzmuskel. Myopathisches Bild mit Faserkaliberschwankungen, vermehrte zentrale Kerne, Makrophageninfiltration der Muskelfasern, basoppile Fasern.
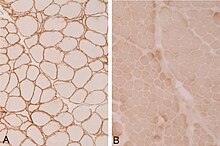
Immunhistochemie: Fehlender Dystrophin-Nachweis (Antikörper gegen N-, C-Terminus und rod domain), bzw. in weniger als 5% der Fasern nachweisbar. Kompensatorische Aufregulation von Utrophin, sekundäre Verminderung von beta-Dystroglykan und Sarcoglykanen.
Prg.: Meist vor dem 13. Lebensjahr Rollstuhlpflichtigkeit und letale kardiorespiratorische Insuffizienz vor dem 20. Lebensjahr. Die Möglichkeit einer häuslichen, nicht invasiven Beatmung kann die Lebenserwartung signifikant erhöhen und die Lebensqualität deutlich verbessern.
DD: Sarcoglykanopatien (insbesondere bei weiblichem Geschlecht), v.a. LGMD 2I, Spinale Muskelatrophie III, kongenitale Muskeldystrophien (CMD).
 |
 |
Weblink: OMIM - Duchenne muscular dystrophy
Muskeldystrophie BECKER-KIENER (BMD)
[Bearbeiten]Ep.: Seltener als DMD.
Ät.: Mutation im Dystrophin-Gen (Expression in Herz, Hirn, Muskel), verändertes Genprodukt mit Restfunktion.
Genetik: X-chromosomal-rezessiv.
Klinik: Progrediente Muskelschwäche, Verlauf langsamer und milder als bei DMD, Beginn sehr variabel (2-35. Lebensjahr)
Histo: Bild wie bei DMD
Immuno: Dystrophin abgeschwächt oder in 10-20% der Fasern negativ. Quantifizierung mit Western Blot möglich. Utrophin kompensatorisch aufreguliert, beta-Dystroglykan und Sarcoglykane sekundär vermindert.
Prg: Hohe Variabilität, mittlere Lebenserwartung: 40 Jahre, Krankheitsdauer: 25-30 Jahre.
Weblink: OMIM - Becker muscular dystrophy
DD: Gliedergürteldystrophie (besonders LGMD 2I), Spinale Muskelatrophie (Typ III), Sarcoglykanopathien, kongenitale Muskeldystrophien (CMD).
Konduktorinnen bei Dystrophinopathien
[Bearbeiten]5-10% der Konduktorinnen können Muskelschwächen aufweisen (ungleiche Inaktivierung des X-Chromosoms).
Immuno: Dystrophin-negative Muskelfasern möglich.
 |
Gliedergürteldystrophien
[Bearbeiten]limb-girdle muscular dystrophy (LGMD)
Ep.: Prävalenz: 0,5-7/100.000
Ät.: Heterogene Gruppe progredienter Muskelschwächen der Becken und Schultergürtelmuskulatur. Ursachen können Defekte von Sarkoglycanen, Calpain-3, Myotilin, Lamin A/C, Dysferlin, Caveolin-3, Telethonin, Fukutin- „related“- Protein oder Titin sein.
Genetik: Heterogen, häufig autosomal-rezessiv (Gruppe 2, 34%), aber auch autosomal-dominant (Gruppe 1, 14%), sonst sporadische Fälle (52%). In 40% der Fälle ist eine genaue Zuordnung nicht möglich. Die bei der LGMD 1B beobachteten LaminA/C-Mutationen können auch bei der Emery-Dreifuss-Muskeldystrophie auftreten. Die bei der LGMD 2B beobachteten Dysferlin-Mutationen können auch bei der Miyoshi-Myopathie auftreten.
Mikro: Myopathisch. Immunhistochemische Spezialfärbungen entsprechend dem klinischen Bild und der vermuteten Ursache. Am häufigsten ist die LGMD 2I, deren klinisches Bild stark der DMD bzw. BMD ähnelt. Bei der LGMD 2I (FKRP) ist meist alpha-Dystroglykan und Laminin alpha2 immunhistochemisch sekundär reduziert.
Klinik: Heterogenes Krankheitsbild mit sehr variablem Beginn (siehe Tabelle). Proximal betonte Muskelschwäche, meist des Beckengürtels, seltener des Schultergürtels (10 %). Im Verlauf auch distale Beteiligung möglich. Kontrakturen, Kardiomyopathie. Verlust der Gehfähigkeit.
Einteilung der Gliedergürteldystrophien nach Mortier[1]
| Typ | Genort | Betrof- fenes Gen- produkt | Erb- gang | Mani-fest- ations- alter (Jahre) | Leitsymptome | Prognose |
|---|---|---|---|---|---|---|
| LGMD 1A | 5q22-q34 | Myotilin | aut.-dom. | 18-35 | Schwäche hüftnaher Beinmuskeln, Jahre später sind Armmuskeln betroffen; Schwäche von Gesichts- und Schlundmuskeln bei 20 %, Dysarthrie bei 25 %. | Rollstuhl- abhängigkeit etwa 20 Jahre nach Beginn, meist normale Lebenserwartung. |
| LGMD 1B | 1q11-21 | Lamin A/C | aut.-dom. | 4-30 | Schwächen in Hüft- und hüftnahen Oberschenkelmuskeln, in zwei Drittel der Fälle Reizüberleitungsstörungen des Herzen und evtl. dilatative Kardiomyopathie. | Lebenslange Gehfähigkeit, jedoch Risiko des plötzlichen Herztods um 50-60 Jahre. |
| LGMD 1C | 3p25 | Caveolin-3 | aut.-dom. | 2-20-70 | Stammnahe Muskelschwäche, Wadenkrämpfe, Wadenpseudohypertrophie, selten auch distale Beteiligung. | Wahrscheinlich lebenslange Gehfähigkeit und normale Lebenserwartung. Zufallsbefunde bei CK-Erhöhung möglich. |
| LGMD 1D | 6q23 | nicht bekannt | aut.-dom. | 20-25, selten unter 20 | Herzrhythmus- störungen und Kardiomyopathie, später zusätzliche stammnahe Muskelschwächen. | Plötzlicher Tod durch AV-Block, ventrikuläre Tachykardie oder Kardiomyopathie möglich. |
| LGMD 1E | 7q | nicht bekannt | ? | 10-30 | Hüftnahe Beinmuskelschwäche | |
| LGMD 1F | 7q32.1-32.2 | nicht bekannt | aut.-dom. | unter 1-58 | Beckengürtel-, Schultergürtelmuskelschwäche | |
| LGMD 1G | 4q21 | nicht bekannt | aut.-dom. | 30-47 | Beckengürtel-, Schultergürtelmuskelschwäche | |
| LGMD 2A | 15q15.1-21.1 | Calpain-3 | aut.-rez. | 3-(10)-30 | Schwäche der Hüft- und Oberschenkelmuskeln, auch Rumpfmuskulatur betroffen, Schultermuskulatur oft 2–5 Jahre später, häufig auch Kontrakturen im Bereich der Wirbelsäule, Fußgelenke, Ellenbogen und Hände. Weltweites Auftreten. | Rascher oder langsamer Verlauf, entsprechend Tod um 20. Lebensjahr möglich, sonst in der 8. Lebensdekade, früher Beginn bedeutet nicht automatisch rasches Fortschreiten. |
| LGMD 2B | 2p13 | Dysferlin | aut.-rez. | 13-(22)-35 | Schwäche vor allem der hinteren Hüft- und hüftnahen Oberschenkelmuskeln, 25 % Wadenpseudohypertrophie, 2-10 Jahre später Schultermuskelschwäche. Scapula alatae. | Rascher oder langsamer Verlauf, in etwa 30 % Gehfähigkeit bis 26-54 Jahren, sonst bis 8. Dekade. |
| LGMD 2C | 13q12 | γ-Sarkoglykan | aut.-rez. | 3-12 | Muskelschwäche im Beckengürtel früher als im Schultergürtel, frühe Wadenpseudohypertrophie, später möglicherweise Gesichtsmuskeln betroffen. | Gehfähigkeit in 25 % 10-15 Jahre, 50 % 15-20 Jahre, 25 % über 20 Jahre, Tod im zweiten Lebensjahrzehnt möglich. |
| LGMD 2D | 17q12-q21 | α-Sarkoglykan | aut.-rez. | 1-16, später | Zunehmende Muskelschwächen im Beckengürtel und Oberschenkel mit verspäteten Gehbeginn oder unsicherem Gang ähnlich wie bei Muskeldystrophie Typ Duchenne. | Rascher oder langsamer Verlauf, Gehfähigkeit bis 16-30 Jahre oder später, vorzeitiger Tod bei raschem Verlauf möglich. |
| LGMD 2E | 4q12 | β-Sarkoglykan | aut.-rez. | 3-12 | Beckengürtel eher betroffen als Schultergürtel, Wadenpseudohypertrophie | Rascher oder langsamer Verlauf, Gehfähigkeit 9-14 Jahre oder bis 38 Jahre, Tod im 2.-3. Lebensjahrzehnt möglich. |
| LGMD 2F | 5q33-q34 | δ-Sarkoglykan | aut.-rez. | 4-10 | Zunehmende Muskelschwächen im Beckengürtel und Oberschenkel mit verspäteten Gehbeginn oder unsicherem Gang ähnlich wie bei Muskeldystrophie Typ Duchenne, Gesichtsmuskeln möglicherweise betroffen, Wadenhypertrophie. | Rasches Fortschreiten mit Gehfähigkeit 9-16 Jahre, Tod am Ende des ersten oder im zweiten Lebensjahrzehnt möglich. |
| LGMD 2G | 7q11-q12 | Telethonin | aut.-rez. | 9-15 | Neben Hüft- und Oberschenkelmuskelschwäche auch Unterschenkelmuskeln und Arm/Schultermuskeln betroffen. | Lange Gehfähigkeit bis 18-25 Jahre nach Beginn. |
| LGMD 2H | 9q31-q34 | Vermutlich E3- Ubiquitin- Ligase | aut.-rez. | 1.-3. Dekade | Beckengürtel eher betroffen als Schultergürtel, möglicherweise Nacken- oder Rückenschmerzen. | Gehschwierigkeiten mit 37-46 Jahren, Rollstuhlabhängigkeit im siebten Lebensjahrzehnt. |
| LGMD 2I | 19q13.3 | Fukutin- „related“- Protein | aut.-rez. | 1.-4- Dekade | Zunächst Schwäche der Hüft- und Oberschenkelmuskeln, später der Schulter- und Oberarmmuskeln, Wadenpseudohypertrophie, Muskelschmerzen bei Belastung, Muskelfaserzerfall (Rhabdomyolyse). | Sehr unterschiedlicher Verlauf, Gehfähigkeit meist bis 30 Jahre. |
| LGMD 2J | 8q24 | Titin | aut.-rez. | 1.-3. Dekade | Muskelschwäche und –atrophie der Hüft- und hüftnahen Oberschenkelmuskeln. | Gehverlust im 3.-5. Lebensjahrzehnt. |
| [LGMD 2K] | 9q34 | POMT | aut.-rez. | 1.-Dekade | Proximal betont. Sehr hohe CK-Werte, Reduzierte Glykosylierung von alpha-Dystroglykan | Milder Verlauf |
| [LGMD 2L] | 11p14 | ANO5 | aut.-rez. | 2.-3. Dekade. | Muskelschmerzen, Atrophien Quadrizeps und Biceps brachii | Progressiv, erhaltene Gehfähigkeit |
| [LGMD 2M] | 9q31 | Fukutin | aut.-rez. | 1 Jahr | Axial und proximal ausgeprägter als Distal, Laminin-α2, alpha-Dystroglykan reduziert | Progressiv. |
DD: Dystrophinopathien, kongenitale Muskeldystrophien (CMD), Emery-Dreifuss-Muskeldystrophie, FSHD, metabolische Myopathien (Glykogenose Typ II, Typ V).
 |
Fazioskapulohumerale Dystrophie (FSHD)
[Bearbeiten]Ep: 1:20.000, Manifestations-Peak um das 30. Lebensjahr, langsam progredienter Verlauf.
Genetik: Autosomal-dominant (D4Z4 auf 4q35), in 90% kann die Diagnose molekulargenetisch gesichert werden, sodaß Muskelbiopsien bei FSHD eher die Ausnahme sind.
Klinik: Variabler Beginn, Manifestation spätestens im 30 Lj. Proximaler Schwerpunkt bevorzugt im Bereich von Gesicht, Schultern und Oberarm, evtl. auch des Oberschenkels. Hypertrophie des M. orbicularis oris, evtl. Hörstörungen, Facies myopathica, Scapula alata.
Labor: CK normal bis 5fach erhöht
Histo: fokale myopathische Cluster mit dystrophischem Bild, in 40-80% begleitende entzündliche Veränderungen (DD: Myositiden!)
Prg.: Sehr variabler Verlauf mit normaler Lebenserwartung. Evtl. in 10-20% Verlust der Gehfähigkeit oder respiratorische Insuffizienz.
Weblink: OMIM - Facioscapulohumeral muscular dystrophy
Okulopharyngeale Muskeldystrophie (OPMD)
[Bearbeiten]Ep: Beginn nach dem 50 Lj, in der Regel vollständige Penetranz mit 70. Lj.
Genetik: meist autosomal-dominant, selten rezessiv: Trinukleotiderkrankung mit GCC-Expansion in Exon 1 von PABPN1 auf Chromosom 14q11.1 (normal: 6, pathologisch 8-11), im frankokanadischen Raum stärker verbreitet. Meist wird die Diagnose molekulargenetisch gesichert,sodaß Muskelbiopsien eher die Ausnahme sind.
Klinik bei late Onset: Leitsymptome: bilaterale Ptosis und Dysphagie, CK normal bis leicht erhöht. Positiver Eiswasser-Test (Unfähigkeit kaltes Wasser schnell zu trinken). Becken- und Schultergürtelschwächen möglich.
Histo: Myopathisch: Typ1-Hypotrophie, Typ2-Hypertrophie, Anguläre Fasern, pyknotische Kernhaufen. Rimmed vacuoles (Trichrom) mit saurer Phosphatase, moth-eaten fibers, core-like areas. Immunhistochemischer Nachweis von PABP-2, Ubiquitin, beta-Amyloid zur Darstellung nuklärer Einschlüsse möglich.
EMI: Vakuolen: osmiophile myelin-ähnliche whorls, intranukläre tubuläre Filamente in 2-8% der Kerne (DD: IBM-Filamente sind größer und auch zytoplasmatisch).
Prg: Gehfähigkeit bis ins hohe Alter. In 5-10% schwere Verlaufsform mit Paresen (meist homzygote PABPN1-Muatationen).
DD: IBM (keinen basophiler Rand in den Vakuolen), myotone Dystrophie Curschmann-Steinert, mitochondriale Myopathien
Distale Myopathien
[Bearbeiten]selten
- Welander (40-50 L.): Extensoren der Finger, myopathisch-dystrophisches Bild, "rimmed vacuoles"
- Tibiale MD (30-40 Lj.): Fussheberschwäche, Steppergang, milde Verläufe möglich, "rimmed vacuoles"
- Late onset distal myopathy (LODM): "rimmed vacuoles", Sarkoplasmische EInschlüsse in der Gomori-Trichrom
- Nonaka-Myopathie (Distale Mypathie mit gerahmten Vakuolen)
- Miyoshi-Myopathie: sehr hohe CK-Werte, Nekrosen, Entzündliche Infiltrate möglich, keine Vakuolen, Dysferlin-Mutationen
- Myofibrilläre Myopathie: Unterschenkel, Hände, Deminopathie
- Distale Myopathie bei Thelethoninopathie (distale Form der LGMD 2G)
DD: Myotone Dystrophie (DM1), CMT, FSHD, IBM, Nemaline Myopathie, Central core disease
Emery-Dreifuss-Muskeldystrophie (EDMD)
[Bearbeiten]Zwei Formen bekannt: x-chromsosomal mit Mutationen von Emerin (Xq28), Missense-Mutationen zeigen mildere Verläufe, Immunhistochemisches Fehlen von Emerin. autosomal dominanter Erbgang mit Missense-Mutationen von LMNA (LaminA/C der Kernhülle)
Klinik: Kardiomyopathien, Kontrakturen im Kindes- und Erwachsenenalter (rigid spine), Muskelbeteiligung in den oberen Extremitäten proximal, in den unteren Extremitäten distal.
Prg: Plötzlicher Herztod durch Rhythmusstörungen möglich, selten schwere Verläufe mit Rollstuhlpflichtigkeit.
Rippling muscle disease (RMD)
[Bearbeiten]autosomal-dominante Caveolinopathie (wie auch LGMD 1C) mit reduzierter Darstellung von Caveolin 3 in der Plasmamembran.
Klinik: mechanische Muskelerregbarkeit, rezidivierende Myoglobinurien, Krämpfe, Myalgien, selten Atrophien und Paresen.
DD: Myotone Dystrophie Typ 2 (PROMM), Myotone Dystrophien
Desmin-Myopathien
[Bearbeiten]heterogene Gruppe von Strukturmyopathien mit Desmin-Ablagerungen
Kongenitale Myopathien
[Bearbeiten]Beschreibung oft nach der Histologie, häufig genetische Ursachen Gemeinsam ist allen Fällen histologisch eine Typ I Faseratrophie, zentral gelegene Kerne, sog. small scattered nuclei
Kongenitale Muskeldystrophien (CMD)
[Bearbeiten]heterogene Gruppe autosomal-rezessiver Erkrankungen mit muskulärer Hypoptonie (floppy infant), Leukodystrophien, CK-Erhöhung
Pt: involvierte Proteine führen meist zu sekundärer Reduktion von alpha-Dystroglykane, am häufigsten ist die primäre Laminin alpha2-Defizienz (MDC1A), immunhistochemisch Verlust des Proteins nachweisbar. Andere Formen: MDC1C (FKRP) mit sekundärem alpha-Dystroglykanmangel, FCMD (Fukutin), UCMD (Kollagen IV), RSMD1 (Rigid-Spine-Syndrom) u.a.
Histo: Typ-I Faseratrophie, Dystrophes Bild (Degeneration, Regeneration, Kerninternalisierung). Endo- und perimysiale Fibrose.
Nemaline Myopathien
[Bearbeiten]Neben kongenitalen Nemalin-Myopathien, können die charakteristischen "nemaline rods" können auch sekundär bei zahlreichen anderen Krankheitsbildern auftreten.
Klinik: häufig proximal betonte Muskelschwäche, Facies myopathica
Genetik: Erbgang autosomal dom./rez. (alpha-Actin, Nebulin, Tropomyosin, Troponin-Muatationen)
Prg: a) schwere kongenitale Verlaufsform, b) intermediäre Form mit Gehverlust um das 10 Lj. c) adulte Form, hier bleibt Gehfähigkeit bis in das hohe Lebensalter erhalten, auch sporadische Formen bekannt.
Histo: Stäbchenförmige Einschlüsse infolge Z-Banden-Überproduktion, meist peripher als Cluster nahe der Kerne (rote Anfärbung in der Trichrom), Typ-I Faseratrophie.
Immuno: alpha-Actinin-2 Ablagerungen im Bereich der "rods"
EMI: Z-Linien:
DD: Central core disease (rods + central cores), andere kongenitale Myopathien, spinale Muskelatrophien.
Central core disease
[Bearbeiten]Genetik: Mutation Ryanodin Rezeptor RYR1, autosomal-dominanter Erbgang
Ko: Pat. haben Risiko für maligne Hyperthermie
Ep: Häufigste kongenitale Myopathie (CK normal-mild)
Histo: Fehlen vom COX bzw. NADH-Aktivität (keine Mitochondrien) am Rand: Desmin + PAS möglich, Cores auch peripheral oder als multiple minicores. Faserkalibervariation, Verbreitung des Fett- und Bindegewebes.
DD: targetoide Fasern
 |
 |
Zentronukläre Myopathien
[Bearbeiten]Man unterschiedet die Myotubuläre Myopathie mit X-chromosomaler Erbgang mit Unreife der Muskelfasern und hoher Letalität im 1. Lebensjahr von den adulten autosomalen Formen. Hier sind die autosomal-dominante Form mit Mutation im Dynamin-2-Gen und die autosomal-rezessive Form mit Mutationen des Amphiphysin-Gens bekannt. Konduktorinnen können milde Symptome mit faszialer Schwäche zeigen.
Histo: kleine abgerundete Fasern (Myotuben), Typ1-Faserpräponderanz, solitäre Kerne mit Halo (in der NADH-Färbung sarkomerfreier Hof).
DD: Myotone Dystrophie, andere kongenitale Muskelerkrankungen.
 |
 |
Myofibrilläre Myopathien
[Bearbeiten]Strukturmyopathien mit unterschiedlichen Einschlüssen wie Spheroidkörperchen oder sarkoplasmatische / zytoplasmatische Einschlüsse, granulomatösen Ablagerungen
Einteilung
- Deminopathien
- Myotillinopathien
- alphaB-Crystallinopathien
- Inclusion Body Myopathy
- Hyaline Body Myopathy
Histo: Eosionophile Einlagerungen, "rimmed vacuoles", Faserkaliberschwankungen, Kerninternalisierung, Split fibers, Verbreiterung des endomysialen Bindegewebes.
Mitochondriale Myopathien
[Bearbeiten]
Mitochondriale Erkrankungen werden maternal vererbt. Das Nebeneinander-Vorliegen von mutierten und nicht mutierten mtDNA wird als Heteroplasmie bezeichnet. In der Regel ist Gewebe mit hohem Energiebedarf (Skelettmuskulatur, ZNS, SInnesorgane) am stärksten betroffen.
Histologisch sind Mitochondriopathien durch ragged red fibers in der Trichrom-Färbung bzw. ragged blue fibers in der SDH sowie durch COX-negative-Fasern gekennzeichnet.
Es sind verschiedene mitochondriale Symptomenkomplexe bekannt:
- Kearns-Sayre-Syndrom (KSS)
- Mitochondriale Myopathie, Enzephalopathie, Laktatazidose, Schlaganfälle (MELAS)
- Myoklonus-Epilepsie und Ragged red fibers (MERRF)
- Leigh-Syndrom
- Chronisch progressive externe Opthalmoplegie (CPEO)
- Neuropathie Ataxie, Retinitis pigmentosa (NARP)
DD: Carnitin-Mangel, Glykogenosen
Metabolische Myopathien
[Bearbeiten]Energiedeckung des Skelettmuskels unter Belastung in folgender Reihenfolge: 1) ATP 2) Creatinphosphat 3) Glucose 4) Fettsäuren.
Klinische Unterscheidung von vier großen Gruppen:
- Störungen der Glycogenolyse (GSD II, III, V), der Glycolyse und der Gluconeogenese - Beschwerden in der Anfangsphase muskulärer Belastung, Besserung bei Fortsetzung („second wind“).
- Defekte der Fettsäureoxidation - Beschwerden nach längerer Belastung.
- Störungen des Purinmetabolismus: MAD-Mangel
- Lipidspeichermyopathien
Glykogenosen
[Bearbeiten]Die Gruppe der Glykogenosen umfasst erbliche Stoffwechselerkrankungen, deren Enzymdefekte die Glykolyse des Muskels stören. Die meisten Glykogenosen betreffen die Leber (Glykogenose Typ I), in der Muskulatur ist am häufigstes die Glykogenose Typ II (saurer Maltase-Mangel) anzutreffen.
Morbus POMPE (Glykogenose Typ II)
[Bearbeiten]Ät.: Das Fehlen der lysosomalen sauren α-1,4-Glucosidase (saure Maltase) führt zur Speicherung von Glykogen in Herz, Muskel, Hirn, Blutzellen und Zunge (die Niere ist frei).
Genetik: Als Ursache können verschiedene Mutationen mit unterschiedlicher enzymatischer Restaktivität vorliegen, daraus resultieren verschiedene Manifestationsalter (frühinfantil, spätinfantil, juvenil, adult).
Klinik: Im Vordergrund stehen eine ausgeprägte Muskelhypotonie und hypertrophische Kardiomyopathie, schwere Atemnot und kardiorespiratorische Störungen. Die frühinfantile Form führt zum floppy infant mit Trinkschwäche. Wichtig: Seit 2006 Enzymersatztherapie möglich!
Weblink: OMIM - Glycogen storage disease II
 |
Morbus CORI (Glykogenose III)
[Bearbeiten]Ät.: Defekt der Amylo-1,6-Glucosidase.
Klinik: Hepatosplenomegalie, Muskelhypotonie, Hypoglykämie
Weblink: OMIM - Glycogen storage disease III
Morbus MC ARDLE (Glykogenose Typ V)
[Bearbeiten]Ät.: Defekt der Glycogen-Phosphorylase (Phosphorylase a).
Ep: Selten: 1:100.000, aber die häufigste unter den Glykogenosen. Meist erst im frühen Erwachsenenalter symptomatisch.
Klinik: Meist Schwäche der oberen Extremitäten, fehlender Laktat-Ansieg im nichtischämischen Test, CK-Erhöhung
Häufigste Punktmutation bei Kaukasiern: R50X
Weblink: OMIM - Glycogen storage disease type V

|
Morbus Tarui (Glykogenese VII)
[Bearbeiten]Ät: Defekt der Phosphofruktokinase
Danon-Erkrankung
[Bearbeiten]Ät: Lysosomale Glykogenspeichererkrankung mit normaler saurer Maltase und X-chromosomalem Erbgang (LAMP-2) und Beginn in der Kindheit.
Histo: Vakuoläre Myopathie mit Glykogen, keine verstärkte Darstellung der sauren Phosphatase, Nachweis sarkolemmaler Proteine in der Membran der Vakuolen
Myoadenylat-Desaminase-Mangel
[Bearbeiten]
Ät: Der MADA- bzw. AMPD1-Mangel ist die häufigste metabolische Erkrankung des Muskels. Das Muskelenzym ist Bestandteil des Purinnukleotid-Zyklus, welcher bei Belastung das Adenosinmonophosphat entfernt und Fumarat dem Citratzyklus bereitstellt.
Enzymhistochemie: Reduzierte Myoadenylatdeaminase-Aktivität.
Klinik: Belastungabhängige Krämpfe, Fehlender Ammoniak-Anstieg im Laktat-Ischämie-Test
Primärer MAD-Mangel: häufigste Mutation: 34C>T führt zu vollständigem Fehlen einer MAD-Aktivität Sekundärer MAD-Mangel: reduzierte Aktivität bei Kollagenosen, Myositiden und Glykogenosen
Lipidmyopathien
[Bearbeiten]Ät: Mitochondrialer Fettsäureabbau, der in der Leber zu Ketonkörpern verstoffwechselt wird, dienen dann bei niedrigem Glykogengehalt der Muskulatur als Energielieferant.
Klinik: Intermittierende Muskelschwächen, Rhabdomyolysen
Einteilung:
- Carnitin-Palmitoyl-Transferase Mangel
- Succinyl-CoA-Transferase-Mangel
- Störungen der mitochondrialen beta-Oxidation
- Störungen der Atmungskette
Amyloid Myopathie
[Bearbeiten]Ät: Ausbildung von Amyloidfibrillen und Ablagerungen in der Muskulatur, meist im Rahmen einer systemischen Amyloidose
Ep: Manifestation zwischen 25-80 Lj.
Klinik: proximale, symmetrische Schwäche der unteren Extremitäten. CK 3-6fach erhöht.
Histo: kongophile Ablagerungen, meist Lambda-Leichtketten in den Gefäßwänden, auch um einzelne Muskelfasern zusätzlich zu myopathischen oder neurogenen Veränderungen.
Ischämie
[Bearbeiten]Vgl. KHK
Ät.: pAVK, arterielle Embolie.
Histo:
- Akute Ischämie:
- nach Stunden: Eosinophilie, Verlust der Zellkerne
- in den ersten Tagen: Leukozytäre Demarkation
- nach Tagen bis wenigen Wochen: Granulationsgewebe (Kapillarproliferate, Fibroblastenaktivierung, Lymphozyten, Plasmazellen, Siderophagen)
- nach Wochen bis Monaten: Zellarmes faserreiches Narbengewebe
- Chronische/chronisch-rezidivierende Ischämie: Muskelzellkaliberschwankungen, „myogene Riesenzellen“ mit peripher gelagerten Zellkernen und Vakuolisierung, lymphoplasmazelluläre Infiltrate.
Toxische Myopathien
[Bearbeiten]Klinik: Myalgien, Rhabdomyolyse
- Statin-, Niacin- und Fibrat-induzierte nekrotisierende Myopathie (Nekrosen, Regeneration (wenig MHC-I) durch Blockade der HMG-CoA-Reduktase
- Statin- oder D-Pencillamin-verursachte inflammatorische Myopathie (oPolymositis-ähnliches Bild)
- Fokale Myopathie (z.B. bei Schlangenbiss oder Lokalanästhetika): lokale Entzündung und Nekrose
- Suchtmittel (Alkohol, Kokain, Heroin, Pentazocin): Fibrosen, Atrophien
- antiretrovirale Therapie bei HIV (AZT): mitochondriale Toxizität: ragged red fibers
- Critical illness myopathie bei Langzeit-Intensivmedizin: Sepsis Organversagen, Funktionsausfall des Motoneurons u.a. durch Hochdosis-Cortison
- Steroid-Myopathie: selektive Typ-II Faseratrophie
- Colchizin-Myopathie: vakuoläre Myopathie mit Lysosomen-Ansammlung und autophagischen Vakuolen
- Eosinophilie-Myalgie-Syndrom und Toxisches-Öl-Syndrom: eosinophile Fasziitis, perimysiale lymphozytäre Infiltrate
Histologie: Muskelfasernekrosen, Myofibrillen, Inflammation
Rhabdomyolyse
[Bearbeiten]
Ät.: Rapider Muskeluntergang mit Myoglobinurie (Gefahr des Nierenschadens), Myalgien und extremen CK-Anstieg (mehr als 5-fach über Norm). In 10% rezidivierendes Auftreten möglich.
Toxine sind die häufigste Ursache. Myopathien oder metabolische Störungen machen 10% aller Rhabdomyolysen aus.
- Stoffwechseldefekte: Mc Ardle-Krankheit (GSD V) - Defekt der Glykogen-Phosphorylase, ein Enzym des Glykogen-Abbaus.
- Ischämie, Reperfusions-Syndrom, Kompartment-Syndrom
- Alkoholexzesse
- Medikamente (Statine): Cytochrom P450-vermittelt
- Maligne Hyperthermie - Ät.: Inhalationsanästhetika, depolarisierende Muskelrelaxantien (Suxamethonium)
- Thyreotoxische Krise (Morbus Basedow)
Pg.: Schädigung von Skelettmuskelzellen mit Freisetzung von Zellproteinen (Kreatinkinase, Myoglobin u.a.).
Histo:
- Muskel: Gruppenförmige Nekrosen bzw. basophile Fasern bei Regeneration.
- Niere: Ablagerung von braunem globulärem Material in den Tubuli (IHC: Myoglobin +).
Labor: Blut: Anstieg von CK, LDH und Myoglobin. Urin: Myoglobin-Nachweis.
Klinik: Muskelschmerzen, Muskelschwäche, Myoglobinurie (dunkler Urin).
Kompl.: Akutes Nierenversagen (15-33% der Patienten mit Rhabdomyolyse)
Radiogene Schäden
[Bearbeiten]Ät.: Z.n. Radiatio
Histo: Narbenfibrose, atrophe Muskelfasern.
Myositis
[Bearbeiten]Myositiden (mit abnehmender Häufigkeit: Dermatomyositis, IBM, Polymyositis, idiopathische Myositis ) haben eine jährliche Inzidenz von 0.5/100.000 Einwohner.
Ät.: Mikroorganismen (erregerbedingt), autoimmunologisch oder i.R. eines paraneoplastischen Syndroms oder unter Statin-Therapie
Klinik: in bis zu 90% der Pat. ANA-Antikörper.
Histo: Perimysium verbreitert und fibrosiert, benachbart atrophe Muskelfasern.
SF: fokale Myositis (häufig M. vastus lateralis) mit variablen Veränderungen von myopathisch, neurogen bis inflammatorisch, oft Remission.
DD: Vaskultis
Polymyositis
[Bearbeiten]Ät: subakute Muskelerkrankung durch T-Zell vermittelte Autoimmunreaktion gegen Muskelfasern
Ep: höheres Erwachsenenalter (50-60-Lj), häufiger Frauen als Männer, oft gehen initial als PM klassifizierte Fälle im Verlauf in eine sIBM über.
Klinik: Muskelschwäche, - druckschmerz, -atrophie, pathologische Spontanaktivitäten im EMG, CK-Anstieg, in der Regel keine distale Beteiligung. Bei schweren nekrotisierenden Verläufen Anti-SRP-AK nachweisbar.
Histo: Faserkalibervariation, einzelne basophile Fasern möglich, split fibers, ödematöse Auflockerung, Invadierende CD8+ Lymphozyten, Makrophagen bevorzugt endomysial. Aufregulation von MHC-I in den betroffenen Muskelfasern (normal nur in den Blutgefäßen).
Prg: gering erhöhtes Malignomrisiko (NHL, Lungen- und Blasenkarzinome)
DD: PROMM (Myotone Dystrophie Typ 2), Morbus Pompe, LGMDs mit inflammatorischer Beteiligung.
 |
Dermatomyositis
[Bearbeiten]Ät: schwere Muskelerkrankung durch humoral- und Komplement-vermittelten vaskulitischen Prozess mit endofazikulärer Hypoperfusion.
Histo: perifaszikuläre Atrophie der Muskelfasern, Extensive vakuoläre Degneration möglich, einzelne nekrotische Fasern, ultrastruktureller Nachweis tubulovesikulärer Einschlüsse, Inflammatorische Zellen perivaskulär und perimysial ohne Eosinophilie.
Immuno: MHC-I Aufregulation, Überwiegen von CD4-lymphozyten, aber auch CD8-positive Lymphozyten intramysial, Nachweis von Makrophagen, Nachweis von Komplementkomplex C5b9 in den Kapillaren
Klinik: Erytheme, Kernig-Zeichen (schmerzhaft erweiterte Kapillaren des Nagelfalzes), Gottron-Zeichen (Kollodiumflecken der Knöchelhaut), subkutane Kalzifikationen. 40% Herzrhythmusstörungen. Overlap mit Anti-Synthetase-Syndrom (Nachweis von Jo-1 AK, MI-2 AK). CK-Anstieg (bis zu 50fach erhöht) korreliert mit Verlauf.
Prg: 17% progredient trotz Steroidgabe, Erhöhtes Malignomrisiko ab dem 50 Lj.
Einschlusskörperchenmyositis
[Bearbeiten]inclusion body myositis (IBM)
Ät: chronische entzündliche Muskelerkrankung: Einteilung in a) sporadische IBM, vermutlich autoimmun-vermittelt und b) hereditäre IBM
EP: Meist erst nach dem 50 Lj.
Klinik: Asymmetrien der betroffenen Muskulatur (lange Fingerbeuger, ulnare Unterarmmuskulatur), kein Ansprechen auf Steroide. Dysphagie in 20%, CK 2-5fach erhöht.
Histo: Vakuolen (2-70%) mit eosinophilen Einschlüssen, kongophil + Abeta+ Ubiquitin+, Vermehrung interner Kerne, Nekrosen, CD8+, keine CD20, öfters mit RRF+ and COX- Fasern. Nachweis filamentöser Einschlüsse in der Elektronenmikroskopie.
DD: Myofibrilläre Myopathie, autosomal-dominante IBM mit Demenz + M. Paget.
 |
Granulomatöse Myositis
[Bearbeiten]Ät: Sarkoidose, Sklerodermie, Lupus erythematosus, Vaskulitiden.
 |
 |
 |
Makrophagen-Myofasziitis
[Bearbeiten]Histo: Perimysiale Makrophagenansammlungen, ultrastruktureller Nachweis von Aluminiumablagerungen als Bestandteil von Impfseren.
Proliferative Myositis
[Bearbeiten]Syn.: Proliferierende Myositis.
Ät: Intramuskulärer, inflammatorischer (Pseudo)Tumor am ehesten myofibroblastären Ursprungs (Pseudosarkom).
Ep: Peak Inzidenz 40. bis 70. Lj.
Histo:
- Spindezellige und große Ganglionzell-artige Proliferate zwischen den Muskelfasern
- Schachbrettartiges Muster
- Gesteigerte Proliferation (Mitosen, Mib1), keine atypischen Mitosen
Verh.: Benigne.
Weblinks:
 |
Tumoren des Skelettmuskels
[Bearbeiten]Rhabdomyosarkom
[Bearbeiten]rhabdomyosarcoma
Ät: Maligner mesenchymaler Weichteiltumor der Skelettmuskulatur.
Ep.: Kinder häufiger betroffen.
Einteilung:
- Embryonales Rhabdomyosarkom
- Alveoläres Rhabdomysosarkom
- Pleomorphes Rhabdomyosarkom
Siehe auch: Rhabdomyosarkom
 |
 |
 |
Rhabdomyom
[Bearbeiten]Ät: Benigner Weichteiltumor, fast immer im Herzen auftretend.
Ep: Selten, kann im Rahmen einer tuberösen Sklerose (Morbus BOURNEVILLE-PRINGLE) auftreten.
 |
Quellen
[Bearbeiten]- ↑ U. Schara, W. Mortier. “Neuromuskuläre Erkrankungen (NME). Teil 2: Muskeldystrophien (MD)”. Monatsschrift Kinderheilkunde, 151:1321-1341, 2003.
Buch-Navigation